Введение
Микроваскулярная стенокардия (МВС) — это заболевание сердечно-сосудистой системы, сопровождающееся типичной для стенокардии болью в грудной клетке и электрокардиографическими изменениями, характерными для ишемии миокарда, без поражения эпикардиальных коронарных артерий, по данным ангиографии [1]. МВС характеризуется затяжными болями в области сердца не только во время физической нагрузки и после нее [2], но и в покое, зачастую сопровождается снижением болевого порога и изменением эмоционального статуса больных. Несмотря на то что прогноз при МВС, как правило, благоприятный, стенокардия значительно ухудшает качество жизни больных и представляет существенную нагрузку для системы здравоохранения. Диагностика МВС в реальной клинической практике зачастую основывается на анамнезе и клинических данных, что ведет к ложноположительным либо ложноотрицательным результатам. При коронарографии можно увидеть только эпикардиальные артерии, а оценить состояние микроциркуляторного русла не представляется возможным [3]. Учитывая широкое распространение МВС среди пациентов с болями в сердце, необходимо глубокое изучение данной патологии, ее диагностики и лечения.
Нестабильная стенокардия
Нестабильная стенокардия — это понятие, под которым объединяют несколько клинических ситуаций: их общей чертой является наличие приступов боли за грудиной.
В последнее время нестабильную стенокардию определяют как обострение ишемической болезни сердца (нарушение кровообращения в артериях, призванных обеспечивать сердечную мышцу (миокард) необходимым запасом крови), угрожающее развитием инфаркта миокарда (гибель участка сердечной мышцы вследствие нарушения кровообращения в нем) или внезапной смерти.
Симптомы нестабильной стенокардии
Главным симптомом нестабильной стенокардии является боль:
- по характеру боли довольно сильные, сжимающие или давящие, нередко ощущается чувство тяжести или нехватки воздуха;
- локализация (расположение) боли – за грудиной или в предсердечной области, то есть по левому краю грудины; боль отдает в левую руку, левое плечо либо в обе руки, область шеи, нижнюю челюсть, между лопаток, левую подлопаточную область;
- длительность – более 10 минут.
Факторы, провоцирующие боль:
- нельзя определить четкую связь боли с определенной физической нагрузкой или другими условиями (например, боль появляется в ветреную погоду или после еды), болевой приступ нередко возникает в состоянии покоя или при минимальной физической нагрузке (наклон, ходьба по квартире);
- окончание болевого приступа – часто после неоднократного приема нитроглицерина;
- приступы возникают чаще, чем раньше.
Постепенно развиваются нарушения ритма сердца:
- учащение сердечного ритма, ощущение сердцебиения;
- сердцебиения становятся нерегулярными, с перебоями.
Присоединяются одышка, возникающая при минимальной физической нагрузке и даже в состоянии покоя, ощущение нехватки воздуха.
Формы
Выделяют несколько форм нестабильной стенокардии:
- впервые возникшая стенокардия (заболевание, проявляющееся дискомфортом или болью в грудной клетке сжимающего, давящего характера, которая локализуется чаще всего за грудиной и может иррадиировать (отдавать) в левую руку, шею, нижнюю челюсть, эпигастральную (« под ложечку») область);
- прогрессирующая стенокардия (увеличение интенсивности и/или продолжительности болевых приступов, возникновение их при значительно меньшей физической нагрузке или в покое, присоединение одышки, чувства нехватки воздуха);
- постинфарктная стенокардия (возникшая через 24 часа и до 8 недель после развития инфаркта миокарда (отмирание части сердечной мышцы вследствие прекращения кровотока на этом участке)) или послеоперационная стенокардия (в течение одного-двух месяцев после успешного операции по восстановлению кровотока).
На практике часто применяют классификацию Браунвальда (1989 г.), подразделяющую нестабильную стенокардию на три класса (чем выше функциональный класс, тем больше вероятность развития осложнений:
- I класс — впервые возникшая стенокардия или усиление имевшейся стенокардии в течение месяца;
- II класс — стенокардия покоя в течение предшествующего месяца;
- III класс — стенокардия покоя в течение последних 48 часов.
В зависимости от условий возникновения также выделяют:
- класс А — вторичная нестабильная стенокардия. К этой группе относятся больные, у которых нестабильная стенокардия развивается при наличии факторов, усугубляющих ишемию (анемия (малокровие), повышение температуры тела, инфекция, пониженное артериальное давление, неконтролируемая гипертензия, нарушения ритма сердца, эмоциональный стресс и других);
- класс В — первичная нестабильная стенокардия. К этой группе относятся больные, у которых нестабильная стенокардия развивается без экстра-кардиальных условий, усиливающих ишемию;
- класс С — постинфарктная нестабильная стенокардия. К этой группе относятся больные, у которых стенокардия развивается в первые 2 недели инфаркта миокарда.
Причины
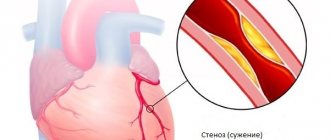
Основной причиной нестабильной стенокардии служит разрыв так называемой нестабильной атеросклеротической бляшки (образование, состоящее из смеси жиров (в первую очередь, холестерина (жироподобное вещество, являющееся « строительным материалом» для клеток организма) и кальция), что провоцирует образование тромба с неполным закрытием просвета сосуда.
Наличие тромба (сгустка крови) в артерии, питающей сердце, препятствует адекватному кровоснабжению сердечной мышцы, что приводит к появлению болевого синдрома и развернутой клиники (совокупность симптомов) нестабильной стенокардии.
Разрыву бляшки способствуют:
- накопление большого количества жиров и недостаточное содержание в ней коллагена (белок, составляющий основу соединительной ткани);
- воспаление и факторы « текучести» крови.
Место МВС в структуре ИБС
Сердечно-сосудистые заболевания (ССЗ) по-прежнему сохраняют лидирующие позиции в структуре смертности по всему миру [4, 5]. Так, по данным Росстата за 2021 г., смертность от ССЗ составила 633 случая на 100 тыс. населения. Годом ранее этот показатель составлял 622,1 случая на 100 тыс. населения. Ежегодная смертность от ишемической болезни сердца (ИБС) среди населения России составляет 27%. При этом только 40–50% больных ИБС знают о своем заболевании и получают комплексное лечение. Более чем у половины госпитализированных больных с диагнозом «острый коронарный синдром» при проведении коронароангиографии обнаруживаются неизмененные коронарные артерии, что указывает на иное происхождение ангинозных болей, не исключая МВС [6]. В настоящее время широко признано, что обструктивное поражение эпикардиальных артерий не является единственной причиной ишемии миокарда [7, 8]. В ретроспективном анализе реестра NCDR Cath только у 37,6% пациентов было диагностировано обструктивное поражение эпикардиальных артерий, в то время как у 69% пациентов была подтверждена преходящая ишемия миокарда при проведении неинвазивных диагностических тестов [9]. Следует отметить, что боли в груди при неизмененных коронарных артериях не всегда являются следствием МВС, поэтому для диагностики требуется применение оптических систем с высокой разрешающей способностью.
Патофизиология коронарной микроваскулярной дисфункции (КМД)
Миокард — это аэробная мышечная ткань, которая нуждается в непрерывном поступлении крови, насыщенной кислородом, для выработки энергии, необходимой для поддержания насосной функции сердца. В базовых условиях работы сердца из артериальной крови можно получить 60–70% необходимого кислорода, поэтому повышенная потребность миокарда в кислороде может быть удовлетворена только путем увеличения коронарного кровотока. Проксимальное коронарное русло состоит из эпикардиальных артерий диаметром от 5 до 0,5 мм и дает начало интрамуральным сосудам. Дистальное коронарное русло представлено преартериолами, артериолами диаметром от 40 до 400 мкм и капиллярами диаметром менее 10 мкм, которые составляют основную систему коронарного кровообращения [10]. В состоянии покоя тонус коронарного микроциркуляторного русла высокий, но диаметр артериол может быстро меняться, реагируя на повышенную потребность миокарда в кислороде и увеличивая коронарный кровоток [11]. Капилляры и венулы являются важным компонентом коронарной микроциркуляции, поэтому структурные и функциональные нарушения на данном уровне (например, падение давления крови в капиллярной сети или микроэмболизация) могут стать причиной развития ишемии миокарда. В зависимости от клинической картины выделяют разные патогенетические механизмы микрососудистой дисфункции (табл. 1) [12].
По мнению A. Faccini et al., воспаление является еще одной потенциально важной причиной развития КМД [13]. Коронарный микрососудистый спазм, первоначально описанный в работе [14], может подобно эпикардиальному спазму вызвать ишемию миокарда при отсутствии повышенных потребностей миокарда в кислороде и инициировать стенокардию покоя. На сегодняшний день нет сомнений в том, что МВС является гетерогенным синдромом, в основе развития которого могут лежать различные патогенетические механизмы. К предполагаемым механизмам КМД относятся измененная регуляция коронарной микроциркуляции вегетативной нервной системой, генерализованные сосудистые нарушения. Так, в одном из крупных исследований P. Ong et al. [15, 16] в ходе тестирования пациентов на ацетилхолин у каждого четвертого наблюдался микрососудистый спазм, характеризующийся ишемическими изменениями на ЭКГ без видимых изменений диаметра эпикардиальных коронарных артерий. A.L. Arrebola-Moreno et al. [17] сообщают, что коронарный микрососудистый спазм, вызванный внутрикоронарным введением ацетилхолина, ведет к нарушениям перфузии и сократимости миокарда. В исследовании V.R. Taqueti et al. [18] была обнаружена непосредственная связь КМД с формированием сердечной недостаточности у пациентов с сохраненной фракцией выброса. Однако в большинстве случаев МВС развивается вследствие изолированной КМД [19] — единственного (или преобладающего) механизма, ответственного за развитие приступа стенокардии или асимптомной ишемии миокарда [20].
Клиническая картина и диагностика МВС
Для МВС характерна триада признаков: 1) типичная стенокардия, обусловленная физической нагрузкой, в сочетании или при отсутствии стенокардии покоя и одышки; 2) наличие признаков ишемии миокарда по данным электрокардиографии (ЭКГ), холтеровского мониторирования (ХМ), стресс-тестов при отсутствии других заболеваний сердечно-сосудистой системы; 3) неизмененные или малоизмененные коронарные артерии (стенозы артерий менее 50%) [21]. Приступы стенокардии могут возникать достаточно часто, до нескольких раз в неделю, но при этом иметь стабильный характер. Боли возникают как при физической нагрузке, эмоциональном стрессе, так и в покое и плохо купируются нитратами. Таким образом, МВС является формой хронической стенокардии и по МКБ-10 относится к коду I20.8 «Другие формы стенокардии».
Выделяют 4 клинических критерия, позволяющих заподозрить МВС [22]:
клиника ишемии миокарда: ангинозные приступы или эквивалентные симптомы (например, одышка) при нагрузке или в покое;
отсутствие обструкции коронарных артерий: сужение просвета артерии на 50% и менее или фракционный резерв кровотока более 0,8, по данным компьютерной томографии или инвазивной коронароангиографии;
объективное подтверждение ишемии миокарда (ишемические изменения на ЭКГ в момент приступа); ангинозная боль, ишемические изменения на ЭКГ и/или при эхокардиографическом исследовании (ЭхоКГ), снижение перфузии миокарда при нагрузочных пробах;
подтверждение микроваскулярных нарушений: резерв коронарного кровотока менее 2,0–2,5 (в зависимости от методики измерения); спазм микрососудов при ацетилхолиновой пробе (ишемические изменения на ЭКГ при отсутствии эпикардиального спазма); увеличение показателей сопротивления микрососудов; замедление коронарного кровотока при сумме баллов по шкале TIMI 25 и более.
При наличии всех 4 критериев диагноз МВС наиболее убедителен. Наличие 1-го и 2-го критериев говорит о возможности МВС, но диагностировать МВС можно, только получив объективные доказательства ишемии миокарда (критерий 3) или нарушения коронарной микрососудистой функции (критерий 4).
Диагностируется ишемия миокарда обычно при проведении нагрузочных тестов (чаще всего используются велоэргометрия (ВЭМ), тредмил-тест и 24-часовое ХМ) путем выявления горизонтальной депрессии сегмента ST более чем на 1 мм от точки J на ЭКГ [23]. Очень важно понимать, что диагноз МВС пациентам с болью в грудной клетке не должен ставиться только методом исключения по результатам коронароангиографии. Необходим комплексный подход с учетом всех неинвазивных и инвазивных методов исследования для верификации ишемии миокарда [24]. Клинические рекомендации предлагают следующий алгоритм подтверждения ишемии миокарда. Диагноз выставляется на основании совокупности жалоб, данных анамнеза (факторов сердечно-сосудистого риска), выявленной скрытой коронарной недостаточности. При подозрении на стенокардию рекомендуется по характеру боли в грудной клетке, возрасту и полу больного рассчитывать предтестовую вероятность ИБС [25]. Однако в ряде крупных исследований последних лет было показано, что такой подход приводит к существенному завышению риска ИБС и сопровождается назначением необоснованных дополнительных диагностических исследований.
Всем пациентам с подозрением на ИБС первым этапом проводится ЭКГ [26]. При неосложненной ИБС специфические признаки ишемии без нагрузки чаще всего отсутствуют. Единственным достаточно специфическим признаком является появление зубца Q после перенесенного инфаркта миокарда. Изолированные изменения зубца T малоспецифичны и чаще всего не учитываются. При проведении ЭКГ с нагрузкой специфическим признаком ишемии миокарда является горизонтальная или косонисходящая депрессия сегмента ST глубиной не менее 0,1 Мв, продолжительностью не менее 0,06–0,08 с от точки J в одном и более ЭКГ-отведениях. Признаками вазоспазма служит транзиторный подъем сегмента ST не менее чем на 0,1 Мв в двух и более отведениях [27]. Однако чувствительность метода снижается у пациентов с рубцовыми изменениями на ЭКГ, при внутрижелудочковых блокадах и гипертрофии левого желудочка (ЛЖ). Хочется отметить, что нагрузочная ЭКГ-проба на велоэргометре или тредмиле неинформативна при полной блокаде левой ножки пучка Гиса, наличии электрокардиостимулятора и синдроме WPW, при которых изменения сегмента ST невозможно интерпретировать. Кроме того, ложноположительные результаты часто обнаруживаются у пациентов с ЭКГ-изменениями в покое вследствие гипертрофии ЛЖ, электролитного дисбаланса, нарушений ритма и проводимости [28].
Всем пациентом с ИБС или подозрением на нее показано проведение ЭхоКГ, которая позволяет оценить систолическую и диастолическую функции ЛЖ, выявить клапанную патологию, исключить гипертрофическую кардиомиопатию, аневризму восходящего отдела аорты, врожденную патологию сердца [22, 26]. Однако при МВС локальные зоны гипокинеза на ЭхоКГ в покое не регистрируются ввиду многочисленности малых зон поражения, но одним из ранних признаков ИБС, а именно микрососудистой дисфункции, может быть нарушенная диастолическая функция ЛЖ [29]. Другими недостатками ЭхоКГ являются низкое качество визуализации базальных сегментов ЛЖ и получение ложноположительных результатов при патологических изменениях в верхушечной области [30]. Наличие у пациента тахикардии/аритмии значительно усложняет интерпретацию результатов ЭхоКГ. Следует отметить, что недостатком всех ультразвуковых методов исследования миокардиального кровотока является зависимость интерпретации от квалификации и опыта специалиста, выполняющего исследование. Чувствительность ЭхоКГ в покое при выявлении ишемии миокарда, по данным разных авторов, составляет 7,5–26,7%. Отсутствие такого признака, как нарушение регионарной и глобальной сократимости у пациентов с МВС, можно объяснить особенностями распространения ишемии, когда она ограничивается отдельными небольшими участками миокарда [31].
Согласно современным европейским и российским рекомендациям ХМ рекомендовано пациентам с болью в грудной клетке и подозрением на аритмию. ХМ в 12 отведениях может быть полезным при подозрении на вазоспастическую стенокардию. Диагностическая ценность данного метода для рутинного обследования больного с подозрением на ишемию миокарда невелика. Депрессия сегмента ST на ЭКГ в покое может быть расценена как признак транзиторной ишемии. Однако депрессия сегмента ST не связана с неблагоприятным прогнозом, не дает дополнительной информации по сравнению с нагрузочными тестами и часто даже не подтверждается как признак преходящей ишемии при проведении визуализирующих нагрузочных тестов. Следует отметить, что депрессия сегмента ST на ЭКГ в покое может быть обусловлена гипертрофией ЛЖ. В связи с этим ХМ не может быть использовано для достоверной диагностики ишемии миокарда, так как результаты исследования не исключают и не подтверждают ИБС, в т. ч. МВС [5, 22].
Нагрузочные тесты очень важны для верификации латентных форм ишемии миокарда путем провокации ишемии фармакологической или физической нагрузкой. Варианты нагрузочных проб разнообразны. В ходе их проведения повышается потребность миокарда в кислороде (тредмил-тест, ВЭМ, добутаминовая проба) или снижается доставка кислорода к миокарду (пробы с дипиридамолом и аденозином) [22, 29].
Тредмил-тест является более физиологичным методом и имеет преимущества перед ВЭМ благодаря возможности дозированно повышать нагрузку с использованием стандартного протокола Bruce до значений больших, чем при ВЭМ. Достоверным признаком ишемии миокарда при выполнении ВЭМ является горизонтальная или косонисходящая депрессия сегмента ST на 1 мм и более [5]. Вероятность диагноза ИБС приближается к 90%, если во время нагрузки депрессия сегмента ST ишемического типа достигает 2 мм и более и сопровождается типичным приступом стенокардии. ВЭМ показана только пациентам, способным выполнить адекватную физическую нагрузку на велотренажере. Следовательно, проведение ВЭМ невозможно, если у пациента имеются заболевания суставов или значимый стеноз артерий нижних конечностей. Из-за относительно низкой чувствительности ВЭМ при ИБС ее отрицательный результат также не исключает этого диагноза. Частота ложноположительных результатов достигает 15% [24, 25]. В многочисленных исследованиях сообщается о меньшей чувствительности ВЭМ и большей частоте ложноположительных результатов у женщин по сравнению с мужчинами. Чувствительность и специфичность тредмил-теста и ВЭМ примерно одинаковы. Ложноотрицательные тесты приводят к недооценке симптомов стенокардии.
По сравнению со стресс-нагрузочными ЭКГ-тестами стресс-ЭхоКГ более предпочтительна. Это один из самых информативных и дешевых методов неинвазивной диагностики ишемии миокарда, доказавший свою высокую диагностическую значимость [32]. Данный метод может быть применен с использованием всех стресс-агентов, обладает высокой чувствительностью (80–85%) и специфичностью (84–86%) в диагностике стенозов, превышающих 50%. Широко изучаются возможности радиоизотопных методов в выявлении МВС, но до сих пор они не стали рутинными ввиду их сложности и дороговизны [21].
Важное место в диагностике МВС занимает позитронно-эмиссионная томография (ПЭТ) сердца с проведением нагрузочных проб [33]. По мнению большинства специалистов, ПЭТ сердца в покое малоинформативна. Нарушение миокардиального кровотока возможно выявить только в условиях функциональной нагрузки, позволяющей обнаружить снижение кровотока в участках миокарда, обусловленное эндотелиальной дисфункцией или ангиоспазмом микроваскулярного русла [34]. Распределение радиофармпрепарата на фоне стрессорного воздействия позволяет выявить даже небольшие участки ЛЖ, в которых отмечается гипоперфузия миокарда. Существуют различные варианты нагрузочных проб: проба с физической нагрузкой на велоэргометре или тредмиле, фармакологическая проба с вазодилататорами, чреспищеводная кардиостимуляция и холодовая проба. В клинической практике при ПЭТ-перфузионных исследованиях с 13N-аммонием чаще всего применяется фармакологическая проба с аденозином. Согласно данным литературы ПЭТ с использованием фармакологических нагрузочных проб обладает высокой специфичностью (78–100%) и чувствительностью (87–97%) в диагностике ишемии миокарда [33, 34]. Метод ПЭТ подобно однофотонной эмиссионной компьютерной томографии (ОФЭКТ) предоставляет информацию о наличии или отсутствии ишемии миокарда, ее локализации и выраженности, рубцовых изменениях. В то же время ПЭТ, в отличие от ОФЭКТ, характеризуется более высоким качеством изображения, обладает уникальными возможностями по расчету кровотока (в мл/мин/г), что позволяет неинвазивно оценивать резерв кровотока и обеспечивает более низкую лучевую нагрузку. Однако ПЭТ в целом меньше используется из-за малой доступности и высокой стоимости. На сегодняшний день проводятся исследования, совмещающие метод ПЭТ с внутривенной фармакологической нагрузкой. В качестве нагрузки используется доступный на фармакологическом рынке радиофармпрепарат аденозинтрифосфат, он хорошо зарекомендовал себя как вазодилататор, имеет короткий период распада, редко вызывает побочные эффекты. Применение добутамина представляется нецелесообразным при МВС, так как ожидаемые эффекты снижения сократимости миокарда вследствие вызываемой им ишемии крайне редки, как и в случае применения стресс-ЭхоКГ [21, 23]. Постановка диагноза вазоспастической стенокардии осуществляется на основании транзиторных ишемических изменений сегмента ST во время приступа стенокардии (характерны подъемы сегмента ST во время приступа). Для исключения вазоспастической стенокардии возможно проведение при коронароангиографии провокации коронарного спазма [35] введением ацетилхолина хлорида [23]. Проба на ангиоспазм считается положительной, если возникают: а) ангинозный приступ; б) ишемические изменения на ЭКГ; в) выраженная вазоконстрикция эпикардиальных артерий [36]. Если проба с ацетилхолином сопровождается болью и ишемическими изменениями на ЭКГ, но нет спазма эпикардиальных артерий, то можно говорить о вазоконстрикции на уровне микроциркуляторного русла.
Стенокардия
Атеросклероз
Сахарный диабет
Инсульт
23447 20 Мая
ВАЖНО!
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Стенокардия: причины появления, симптомы, диагностика и способы лечения.
Определение
Стенокардия – клинический синдром, проявляющийся чувством стеснения или сжимающей давящей болью в грудной клетке, которая локализуется чаще всего за грудиной и может иррадиировать («отдавать») в левую руку, шею, нижнюю челюсть, в подложечную область (эпигастрий).
Боль возникает при физической нагрузке или воздействии других факторов, повышающих потребность сердца в кислороде, и длится от 1 до 15 минут. Проходит в покое (при прекращении нагрузки) или через 1–3 минуты после приема нитроглицерина.
В переводе с древнегреческого языка стенокардия обозначает «узкое (слабое, тесное) сердце».
Причины появления стенокардии
В основе развития стенокардии лежат три механизма:
- атеросклеротическое поражение коронарных артерий;
- преходящее сосудистое тромбообразование;
- снижение коронарного кровотока из-за спазма или повышения тонуса коронарных артерий.
Стенокардия дает о себе знать во время физической нагрузки или стрессовых ситуаций при наличии сужения просвета коронарной артерии на 50-70%.
Тяжесть стенокардии зависит от степени стеноза коронарных артерий, его локализации и протяженности, количества и числа пораженных артерий. Атеросклеротическая бляшка может перекрывать сосуд полностью или частично. При повышении артериального давления поврежденный атеросклеротическим процессом внутренний слой коронарных артерий (эндотелий) может легко повреждаться, кровь проникает внутрь бляшки, активируется процесс свертывания крови и формируется тромб, который может частично или полностью закупорить сосуд.
Образование тромба, особенно на фоне спазма сосуда, может привести к его полной или частичной закупорке.
При повреждении тканей миокарда высвобождаются медиаторы боли (серотонин, гистамин, брадикинин и др.), которые воздействуют на болевые рецепторы.
Выделяют модифицируемые (те, на которые можно повлиять) и немодифицируемые факторы, которые могут провоцировать развитие стенокардии. К модифицируемым относят дислипопротеидемию (нарушение нормального соотношения липидов крови), артериальную гипертонию, сахарный диабет, курение, низкую физическую активность, ожирение, стресс. Немодифицируемые факторы — мужской пол, возраст, отягощенный семейный анамнез по сердечно-сосудистым заболеваниям (инфаркт миокарда или ишемический инсульт у ближайших родственников — до 65 лет (у женщин) и до 55 лет (у мужчин)).
Классификация заболевания
Наибольшее распространение получила классификация стенокардии, разработанная
на основе рекомендаций экспертов ВОЗ
:
- Стабильная стенокардия напряжения (с указанием функционального класса от I до IV).
- I класс – больной хорошо переносит физические нагрузки, приступы стенокардии возникают только при нагрузках высокой интенсивности; II класс – небольшое ограничение обычной физической активности, приступы стенокардии возникают при ходьбе по ровному месту на расстояние более 500 м, при подъеме более чем на один этаж; III класс – выраженное ограничение обычной физической нагрузки, приступы возникают при ходьбе в нормальном темпе по ровному месту на расстояние 100-150 м, при подъеме на один этаж; IV класс — стенокардия возникает при небольшой физической нагрузке, ходьбе по ровному месту на расстояние менее 100 м.
- Нестабильная стенокардия:
- впервые возникшая стенокардия (давность < 1 месяца с момента появления приступов);
- прогрессирующая стенокардия (нарастание приступов по частоте, длительности, интенсивности с расширением локализации и иррадиации);
- ранняя постинфарктная (в течение 2 недель после перенесенного острого инфаркта миокарда) или постоперационная стенокардия.
- Спонтанная (вазоспастическая, вариантная, Принцметала) стенокардия.
На практике врачи также пользуются клинической классификацией стабильной стенокардии
:
- стенокардия напряжения стабильная (с указанием функционального класса);
- стенокардия вазоспастическая;
- стенокардия микрососудистая.
Симптомы стенокардии
Боль при стенокардии иногда может восприниматься не как истинная боль, а как ощущение дискомфорта, чувство тяжести, сжатия, стеснения, распирания, жжения или нехватки воздуха.
Чаще всего боль локализуется за грудиной или по левому краю грудины. Может иррадиировать в шею, нижнюю челюсть, зубы, межлопаточное пространство, реже – в локтевые или лучезапястные суставы, сосцевидные отростки.
Продолжается боль при стенокардии обычно от 1 до 15 мин.
Возникает боль на пике физической или эмоциональной нагрузки. Стрессовые ситуации за счет повышения активности симпатоадреналовой системы приводят к увеличению частоты сердечных сокращений, повышению артериального давления и сократимости миокарда, а значит, повышается потребность миокарда в кислороде. После приема нитроглицерина или прекращения нагрузки боль купируется, причем болевой приступ быстрее купируется в положении сидя или стоя.
При прогрессировании стенокардии наступает такой момент, когда приступы возникают даже при минимальной нагрузке, а затем и в условиях физического покоя.
Стенокардия покоя присоединяется к стенокардии напряжения и сочетается с ней. В таких случаях приступы возникают во время повышенного потребления кислорода сердечной мышцей, например, во время быстрой фазы сна, когда сокращения сердце начинает биться чаще.
У некоторых пациентов приступ стенокардии может возникнуть в горизонтальном положении из-за увеличенного притока крови к сердцу.
Вазоспастическая стенокардия развивается вне связи с физической и эмоциональной нагрузкой, вызвана спазмом коронарных артерий, обычно встречается в более молодом возрасте, чем стенокардия напряжения на фоне атеросклероза коронарных артерий. У пациентов с вазоспастической стенокардией не удается выявить многие типичные факторы риска атеросклероза. Заболевание может сопровождаться угрожающими нарушениями ритма сердца, приводить к развитию инфаркта миокарда и/или внезапной смерти.
Особенностью вазоспастической стенокардии является очень сильные приступы, обычно локализующиеся в типичном месте. Они случаются ночью или рано утром, а также под воздействием холода на открытые участки тела.
Для микрососудистой стенокардии характерны приступы, возникающие через некоторое время после физической нагрузки, при эмоциональном напряжении и в покое, — они плохо купируются нитроглицерином. Причиной микрососудистой стенокардии считается дисфункция мелких коронарных артерий (100—200 мкм в диаметре) в преартериолярном сегменте коронарного русла. Более чем в 70% случаев микрососудистая стенокардия сосуществует с классической стенокардией у больных с атеросклеротическими стенозами.
Диагностика стенокардии
Диагноз «стенокардия» устанавливается на основании совокупности жалоб (боль, характерная для стенокардии) и полученных от пациента сведений о течении заболевания.
У всех больных с подозрением на ишемическую болезнь сердца уточняются следующие вопросы:
- курение в настоящее время или в прошлом;
- наличие сердечно-сосудистых заболеваний и/или случаев смерти от сердечно-сосудистых заболеваний у ближайших родственников пациента (отца, матери, родных братьев и сестер);
- предыдущие случаи обращения за медицинской помощью и наличие ранее зарегистрированных электрокардиограмм, исследований и заключений;
- наличие сопутствующих заболеваний с целью оценки дополнительных рисков;
- принимаемые в настоящее время лекарственные препараты.
Для уточнения диагноза, имеющихся осложнений применяют данные лабораторных и инструментальных методов обследования.
Всем пациентам с подозрением на стенокардию рекомендуют исследование липидного профиля для выявления дислипопротеидемии:
- триглицериды (Triglycerides);
Лечение МВС
Лечение МВС включает стандартную терапию ИБС: β-адреноблокаторы, нитраты, антагонисты кальция, статины, дезагреганты, препараты второй линии (ингибиторы ангиотензинпревращающего фермента (АПФ), никорандил, ивабрадин, ранолазин, триметазидин), немедикаментозные методы лечения (стимуляция спинного мозга, психотерапия) [37].
Традиционные антиангинальные препараты назначают на первых этапах лечения. Короткодействующие нитраты рекомендуют для купирования ангинозных приступов, но они часто не оказывают эффекта. Так, только менее 50% пациентов отмечали улучшение состояния при использовании сублингвального нитроглицерина. И наоборот, сообщается, что никорандил, открывающий калиевые АТФ-каналы и обладающий нитратоподобным действием, оказывает положительный эффект при МВС [38].
У пациентов с доминирующей симптоматикой стенокардии напряжения рациональной представляется терапия β-адреноблокаторами, которые доказанно устраняют симптомы стенокардии. Это препараты первого выбора, особенно у больных с очевидными признаками повышенной адренергической активности (высокой частотой пульса в покое или при физической нагрузке) [39]. Однако пациентам с микрососудистым или эпикардиальным спазмом следует соблюдать осторожность при использовании β-адреноблокаторов (особенно тех, у которых отсутствуют вазодилатирующие свойства), поскольку эти препараты могут усиливать коронарную вазоконстрикцию, маскируя α-адренорецепторы в коронарных сосудах [37].
Другим препаратом, снижающим потребность миокарда в кислороде благодаря его урежающим частоту сердечных сокращений эффектам, является ивабрадин [40]. Антагонисты кальция как препараты первой линии показаны в случае вариабельности порога стенокардии напряжения, особенно при ангиоспастическом генезе ишемии миокарда. Пациентам с клиникой МВС и нарушениями липидного обмена показаны статины, которые, как известно, положительно влияют на эндотелиальную функцию. Ингибиторы АПФ улучшают переносимость физической нагрузки и облегчают симптомы стенокардии [41]. Известно положительное влияние ранолазина на эндотелиальную функцию. В работе E. Rayner-Hartley et al. [42] оценивалось влияние ранолазина на качество жизни пациентов с тяжелой рефрактерной стенокардией, вызванной МВС. Пациенты получали ранолазин в дозе 1000 мг/сут совместно с сулодексидом в течение 4 нед. Применение ранолазина позволило улучшить качество жизни и уменьшить количество обращений за медицинской помощью. С целью коррекции эндотелиальной дисфункции также применяется триметазидин, улучшающий метаболизм кардиомиоцитов при ишемии миокарда. В исследовании С.А. Болдуевой и соавт. [43] показана эффективность применения у больных МВС, помимо стандартной антиангинальной терапии, триметазидина с улучшением клинической картины, качества жизни, перфузии миокарда и функции эндотелия.
К сожалению, традиционная терапия МВС не всегда эффективна, качество жизни из-за болевого синдрома остается низким, пациентов часто госпитализируют. Поэтому всем пациентам с МВС необходима активная коррекция традиционных факторов риска, таких как гипертония, сахарный диабет, курение, ожирение, малоподвижный образ жизни, гиперлипидемия.
Синдром Х в кардиологии («микроваскулярная стенокардия»)
Приблизительно у 10–20% больных, которым проводится диагностическая коронарография в связи с острым или хроническим кардиальным ишемическим синдромом, коронарные артерии оказываются интактными. Если даже предположить, что у части из них симптомы ишемии могут быть обусловлены другими кардиальными и некардиальными причинами, то, по крайней мере, у одного из десяти больных с наличием типичной стенокардии отсутствуют гемодинамически значимые стенозы коронарных артерий. Наличие типичной стенокардии при неизмененных коронарных артериях впервые описал Н. Kemp в 1973 году [1]. Этот синдром получил название «синдром Х (икс)».
Кардиальный синдром Х – это патологическое состояние, характеризующееся наличием признаков ишемии миокарда на фоне отсутствия атеросклероза коронарных артерий и спазма эпикардиальных венечных артерий на коронарографии (признаки ишемии миокарда: типичных приступов стенокардии и депрессии сегмента ST ≥ 1,5 мм (0,15 мВ) продолжительностью более 1 минуты, установленной при 48-часовом мониторировании ЭКГ). Таким образом, кардиальный синдром Х диагностируется у больных:
• с типичными загрудинными болями;
• с положительными нагрузочными тестами;
• с ангиографически нормальными эпикардиальными коронарными артериями и отсутствием клинических или ангиографических доказательств наличия спазма коронарных артерий;
• с отсутствием системной артериальной гипертонии с гипертрофией левого желудочка и без нее, а также с отсутствием нарушений систолической функции левого желудочка в покое.
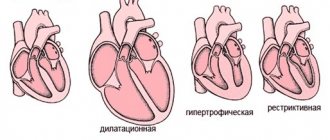
В редких случаях у больных с синдромом Х возникает блокада левой ножки пучка Гиса с последующим развитием дилатационной кардиомиопатии. Следует обратить внимание на то, что при отсутствии изменений в коронарных артериях при ангиографии часто имеется окклюзионная патология дистальных сосудов (микроваскулярная стенокардия).
Некоторые авторы используют термин «микроваскулярная стенокардия», подразумевая под этим наличие у больных с типичной стенокардией нормальной коронарограммы и сниженного коронарного резерва.
Синдром Х обычно относят к одной из клинических форм ИБС, поскольку понятие «ишемия миокарда»’ включает все случаи дисбаланса поступления кислорода и потребности миокарда в нем, независимо от причин, его вызывающих.
Следует отметить, что возможности метода ангиографии при оценке состояния коронарного русла, в частности, микрососудистого, ограничены. Поэтому понятие «ангиографически неизмененные коронарные артерии» весьма условно и свидетельствует только об отсутствии суживающих просвет сосудов атеросклеротических бляшек в эпикардиальных коронарных артериях. Анатомические особенности мелких коронарных артерий остаются «ангиографически невидимыми». Причины кардиального синдрома Х:
Этиология кардиального синдрома Х остается до конца не выясненной и установлены лишь некоторые патофизиологические механизмы, приводящие к развитию типичных клинико–инструментальных проявлений заболевания:
• увеличенная симпатическая активация; • дисфункция эндотелия; • структурные изменения на уровне микроциркуляции; • изменения метаболизма (гиперкалиемия, гиперинсулинемия, «окислительный стресс» и др.); • повышенная чувствительность к внутрисердечной боли; • хроническое воспаление; • повышенная жесткость артерий и др.
Существует ряд гипотез, которые определяют патогенез синдрома Х. Согласно первой из них болезнь обусловлена ишемией миокарда вследствие функциональных или анатомических нарушений микроциркуляции в интрамускулярных (интрамуральных) преартериолах и артериолах, т.е. в сосудах, которые не могут быть визуализированы при коронароангиографии. Вторая гипотеза предполагает наличие метаболических нарушений, приводящих к нарушению синтеза энергетических субстратов в сердечной мышце. Третья гипотеза предполагает, что синдром Х возникает при повышении чувствительности к болевым стимулам (снижение болевого порога на уровне таламуса) от различных органов, включая сердце.
Несмотря на интенсивные исследования в последние 35 лет относительно патогенеза коронарного синдрома Х, многие важные вопросы остаются без ответа.
Среди больных с кардиальным синдромом Х преобладают лица среднего возраста, в основном женщины. Менее чем у 50% больных с кардиальным синдромом Х наблюдается типичная стенокардия напряжения, у большей части – болевой синдром в груди атипичен.Симптомы кардиального синдрома Х:
В качестве основной жалобы фигурируют эпизоды болей за грудиной стенокардитического характера, возникающих во время физической нагрузки или провоцирующихся холодом, эмоциональным напряжением; с типичной иррадиацией в ряде случаев боли более продолжительные, чем при ИБС, и не всегда купируются приемом нитроглицерина (у большинства больных препарат ухудшает состояние). Сопутствующие кардиальному синдрому Х симптомы напоминают вегето-сосудистую дистонию. Нередко кардиальный синдром Х обнаруживают у людей мнительных, с высоким уровнем тревожности, на фоне депрессивных и фобических расстройств. Подозрение на эти состояния требует консультации у психиатра. В качестве диагностических критериев кардиального синдрома Х выделяются: • типичная боль в грудной клетке и значительная депрессия сегмента ST при физической нагрузке (в том числе на тредмиле и велоэргометре); • преходящая ишемическая депресси сегмента ST ≥ 1,5 мм (0,15 мВ) продолжительностью более 1 минуты при 48-часовом мониторировании ЭКГ; положительная дипиридамоловая проба; • положительная эргометриновая (эрготавиновая) проба, снижение сердечного выброса на ее фоне; • отсутствие атеросклероза коронарных артерий при коронароангиографии; • повышенное содержание лактата в период ишемии при анализе крови из зоны коронарного синуса; • ишемические нарушения при нагрузочной сцинтиграфии миокарда с 201 Tl.
Синдром Х напоминает стабильную стенокардию. Однако клинические проявления у больных с синдромом Х весьма вариабельные, а помимо стенокардии напряжения могут наблюдаться и приступы стенокардии покоя.
При диагностике кардиального синдрома Х также должны быть исключены: • пациенты со спазмом коронарных артерий (вазоспастическая стенокардия), • пациенты, у которых объективными методами документированы внесердечные причины болей в грудной клетке, например:
— мышечно-костные причины (остеохондроз шейного отдела позвоночника и др.); — нервно-психические причины (тревожно–депрессивный синдром и др.); — желудочно-кишечные причины (спазм пищевода, желудочно–пищеводный рефлюкс, язва желудка или двенадцатиперстной кишки, холецистит, панкреатит и др.); — легочные причины (пневмония, туберкулезный процесс в легких, плевральные наложения и др.); — латентно протекающие инфекции (сифилис) и ревматологические заболевания.
Лечение кардиального синдрома Х:
Лечение группы больных с синдромом Х остается до конца не разработанным. Выбор лечения часто затруднен как для лечащих врачей, так и для самих больных. Успешность лечения обычно зависит от идентификации патологического механизма заболевания и в конечном итоге определяется участием самого пациента. Часто необходим комплексный подход к лечению больных с кардиальным синдромом Х.
Существуют различные подходы к медикаментозному лечению: антиангинальные препараты, ингибиторы АПФ, антагонисты рецепторов ангиотензина II, статины, психотропные препараты и др. Антиангинальные препараты, такие как антагонисты кальция (нифедипин, дилтиазем, верапамил, амлодипин) и β–адренергические блокаторы (атенолол, метопролол, бисопролол, небиволол и др.) необходимы больным с документированной ишемией миокарда или с нарушенной миокардиальной перфузией. Сублингвальные нитраты эффективны у 50% больных с кардиальным синдромом Х. Имеются доказательства в отношении эффективности никорандила, обладающего брадикардическим эффектом, α1–адреноблокатора празозина, L–аргинина, ингибиторов АПФ (периндоприла и эналаприла), цитопротекторов (триметазидина).
Общие советы по изменению качества жизни и лечению факторов риска, особенно проведение агрессивной липидснижающей терапии статинами (снижение общего холестерина до 4,5 ммоль/л, холестерина ЛПНП менее 2,5 ммоль/л), должны рассматриваться в качестве жизненно необходимых компонентов при любой выбранной стратегии лечения.
Физические тренировки. При кардиальном синдроме Х снижается толерантность к физическим нагрузкам, наблюдается физическая детренированность и неспособность выполнять нагрузку из–за низкого болевого порога. Физические тренировки увеличивают болевой порог, нормализуют эндотелиальную функцию и «отодвигают» появление боли при нагрузке у этой категории больных.
Прогноз.
Прогноз больных с кардиальным синдромом «Х», как правило, благоприятный. Осложнения, характерные для больных ИБС со стенозирующим атеросклерозом коронарных артерий (в частности, инфаркт миокарда), встречаются крайне редко. Выживаемость при длительном наблюдении составляет 95–97%, однако у большей части больных повторные приступы стенокардии на протяжении многих лет отрицательно влияют на качество жизни. Если кардиальный синдром Х не связан с увеличением смертности или с увеличением риска кардиоваскулярных «событий», то он часто серьезно ухудшает качество жизни пациентов и представляет существенную нагрузку для системы здравоохранения. Необходимо подчеркнуть, что прогноз благоприятный при отсутствии эндотелиальной дисфункции. В этих случаях пациента следует информировать о доброкачественном течении заболевания. При исключении больных с блокадой левой ножки пучка Гиса и пациентов с вторичной микроваскулярной стенокардией вследствие серьезных системных заболеваний, таких как амилоидоз или миеломная болезнь, прогноз больных с кардиальным синдромом Х благоприятный как в отношении выживаемости, так и сохранения функции левого желудочка, однако у некоторых пациентов клинические проявления заболевания сохраняются достаточно долго.