Вегетососудистая дистония — это патологическое состояние, при котором нарушается работа вегетативной нервной системы. У пациентов с этим синдромом часто диагностируются изменения со стороны сердечно-сосудистой системы, что проявляется в том числе периодическими приступами тахикардии. У больного возрастает частота сердечных сокращений до 90 ударов в минуту и более, также возникают слабость и головокружение, ощущение страха и тревоги. Однако в большинстве случаев все симптомы проходят еще до приезда медиков, при этом они исчезают так же внезапно, как и начинаются. Лечение основано на поддержании здорового образа жизни, контроля за психологическим состоянием пациента, а также на периодическом приеме препаратов.
Физиологические аспекты вегетососудистой дистонии
Вегетососудистая дистония — это распространенный диагноз. В норме сердце работает как автономный механизм, постоянно обеспечивая ток крови по сосудам. Частота, сила и ритм сердечных сокращений регулируются проводящей системой миокарда, железами внутренней секреции и вегетативной нервной системой. В комплексе эти механизмы обеспечивают правильную работу сердечной мышцы как в состоянии покоя, так и в условиях физических нагрузок.
Вегетативная нервная система подразделяется на симпатический и парасимпатический отделы. При возбуждении первого частота пульса увеличивается, второго — уменьшается. Тахикардия при ВСД связана с чрезмерной активацией симпатической нервной системы и одновременно угнетением парасимпатической, в результате чего баланс нарушается.
СПРАВКА! На работу сердца влияют в том числе внешние факторы. Так, в условиях гипоксии и после нагрузок незначительное ускорение пульса считается нормальным. О тахикардии, которую нужно устранять медикаментозным способом, свидетельствует учащенный, до 90 ударов в минуту, пульс в состоянии полного покоя.
Особенности лечения и оказание первой помощи
Выявив симптомы тахикардии, возникшей при ВСД, больному необходимо обратиться к врачу-кардиологу. Специалист назначит ряд обследований для исключения прочих заболеваний. После постановки диагноза схема терапии составляется на основе течения болезни. Преимущественно в нее входят медикаменты, сеансы психотерапии и средства народной медицины.
Если приступ уже начался, то необходимо запомнить нижеприведенный алгоритм действий:
- отложить выполняемую работу;
- постараться успокоиться и не думать о плохом;
- найти хорошо проветриваемое помещение;
- прилечь, положив на лоб холодный предмет.
Для более быстрого избавления от пароксизма подойдут следующие методики:
- делать быстрые глубокие вдохи, и в 2 раза медленнее выдыхать;
- задержать дыхание, держа в напряжении мышцы пресса;
- слегка надавить пальцем на корень языка для вызова рвоты;
- подержать голову под струей холодной воды;
- надавить с применением силы на угол нижней челюсти;
- использовать седативные капли («Валерьянки», «Корвалола);
При нехватке воздуха рекомендуется подышать 10 минут в бумажный пакет. Если бороться с приступом не получается и он прогрессирует, то необходимо вызвать скорую помощь.
Медикаментозный курс лечения
Медикаментозное лечение тахикардии при ВСД заключается в приеме эффективных седативных и антиаритмических препаратов. Ознакомиться с их особенностями можно ниже:
- Таблетки, созданные на основе трав с успокоительным эффектом (боярышник, пустырник, валерьяны, перечная мята, мелисса), недорогие и общедоступные. Оказанное ими воздействие способствует снижению нервного напряжения инормализации пульса и кровяного давления. Преимущество подобных медикаментов в малом количестве противопоказаний и побочных эффектов, благодаря чему их применяют длительное время. Приобрести препараты на растительной основе можно в любой аптеке без рецепта врача.
- Медикаменты с седативным воздействием, сделанные из химических соединений, более эффективны(«Реланум», «Празепам»). Врачи рекомендуют применять подобные средства при частом пребывании в стрессовых ситуациях. Они обладают обширным списком побочных реакций, но оказывают выраженное успокаивающее действие, благодаря которому снижается частота сердечных сокращений и стабилизируется давление. Большинство видов подобных таблеток выписывается по рецепту.
- Препараты с антиаритмическим эффектом используют в качестве средства устранения тахикардии. Они стабилизируют сердечный ритм и предотвращают появление рецидивов. Минусом данных лекарств является большое количество противопоказаний
Медикаменты из выше озвученных групп назначает лечащий врач, ориентируясь на течение болезни. Как избавиться от тахикардии при ВСД с помощью антиаритмических средств? Помогут следующие группы:
- Бета-адреноблокаторы снижают степень воздействия адреналина на сердечную мышцу путем блокирования его рецепторов. Они бывают кардиоселективные («Бетакард»,«Бетофтан», «Корбис») и неселективные («Обзидан», «Соталол», «Ниолол»). Медикаменты из первой группы воздействуют на бета-1 адренорецепторы, которые находятся в сердечной мышце.Их блокировкаспособствует падению кровяного давления и уменьшению частоты пульса. Неселективные препараты влияют на бета-1 и 2 адренорецепторы. Оказываемое воздействие схоже с первой группой. Минусом данных таблеток является повышенный риск развития бронхоспазма. При ВСД можно ограничиться кардиоселективными блокаторами, так как бета-2 рецепторы локализованы в бронхах, затрагивать их нет нужды.
- Блокаторы каналов калия не дают элементу попадать в клетки сердца, вследствие чего замедляется электрическая активность, падает давление и снижается выраженность тахикардии. Наиболее актуальным среди них является «Амиодарон». У препарата небольшое количество противопоказаний, его с успехом применяют для лечения аритмии и высокого давления в сочетании с сердечной недостаточностью. Минусом лекарственного средства является высокий риск развития побочных реакций (слабость, снижение остроты зрения, дисфункции щитовидной железы) при длительном применении.
Назначаются лекарства с антиаритмическим эффектом не для устранения причины сбоя, а с целью купирования тахикардии и предотвращения развития осложнений. Помочь снизить нервное напряжение и улучшить работу сердца могут нижеприведенные средства:
- Ноотропные медикаменты («Пирацетам», «Пантогам», «Фенибут») используются, чтобы повысить устойчивость больного к стрессовым ситуациям, физическим и умственным перегрузкам и прочим внешним факторам. Их прием позволит улучшить когнитивные способности и восстановить баланс между симпатическим и парасимпатическим отделом, что приведет к устранению причины тахикардии.
- Транквилизаторы дневного типа («Празепам», «Триметозин», «Гидазепам»)прекрасно справляются с приступами паники и необоснованного страха. После их приема улучшается сон и снижается нервная возбудимость. В отличие от простых транквилизаторов, у медикаментов из данной подгруппы более выражен противотревожный эффект и менее успокаивающий и снотворный. Больные имеют возможность принимать лекарство днем и заниматься повседневной работой без причиняющей дискомфорт сонливости. За счет снижения напряжения с нервной системы уменьшается влияние симпатического отдела и устраняется тахикардия.
Частые пароксизмы тахикардии постепенно истощают сердце. Для предотвращения развития осложнений врачи советуют комбинировать седативные и антиаритмические средства с витаминными комплексами:
- «Аскорутин» богат аскорбиновой кислотой и рутином. Его рекомендуют применять для нормализации обменных процессов, укрепления стенок сосудов и иммунной системы.
- «Направит» содержит большую концентрацию витаминов группы В, магния, калия и прочих элементов жизненно важных для стабильной работы сердца и нервной системы. Если принимать таблетки в течение длительного времени, то можно остановить развитие атеросклероза и осложнений, спровоцированных тахикардией.
- «Аспаркам» ценится за большое количество калия и магния в своем составе. Врачи рекомендуют препарат для устранения аритмии, улучшения сердечной проходимости и стабилизации электролитного баланса. Для повышения эффективности его можно комбинировать с антиаритмическими препаратами.
Психотерапия
Тахикардия, возникшая из-за вегетососудистой дистонии, эффективно устраняется путем лечения проблем психического характера. Поможет решить проблему психотерапия. Суть ее заключается в улучшении эмоционального состояния и повышении сопротивляемости пациента к стрессам для предотвращения приступов. Проводит сеансы опытный психотерапевт.
Стабилизация состояния наблюдается не ранее 5 посещения врача. Всего желательно пройти не менее 10 сеансов, чтобы специалист смог снизить воздействие факторов, влияющих на психику больного. В запущенных случаях для улучшения лечебного эффекта сочетают психотерапию с медикаментами, обладающими седативным, антиаритмическим и противотревожным действием.
Физиотерапия
Устранить нервное напряжение, которое часто является причиной развития ВСД, можно с помощью методов физиотерапии:
- иглорефлексотерапии;
- электрофареза;
- упражнений на дыхательном аппарате;
- массажа спины;
- целебных ванн;
- магнитнолазерной терапии.
Народная медицина
Учащение ритма сердца, возникшее по вине вегетососудистой дистонии, можно купировать, используя методы народной медицины. Они фактически не вызывают побочных реакций и имеют минимальное количество противопоказаний, поэтому востребованы при лечении многих патологий. Перечень наиболее эффективных рецептов расположен ниже:
- Чай каркаде представляет собой ароматный напиток, приготовленный из суданской розы. Он обладает выраженным успокоительным эффектом, за счет которого уменьшается частота сердечных сокращений. Готовиться отвар путем заливания 2 бутонов 1 стаканом кипятка. Пить его допускается по 1-2 чашки каждый день.
- Сборы целебных трав продаются фактически в любой аптеке. Они оказывают седативное, гипотензивное и сосудорасширяющее воздействие. Сделать лекарство можно самостоятельно, собрав в необходимом количестве все ингредиенты. Для приготовления отвара потребуется залить 50 г сбора 450 мл кипятка. Принимать его по 50 мл 5 раз в день не более 1 месяца.
- Хвоя богата фитонцидами, которые способствуют снижению давления и устранению аритмии за счет уменьшения частоты сердечных сокращений. После пройденного курса терапии у больных пропадает бессонница и повышается устойчивость к стрессам. Добавлять хвою можно в виде масел (можжевельника, сосны) в ванну.
- Можжевельник стабилизирует работу сердца и снимает нервное напряжение. Достаточно в сутки есть по 1 ягоде, увеличивая дозировку на 1 шт. каждый день. Через 2 недели принимать в обратном порядке. Продолжать лечение на протяжении 28 дней.
- Отвар боярышника позволяет снизить интенсивность проявлений ВСД, уменьшив артериальное давление и частоту сердечных сокращений. Для приготовления достаточно смешать 30 г плодов растения с 1 стаканом кипятка. Затем оставить лекарство настаиваться. Через 20 минут его можно пить утром и вечером по ½ чашки.
- Мед является ценным источником витаминов группы В и прочих полезных веществ. Его можно добавить в стакан с молоком в количестве 25-30 мл для получения хорошего лекарства с седативным эффектом. Выпить его лучше всего перед сном.
Профилактика
Соблюдение правил профилактики позволит предотвратить развитие дальнейших приступов тахикардии и улучшит общее состояние. Их перечень расположен ниже:
- уделять сну не мене 7-8 часов в день;
- периодически делать 5-и минутные перерывы на работе;
- подкорректировать ежедневное меню;
- стараться избегать конфликтов;
- применять методики самовнушения;
- заниматься спортом.
Тахикардия, проявившаяся на фоне ВСД, встречается достаточно часто, особенно при наличии сбоев в нервной и эндокринной системе. Ее синусовая разновидность не требует особого лечения, но более серьезные формы необходимо сразу выявлять, чтобы они не привели к развитию тяжелых осложнений. Снизить аритмию можно медикаментами, народными средствами и сеансами психотерапии. Подбирать курс лечения должен врач, ориентируясь на основную причину сбоя в вегетативном отделе нервной системы.
Тахикардия — определение и классификация
Тахикардия — это увеличение частоты сердечных сокращений. В норме этот показатель составляет 60-90 ударов в минуту, но может варьировать в зависимости от многих факторов. Так, высокому человеку либо при наличии избыточного веса необходимо большее количество кислорода и питательных веществ, поэтому сердце будет биться чаще. Также пульс увеличивается после интенсивных нагрузок и в жаркое время года, в помещениях с недостаточной вентиляцией. Патологической тахикардией считается учащение пульса без видимой причины, которое сопровождается дополнительными признаками.
Существует несколько классификаций тахикардии при ВСД. Первая из них выделяет несколько разновидностей синдрома в зависимости от причины его возникновения:
- интракардиальная — развивается вследствие нарушений сердечной деятельности;
- экстракардиальная — учащенный пульс является симптомом патологий, не связанных непосредственно с работой сердца.
Также необходимо различать основные виды тахикардии в зависимости от локализации очага, в котором возникает импульс:
- пароксизмальная (эктопическая) — может быть желудочковой, если импульс берет начало в области желудочков, либо наджелудочковой, если он возникает в предсердиях;
- синусовая — импульс происходит непосредственно из синусового узла.
При вегетососудистой дистонии характерна экстракардиальная тахикардия, то есть ускорение пульса не свидетельствует о патологиях со стороны сердечно-сосудистой системы. Выделяют также несколько вариантов проявления этого синдрома:
- одиночные приступы, при которых частота пульса может достигать до 120-240 ударов в минуту, но показатели быстро нормализуются;
- постоянная тахикардия — в состоянии покоя частота сокращения сердца в минуту составляет 90-120 ударов, а симптомы могут оставаться незамеченными в течение длительного времени;
- синусовая — частое повышение показателей пульса до 120—130 ударов в минуту.
При отсутствии лечения тахикардия при ВСД опасна, несмотря на то, что органические повреждения сердца отсутствуют. Увеличение нагрузки на миокард со временем может приводить к прогрессирующей гипоксии (ишемическая болезнь сердца), а также становиться причиной инфаркта либо инсульта.
При учащении пульса часто возникают панические атаки, но стоит помнить, что даже значительная тахикардия, обусловленная ВСД, безопасна для здоровья
Состояние сердечно-сосудистой системы при патологии верхнего отдела желудочно-кишечного тракта
Болезни органов пищеварения занимают важное место в структуре общей заболеваемости, представляя собой важную экономическую, социальную и медицинскую проблему. Результаты эпидемиологических исследований свидетельствуют об изменении структуры основных заболеваний верхнего отдела пищеварительного тракта: констатируется снижение частоты язвенной болезни и увеличение числа больных гастроэзофагеальной рефлюксной болезнью (ГЭРБ) в мире. В настоящее время ГЭРБ признана лидирующим по частоте заболеванием в гастроэнтерологии.
В последние годы все большее внимание уделяется «внепищеводным» проявлениям ГЭРБ, в том числе кардиальным. Кардиальные проявления ГЭРБ представляют наибольший интерес как с научной, так и практической точки зрения. Они могут быть в виде болей в груди, не связанных с ишемической болезнью сердца (ИБС) (так называемые «некардиальные боли в груди», noncardiac chest pain) и нарушениями ритма и проводимости сердца. На основании клинических исследований предполагается, что ГЭРБ является второй по частоте (после ИБС) причиной болей в груди, хотя реальная частота их в разных популяциях не известна. Такие боли в груди требуют дифференциальной диагностики с ишемической болезнью сердца с использованием затратных и инвазивных технологий. Так, ежегодно практически 600 тыс. американцам делают коронарную ангиографию по поводу загрудинных болей, при этом у 10–30% обследованных не обнаруживают значимых изменений. Сходные данные (30%) приводят и отечественные авторы (В. А. Кузнецов и соавт., 2000). Своевременная диагностика пищеводной причины болей в груди имеет как экономический, так и социальный аспекты. Дело в том, что диагностика ГЭРБ часто осуществляется только на основании эндоскопических методов исследования. Это в корне неправильно, так как в 60% случаев ГЭРБ протекает как эндоскопически негативный вариант (когда эндоскопист описывает нормальный пищевод, а рефлюкс может быть очень выраженным), но именно при этом варианте чаще наблюдается атипичная (кардиальная) симптоматика, существенно нарушающая качество жизни больных. В то же время у людей пожилого возраста ГЭРБ может сочетаться с ИБС (частота сочетаний и сопутствующих условий требует изучения). В этом случае вычленение пищеводного компонента боли и его грамотная коррекция резко облегчают течение ИБС и, соответственно, качество жизни больных.
Несмотря на то что за последние 20 лет значительно увеличилось число работ, посвященных гастроэзофагеальной рефлюксной болезни, количество исследований по «кардиальным» проявлениям ГЭРБ остается небольшим, а изучению аритмических аспектов ГЭРБ не уделяется должного внимания. Все указанное выше явилось предпосылкой для изучения характера поражений сердечно-сосудистой системы при патологии пищевода и кардии.
Взаимодействие между ЖКТ и ССС представляет несомненный интерес. Близость расположения с сердцем, общность иннервации способны при переполнении желудка, патологии пищевода по типу висцеро-висцеральных рефлексов провоцировать аритмии, имитировать ИБС. Патология верхнего отдела ЖКТ может приводить к функциональным расстройствам сердечно-сосудистой системы, возникающим опосредованно через ВНС. Большинство клинических проявлений ВСД, включая изменения синусового ритма и отчасти эктопические аритмии, зависит от дисбаланса вегетативных влияний. Так, не вызывает сомнения значительная роль нейровегетативных влияний на сердце, способствующих при их дисбалансе возникновению и поддержанию пароксизмальной фибрилляции предсердий (S. H. Hohnloser, A. van de Loo, M. Zabel 1994; P. Coumel 1992; Ю. Р. Шейх-Заде, 1990; Н. П. Потапова, Г. Г. Иванов, Н. А. Буланова, 1997; С. Г. Канорский, В. В. Сибицкий, 1999).
Далеко не последнюю роль в возникновении дисрегуляции ВНС занимают заболевания ЖКТ. Ю. В. Нявяраускус (диссер., 1987 г.) описал повышение тонуса парасимпатической НС, совпадающее с обострениями хронических заболеваний внутренних органов (желчнокаменная болезнь, грыжа пищеводного отверстия диафрагмы (ГПОД), ЯБ). Это дает основание полагать, что первичные заболевания внутренних органов у таких больных являлись главными этиопатогенетическими факторами, способствующими развитию вегетативной дисфункции синусового узла (ВДСУ).
Всего нами обследовано 99 пациентов, из них: первая группа — 35 пациентов с патологией пищевода и кардии (ГЭРБ и/или ГПОД); вторая группа — 31 человек с сочетанием ГЭРБ и/или ГПОД с ЯБ; третья группа — 33 пациента с ЯБ (условная группа сравнения). Средний возраст составил 37,0±10,1 лет.
В нашем исследовании в качестве группы сравнения были выбраны больные ЯБ.
ЯБ считается наиболее ярким примером психосоматических заболеваний в связи с тем, что изменения со стороны вегетативной нервной системы играют значимую роль как в возникновении самой болезни, так и ее клиническом течении. Вегетативные нарушения встречаются у 75–82% больных ЯБ (А. М. Вейн). При этом изменения ВНС выступают в качестве механизма, через который реализуются психосоматические взаимодействия.
Всем больным было проведено полное клиническое и инструментальное обследование в период обострения и через 6–8 нед после стандартной терапии основного заболевания.
Состояние слизистой оболочки пищевода оценивалось по модифицированной классификации M. Savary & G. Miller (1994) с учетом протяженности воспалительных изменений слизистой оболочки пищевода.
При полипозиционном рентгеноскопическом обследовании c контрастированием (cульфат бария) диагностировали грыжу пищеводного отверстия диафрагмы, устанавливали ее размеры и характер согласно классификации В. Х. Василенко и А. Л. Гребенева (1978), а также исключали осложненные формы болезни (стриктуры, язвы, опухоли).
Для верификации ГЭРБ всем больным проводили 24-часовое мониторирование рН пищевода и желудка с помощью аппарата «Гастроскан-24» (НПО «Исток», Фрязино, Московская область).
Ультразвуковое исследование сердца (UltraMark-9, Канада) позволяло исключить клапанную патологию, множественные добавочные хорды, гемодинамически значимый пролапс клапанов, рубцовые изменения сердечной ткани, признаки сердечной недостаточности.
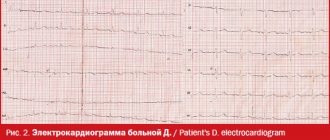
Проводили количественный и качественный анализ стандартной ЭКГ, при суточном мониторировании ЭКГ (Brentwood Holter System, Канада) оценивали качественные показатели ЭКГ и характеристики вариабельности сердечного ритма.
Для уточнения функционального состояния синусового узла и проводящей системы сердца, выявления и идентификации нарушений сердечного ритма проводили неинвазивное чреспищеводное электрофизиологическое исследование (ЭФИ) сердца с помощью аппарата «Элкарт» (Томск, Россия).
Состояние ВНС определяли по стандартизованному опроснику А. М. Вейна (1985) «Вопросник для выявления признаков вегетативных изменений». Каждый симптом оценивали по пятибалльной системе, устанавливали преобладание симпатических или парасимпатических влияний. Кроме того, оценивали вегетативные индексы Кердо, Хильдебранта, минутный объем крови (МОК).
Из 68 больных с патологией пищевода и кардии 89,7% предъявляли жалобы на изжогу, 51,5% — эпигастральный дискомфорт, 66,2% — боли в эпигастрии. Наличие загрудинных болей отметили 20,6%; ощущение «комка в горле» — 7,4%; сердцебиение и перебои в работе сердца — 10,3% обследованных. По данным эндоскопического исследования, рефлюкс-эзофагит (РЭ) 0 стадии выявлен у 22,1% больных, I стадии —у 42,6%, II стадии — у 35,3%. ГПОД рентгенологически диагностирована у 28 человек, в большинстве случаев кардиоэзофагеальная (92,9%) и нефиксированная (60,7%).
Успешность проведенной терапии оценивали по данным суточной рН-метрии и эндоскопии. Достоверных межгрупповых отличий в показателях суточной рН-метрии пищевода у больных основных групп не было выявлено.
Необходимо отметить, что 11 больным проведено одномоментное суточное мониторирование рН и ЭКГ. Цель исследования — проведение дифференциальной диагностики эзофагеальной псевдокоронарной боли от других возможных причин, установить индекс симптома, т. е. совпадение кардиальных симптомов (загрудинных болей, перебоев) с эпизодами ГЭР по данным суточной рН-метрии.
В 81,8% случаев эпизоды загрудинных болей ассоциировались с ГЭР и не сопровождались изменениями на ЭКГ. Положительный симптоматический индекс был отмечен у 63,6% пациентов.
В процессе лечения улучшилась эндоскопическая картина: уменьшилась доля эрозивных поражений пищевода РЭ II стадии с 35,3 до 2,9% и РЭ I стадии с 42,6 до 27,9%.
Исходно нормальная ЭКГ регистрировалась от 16 до 24% обследованных. Нарушения функции автоматизма определялись у 25,7–38,7% обследованных; нарушение проводимости — от 15 до 23% и сочетание этих 2 нарушений — у 13–23%, достоверно не отличаясь в отдельных группах.
При сравнении качественных показателей ЭКГ с помощью критерия Пирсона достоверные межгрупповые отличия отмечены только для нарушения внутрижелудочковой проводимости (НВЖП): наличие ГЭРБ увеличивало ее частоту по сравнению с больными язвенной болезнью (χІ = 6,171; р = 0,013). Это касалось как «чистой» ГЭРБ, так и ее комбинаций с ГПОД и ЯБ (χІ = 6,467; р = 0,011; χІ = 4,728; р = 0,03 соответственно).
Эктопическая активность, выявлявшаяся в среднем в 6% случаев на стандартной ЭКГ, фиксировалась значительно чаще при холтеровском мониторировании (ХМ) ЭКГ. При этом эктопическая активность при сочетании ГЭРБ и ЯБ оказалась выше, чем при изолированной ЯБ (χІ = 5,295; р = 0,021) за счет СВ экстрасистолии (χІ = 4,28; р = 0,039). По данным ХМ, отмечен прирост частоты сердечных сокращений (ЧСС) (минимальной, максимальной, средней; не более чем на 7%) после курса лечения. Значимых межгрупповых отличий не получено. С учетом качественных параметров ЭКГ и ХМ можно сделать вывод, что нарушения внутрижелудочковой проводимости встречались достоверно чаще у пациентов с рефлюкской болезнью и при ее сочетании с ЯБ в сопоставлении с группой сравнения. Кроме того, эктопическая активность, в том числе и суправентрикулярная экстрасистолия, была более характерна для больных ЯБ и РБ. При этом у лиц с эктопической активностью по сравнению без таковой не было достоверных отличий в ЭФИ-показателях (хотя только у больных первой и второй группы были больные с высокой точкой Венкебаха) и вегетативном тонусе, в то время как отмечена разница в некоторых спектральных параметрах. Так, для максимальной ЧСС F = 6,911 (р = 0,011); LF F = 4,102 (р = 0,047); SDNN F = 4,288 (р = 0,042). Можно предположить, что повышенная эктопическая активность у больных ГЭРБ связана с одновременным повышением симпатических и парасимпатических влияний на сердце, что не противоречит литературным данным, так как такие изменения вариабельности сердечного ритма (ВСР) считаются потенциально неблагоприятными. Наиболее аритмогенна ситуация с одновременным повышением симпатического и парасимпатического тонуса ВНС (R. D. Riley, E. L. Pritchett, 1997).
Существуют эпидемиологические работы, посвященные изучению частоты нарушений ритма и проводимости сердца. Так, Н. Г. Гоголашвили провел обследование 673 коренных жителей Республики Саха (82,1% жителей 5 типичных поселков). По данным стандартной ЭКГ, номотопные аритмии наблюдались у 49,9%; гетеротопии — у 6,7% обследованных; нарушения проводимости сердца — 9,5%; блокады сердца — 6,9%. Частота аритмий и нарушений проводимости в якутской популяции была следующей: синусовая аритмия — 33,9%; синусовая брадикардия — 12,8%; синусовая тахикардия —3,2%; АВБ — 3,9%; САБ — 0,2%; блокады правой ножки пучка Гиса (полная и неполная встречались в равной степени); желудочковая экстрасистолия (1-2 градации) — 4,2%; наджелудочковая экстрасистолия — 2,7%; мерцательная аритмия — 0,9%. Все случаи мерцательной аритмии изучались в возрасте 40 лет и старше. У 42,2% обследованных с гетеротопными нарушениями ритма сердца выявить заболевание сердца не удалось. У мужчин в возрасте от 16 до 39 лет сердечно-сосудистые заболевания вообще не выявлялись. ХМ было проведено методом случайной выборки у 174 человек. При ХМ, так же как и в нашем исследовании, наблюдалось увеличение гетеротопной активности: так, желудочковая экстрасистолия отмечена у 37,6% и наджелудочковая у 34,9%. Реже всего выявлялась пароксизмальная тахикардия (1,4% случаев) и мерцательная аритмия (1,4% случаев). Для диагностики ДСУ 46 пациентам была проведена чреспищеводная электрокардиостимуляция. Вегетативная дисфункция наблюдалась у 1,9%; синдром слабости синусового узла у 0,7% обследованных. По данным НИИ терапии СО РАМН, при изучении распространенности ЭКГ-изменений в неорганизованной популяции г. Новосибирска (1563 мужчин и 1550 женщин в возрасте 25–64 лет) нарушения АВ-проводимости регистрировались у 1,9% мужчин и 1,7% женщин; НВЖП — у 4,3% мужчин и у 2,2% женщин; полная блокада левой ножки пучка Гиса — 0,1%; аритмии у 7,2% мужчин и у 3,5% женщин; изменения зубца Т — 4,9% и 6,2% соответственно.
Для оценки функции синусового и атривентрикулярного (АВ) узлов было проведено ЭФИ сердца. Исходные данные превышали нормативные значения: ВВФСУмакс у 25,7%; 30,3% и 45,2% сравниваемых групп и КВВФСУсредн. у 20%, 18,2% и 22,58% соответственно. Дисфункция синусового узла вегетативного генеза была выявлена у 25,7% больных первой группы; 30,3% — второй и 45,2% — группы сравнения. Были определены особенности функционирования АВ-проводящей системы: у 1 больного (2,9%) первой группы и у 2 больных (6,1%) второй группы отмечено возникновение точки Венкебаха на частотах, превышающих 180 имп/мин. Межгрупповые отличия были значимы для показателей ВВФСУсредн., КВВФСУмин и ВВФСУмакс отличались у больных первой группы (р < 0,05) и второй группы (р < 0,01) по сравнению с больными ЯБ, точка Венкебаха отличалась (р < 0,05) у больных первой группы от группы сравнения и ВВФСУмин у больных первой и второй группы (р < 0,05).
В процессе лечения произошло достоверное уменьшение показателей КВВФСУсредн. за счет снижения КВВФСУмакс для всех 3 исследуемых групп, а также ВВФСУмин и ВВФСУмакс во второй основной группе, что косвенно указывает на снижение парасимпатического влияния ВНС.
ЭФИ-показатели функции синусового узла оказались нормальными у всех групп обследованных и не превышали допустимых значений после курса терапии. После курса терапии прокинетиками показатели АВ-проводимости не отличались от допустимых. ВВФСУмин после курса лечения было достоверно выше у больных ЯБ, чем при патологии пищевода и кардии (р < 0,05).
При изучении вегетативного обеспечения ССС получено преобладание ваготонии во всех группах по опроснику Вейна, индексу Кердо и МОК. После лечения отмечено достоверное снижение исходной парасимпатикотонии и достоверное изменение вегетативных показателей, свидетельствовавших об исходной эутонии, — QWm и индекса Хильдебранта, что подтверждает повышение активности симпатического звена. Межгрупповых различий не получено. Полученные результаты не противоречат литературным данным. Так, Ф. И. Комаровым было показано, что при впервые выявленной язвенной болезни или ее обострении в первые 2 нед преобладает тонус симпатического отдела ВНС, обусловленный болевым синдромом. Затем, по мере купирования болевого синдрома, функциональная активность СНС оказывается резко сниженной и начинает преобладать тонус ПНС. Другими российскими исследователями (Э. В. Минаков, М. М. Романов, 1999) отмечены достоверные отличия в показателях ВСР у больных ЯБ с различным течением. Для большинства пациентов с впервые выявленной язвой была характерна симпатикотония, у больных с легким течением показатели ВСР находились в пределах стандартных отклонений величин. У больных средней и тяжелой степени отмечалась парасимпатикотония в состоянии покоя. Полученные данные в какой-то мере перекликаются с теорией
G. Beigman, считавшего, что предпосылкой к язвообразованию могут служить не столько поражения блуждающего нерва, сколько нарушение сбалансированного влияния на ЖКТ обоих отделов ВНС. Сибирские коллеги (Э. И. Белобородова и др., 2002) также изучали состояние вегетативного тонуса у больных ЯБ с использованием кардиоинтервалографии. В состоянии покоя при легком и среднетяжелом течении отмечено снижение симпатического звена, при тяжелом — увеличение. Авторами был сделан вывод, что психофизиологические характеристики коррелируют с тяжестью течения язвенной болезни: выраженность вегетативных и психологических нарушений увеличивается пропорционально утяжелению заболевания, достигая максимальных показателей при тяжелом течении. Было предложено использовать вегетативные и психологические показатели в качестве критериев прогнозирования характера течения ЯБ ДПК у лиц молодого возраста.
Большинство показателей вариабельности сердечного ритма исходно не отличалось от нормативных значений, кроме RMSSD (р < 0,001). Межгрупповые отличия имелись только по одному показателю: iSDNN достоверно различался у больных с сочетанием ГЭРБ и ЯБ от больных изолированной ЯБ (р < 0,05).
На фоне успешной терапии основного заболевания отмечен достоверный прирост iSDNN и PNN50; снижение iSDАNN и нормализация RMSSD (р < 0,01) были во всех изученных группах.
Анализ частотных характеристик ВСР показал исходное превышение нормативных значений ULF у больных ГЭРБ и ЯБ и LF во всех группах и снижение показателей VLF, повышение НF при патологии пищевода и кардии. После лечения показатели ULF и VLF повысились во всех группах (р < 0,001), только ультранизкий спектр частот не достигал нормальных значений. Исходно повышенный спектр LF на фоне лечения нормализовался (р < 0,001). Отмечено снижение спектра высоких частот (р < 0,001). Наши данные исследования ВСР у больных ЯБ не отличались от результатов, полученных Э. В. Минаковым и соавт. Корреляционный и факторный анализ, выполненный у исследованных нами пациентов, выявил меньше связанных переменных по сравнению с приведенными параметрами. Так, время с рН < 4,0 в пищеводе (%) коррелировало только с показателем rMSSD (-0,36*) лишь у больных рефлюксной болезнью. В то время как анализ выявил, что на показатели ВСР большее влияние оказали такие факторы, как минимальная, максимальная и средняя ЧСС, хотя в некоторых моделях имели значение и продолжительность ГЭР, КВВФСУмакс, уровень САД. Результаты исследования ВСР у здоровых и кардиологических больных установили зависимость показателей ВСР главным образом от ЧСС (И. С. Явелов, Н. А. Грацианский, 1999). Существуют свидетельства наличия линейной зависимости между средней ЧСС и показателями ВСР, полученными как при суточном мониторировании ЭКГ (здоровые лица), так и при анализе коротких участков записи ЭКГ (больные нестабильной стенокардией). В проведенном исследовании наличие этой связи подтверждено для больных ГЭРБ (ГПОД). По-видимому, такая зависимость имеет общую тенденцию, поскольку существует мнение, что ритм сердца в большей степени зависит от вегетативной регуляции, чем от нозологии. Из характеристик ВСР наиболее тесная корреляция получена для iSDNN, rMSSD. В наименьшей степени с минимальной и максимальной ЧСС были связаны значения ОНЧ во второй группе и показатели функциональной активности синусового узла (КВВФСУмакс и ВВФСУмакс, QVm) rMSSD и LF в третьей группе.
Обобщая результаты исследования ВНС, полученные при исследовании различных вегетативных индексов и ВСР, можно говорить о том, что у всех исследованных больных имелись признаки дисбаланса ВНС по смешанному типу. Динамика указанных параметров говорит о снижении избыточных симпатических и парасимпатических влияний и о восстановлении симпатико-парасимпатического баланса при лечении основной патологии. Таким образом, на фоне лечения произошло небольшое, но достоверное увеличение ЧСС. Одной из причин уменьшения парасимпатической активности могла явиться стабилизация состояния больных в результате лечения основной патологии. При этом соотношение симпатических и парасимпатических влияний на синусовый ритм существенно изменялось в сторону гармонизации влияний обоих отделов ВНС.
Все вышеизложенное позволяет говорить о взаимосвязи вегетативных, электрофизиологических изменений, что, по-видимому, во многом и определяет состояние организма и характер течения болезни. В проведенной работе использованы неинвазивные методы исследования, которые, уступая по точности инвазивным, имеют целый ряд достоинств, а именно: доступность, безопасность, возможность многократного применения, относительную простоту и неинвазивность. Все это увеличивает ценность этих методик. Возможно использование показателей ВСР для оценки эффективности проводимого лечения.
Выводы
- У больных ГЭРБ в 29,4% случаев отмечается атипичная (кардиальная) симптоматика.
- При стандартной записи ЭКГ у больных ГЭРБ, в том числе при сочетании с ЯБ, чаще (по сравнению с больными ЯБ) выявляются НВЖП.
- При суточной записи ЭКГ у больных с сочетанием ГЭРБ и ЯБ регистрируется суправентрикулярная экстрасистолия достоверно чаще, чем при ЯБ.
- При параллельном суточном мониторировании внутрипищеводного рН и ЭКГ индекс симптома составляет 60– 80%, что подтверждает связь между нарушениями сердечного ритма и ГЭРБ.
- Исходный показатель времени восстановления функции синусового узла при ЭФИ достоверно выше у больных ЯБ, чем при патологии пищевода и кардии.
- У больных с патологией верхних отделов ЖКТ при исследовании вегетативного тонуса и ВСР выявляется дисбаланс ВНС с преобладанием парасимпатических влияний.
- На фоне нормализации показателей суточного мониторирования внутрипищеводного рН, ЭКГ и ХМ отмечаются улучшение показателей проводимости, уменьшение частоты нарушений сердечного ритма и гармонизация вегетативных влияний.
- У больных ГЭРБ максимальная длительность рефлюкса ассоциирована с ультранизким спектром частот вариабельности сердечного ритма.
- Продолжительность закисления пищевода ассоциирована с показателем RMSSD вариабельности сердечного ритма.
- Лечение прокинетиками в течение 6–8 нед привело к удлинению QT в группе больных ГЭРБ в сочетании с ЯБ, однако в пределах нормативных значений.
А. Ю. Кузьмина НИИ терапии, г. Новосибирск
Причины учащения пульса при ВСД
Пациенты с вегетососудистой дистонией периодически страдают от нарушения пульса и давления. Эти приступы могут быть спонтанными, но в большинстве случаев их можно заранее предугадать. Так, тахикардия может быть спровоцирована следующими изменениями:
- резкими переменами погодных условий, в том числе в межсезонье;
- приемом большого количества пищи;
- интенсивными физическими нагрузками, а также резкими движениями и сменой положения тела;
- нарушением диеты (особенно опасны растворимый кофе, алкогольные и газированные напитки);
- любые стрессовые ситуации.
Здоровый образ жизни и стабильное психологическое состояние — это основные условия, как предотвратить очередной приступ. Однако повышенная забота о собственном здоровье может становиться причиной развития кардионевроза. При этом состоянии пациент постоянно прислушивается к ритму работы сердца, подсчитывает пульс и измеряет давление, что может активировать очередное обострение.
Признаки приступа
В норме человек не ощущает работу сердца. При проявлении первых симптомов тахикардии у больного учащается пульс, как после бега или при сильном волнении. Также появляется ощущение страха и тревожности, которое во многом спровоцировано наличием дополнительных симптомов. Несмотря на то, что тахикардия при ВСД не является угрожающим для жизни состоянием, она часто становится основанием для вызова медиков. Больного беспокоят следующие признаки:
- сильная слабость;
- частое и сильное сердцебиение;
- боль в области грудной клетки, что вызывает подозрения на инфаркт миокарда;
- тяжелое дыхание, одышка;
- головная боль и головокружение;
- приступы паники, которые еще больше усугубляют клиническую картину.
Наиболее частая разновидность синдрома — это синусовая тахикардия. Она характеризуется повышением возбудимости синусового узла, вследствие чего частота сердечных сокращений увеличивается до 120-130 ударов в минуту. Такая клиническая картина может развиваться в любом возрасте и не является поводом для беспокойства, если не сопровождается дополнительными признаками.
СПРАВКА! Синусовая тахикардия, которая чаще всего проявляется при ВСД, не вызывает нарушений сердечного ритма. Любые проявления аритмии говорят о необходимости дополнительной диагностики состояния сердца и сосудов.
3.Симптомы пароксизмальной тахикардии
Сердечный приступ обычно начинается с задержки пульса и затем сильного толчка, который сам больной отчётливо ощущает. После этого развивается частое сердцебиение. Продолжительность приступа
— от нескольких секунд до суток и более. Иногда приступ ограничивается начальным толчком. Больной рефлекторно прижимает руку к груди, ссутуливается и тем самым блокирует развитие этого состояния.
Приступ в динамике даёт высокие показатели частоты сердечных сокращений, может сопровождаться головокружением, шумом в голове, ощущениями общего замерзания, слабости и сдавленности в области грудины, снижением температуры конечностей. Часто приступу сопутствует повышение артериального давления. Характерным признаком является также полиурия (выделение большого количества мочи) в конце или в течение нескольких часов после нормализации сердечного ритма.
О нашей клинике м. Чистые пруды Страница Мединтерком!
Необходимые обследования
Если приступ тахикардии возникает впервые, показана полная диагностика сердечно-сосудистой системы. Учащение пульса также вызывает дополнительные симптомы, которые необходимо принять во внимание. Состояния больного можно оценить по комплексу исследований:
- электрокардиография — один из основных методов диагностики работы миокарда;
- эхокардиография — обследование состояния сердца на УЗИ;
- по необходимости — тонометрия с использованием МРТ.
ВСД выделено в качестве самостоятельного заболевания. Его вынесли в отдельную категорию в классификации МКБ-10. Нарушения частоты сердечных сокращений, вызванные недостаточностью вегетативной нервной системы, не несут опасности для жизни пациента. Комплекс обследований, которые предлагаются после первого приступа, а также для мониторинга состояния сердца и сосудов, не показывают никаких серьезных отклонений.