Глиома – опухоль головного мозга, которая берет начало из клеток нейроглии. Новообразования являются наиболее распространенным видом патогенеза злокачественного характера различной степени агрессивности. Симптомы глиомы у взрослых и детей будут зависеть от места ее образования. Основными методами диагностики являются КТ и МРТ, самый точный результат получают при проведении цитогистологического анализа отобранного материала (биопсия). Основной метод лечения глиомы головного мозга – хирургическое удаление патологического новообразования. Лечение всегда носит комплексный характер, кроме операции назначается химио- и радиотерапия. Восстановление и продолжительность жизни после удаления опухоли зависит от многих факторов: адекватности лечения, степени злокачественности новообразования головного мозга, стадии заболевания, общего состояния больного и многих других факторов. Наилучший прогноз имеют доброкачественные глиомы, наихудший – глиомы 3 и 4 степени злокачественности. Например, при глиобластоме продолжительность жизни, как правило, не более двух лет.
Происхождение глиом головного мозга и характеристика
До сих пор нет единого мнения насчет того, какие именно клетки дают начало глиальным опухолям. Классическое мнение основано на том, что глиомы развиваются из зрелых клеток глии (олигодендроцитов и астроцитов). В последнее время больше склоняются к тому, что они образуются в так называемых «промежутках злокачественности». Это значит, что опухоли головного мозга данного типа формируются из незрелых медленно пролиферирующих клеток, которые постепенно малигнизируются (перерождаются в рак). Как именно будет развиваться новообразование зависит от трансформаций в геноме, например, астроцитомы (разновидность глиомы) формируются при мутациях в гене TP53,
Доля глиом в общей популяции опухолей головного мозга составляют около 60%. Чаще всего новообразования формируются в головном мозге, имеют первичный характер. Глиома ствола головного мозга диагностируется сравнительно редко. Цвет неоплазий от темно-красного до нежного розового, форма в большинстве случаев напоминает круг или веретено, но может иметь и неправильные очертания. Величина зависит от стадии болезни: от нескольких миллиметров до 10-14 см.
Наиболее частым местом локации опухоли является зона хиазм или мозговых желудочков. Доброкачественная глиома, как правило, не распространяется на костные структуры черепа и не прорастает в оболочки головного мозга, однако, этого нельзя исключать. Злокачественная глиома растет сначала медленно, но по мере прогрессирования канцерогенеза, ее рост ускоряется. Характерен инфильтративный рост, т. е. способность врастать в соседние ткани, что при диагностике не позволяет определить четкие границы патогенного очага.
Обратите внимание. Для глиом головного мозга не характерно метастазирование, однако, они приводят к вырождению соседних тканей.
Возможные осложнения
{banner_banstat9}
Последствия встречаются сравнительно редко. От момента развития микроангиопатии и до конечного исхода протекают годы. Однако расслабляться нельзя.
Среди возможных проблем:
- Инсульт. Острое нарушение мозгового кровообращения. Провоцирует отмирание нервных тканей. Тяжелую инвалидность с неврологическим дефицитом. Возможна и даже вероятна гибель человека.
- Дисциркуляторная энцефалопатия. Процесс схожий, но пока нет деструкции церебральных структур.
- Сосудистая деменция. Слабоумие на фоне недостаточного питания головного мозга.
Осложнения развиваются спонтанно. Лечение — единственный способ их предотвратить.
Причины возникновения и факторы риска
Рак и доброкачественные дисплазии могут формироваться в головном мозге в любом возрасте, однако вероятность развития патологии увеличивается по мере взросления. Общий пик заболеваемости приходится на седьмой десяток лет. Опухолевый процесс чаще развивается у мужчин, нежели у женщин.
Основные причины возникновения глиомы головного мозга, следующие:
- воздействие ионизирующего облучения (радиация – основной фактор риска);
- генетические предпосылки, обусловленные наследственностью;
- поражение онкогенными вирусами;
- травмы головы и шейного отдела головного мозга;
- вредные привычки.
Важно. Специфической профилактики против рака головного мозга нет. Уменьшает вероятность развития опухолевого процесса минимизация факторов риска, здоровый образ жизни, качественное питание, регулярные занятия спортом и спокойный эмоциональный фон.
Демиелинизация
Демиелинизирующее заболевание головного мозга по МКБ-10 имеет коды G35, G36 и G77. Процесс, вызванный поражением нервной ткани, негативно сказывается на функционировании всего организма в целом. Определенные нервные окончания покрыты миелиновой оболочкой, которая выполняет в организме важные функции. Например, миелин обеспечивает быструю передачу электрических импульсов и соответственно при нарушении этого процесса страдает вся система. Миелин состоит из липидов и белковых соединений в пропорции 70/30.
Демиелинизирующее заболевание — это не только рассеянный склероз, это еще и оптиконевромиелит и острый диссеминированный энцефаломиелит. Эти болезни не лечатся, но развитие их можно замедлить. В целом медики дают благоприятный прогноз при лечении этих патологий. Диагноз «рассеянный склероз» сейчас ставят чаще, но само заболевание протекает легче, чем 30-40 лет назад.
Записаться на приём
Классификация
Зависимо от вида клеток головного мозга, которые переродились и дали начало патогенезу, различают следующие виды опухолей:
- астроцитомы – самый часто встречаемый вид, их доля в общей популяции составляет около 50%;
- олигодендроглиомы – доля в общей популяции опухолей этого типа составляет до 10%;
- эпендимомы – самые редкие формы (встречаемость менее 7%).
По классификации ВОЗ (которая является общепринятой) неоплазии ранжируют зависимо от степени злокачественности.
Доброкачественные глиомы
Это опухоли первой степени злокачественности, например, астроцитомы: гигантоклеточная, пилоцитарная, ювенильная субэпендимальная. Они являются доброкачественными, потому что медленно растут, не имеют признаков рака, легко поддаются лечению. Прогноз жизни при доброкачественной глиоме благоприятный. После удаления новообразования пациенты живут 10 лет и дольше.
Глиома низкой степени злокачественности
Вторая степень злокачественности. Ее также относят к доброкачественным новообразованиям, но уже с пограничной степенью злокачественности. Рост патологической ткани медленный (low-grade), они хорошо дифференцированы, как правило, есть только один признак рака (атипия клеток). Опухоли данного вида могут перерождаться в рак и легко переходить на третью и четвертую степень злокачественности. К ним относятся диффузная и фибриллярная астроцитомы. Лечение комплексное: операция по удалению атипичных тканей, дополнительно радио- и химиотерапия.
Злокачественные глиомы
Сюда относят глиомы 3 и 4 степени злокачественности:
- Третья степень злокачественности. Есть все признаки злокачественности, кроме некроза тканей. Ткани теряют четкую дифференциацию, рост опухоли ускоряется (high-grade), границы нечеткие, характерно прорастание в ближайшие ткани. Наиболее яркий пример – анапластическая астроцитома, которая чаще развивается у лиц среднего и старшего возраста. Лечение затрудняется отсутствием четких границ опухоли, продолжительность жизни зависит от того, сколько будет удалено атипичной ткани, а также стадии канцерогенеза в начале лечения.
- Самая опасная – четвертая степень злокачественности (глиобластома). Она развивается в возрасте от 40 до 70 лет. В этом случае присутствуют все признаки злокачественности, в том числе и некрозы. Опухоль растет быстро, проникает в другие ткани и не имеет четких границ. Это существенно осложняет терапию. Прогноз неблагоприятный.
Неоплазии делят на два вида, зависимо от особенностей роста:
- Опухоли узлового роста. Как правило, это доброкачественные новообразования с четкими контурами. Для них характерно образование в любом месте головного мозга и наличие кист. Примеры: плеоморфная ксантоастроцитома и пилоидная астроцитома.
- Образования диффузного типа. Нет явных границ, величина может достигать значительных размеров, неоплазия прорастает в соседние ткани головного мозга, что осложняет удаление дисплазии. Часто это злокачественные опухоли, например, глиобластома или анапластическая астроцитома, или те, которые способны быстро перерождаться.
Симптоматика
Клинические проявления подразделяют на общие и очаговые. Последние проявляются зависимо от того, в каком отделе мозга формируется патологическое образование.
Общие симптомы
Общие признаки рака головного мозга (или доброкачественной опухоли) возникают по причине увеличения давления внутри черепа, сдавливания телом опухоли соседних тканей и негативного влияния ее метаболитов. К общим симптомам относят:
- головокружение, головную боль, дискомфорт в голове;
- диспепсические проявления, не связанные с приемом пищи или отравлением;
- потеря аппетита, похудение;
- ухудшение зрения;
- изменение привычного для человека психоэмоционального поведения;
- проблемы с памятью, ослабевание умственной деятельности;
- признаки эпилепсии.
Важно понимать. Что общие симптомы не являются специфичными. Если они беспокоят регулярно, нужно срочно посетить врача.
Патологический процесс на ранних стадиях, как правило, протекает латентно или признаки его слабы. Часто новообразования находят случайно, при обследовании пациента на предмет другой болезни или в профилактических целях.
Очаговые симптомы
Это специфические признаки, возникающие в результате поражения церебральных структур ЦНС. Клиническая картина зависит от места локации патологического очага:
- Глиома зрительного нерва формируется из клеток его ствола. Рост тканей медленный, сопровождается инфильтрацией, но не прорастает в твердую мозговую оболочку. Новообразование считается доброкачественным, оно может формироваться по всей длине нерва, но чаще располагается в орбитальной части. Симптомы глиомы зрительного нерва: сначала снижается острота зрения (по мере поражения нерва и элементов глаза), затем развивается пучеглазие.
- Диффузная глиома ствола головного мозга является высокозлокачественной. Поскольку диффузная дисплазия формируется в области расположения нервов, отвечающих за работу конечностей, то при их поражении нарушается координация рук и ног, вплоть до парезов и паралича. Клинические признаки диффузной глиомы моста существенны даже при небольших размерах дисплазии. Через мост проходит много нервных тяжей, поэтому клиника может быть разнообразнее.
- Глиома лобной доли головного мозга проявляется апатией, изменением психики, человек становится нервным, вспыльчивым, характерны резкие перемены настроения. Для поздних стадий болезни свойственно наступление паралича.
- Глиома височной области вызывает нарушение координации движений, ухудшается память, страдает дикция. Кроме этого, глиома височной доли негативным образом влияет на обоняние.
- Глиома мозжечка и червя мозжечка приводит к аномалиям движения. Нарушается походка, кажется, что человек пьян. Все потому, что больному становится трудно держать равновесие, руки и ноги не слушаются, поддержание тела в пространстве становится проблематичным.
- Глиома теменной доли сопровождается нарушениями мелкой моторики, поэтому у человека изменяется почерк, со временем писать становится трудно. Притупляются тактильные ощущения.
- Глиома четверохолмия или четверохолмной пластинки вызывает зрительные нарушения, появляются аномалии движения глаз, нарушается слух.
- Глиома мозолистого тела сопровождается зрительными галлюцинациями (такие же возникают при наличии опухоли в затылочной доле), нарушениями логики, а также многими другими признаками: изменение чувствительности, слабость мускулатуры и так далее.
- Глиома варолиева моста (диффузная или обычная) приводит к нарушению проводниковых функций, поскольку в этой зоне локализованы ядра черепных нервов. Поэтому клиническая картина будет довольно широкой. Фиксируется нарушение сенсорики, движений и так далее.
- Глиома желудочка головного мозга приводит к увеличению внутричерепного давления за счет нарушения оттока ликвора. Возможно развитие гидроцефалии.
Хроническая ишемия мозга
Цереброваскулярные заболевания являются одной из основных проблем современной медицины. Известно, что в последние годы структура сосудистых болезней мозга меняется за счет нарастания ишемических форм. Это обусловлено повышением удельного веса артериальной гипертензии и атеросклероза как основной причины цереброваскулярной патологии. При изучении отдельных форм нарушений мозгового кровообращения первое место по распространенности занимает хроническая ишемия.
Хроническая ишемия мозга (ХИМ) — особая разновидность сосудистой церебральной патологии, обусловленная медленно прогрессирующим диффузным нарушением кровоснабжения головного мозга с постепенно нарастающими разнообразными дефектами его функционирования. Термин «хроническая ишемия мозга» используется в соответствии с Международной классификацией болезней 10-го пересмотра вместо применявшегося ранее термина «дисциркуляторная энцефалопатия».
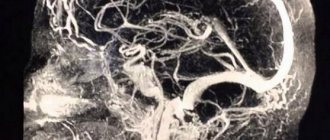
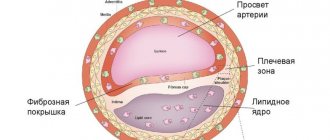
Развитию хронической ишемии мозга способствует ряд причин, которые принято называть факторами риска. Факторы риска делятся на корригируемые и некорригируемые. К некорригируемым факторам относятся пожилой возраст, пол, наследственная предрасположенность. Известно, например, что инсульт или энцефалопатия у родителей увеличивает вероятность сосудистых заболеваний у детей. На эти факторы нельзя повлиять, но они помогают заранее выявить лиц с повышенным риском развития сосудистой патологии и помочь предотвратить развитие болезни. Основными корригируемыми факторами развития хронической ишемии являются атеросклероз и гипертоническая болезнь. Сахарный диабет, курение, алкоголь, ожирение, недостаточная физическая нагрузка, нерациональное питание — причины, приводящие к прогрессированию атеросклероза и ухудшению состояния больного. В этих случаях нарушается свертывающая и противосвертывающая система крови, ускоряется развитие атеросклеротических бляшек. За счет этого просвет артерии уменьшается или полностью закупоривается (рис.). При этом особую опасность представляет кризовое течение гипертонической болезни: оно приводит к возрастанию нагрузки на сосуды головного мозга. Измененные атеросклерозом артерии не в состоянии поддерживать нормальный мозговой кровоток. Стенки сосуда постепенно истончаются, что в конечном счете может привести к развитию инсульта.
| Рисунок. МР-ангиограмма: окклюзия правой средней мозговой артерии |
Этиология ХИМ связана с окклюзирующими атеросклеротическими стенозами, тромбозами, эмболиями. Определенную роль играют посттравматическое расслоение позвоночных артерий, экстравазальные компрессии при патологии позвоночника или мышц шеи, деформация артерий с постоянными или периодическими нарушениями их проходимости, гемореологические изменения крови (повышение гематокрита, вязкости, фибриногена, агрегации и адгезии тромбоцитов). Необходимо иметь в виду, что симптоматика, аналогичная той, что имеет место при хронической ишемии, может быть обусловлена не только сосудистыми, но и другими факторами — хронической инфекцией, неврозами, аллергическими состояниями, злокачественными опухолями и прочими причинами, с которыми следует проводить дифференциальный диагноз. При предполагаемом сосудистом генезе описанных нарушений необходимо инструментальное и лабораторное подтверждение поражения сердечно-сосудистой системы (ЭКГ, УЗ-допплерография магистральных артерий головы, МРА, МРТ, КТ, биохимические исследования крови и др.).
Для постановки диагноза следует придерживаться строгих диагностических критериев: наличие причинно-следственных связей (клинических, анамнестических, инструментальных) поражений головного мозга с нарушениями гемодинамики с развитием клинической, нейропсихологической, психиатрической симптоматики; признаков прогрессирования сосудистой мозговой недостаточности. Следует учитывать возможность субклинически протекающих острых церебральных дисциркуляторных нарушений, включая мелкоочаговые, лакунарные инфаркты, формирующих характерную для энцефалопатии симптоматику. По основным этиологическим причинам выделяют атеросклеротическую, гипертоническую, смешанную, венозную энцефалопатии, хотя возможны и иные причины, приводящие к хронической сосудистой мозговой недостаточности (ревматизм, васкулиты другой этиологии, заболевания крови и др.).
Патоморфологическая картина ХИМ характеризуется участками ишемически измененных нейронов или их выпадения с развитием глиоза. Развиваются мелкие полости (лакуны) и более крупные очаги. При множественном характере лакун формируется так называемое «лакунарное состояние». Эти изменения преимущественно наблюдаются в области базальных ядер и имеют типичное клиническое выражение в виде амиостатического и псевдобульбарного синдромов, деменции, описанных в начале ХХ в. французским неврологом P. Marie. В наибольшей степени развитие status lacunaris характерно для артериальной гипертонии. В этом случае наблюдаются изменения сосудов в виде фибриноидного некроза стенок, их плазматического пропитывания, формирования милиарных аневризм, стенозов.
В качестве характерных для гипертонической энцефалопатии изменений выделяются так называемые криблюры, представляющие собой расширенные периваскулярные пространства. Таким образом, хронический характер процесса патоморфологически подтверждают множественные зоны ишемии мозга, особенно его подкорковых отделов и коры, сопровождающиеся атрофическими изменениями, развивающимися на фоне соответствующих изменений церебральных сосудов. С помощью КТ и МРТ выявляются в типичных случаях множественные микроочаговые изменения, в основном в подкорковых зонах, перивентрикулярно, сопровождающиеся нередко атрофией коры, расширением желудочков мозга, феноменом лейкоареоза («перивентрикулярное свечение»), являющимся отражением процесса демиелинизации. Однако сходные изменения могут наблюдаться при нормальном старении и первичных дегенеративно-атрофических процессах мозга.
Клинические проявления ХИМ не всегда выявляются при КТ- и МРТ-исследованиях. Поэтому нельзя переоценивать диагностическую значимость методов нейровизуализации. Постановка пациенту правильного диагноза требует от врача объективного анализа клинической картины и данных инструментального исследования.
Патогенез ишемии мозга обусловлен недостаточностью мозгового кровообращения в относительно стабильной ее форме или в виде повторных кратковременных эпизодов дисциркуляции.
В результате патологических изменений сосудистой стенки, развивающихся вследствие артериальной гипертонии, атеросклероза, васкулитов и др., происходит нарушение ауторегуляции мозгового кровообращения, возникает все большая зависимость от состояния системной гемодинамики, также оказывающейся нестабильной вследствие тех же заболеваний сердечно-сосудистой системы. К этому добавляются нарушения нейрогенной регуляции системной и церебральной гемодинамики. Сама же по себе гипоксия мозга приводит к дальнейшему повреждению механизмов ауторегуляции мозгового кровообращения. Патогенетические механизмы острой и хронической ишемии мозга имеют много общего. Основные патогенетические механизмы ишемии мозга составляют «ишемический каскад» (В. И. Скворцова, 2000), включающий в себя:
- снижение мозгового кровотока;
- нарастание глутаматной эксайтотоксичности;
- накопление кальция и лактат ацидоз;
- активацию внутриклеточных ферментов;
- активацию местного и системного протеолиза;
- возникновение и прогрессирование антиоксидантного стресса;
- экспрессию генов раннего реагирования с развитием депрессии пластических белковых и снижением энергетических процессов;
- отдаленные последствия ишемии (локальная воспалительная реакция, микроциркуляторные нарушения, повреждения ГЭБ).
Основную роль в поражении нейронов головного мозга играет состояние, получившее название «оксидантный стресс». Оксидантный стресс — это избыточное внутриклеточное накопление свободных радикалов, активация процессов перекисного окисления липидов (ПОЛ) и избыточное накопление продуктов ПОЛ, усугубляющее перевозбуждение глутаматных рецепторов и усиливающее глутаматные эксайтоксические эффекты. Под глутаматной эксайтотоксичностью понимают гиперстимуляцию медиаторами возбуждения NDMA-рецепторов N-метил-D-аспартата, провоцирующую дилатацию кальциевых каналов и, как следствие, массивное поступление кальция в клетки, с последующей активацией протеаз и фосфолипаз. Это приводит к постепенному снижению нейрональной активности, изменению соотношения нейрон-глия, что вызывает ухудшение мозгового метаболизма. Понимание патогенеза ХИМ необходимо для адекватной, оптимально подобранной стратегии лечения.
По мере нарастания выраженности клинической картины усиливаются патологические изменения в сосудистой системе головного мозга. Если вначале процесса выявляются стенозирующие изменения одного-двух магистральных сосудов, то далее оказываются существенно измененными большинство или даже все магистральные артерии головы. При этом клиническая картина нетождественна поражению магистральных сосудов, вследствие наличия у пациентов компенсаторных механизмов ауторегуляции мозгового кровотока. Важную роль в механизмах компенсации нарушений мозгового кровообращения играет состояние внутричерепных сосудов. При хорошо развитых и сохранившихся путях коллатерального кровообращения возможна удовлетворительная компенсация, даже при значительном поражении нескольких магистральных сосудов. Напротив, индивидуальные особенности строения мозговой сосудистой системы могут быть причиной декомпенсации (клинической или субклинической), усугубляющей клиническую картину. Этим можно объяснить факт более тяжелого клинического течения ишемии мозга у больных среднего возраста.
По основному клиническому синдрому различают несколько форм ХИМ: с диффузной цереброваскулярной недостаточностью; преимущественной патологией сосудов каротидной или вертебрально-базилярной систем; вегето-сосудистыми пароксизмами; преимущественными психическими расстройствами. Все формы имеют сходные клинические проявления. В начальных стадиях заболевания все пациенты жалуются на головную боль, несистемное головокружение, шум в голове, ухудшение памяти, снижение умственной работоспособности. Как правило, эти симптомы возникают в период значительного эмоционального и умственного напряжения, требующего существенного усиления мозгового кровообращения. Если два и более из этих симптомов часто повторяются или существуют длительно (не менее 3 последних месяцев) и при этом отсутствуют признаки органического характера, неустойчивости при ходьбе, поражения нервной системы, ставится предположительный диагноз.
Клиническая картина ХИМ имеет прогрессирующее развитие и по выраженности симптоматики делится на три стадии: начальных проявлений, субкомпенсации и декомпенсации.
В 1-й стадии доминируют субъективные расстройства в виде головных болей и ощущения тяжести в голове, общей слабости, повышенной утомляемости, эмоциональной лабильности, головокружения, снижения памяти и внимания, нарушения сна. Эти явления сопровождаются хотя и легкими, но достаточно стойкими объективными расстройствами в виде анизорефлексии, дискоординаторных явлений, глазодвигательной недостаточности, симптомов орального автоматизма, снижения памяти и астении. В этой стадии, как правило, еще не происходит формирования отчетливых неврологических синдромов (кроме астенического) и при адекватной терапии возможно уменьшение выраженности или устранение как отдельных симптомов, так и заболевания в целом.
В жалобах больных со 2-й стадией ХИМ чаще отмечаются нарушения памяти, потеря трудоспособности, головокружение, неустойчивость при ходьбе, реже присутствуют проявления астенического симптомокомплекса. При этом более отчетливой становится очаговая симптоматика: оживление рефлексов орального автоматизма, центральной недостаточности лицевого и подъязычного нервов, координаторные и глазодвигательные расстройства, пирамидная недостаточность, амиостатический синдром, усиление мнестико-интеллектуальных нарушений. В этой стадии возможно вычленить определенные доминирующие неврологические синдромы — дискоординаторный, пирамидный, амиостатический, дисмнестический и др., которые могут помочь при назначении симптоматического лечения.
При 3-й стадии ХИМ более выраженными оказываются объективные неврологические расстройства в виде дискоординаторного, пирамидного, псевдобульбарного, амиостатического, психоорганического синдромов. Чаще наблюдаются пароксизмальные состояния — падения, обмороки. В стадии декомпенсации возможны нарушения мозгового кровообращения в виде «малых инсультов», или пролонгированного обратимого ишемического неврологического дефицита, длительность очаговых расстройств при котором составляет от 24 ч до 2 нед. При этом клиника диффузной недостаточности кровоснабжения мозга соответствует таковой при энцефалопатии средней степени выраженности. Другим проявлением декомпенсации могут быть прогрессирующий «законченный инсульт» и остаточные явления после него. Этой стадии процесса при диффузном поражении соответствует клиническая картина выраженной энцефалопатии. Очаговая симптоматика нередко сочетается с диффузными проявлениями мозговой недостаточности.
При хронической ишемии мозга четко прослеживается корреляция между выраженностью неврологической симптоматики и возрастом пациентов. Это необходимо иметь в виду при оценке значения отдельных неврологических признаков, которые считаются нормальными для лиц пожилого и старческого возраста. Данная зависимость отражает возрастные проявления дисфункций сердечно-сосудистой и других висцеральных систем, воздействующих на состояние и функции головного мозга. В меньшей степени эта зависимость прослеживается при гипертонической энцефалопатии. В этом случае тяжесть клинической картины во многом обусловлена течением основного заболевания и его длительностью.
Наряду с прогрессированием неврологической симптоматики, по мере развития патологического процесса в нейронах головного мозга, происходит нарастание когнитивных расстройств. Это касается не только памяти и интеллекта, нарушающихся в 3-й стадии до уровня деменции, но и таких нейропсихологических синдромов, как праксис и гнозис. Начальные, по существу субклинические расстройства этих функций наблюдаются уже в 1-й стадии, затем они усиливаются, видоизменяются, становятся отчетливыми. 2-я и особенно 3-я стадии болезни характеризуются яркими нарушениями высших мозговых функций, что резко снижает качество жизни и социальную адаптацию больных.
В картине ХИМ выделяют несколько основных клинических синдромов — цефалгический, вестибуло-атаксический, пирамидный, амиостатический, псевдобульбарный, пароксизмальный, вегетососудистый, психопатологический. Особенностью цефалгического синдрома является его полиморфность, непостоянство, отсутствие в большинстве случаев связи с конкретными сосудистыми и гемодинамическими факторами (исключая головную боль при гипертонических кризах с высокими цифрами артериального давления), уменьшение частоты встречаемости по мере прогрессирования болезни.
Вторым по частоте встречаемости является вестибуло-атаксический синдром. Основными жалобами пациентов являются: головокружение, неустойчивость при ходьбе, координаторные нарушения. Иногда, особенно в начальных стадиях, больные, жалуясь на головокружение, не отмечают нарушений координации. Недостаточно показательными бывают также результаты отоневрологического исследования. В более поздних стадиях заболевания субъективные и объективные дискоординаторные нарушения четко взаимосвязаны. Головокружение, неустойчивость при ходьбе частично могут быть связаны с возрастными изменениями вестибулярного аппарата, двигательной системы и ишемической невропатии преддверно-улиткового нерва. Поэтому для оценки значимости субъективных вестибуло-атаксических нарушений важен их качественный анализ при опросе больного, неврологическом и отоневрологическом обследовании. В большинстве случаев эти расстройства обусловлены хронической недостаточностью кровообращения в бассейне кровоснабжения вертебробазилярной артериальной системы, поэтому необходимо основываться не на субъективных ощущениях больных, а искать признаки диффузного поражения отделов мозга, кровоснабжение которых осуществляется из этого сосудистого бассейна. В некоторых случаях у больных с ХИМ 2–3-й стадий атаксические нарушения бывают обусловлены не столько мозжечково-стволовой дисфункцией, сколько поражением лобно-стволовых путей. Возникает феномен лобной атаксии, или апраксии ходьбы, напоминающей гипокинезию больных паркинсонизмом. При КТ-исследовании выявляется значительная гидроцефалия (наряду с корковой атрофией), т. е. возникает состояние, близкое к нормотензивной гидроцефалии. В целом синдром недостаточности кровообращения в вертебробазилярном бассейне диагностируется при ХИМ чаще, чем недостаточность каротидной системы.
Особенностью пирамидного синдрома является его умеренная клиническая манифестация (анизорефлексия, мимическая асимметрия, минимально выраженные парезы, оживление рефлексов орального автоматизма, кистевые симптомы). Отчетливая асимметрия рефлексов указывает либо на имевшийся ранее мозговой инсульт, либо на другое заболевание, текущее под маской ХИМ (например, объемные внутричерепные процессы, последствия травматического повреждения головного мозга). Диффузное и достаточно симметричное оживление глубоких рефлексов, как и патологические пирамидные рефлексы, часто сочетающиеся со значительным оживлением рефлексов орального автоматизма и развитием псевдобульбарного синдрома, особенно в пожилом и старческом возрасте, указывает на многоочаговое сосудистое поражение мозга (при исключении иных возможных причин).
У больных с клиническими проявлениями недостаточности кровообращения в бассейне вертебробазилярной системы часто наблюдаются пароксизмальные состояния. Эти состояния могут быть обусловлены сочетанным или изолированным воздействием на позвоночные артерии вертеброгенных факторов (компрессионные, рефлекторные), что связано с изменением шейного отдела позвоночника (дорсопатии, остеоартроз, деформации).
Достаточно характерными и разнообразными по форме в разных стадиях ХИМ являются психические расстройства. Если в начальных стадиях они носят характер астенических, астенодепрессивных и тревожно-депрессивных нарушений, то во 2-й и особенно в 3-й стадии к ним присоединяются выраженные дисмнестические и интеллектуальные расстройства, формирующие синдром сосудистой деменции, выходящий в клинической картине нередко на первое место.
Электроэнцефалографические изменения неспецифичны для ХИМ. Они заключаются в прогрессирующем снижении β-ритма, нарастании доли медленной θ- и δ-активности, акцентуации межполушарной асимметрии, снижении реактивности ЭЭГ на внешнюю стимуляцию.
КТ-характеристики претерпевают динамику от нормальных показателей или минимальных атрофических признаков в 1-й стадии к более выраженным мелкоочаговым изменениям вещества мозга и атрофическим (наружным и внутренним) проявлениям во 2-й стадии до резко обозначенной корковой атрофии и гидроцефалии с множественными гиподенсивными очагами в полушариях — в 3-й стадии.
Сопоставление клинических и инструментальных характеристик у пациентов с атеросклеротической, гипертонической и смешанной формами ХИМ не выявляет отчетливых различий. При тяжелом течении гипертонической болезни возможны более быстрый темп нарастания психоневрологических расстройств, раннее проявление церебральных нарушений, большая вероятность развития лакунарного инсульта.
Лечение ХИМ должно основываться на определенных критериях, включающих понятия патогенетической и симптоматической терапии. Для правильного определения патогенетической стратегии лечения следует учитывать: стадию заболевания; выявленные механизмы патогенеза; наличие сопутствующих заболеваний и соматических осложнений; возраст и пол пациентов; необходимость восстановления количественных и качественных показателей мозгового кровотока, нормализации нарушенных функций головного мозга; возможность профилактики повторных церебральных дисгемий.
Важнейшим направлением терапии ХИМ является воздействие на имеющиеся факторы риска, такие, как артериальная гипертония и атеросклероз. Лечение атеросклероза проводится по общепринятым схемам с применением статинов, в комплексе с коррекцией режима питания и стиля жизни пациентов. Подбор антигипертензивных средств и порядок их назначения осуществляется врачом-терапевтом с учетом индивидуальных особенностей больных. Комплексная терапия ХИМ включает в себя назначения антиоксидантов, антиагрегантов, препаратов, оптимизирующих метаболизм мозга, вазоактивных препаратов. Антидепрессанты назначаются при выраженных астенодепрессивных проявлениях заболевания. Таким же образом назначаются антиастенические препараты.
Важным компонентом лечения ХИМ является назначение препаратов, обладающих антиоксидантной активностью. В настоящее время в клинической практике используются следующие препараты данного ряда: актовегин, мексидол, милдронат.
Актовегин — современный антиоксидант, представляющий собой депротеинизированный экстракт крови молодых телят. Его основное действие — улучшение утилизации кислорода и глюкозы. Под влиянием препарата значительно улучшается диффузия кислорода в нейрональных структурах, что позволяет уменьшить выраженность вторичных трофических расстройств. Отмечается также значительное улучшение церебральной и периферической микроциркуляции на фоне улучшения аэробного энергообмена сосудистых стенок и высвобождения простациклина и оксида азота. Происходящая при этом вазодилятация и снижение периферического сопротивления являются вторичными по отношению к активации кислородного метаболизма сосудистых стенок (А. И. Федин, С. А. Румянцева, 2002).
При ХИМ целесообразно применение актовегина, особенно при отсутствии эффекта от других методов лечения (Е. Г. Дубенко, 2002). Методика применения заключается в капельном введении 600–800 мг препарата в течение 10 дней, с последующим переходом на пероральное применение.
Постоянным в схеме терапии ХИМ является применение препаратов, оптимизирующих мозговое кровообращение. Наиболее часто используются следующие лекарственные средства: кавинтон, галидор, трентал, инстенон.
Галидор (бенциклан) — препарат, имеющий многонаправленный механизм действия, обусловленный блокадой фосфодиэстеразы, антисеротониновым действием, кальциевым антагонизмом. Он тормозит агрегацию и адгезию тромбоцитов, препятствует агрегации и адгезии эритроцитов, повышая эластичность и осмотическую резистентность последних. Галидор уменьшает вязкость крови, нормализует внутриклеточный метаболизм глюкозы, АТФ, воздействует на фосфокиназу и лактатдегидрогеназу, усиливает оксигенацию ткани. Доказано, что применение данного препарата в течение 8 нед устраняет клинические проявления хронической сосудистой недостаточности мозга у 86% пациентов. Препарат положительно влияет на эмоциональную среду человека, уменьшает забывчивость и рассеянность внимания. Галидор назначается в суточной дозе 400 мг в течение 6–8 нед.
Инстенон — комбинированный препарат нейропротекторного действия, включающий вазоактивный агент из группы пуриновых производных, вещество, влияющее на состояние восходящей ретикулярной формации и корково-подкорковые взаимоотношения, и, наконец, активатор процессов тканевого дыхания в условиях гипоксии (С. А. Румянцева, 2002; В. В. Ковальчук, 2002).
Три компонента инстенона (этофиллин, этамиван, гексобендин) совместно действуют на различные звенья патогенеза ишемического поражения мозга.
Этофиллин, вазоактивный компонент пуринового ряда, активизирует метаболизм миокарда с увеличением ударного объема. Переход гипокинетического типа кровообращения в нормокинетический сопровождается усилением мозгового кровотока. Немаловажным действием компонента являются повышение почечного кровотока и, как следствие, дегидратационный и диуретический эффекты.
Этамиван оказывает ноотропный эффект в виде прямого воздействия на процессы памяти, внимания, умственную и физическую работоспособность в результате повышения активности ретикулярной формации головного мозга.
Гексобендин избирательно стимулирует обмен веществ на основе повышения утилизации кислорода и глюкозы, вследствие усиления анаэробного гликолиза и пентозных циклов. При этом стабилизируются физиологические механизмы ауторегуляции церебрального и системного кровотока.
Инстенон применяют внутримышечно 2,0 мл, курс — 5–10 процедур. Затем продолжается пероральный прием инстенона-форте по 1 таблетке 3 раза в день в течение месяца (С. В. Котов, И. Г. Рудакова, Е. В. Исакова, 2003). Отчетливый регресс неврологической симптоматики отмечается к 15–20-му дню лечения. Особенно хороший эффект отмечается при сочетанном использовании актовегина (капельно) и инстенона (внутримышечные инъекции или пероральное применение). Терапия инстеноном положительно влияет на когнитивные функции, особенно на регуляцию мнестической деятельности и психомоторных функций.
Большое внимание в комплексной терапии ХИМ уделяется препаратам ноотропного действия, которые повышают устойчивость ткани мозга к различным неблагоприятным метаболическим воздействиям (ишемии, гипоксии). К собственно «ноотропным» относятся производные пирацетама (ноотропил, луцетам), энцефабол.
Пирацетам увеличивает синтез макроэргических фосфатов (АТФ), усиливает аэробный метаболизм в условиях гипоксии, облегчает проведение импульса, нормализует соотношение фосфолипидов клеточных мембран и их проницаемость, повышает плотность и чувствительность рецепторов, улучшает взаимодействие между полушариями головного мозга, улучшает метаболические процессы в ЦНС, облегчает нейрональную передачу.
Пирацетам улучшает микроциркуляцию за счет дезагрегантных свойств, облегчает проведение нервного импульса, улучшает взаимодействие между полушариями головного мозга. Препарат нормализует соотношение фосфолипидов клеточных мембран и усиливает их проницаемость, предотвращает адгезию эритроцитов, снижает агрегацию тромбоцитов, уменьшает уровни фибриногена и фактора VIII, снимает спазм артериол. Препарат назначается в суточной дозе 2,4–4,8 г в течение 8–12 нед.
Энцефабол — производное пиритинола. Препарат повышает плотность и чувствительность рецепторов, нормализует нейропластичность. Он обладает нейропротекторным эффектом, стимулирует процессы обучения, улучшает память, способность к запоминанию и концентрацию внимания. Энцефабол стабилизирует клеточные мембраны нейронов за счет ингибирования лизосомальных ферментов и предотвращения образования свободных радикалов, улучшает реологические свойства крови, повышает конформационную способность эритроцитов, увеличивая содержание АТФ в их мембране. Для взрослых средняя суточная доза составляет 600 мг в течение 6–8 нед.
К препаратам антиагрегантного ряда относятся ацетилсалициловая кислота и ее производные (кардиомагнил, тромбо АСС). Учитывая наличие противопоказаний при назначении ацетилсалициловой кислоты, часто применяют другие препараты с антиагрегантной активностью (курантил, тиклид, плавикс).
Симптоматическая терапия ХИМ включает назначение препаратов, уменьшающих проявления различных симптомов заболевания. Всем пациентам со 2–3-й стадиями болезни целесообразно назначение противотревожных или антидепрессантных средств. Наиболее безопасными при длительном применении являются препараты бензодиазепинового ряда.
Грандаксин — атипичное производное бензодиазепина, селективный анксиолитик. Препарат эффективно устраняет тревогу, страх, эмоциональное напряжение без седации и миорелаксации. Препарат обладает вегетокорректирующим действием, что делает возможным его применение у пациентов с выраженным вегетососудистым синдромом.
В неврологической практике используется суточная доза 50–100 мг, длительность употребления определяется индивидуально для каждого пациента.
Распространенность хронической сосудистой патологии головного мозга, прогредиентность течения, высокая степень инвалидизации пациентов определяют социальную и медицинскую значимость проблемы терапии ХИМ. В настоящее время в клинической практике прослеживается тенденция к увеличению использования немедикаментозных методов лечения. Это связано с отсутствием у пациентов феномена привыкания к лекарственным веществам с длительным периодом лечебного последействия.
Учитывая сложность патогенетических механизмов ХИМ, в процессе терапии необходимо добиться нормализации системного и мозгового кровообращения, скорректировать обмен в мозговой ткани, состояние гемореологии. В настоящее время возможности фармакологической коррекции проявлений ХИМ довольно обширны, они позволяют использовать различные препараты, влияющие на все звенья патогенеза постишемического и постгипоксического повреждения нервной ткани.
Таким образом, распознавание причин, выявление факторов риска и, следовательно, реальная возможность эффективного адресного лечения и предупреждение развития хронической патологии сосудов головного мозга предполагает точное знание структурных, физиологических и клинических особенностей проявления заболевания. Это становится возможным благодаря системному подходу к изучению этиологии, патогенеза, клиники и современным методам терапии.
М. В. Путилина, доктор медицинских наук, профессор
РГМУ, Москва
Диагностика
После устной беседы и физикального осмотра (изучается координация, состояние психики, работа анализаторов и другие внешние признаки) больной обследуется при помощи:
- томографии (КТ, МРТ, ПЭТ);
- ультразвуковых методов диагностики (эхоэнцефалография);
- ЭЭГ (электроэнцефалограмма);
- ангиография сосудов головного мозга;
- офтальмологическое обследование;
- сцинтиграфия и прочие.
Наиболее достоверный метод – биопсия (забор ткани выполняется при удалении рака или стереотаксической биопсии). Гистологический анализ образцов ткани дает полное представление о виде новообразования и всех его особенностях.
Лечение глиомы головного мозга
Хирургическое удаление глиомы головного мозга – является основным методом выбора. Лечение всегда носит комплексный характер. Результаты операции подкрепляются назначением радио и химиотерапии (до и после операции). Как правило, операция по удалению глиом дает хороший результат только в случае неоплазий доброкачественного характера, находящихся на первой стадии патогенеза. В это время удается произвести полное удаление аномальных тканей.
В других случаях это сделать трудно или невозможно. Патологические ткани прорастают в соседние, их границы четко неразличимы, поэтому контур опухоли не поддаётся идентификации, например, при диффузных типах рака. Вне зависимости от метода выполнения операции: радикального (трепанация или резекция черепа) или малоинвазивного (стереотаксические методики и другие), их смысл остается неизменным – важно постараться удалить всю патологическую ткань (тотальное удаление) или ее большую часть (субтотальное).
Чаще данные опухоли обнаруживаются на прогрессирующем этапе развития, что не дает возможности выполнить тотальное удаление. В таком случае основным методом лечения становится радиотерапия, например, так осуществляется лечение диффузной глиомы ствола мозга. Противопоказаниями к проведению операции может быть наличие других видов рака, слабое здоровье пациента или его преклонный возраст, близость рака к жизненно важным структурам, прорастание неоплазии в оба полушария, локация с трудным доступом.
Кто входит в группу риска
Любое заболевание имеет свои группы риска. Относящиеся к таким группам люди, должны внимательно следить за своим здоровьем и при первых подозрительных симптомах сразу обращаться к врачу. При очаговых патологиях к такой группе относятся больные:
- Гипертонической, гипотонической болезнью.
- Диабетом.
- Атеросклерозом.
- Ревматизмом.
- Ожирением.
- Чувствительные, эмоциональные люди, живущие в постоянном стрессе.
- Ведущие малоподвижную жизнь.
- Люди преклонного возраста, невзирая на половую принадлежность (начиная с 55-60 лет).
Также провоцируют развитие сосудистых патологий:
- Метеозависимость.
- Злоупотребление алкоголем.
- Остеохондроз.
- Наркомания.
- Аритмия.
- Аневризмы сосудов мозга.
Период восстановления и прогноз жизни
Период восстановления после удаления глиомы головного мозга будет зависеть от многих факторов. Самые главные из них: качество новообразования, стадийность, успех оперативного лечения и общее состояние больного. Если говорить в целом, то прогноз жизни при глиоме неблагоприятный. При субтотальном удалении опухоли существуют высокие риски рецидива, поэтому продолжительность жизни после операции на глиоме головного мозга при частичном ее удалении невысока. Полное удаление возможно на первой стадии доброкачественной опухоли. Около 80% больных проживают дольше пяти лет при условии тотального иссечения опухоли первой степени злокачественности. При рецидиве глиомы 3 или 4 степени злокачественности прогноз не превышает двух лет.
Причины поражения ГМ
Очаговые поражения могут вызываться самыми разными причинами.
- Как проверить сосуды головного мозга, какие методики используются
При очаговых поражениях головного мозга дисциркуляторного характера причиной может быть нехватка поступления питательных веществ, вызванная нарушением кровообращения (при ИБ, инсульте и прочих патологиях). Нередко причиной болезни является новообразование. Оно оказывает негативное воздействие на соседние участки головного мозга, вызывая в них различные изменения, вплоть до отмирания клеток ГМ.