Из статьи вы узнаете норму лимфоцитов (LYM, LYMPH в анализе крови) для взрослых и детей, причины увеличения и уменьшения концентрации клеток.
Лимфоциты (LYM, LYMPH) – это главные клетки иммунной системы, которые отвечают за всю нашу внутреннюю защиту. Если расшифровать само слово «лимфоциты», то оно состоит из двух древнегреческих слов – лимфа и цитос.
Лимфа – это вместилище, а цитос – это клетка. Лимфоциты – представители клеток белой крови, которые являются главными клетками иммунной системы. С момента их появления в костном мозге, и до момента пока они должны выполнять свою особо важную функцию – стоять на нашей внутренней генетической чистоте – проходит определённый промежуток времени.
Виды лимфоцитов
Когда костный мозг выбрасывает в кровеносное русло молодой лимфоцит, он ещё не готов к выполнению своих тончайших функций. Часть из молодых клеток, лимфоцитов, уходит в тимус, или вилочковую железу, и там они должны пройти дозревание или «обучение». Что значит «обучение»? Молодой лимфоцит должен познакомиться с теми антигенами, с которыми наш организм встречался на протяжении всей жизни, начиная с внутриутробного развития. После дозревания тимусозависимые лимфоциты (Т-лимфоциты) начнут распознавать антигены, понимать, что это генетические чужаки и будут готовы к выполнению своих задач.
Т-лимфоциты
Всего Т-лимфоцитов выделяют несколько видов.
Первый вид – это Т-киллеры. Киллеры – это убийцы. Именно они заточены на то, чтобы распознать генетического чужака и попытаться сразу его убить.
Второй вид – это Т-хелперы, или клетки-помощники. Именно Т-хелперы будут включать следующие клетки, которые будут вырабатывать для нас антитела или защитные белковые структуры.
Третий тип — Т-супрессоры – те клетки, которые будут останавливать иммунный ответ.
И так, если в организм человека попадает генетический чужак, первыми распознавать его будут киллеры, и попытаются сразу убить. Что может выступать в роли генетического чужака? Это вирусы, бактерии, паразиты, грибы, онкоклетки, которые могут появляться ежесекундно. Клетки организма в которых произошёл сбой на генетическом уровне. Если у человека есть непереносимость продуктов питания, то они, к сожалению, тоже могут превратиться в генетических чужаков и тоже истощать лимфоцитарное звено иммунной системы.
В-лимфоциты
Это тоже лимфоциты, которые, выйдя молодыми из костного мозга в кровеносное русло, устремляются в лимфатические узлы, в селезёнку, или в печень, где тоже будет происходить их дозревание. Основная функция В-клеток – это вырабатывать для нас представителей гуморального иммунитета, или кровяного иммунитета. Это именно В-клетки будут вырабатывают антитела, которые будут бороться с вирусами, бактериями – с другими генетическими чужаками.
NK-клетки или натуральные киллеры
Это группа клеток, которое в первую очередь будет заточено на охрану нас от онкозаболеваний. В первую очередь, натуральные киллеры будут работать в противоопухолевой защите, в противопаразитарной защите. NK-клетки — это основные виды лимфоцитов.
Общая характеристика
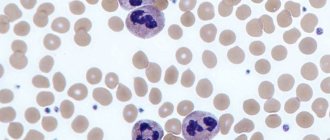
К семейству лейкоцитов относятся лимфоциты. Эти белые клетки, размер которых не превышает 10 мкм, были открыты давно. Их норма в крови составляет 20-40% от общего количества лейкоцитов. Лимфоциты – это клетки, большая часть которых образуется в красном костном мозге. Их обнаруживают при самых разнообразных событиях, происходящих в организме. Функции самых маленьких клеток семейства лейкоцитов разнообразные.
Прежде всего, благодаря им иммунная система узнает о проникновении патогенных элементов в организм, обладающих разрушительным воздействием. После получения такой информации включаются природные защитные реакции. Кроме того лимфоциты формируют иммунный барьер, который минимизирует риски заражения инфекцией.
Под воздействием этик клеток происходит отторжение чужеродных тканей. В частности, это происходит при трансплантации. Также важную роль играют лимфоциты в борьбе со злокачественным перерождением тканей в организме. Они всегда присутствуют при клеточном делении, независимо от его характера: естественного или патологического.
Норма лимфоцитов в крови у взрослых и детей
К сожалению, бывают часто ситуации, когда лимфоциты в крови могут отклоняться от нормы — повышать или понижаться. Это может быть при различных ситуациях. Прежде, чем говорить о том, когда количество лимфоцитов меняется в крови, нужно поговорить о том, сколько же их нормальная составляющая.
Если говорить о клонах клеток, то:
Т-клетки составляют от общего количества лимфоцитов 75%;
В-клетки где-то 15%;
Естественные киллеры где-то 10%.
И говоря о нормах лимфоцитов, нужно сказать, что в разные периоды жизни человека нормы отличаются.
Лимфоциты начинают вырабатываться костным мозгом уже внутриутробно, и продолжается этот процесс всю жизнь. Продолжительность жизни этих клеток тоже бывает различной – от нескольких месяцев, до шестидесяти лет. И это всё будут лимфоциты.
- До 1 года содержание лимфоцитов в крови от общего количества всех клеток — 45-70%.
- От 1-2 лет концентрация лимфоцитов должна снижаться — где-то 39-60%.
- От 2-4 то где-то от 33-50% всех белых клеток.
- От 4-10 лет, уже 30-50%.
- От 10-18 лет, то это уже 30-44%.
- У взрослого человека лимфоцитов в крови должно быть от 19-37%.
В таблице представлены величины допустимых норм лимфоцитов (отдельных субпопуляций) в крови у детей и взрослых.
| Возраст | Доля от общего числа лимфоцитов, % | Абсолютное количество клеток, *106/л |
| CD 3 + (Т-лимфоциты) | ||
| До 3 месяцев | 50 – 75 | 2065 – 6530 |
| До 1 года | 40 – 80 | 2275 – 6455 |
| 1 – 2 года | 52 – 83 | 1455 – 5435 |
| 2 – 5 лет | 61 – 82 | 1600 – 4220 |
| 5 – 15 лет | 64 – 77 | 1410 – 2020 |
| Старше 15 лет | 63 – 88 | 875 – 2410 |
| CD3+CD4+ (Т-хелперы) | ||
| До 3 месяцев | 38 – 61 | 1450 – 5110 |
| До 1 года | 35 – 60 | 1695 – 4620 |
| 1 – 2 года | 30 – 57 | 1010 – 3630 |
| 2 – 5 лет | 33 – 53 | 910- 2850 |
| 5 – 15 лет | 34 – 40 | 720 – 1110 |
| Старше 15 лет | 30 – 62 | 540 – 1450 |
| CD3+CD8+ (Т-цитотоксические лимфоциты) | ||
| До 3 месяцев | 17 – 36 | 660 – 2460 |
| До 1 года | 16 – 31 | 710 – 2400 |
| 1 – 2 года | 16 – 39 | 555 – 2240 |
| 2 – 5 лет | 23 – 37 | 620 – 1900 |
| 5 – 15 лет | 26 – 34 | 610 – 930 |
| Старше 15 лет | 14 – 38 | 230 – 1230 |
| CD19+ (В-лимфоциты) | ||
| До 2 лет | 17 – 29 | 490 — 1510 |
| 2 – 5 лет | 20 – 30 | 720 – 1310 |
| 5 – 15 лет | 10 – 23 | 290 – 455 |
| Старше 15 лет | 5 – 17 | 100 – 475 |
| CD3-CD16+CD56+ (NK-клетки) | ||
| До 1 года | 2 – 15 | 40 – 910 |
| 1 – 2 года | 4 – 18 | 40 – 915 |
| 2 – 5 лет | 4 – 23 | 95 – 1325 |
| 5 – 15 лет | 4 – 25 | 95 – 1330 |
| Старше 15 лет | 4 – 27 | 75 – 450 |
| Старше 15 лет | 1 – 15 | 20-910 |
Работа резидентных Т-клеток: не стоит путать туризм с эмиграцией
Мышиные резидентные клетки тканей в нормальной ситуации почти не перемещаются внутри нелимфоидной ткани и достаточно прочно прикреплены молекулами адгезии к строме органа. Когда резидентные макрофаги той же ткани секрецией цитокинов инициируют реакцию воспаления, ТRM приобретают большую подвижность и патрулируют близлежащий эпителий в поисках зараженных клеток.
Если воспалительная реакция усиливается, то клетки понимают это как сигнал о подкреплении: к работе патрульных TRM подключаются вновь прибывающие из крови TCM- и TEM-клетки. Эти клетки крови куда более подвижны и лучше перемещаются в эпителии. Значит ли это, что именно в крови находятся готовые действовать Т-киллеры среди TEM, а CD8+ TRM выполняют в ткани хелперные и регуляторные функции?
С одной стороны, Т-хелперы по спектру Т-клеточных рецепторов более тканеспецифичны, т.е. пересечений между репертуарами TCR клеток, взятых из разных тканей, совсем мало, тогда как клетки одного клона Т-киллера встречаются в разных тканях среди TEM []. Спектр функций и репертуар антигенной специфичности TRM еще предстоит исследовать, но способности к уничтожению зараженных клеток тканей у TRM-киллеров точно есть. Более того, в модели мышиной инфекции полиомавирусом, протекающей в ткани головного мозга, аффинность вирусоспецифичных Т-клеточных рецепторов резидентных киллерных клеток выше, чем у вирусоспецифичных клеток центральной памяти [].
Однако размер популяции Т-клеток зависит не только от специфичности TCR к инфекциям, которые раньше протекали в данном органе, но и от гомеостатической пролиферации Т-клеток — размножения более удачливых клеток для заполнения емкости органа по числу Т-лимфоцитов. По маркерам CD28 и CD127 на поверхности клеток можно отличить недавно и давно активированные через TCR клетки от тех, которые получили только гомеостатический сигнал к пролиферации от фактора роста IL-7. При старении ткани гомеостатическое размножение клеток начинает преобладать над пролиферацией активированных через TCR клеток.
Независимо от Т-клеточных рецепторов часто функционируют NKT-клетки, тип резидентных клеток печени, встречающихся и в других тканях. Они могут быть активированы NK-клеточными рецепторами через распознавание не индивидуальных антигенов, а общих молекулярных паттернов опасности и тканевого стресса. При активации CD8+ NKT-клетки выделяют цитотоксические гранулы и лизируют подозрительные клетки ткани, к примеру единичные опухолевые клетки и зараженные вирусами клетки, экспрессирующие и выставляющие на внешней мембране стрессорные молекулы. При старении тенденция TRM к активации без Т-клеточного рецептора, через NK-клеточные рецепторы или цитокиновые сигналы, может приводить к ошибочному лизису клеток ткани, недостаточному контролю над хронически зараженными или перерождающимися участками эпителия.
Патологические проявления, связанные с работой резидентных Т-клеток, включают органоспецифичные аутоиммунные синдромы и синдромы хронического воспаления в ткани. Примеры хронического воспаления, поддерживаемого резидентными Т-лимфоцитами, — контактный дерматит и псориаз, а механизмом служит выделение воспалительных факторов IL-17 резидентными Т-киллерами и IL-22 резидентными Т-хелперами дермы. CD8+ эффекторные Т-киллеры, находящиеся в головном мозге, похожи по совокупности мембранных молекул-маркеров на TRM кожи, кишечника и легких и способны подталкивать развитие перемежающегося рассеянного склероза при периодических выбросах воспалительных цитокинов. Неясно, однако, есть ли в норме в головном мозге популяция TRM или же это Т-лимфоциты, оставшиеся в ткани после нейротропной вирусной инфекции [].
Функции резидентных клеток памяти в норме — при отсутствии инфекции или хронического воспаления — могут включать cross-talk
(взаимную регуляцию преимущественно через секрецию цитокинов и костимуляторные молекулы) с неклассическими малоизученными лимфоидными клетками. Ими могут быть ассоциированные со слизистыми γ/δ Т-клетки, несущие альтернативный вариант сборки Т-клеточного рецептора, или лимфоидные клетки врожденного иммунитета (
Innate Lymphoid Cells
, ILC), которые делят с Т- и В-лимфоцитами общие черты эпигенетического ландшафта, но не имеют Т-/В- или NK-клеточных рецепторов [, ].
Предполагаемые функции резидентных Т-лимфоцитов тканей. Часть функций может выполняться во взаимодействии с резидентными макрофагами
TRM клетки контактируют с антигенпрезентирующими клетками тканей — дендритными клетками кожи и резидентными макрофагами тканей. Резидентные миелоидные клетки в разных тканях дифференцированы и слабо похожи друг на друга. К примеру, макрофаги маргинальной зоны селезенки, макрофаги печени и микроглия (макрофаги мозга) будут сильно отличаться и по морфологии, и по спектру функций. Кроме обнаружения антигенов в ткани, резидентные макрофаги заняты регуляцией процессов старения и самообновления тканей, в частности, выделяют факторы роста и цитокины, стимулирующие деление стволовых клеток тканей. В жировой ткани, к примеру, макрофаги стимулируют дифференцировку новых жировых клеток, но при переходе в активированное M1-состояние запускают воспаление и вместо дифференцировки заставляют увеличиваться и набухать имеющиеся жировые клетки. Сопутствующие изменения метаболизма жировой ткани приводят к накоплению жировой массы и в последние годы связываются с механизмами развития ожирения и диабета II типа. В коже цитокины, выделяемые макрофагами и резидентными γ/δ Т-клетками, стимулируют деление стволовых клеток при регенерации эпидермиса и стволовых клеток волосяных фолликулов [, ]. Можно предположить, что хелперные TRM-клетки при патрулировании эпителия и образовании контактов с тканевыми макрофагами могут модулировать спектр и объем выделяемых последними факторов роста для стволовых клеток, воспалительных цитокинов и факторов ремоделирования эпителия — и тем самым участвовать в обновлении тканей.
Причины повышения лимфоциты в крови у взрослых
Что это значит? Причины повышенных лимфоцитов в крови у женщин и мужчин, могут быть разные, но есть несколько типов заболеваний, которые чаще всего приводят к такому явлению:
- инфекционные заболевания;
- бактериальные инфекции;
- аутоиммунные заболевания;
- возможна острая аллергия, а также анафилактический шок;
- появление и рост злокачественных и доброкачественных опухолей и новообразований;
- особо выраженный лимфоцитоз будет в анализах при заболеваниях, которыми можно болеть один раз (корь, краснуха, ветрянка, мононуклеоз, и.т.д.);
- аутоиммунные процессы.
Как отличить резидентные клетки тканей от примесей клеток крови?
Резидентные Т-клетки корректно, но неудобно каждый раз определять по способности индивидуальной клетки мигрировать в лимфоузлы, поэтому необходимо составить список характерных признаков, по которым можно выявить принадлежность к этой субпопуляции. Резидентные Т-лимфоциты в тканях — естественных барьерах организма (например в легких и слизистой тонкого кишечника) немного похожи на классические эффекторные клетки крови: экспрессируют маркер активированных клеток CD69, причем экспрессия стабильна в течение жизни при взрослении и старении и характерна для всех нелимфоидных тканей. Но вдобавок CD69 колокализуется с маркером CD103, который обозначает группу молекул адгезии — интегринов, способствующих прикреплению резидентной Т-клетки к эпителию и к фибробластам в подслизистой выбранного органа. Для эффекторных Т-клеток во вторичных лимфоидных органах экспрессия интегринов CD103 совершенно нехарактерна: TEM-клетки постоянно сохраняют подвижный фенотип.
У карты, составленной коллективом Донны Фарбер, есть крупный недочет: неясно, насколько чисто удается выделить Т-лимфоциты из органа, какую долю анализируемых клеток на самом деле составляют Т-лимфоциты крови из капилляров внутри органа.
Особенно остро вопрос загрязнения клетками крови стоит для легких — неслучайно субпопуляционный состав Т-клеток легких неожиданно похож на Т-клетки крови и лимфоузлов. Вопрос загрязнения клетками крови был изящно решен для Т-лимфоцитов мыши: подопытных животных заражали вирусом лимфоцитарного хориоменингита после пересадки трансгенного клона Т-клеток P14, специфичного к данному вирусу. В результате при инфекции большая часть циркулирующих клеток была представлена вирусоспецифичным клоном P14, а его присутствие в тканях можно было выявить с помощью флуоресцирующих антител к TCR P14. Мышам в кровь вводили антитело анти-CD8 к маркеру Т-киллерных клеток, оно быстро распространялось по кровотоку и связывалось со всеми Т-киллерами в крови (но не в тканях). При микроскопии срезов органов легко было отличить резидентные киллерные TRM от только недавно вышедших из крови в орган клеток, помеченных анти-CD8 антителом []. Численность резидентных клеток, подсчитанная этим методом, в 70 раз превышала количество, определенное методом проточной цитометрии; разница меньше чем в два раза наблюдалась только для резидентных клеток лимфоузлов и селезенки. Получается, стандартные методики выделения лимфоцитов из органов плохо подходят для анализа киллерных резидентных клеток и существенно занижают размеры популяции.
Лимфоциты выше нормы у детей
У детей 4-5 дня и 4-5 года жизни в крови отмечается физиологический лимфоцитоз, не требующий лечения. Состояние ребенка при этом остается совершенно нормальным, лимфатические узлы не увеличиваются. Такая ситуация обусловлена перестройкой кроветворной системы ребенка.
Тем не менее, повышенное количество лимфоцитов у детей может быть вызвано:
- Лейкемией;
- Бронхиальной астмой;
- Инфекцией: грипп, ОРВИ, ангина и прочие;
- Гнойно-воспалительными процессами;
- Вирусным заболеванием: лишай, коклюш, малярия, ветряная оспа (ветрянка), корь, вирусный гепатит и другие.
Повышены лимфоциты могут быть и при протекании других заболеваний, при различных индивидуальных особенностях организма. Точные причины можно определить только после проведения полного обследования.
Использованная литература
- Хаитов, Р.М. Аллергология и иммунология : национальное руководство / под ред. Р.М. Хаитова, Н.И. Ильиной. — М. : ГЭОТАР-Медиа, 2009. — 656 с.
- Майоров, Р.В., Нусинов, Е.В. Методы оценки иммунного статуса. Рекомендации для студентов, 2012.
- Гистология (введение в патологию» / под ред. Э.Г. Улумбекова, Ю.А. Челышева. — М. : ГЭОТАР-Медиа, 1997. — С. 527-545.
- Serrano-Villar, S., Deeks, S. CD4/CD8 ratio: an emerging biomarker for HIV. Lancet HIV, 2015. — Vol. 2. — P. 76-7.
- Castilho, J., Shepherd, B. CD4+/CD8+ ratio, age, and risk of serious noncommunicable diseases in HIV infected adults on antiretroviral therapy. AIDS, 2021. — Vol. 30. — P. 899–908.
- Leach, М., Drummond, М., Doig, A. Practical Flow Cytometry in Haematology Diagnosis Hardcover. WILEY-BLACKWELL, 2013.
- Tietz Clinical guide to laboratory tests. 4-th ed. Ed. Wu A.N.B. – USA: W.B Sounders Company, 2006. — 1798 p.
Что делать, когда в анализе крови высокие лимфоциты
Если лимфоциты повышены, что делать в этом случае? Ответ может быть только один: выявлять и устранять причину этого состояния. Когда лимфоциты повышены, лечение должно быть направлено не на снижение их уровня, а на саму болезнь.
В зависимости от заболевания терапия занимает от нескольких дней до нескольких месяцев и обычно способствует стабилизации уровня лимфоцитов. К примеру, при большинстве инфекционных процессов назначаются противовоспалительные, жаропонижающие, противовирусные препараты, а также антибиотики. Курс лечения миеломы и лейкоза весьма своеобразен и нередко требует химиотерапии и трансплантации костного мозга.
Особенности лимфоцитоза
Термин указывает на нарушения в работе женского организма, активности иммунитета для борьбы с проникшими:
- бактериями, вирусами;
- простейшими, паразитами.
К иным причинам увеличенной концентрации лимфоцитов становится их повреждение или гибель на фоне:
- ожоговой болезни;
- некроза тканей;
- воспалительных процессов;
- аллергий;
- аутоиммунных болезней;
- онкологических патологий.
Клетки достигают проблемных очагов, но при дальнейшем прогрессировании заболеваний начинают массово погибать.
Хроническая форма лимфоцитоза является результатом болезней крови или системы кроветворения, лимфатического отдела. Тельца полностью не вызревают и не могут полноценно выполнять возложенные на них функции. Для нормализации балансам костным мозгом продуцируется еще больше лимфоцитов, но пользы от усиленной работы минимум.
Скопление клеток-защитников может быть обусловлено проблемами их утилизации в селезенке. Врачи считают, что наибольшую важность представляют не отклонения в анализах, а источники их возникновения. Дисфункция иммунной системы приводит к развитию инфекций хронического типа, аутоиммунных болезней с атаками на собственные клетки, формированию и дальнейшему размножению атипичных структурных единиц.
Жизненный цикл Т-лимфоцита
Каждая Т-клетка после сборки Т-клеточного рецептора проходит тестирование на функциональность случайно собранного рецептора (положительная селекция) и отсутствие специфичности к собственным антигенам организма (отрицательная селекция), то есть на отсутствие очевидной аутоиммунной угрозы. Этапы селекции происходят в вилочковой железе, тимусе; при этом более 90% клеток-предшественников погибает, не сумев правильно собрать рецептор либо пройти селективный отбор. Выжившие Т-клетки пролиферируют и выходят из тимуса в кровоток — это наивные Т-лимфоциты, не встречавшиеся с антигеном. Наивная Т-клетка циркулирует по крови и периодически заходит в лимфоузлы, где в Т-клеточной зоне контактирует со специализированными антигенпрезентирующими клетками.
После встречи с антигеном в лимфоузле Т-клетка приобретает способность снова делиться — становится предшественницей Т-клеток памяти (TSCM, stem cell memory T cells). Cреди клона её потомков появляются клетки центральной памяти (TCM), короткоживущие эффекторные клетки, осуществляющие иммунную реакцию (SLEC или TEMRA-клетки), и эффекторные клетки-предшественники памяти TEM, в свою очередь при делении дающие TEMRA[3]. Все эти клетки выходят из лимфоузла и перемещаются по крови. Эффекторные клетки затем могут выйти из кровотока для осуществления иммунной реакции в периферической ткани органа, где находится патоген. Что потом — снова путешествие по крови и лимфоузлам?
Рисунок 1. Эмиграция эффекторной Т-клетки в ткань при вирусной инфекции. Сигналы воспаления от зараженных эпителиальных клеток при участии резидентных клеток передаются эндотелию сосудов, клетки эндотелия привлекают эффекторные Т-клетки хемокинами CXCL9, CXCL10. Роллинг: при движении по посткапиллярной венуле в ткани эффекторная клетка замедляется, образуя временные контакты между Е-селектинами и P-селектинами на клетках эндотелия. Остановка: эффекторная клетка плотно прикрепляется к эндотелию при взаимодействии LFA-1 и других альфа-интегринов с ICAM-1/VCAM-1/MAdCAM-1 (на эндотелии). Трансмиграция: эффекторная Т-клетка связывает эндотелиальный JAM-1 молекулами PECAM, CD99, LFA-1 и проникает через клетки эндотелия в подслизистую. Рисунок из [3].
Процесс трансмиграции лейкоцита.
Клетки стромы, то есть основы лимфоузла, выделяют сигнальные вещества для того, чтобы позвать Т-клетку в лимфоузел — хемокины. Распознают хемокины лимфоузлов рецепторы хоуминга CCR7 и CD62L. Но на эффекторных клетках отсутствуют оба этих рецептора. Из-за этого долгое время было загадкой, как эффекторные клетки могут попасть из периферической ткани обратно во вторичные лимфоидные органы — селезенку и лимфоузлы.
В то же время стали накапливаться данные о различиях в репертуарах мембранных маркеров и профилях транскрипции между Т-клетками памяти в крови (TEM) и Т-клетками памяти в других органах, которые никак не укладывались в концепцию постоянной миграции Т-клеток между тканями и кровью. Решено было выделить новую субпопуляцию: резидентные клетки памяти, которые населяют определенный орган и не рециркулируют — TRM-клетки [4].
Рисунок 2. Схема перехода потомков активированных Т-лимфоцитов между популяциями. Рисунок из [14].