Синдром ранней реполяризации желудочков — что это такое. Общие сведения
Специфический кардиологический синдром обнаруживается не только у пациентов с патологией сердца, но и у абсолютно здоровых людей. Ранняя реполяризация желудочков это и есть синдром преждевременной реполяризации. Очень часто ошибочно синдром WPW путают с преждевременной реполяризацией, несмотря на то, что это совершенно разные патологии.
Патологические изменения на ЭКГ в течение длительного времени считались вариантом нормы, пока не выявилась чёткая взаимосвязь с нарушениями сердечного ритма. Заболевание протекает бессимптомно, что значительно затрудняет своевременную диагностику.
Для синдрома ранней (преждевременной, ускоренной) реполяризации желудочков сердца характерны специфические изменения на электрокардиограмме при отсутствии явных причин. Код по МКБ-10: I45.6
Лечение синдрома ранней реполяризации желудочков
Специфического лечения синдром реполяризации не требует. Единственное, что предлагается пациенту – это наблюдение у кардиолога.
Тем не менее, человеку с СРРЖ необходимо исключить употребление алкоголя и интенсивные физические нагрузки, чтобы не спровоцировать приступ тахикардии.
В некоторых случаях производят радиочастотную аблацию дополнительного пучка инвазивным способом (катетер подводится к месту пучка и уничтожает его).
Иногда применяют энерготропную терапию (витамины группы В, карнитин, препараты фосфора и магния, мексидол, кудесан), антиаритмические препараты (амиодарон).
Важно! Пациенту следует сохранять все прежние ЭКГ, что требуется для исключения диагноза инфаркта миокарда при возникновении болей в сердце.
Патогенез
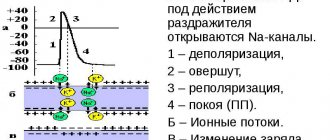
Сокращение камер сердца происходит в результате изменений электрического заряда в клетках миокарда – кардиомиоцитах. В результате ионы натрия, кальция и калия переходят в межклеточное пространство и обратно. Процесс осуществляется поочередно сменяющими друг друга основными фазами:
- деполяризация – сокращение;
- реполяризация желудочков это расслабление перед новым сокращением.
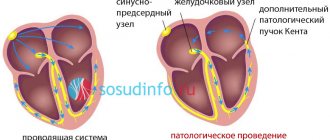
Ранняя реполяризация желудочков формируется в результате неправильного проведения импульса по проводящей системе сердца от предсердий к желудочкам. Для передачи электрического импульса активируются аномальные пути проведения. Развитие феномена обусловлено дисбалансом между реполяризацией и деполяризацией в базальных отделах, верхушке сердца. Характерно значительное сокращение периода расслабления миокарда. На ЭКГ часто вместе с СРРЖ регистрируется нарушение процессов реполяризации в миокарде, в частности – нарушение реполяризации нижней стенки левого желудочка.
Деполяризация и реполяризация
В разделе «Основные принципы электрокардиографии и нарушения» рассматривается общее понятие «электрическое возбуждение», которое означает распространение электрических импульсов по предсердиям и желудочкам. Точное название электрического возбуждения, или активации сердца, – деполяризация. Возврат кардиомиоцитов к состоянию расслабления после возбуждения (деполяризации) – реполяризация. Эти термины подчёркивают, что в состоянии покоя клетки миокарда предсердий и желудочков поляризованы (их поверхность электрически заряжена). На рисунке 2-1, А изображено состояние поляризации нормальной мышечной клетки предсердий или желудочков
Рис. 2-1. Процессы деполяризации и реполяризации А – мышечная клетка сердца в состоянии покоя поляризована, т.е. наружная поверхность клетки заряжена положительно, а внутренняя – отрицательно; Б — при возбуждении клетки (S) происходит её деполяризация (возбуждённый участок электроотрицателен по отношению к соседним участкам); В – полностью деполяризованная клетка заряжена положительно внутри и отрицательно – снаружи; Г – реполяризация происходит, когда клетка возвращается из состояния возбуждения в состояние покоя. Направление деполяризации и реполяризации указано стрелками. Деполяризации (возбуждению) предсердий на ЭКГ соответствует зубец Р, а деполяризации желудочков – комплекс QRS. Реполяризации желудочков соответствует комплекс ST-T.
Внешняя сторона клетки в состоянии покоя заряжена положительно, а внутренняя сторона – отрицательно [около -90 мВ (милливольт)]. Поляризация мембраны обусловлена разницей концентраций ионов внутри и вне клетки.
При возбуждении мышечной клетки сердца происходит её деполяризация. В результате внешняя сторона клетки в области возбуждения становится отрицательной, а внутренняя сторона – положительной. Возникает разница электрического напряжения на внешней поверхности мембраны между деполяризованным участком в состоянии возбуждения и невозбуждённым поляризованным участком см. рис. 2-1, Б. Затем возникает небольшой электрический ток, который распространяется вдоль клетки до её полной деполяризации см. рис. 2-1, В.
Направление деполяризации показано стрелкой см. рис. 2-1, Б. Деполяризация и реполяризация отдельных мышечных клеток (волокон) происходит в одном направлении. Однако во всём миокарде деполяризация идёт от внутреннего слоя (эндокардиального) к наиболее удалённому слою (эпикардиальному), а реполяризация – в противоположном направлении. Механизм этого различия до конца не ясен.
| Примечание: Деполяризация миокарда желудочков происходит от эндокарда к эпикарду, а реполяризация – от эпикарда к эндокарду. Это обусловлено тем, что длительность ТМПД в субэпикардиальных отделах желудочков на 0,03-0.04 с меньше, чем в субэндокардиальных отделах, и процесс реполяризации раньше начнётся именно под эпикардом. | |
Деполяризующий электрический ток регистрируют на электрокардиограмме в виде зубца Р (возбуждение и деполяризация предсердий) и комплекса QRS (возбуждение и деполяризация желудочков).
Через некоторое время полностью охваченная возбуждением деполяризованная клетка начинает возвращаться к состоянию покоя. Этот процесс называют реполяризацией. Небольшой участок на внешней стороне клетки вновь приобретает положительный заряд см. рис. 2-1, Г, затем процесс распространяется вдоль клетки до её полной реполяризации. Реполяризации желудочков на электрокардиограмме соответствуют сегмент ST, зубцы и (реполяризация предсердий обычно скрыта потенциалами желудочков).
На электрокардиограмме отражена электрическая активность всех клеток предсердий и желудочков, а не отдельных клеток. В сердце деполяризация и реполяризация обычно синхронизированы, поэтому на электрокардиограмме можно записать эти электрические потоки в виде определённых зубцов (зубцы P, T, U, комплекс QRS, сегмент ST).
| Любая электрокардиограмма – и нормальная, и патологически изменённая – отражает два основных процесса: деполяризацию – распространение импульса по миокарду – и реполяризацию – возвращение возбуждённого миокарда в состояние покоя. | |
Классификация
У детей и взрослых синдром ранней реполяризации желудочков может иметь 2 варианта развития:
- без поражения сердечно-сосудистой системы;
- с поражением.
По характеру течения выделяют:
- преходящая форма;
- постоянная форма.
В зависимости от локализации ЭКГ признаков СРРЖ подразделяют на 3 типа.
- I характерные признаки наблюдаются у здорового человека. ЭКГ признаки регистрируются только в грудных отведениях V1, V2. Вероятность развития осложнений крайне низкая.
- II ЭКГ признаки регистрируются в нижнебоковых и нижних отделах, отведениях V4-V6. Риск развития осложнений повышен.
- III ЭКГ изменения регистрируются во всех отведениях. Риск развития осложнений самый высокий.
Диагностика
Так как данный синдром является электрокардиографическим феноменом, установить его можно только при определенном обследовании:
- ЭКГ;
- УЗИ сердца (эхокардиография): стресс-эхокардиография (на предмет нарушения сократительной способности желудочков)
- эхокардиография покоя;
Помимо этого, проводят тесты на велоэргометре или тредмиле: после физической нагрузки частота сердечных сокращений повышается, и ЭКГ-признаки СРРЖ исчезают.
Используют пробу с калием: после приема хлорида калия, панангина или ритмокора не меньше 2-х грамм выраженность ЭКГ-признаков синдрома реполяризации усиливается.
Пробу с изопротеренолом и атропином не применяют из-за выраженных побочных явлений.
Важно разграничить СРРЖ и инфаркт миокарда, перикардит, синдром Бругада. С этой целью проводят дифференциальную диагностику.
Причины
Достоверные причины изучены не до конца. Существуют только гипотезы возникновения ранней реполяризации:
- Генетическая предрасположенность. Мутация генов, которые отвечают за балансирование процессов поступления определённых ионов в клетку и выход их наружу.
- Нарушение процессов сокращения и расслабления отдельных участков миокарда, что характерно при синдроме Бругада I типа.
- Изменение потенциалов действия кардиомиоцитов. Процесс связан с механизмом выхода из клеток ионов калия. Сюда же относится повышенная восприимчивость к сердечному приступу при ишемии.
Согласно статистике, синдром ускоренной реполяризации характерен для 3-10% здоровых людей самых разных возрастов. Чаще всего изменения регистрируются у молодых лиц в возрасте 30 лет, у лиц, ведущих здоровый образ жизни и у спортсменов.
Неспецифические факторы, влияющие на развития синдрома ранней реполяризации желудочков:
- врождённая форма гиперлипидемии, которая провоцирует развитие атеросклеротических изменений;
- длительное применение определённых медикаментов, либо передозировка ими (например, бета-адреномиметики);
- дисплазия соединительной ткани, для которой характерны дополнительные хорды в полости желудочков;
- высокий уровень холестерина в крови;
- электролитный дисбаланс;
- нейроэндокринные изменения;
- гипертрофическая кардиомиопатия;
- пороки сердца: врождённые, приобретённые;
- нарушения в работе вегетативной нервной системы;
- переохлаждение организма;
- чрезмерные физические нагрузки.
Синдром преждевременного возбуждения желудочков.
Нарушения ритма сердца считаются важной кардиологической проблемой, поскольку нередко осложняют течение и ухудшают прогноз многих заболеваний и являются одной из самых частых причин внезапной смерти.
Особый интерес как клиницистов, так и электрофизиологов вызывает синдром преждевременного возбуждения желудочков (СПВЖ), который в одних случаях, при отсутствии клинических проявлений, может быть электрокардиографической находкой, а в других – сопровождаться опасными для жизни тахиаритмиями.
Несмотря на успехи, достигнутые в изучении СПВЖ, вопросы его диагностики, тактики ведения больных и лечения остаются актуальными и в настоящее время.
Определение. Классификация
СПВЖ (синдром предвозбуждения, преэкситации, preexcitation syndrome) – это ускоренное проведение импульса возбуждения от предсердий к желудочкам по дополнительным аномальным проводящим путям. В результате часть миокарда или весь миокард желудочков начинают возбуждаться раньше, чем при обычном распространении возбуждения по атриовентрикулярному узлу, пучку Гиса и его ветвям.
Согласно рекомендациям группы экспертов ВОЗ (1980) преждевременное возбуждение желудочков, не сопровождающееся клинической симптоматикой, называют «феноменом предвозбуждения», а в случае, когда имеются не только электрокардиографические признаки предвозбуждения, но и развиваются пароксизмы тахиари.
Анатомическим субстратом СПВЖ служат пучки специализированных мышечных волокон вне проводящей системы сердца, способные проводить электрические импульсы к разным участкам миокарда, вызывая их преждевременное возбуждение и сокращение.
Дополнительные предсердно-желудочковые соединения классифицируют по их расположению относительно фиброзных колец митрального или трикуспидального клапанов, типу проводимости (декрементный тип – нарастающее замедление проведения по дополнительному пути в ответ на увеличение частоты стимуляции – или недекрементный), а также по их способности на антеградное, ретроградное или сочетанное проведение. Обычно дополнительные проводящие пути имеют быстрое недекрементное проведение, аналогичное таковому в нормальной ткани проводящей системы Гиса–Пуркинье и миокарда предсердий и желудочков.
В настоящее время известно несколько видов аномальных проводящих путей (трактов):
- предсердно-желудочковый (Кента), соединяющий миокард предсердий и желудочков в обход атриовентрикулярного узла;
- атрионодальный (Джеймса), расположенный между синоатриальным узлом и нижней частью атриовентрикулярного узла;
- нодовентрикулярный (Махейма), связывающий атриовентрикулярный узел (или начало пучка Гиса) с правой стороной межжелудочковой перегородки или разветвлениями правой ножки пучка Гиса;
- атриофасцикулярный (Брешенмаше), соединяющий правое предсердие с общим стволом пучка Гиса.
Существуют также и другие дополнительные пути проведения, в том числе «скрытые», способные проводить электрический импульс ретроградно от желудочков к предсердиям. У небольшой (5–10 %) части больных имеется несколько аномальных путей проведения.
В клинической практике выделяют:
- синдром Вольфа–Паркинсона–Уайта (синдром WPW), обусловленный наличием пучков Кента;
- синдром Клерка–Леви–Кристеско (синдром CLC, синдром укороченного интервала Р-Q (R)), обусловленный наличием пучка Джеймса.
Электрокардиографические проявления СПВЖ зависят от степени преэкситации и постоянства проведения по дополнительным путям. В связи с этим выделяют следующие варианты синдрома:
- манифестный СПВЖ (на ЭКГ постоянно имеются признаки предвозбуждения);
- интермиттирующий (преходящий) СПВЖ (на ЭКГ признаки предвозбуждения имеют преходящий характер);
- латентный СПВЖ (ЭКГ в обычных условиях нормальная, признаки предвозбуждения появляются только в период пароксизма тахикардии или при провокации – физической нагрузке, электрофизиологическом исследовании (ЭФИ), вагусных или медикаментозных пробах);
- скрытый (на стандартной ЭКГ изменения не выявляются из-за проведения возбуждения по дополнительным путям только ретроградно).
Распространенность
По разным данным, распространенность СПВЖ в общей популяции составляет примерно 0,15 %. При этом пароксизмы тахиаритмий возникают у каждого второго пациента (в 80–85 % случаев – ортодромная тахикардия, 20–30 % – фибрилляция предсердий (ФП), 5–10 % – трепетание предсердий и антидромная тахикардия). Скрытый СПВЖ выявляют у 30–35 % больных.
СПВЖ – это врожденная аномалия, но клинически может проявиться в любом возрасте, спонтанно или после какого-либо заболевания. Обычно данный синдром манифестирует в молодом возрасте. В большинстве случаев иной патологии сердца у пациентов нет. Однако описываются сочетания СПВЖ с аномалией Эбштейна, кардиомиопатиями, пролапсом митрального клапана. Существует предположение о наличии взаимосвязи между СПВЖ и дисплазией соединительной ткани.
В семьях больных, страдающих этим синдромом, был выявлен аутосомно-доминантный тип наследования дополнительных проводящих путей у родственников I, II, III степени родства с различными клинико-электрокардиографическими проявлениями.
Частота случаев внезапной смерти у пациентов с СПВЖ составляет 0,15–0,6 % в год. Почти в половине случаев остановка сердца у лиц с СПВЖ – его первое проявление.
Исследования больных с СПВЖ, перенесших остановку сердца, ретроспективно определили ряд критериев, с помощью которых можно выявить лиц с повышенным риском внезапной смерти. К ним относят наличие следующих признаков:
- укороченного интервала R-R – менее 250 мс во время спонтанной или индуцированной ФП;
- симптоматической (гемодинамически значимой) тахикардии в анамнезе;
- множественных дополнительных путей;
- аномалии Эбштейна.
История
ЭКГ с укороченным интервалом P-Q и одновременно уширенным комплексом QRS впервые описали A. Cohn и F. Fraser в 1913 г. Единичные подобные случаи были описаны в последующем и некоторыми другими авторами, однако в течение многих лет причиной такой картины ЭКГ считалась блокада ветвей пучка Гиса.
В 1930 г. L. Wolff, J. Parkinson и P. White представили доклад, в котором электрокардиографические изменения такого типа рассматривали как причину пароксизмальных нарушений ритма сердца. Эта работа дала основание для проведения всесторонних исследований, направленных на выяснение патогенеза указанных изменений на ЭКГ, названных в последующем синдромом Вольфа–Паркинсона–Уайта.
Спустя два года M. Holzman и D. Scherf предположили, что в основе синдрома WPW лежит распространение импульса возбуждения по дополнительным предсердно-желудочковым путям. В 1942 г. F. Wood предоставил первое гистологическое подтверждение наличия мышечного соединения между правым предсердием и правым желудочком, выявленного при аутопсии больного 16 лет с эпизодами пароксизмальной тахикардии в анамнезе.
Несмотря на эти данные, активный поиск альтернативных механизмов развития синдрома продолжался до 1970-х, когда ЭФИ и хирургические методы лечения подтвердили теорию дополнительных проводящих путей.
Патогенез
Проведение импульсов от предсердий к желудочкам при СПВЖ происходит одновременно по нормальной проводящей системе сердца и по дополнительному пути. В проводящей системе на уровне атриовентрикулярного узла всегда наблюдается некоторое замедление проведения импульсов, не характерное для аномального тракта. В результате этого деполяризация определенного участка миокарда желудочков начинается преждевременно еще до распространения импульса по нормальной проводящей системе.
Степень предвозбуждения зависит от соотношения скоростей проведения в нормальной проводящей системе сердца, прежде всего в атриовентрикулярном узле, и в дополнительном пути проведения. Увеличение скорости проведения по дополнительному проводящему пути или замедление скорости проведения по атриовентрикулярному узлу приводят к повышению степени предвозбуждения желудочков. В некоторых случаях деполяризация желудочков может быть целиком обусловлена проведением импульсов по дополнительному пути. В то же время при ускорении проведения импульсов по атриовентрикулярному узлу или замедлении проведения по дополнительному пути степень аномальной деполяризации желудочков снижается.
Основное клиническое значение дополнительных путей проведения состоит в том, что они нередко включаются в петлю кругового движения волны возбуждения (re-entry) и способствуют таким образом возникновению наджелудочковых пароксизмальных тахиаритмий.
При СПВЖ чаще всего встречается ортодромная реципрокная наджелудочковая тахикардия, при которой импульс проводится антеградно по атриовентрикулярному узлу, а ретроградно – по дополнительному проводящему пути. Пароксизм ортодромной наджелудочковой тахикардии характеризуется частыми (140–250 в 1 мин), лишенными признаков преэкситации нормальными (узкими) комплексами QRS. В ряде случаев после комплекса QRS наблюдаются инвертированные зубцы Р, что указывает на ретроградную активацию предсердий.
При антидромной наджелудочковой тахикардии импульс циркулирует в противоположном направлении: антеградно – по аномальному проводящему пути, ретроградно – по атриовентрикулярному узлу. Пароксизм антидромной наджелудочковой тахикардии у больных с СПВЖ проявляется на ЭКГ частым регулярным ритмом (150–200 в 1 мин) с желудочковыми комплексами по типу максимально выраженной преэкситации (QRS і 0,11 с), после которых иногда выявляются инвертированные зубцы Р.
У 20–30 % пациентов с СПВЖ возникают пароксизмы ФП, при которых в результате антеградного проведения по дополнительному пути большого числа предсердных импульсов частота сокращений желудочков (ЧСЖ) может превышать 300 в 1 мин.
Клиника
Во многих случаях СПВЖ протекает бессимптомно и выявляется только электрокардиографически. У 50–60 % больных имеются жалобы на приступы сердцебиений, одышку, боль или дискомфорт в груди, чувство страха и обмороки. Особую опасность при СПВЖ приобретают пароксизмы ФП, поскольку они сопровождаются большой ЧСЖ, гемодинамическими нарушениями и нередко могут трансформироваться в фибрилляцию желудочков. В таких случаях у больных не только наблюдают синкопальные состояния, но и имеется высокий риск внезапной смерти.
Независимыми факторами риска развития ФП у пациентов с СПВЖ являются возраст, мужской пол и наличие в анамнезе синкопальных состояний.
Диагностика
Основным методом диагностики СПВЖ является ЭКГ.
При синдроме WPW на фоне синусового ритма выявляют укорочение интервала P-Q (<0,12 с) и D-волну (пологий наклон в первые 30–50 мс) на восходящей части зубца R или нисходящей части зубца Q, комплекс QRS обычно расширен (і0,11 с). Характерно также отклонение сегмента SТ и зубца Т в сторону, противоположную D-волне и основному направлению комплекса QRS.
Электрокардиографическими признаками синдрома CLC являются укорочение интервала P-Q (R), продолжительность которого не превышает 0,11 с, отсутствие в составе комплекса QRS дополнительной волны возбуждения – D-волны, наличие неизмененных (узких) и недеформированных комплексов QRS (за исключением случаев сопутствующей блокады ножек или ветвей пучка Гиса).
При СПВЖ, обусловленном функционированием пучка Махейма, определяется нормальный интервал P-Q при наличии D-волны.
Одновременное функционирование пучков Джеймса и Махейма приводит к появлению на ЭКГ признаков, характерных для синдрома WPW (укорочение интервала P-Q (R) и наличие D-волны).
В связи с распространением в последние годы хирургических методов лечения больных с СПВЖ (деструкция аномального пучка) постоянно совершенствуются способы точного определения его локализации.
На ЭКГ местоположение пучка Кента обычно определяют по направлению начального моментного вектора деполяризации желудочков (первых 0,02–0,04 с), который соответствует времени формирования аномальной D-волны. В тех отведениях, активные электроды которых располагаются непосредственно над участком миокарда, возбуждающимся аномально за счет пучка Кента, регистрируется отрицательная D-волна. Это указывает на распространение раннего аномального возбуждения в сторону от активного электрода данного отведения.
Особый практический интерес представляют возможности метода пространственной вектор-электрокардиографии, позволяющего с высокой точностью установить локализацию дополнительных проводящих путей.
Более подробную, по сравнению с данными ЭКГ, информацию о местоположении дополнительных путей проведения можно получить с помощью магнитокардиографии.
Однако наиболее достоверными и точными являются методы внутрисердечного ЭФИ, в частности эндокардиальное (предоперационное) и эпикардиальное (интраоперационное) картирование. При этом с помощью сложной методики определяют область наиболее ранней активации (предвозбуждения) миокарда желудочков, которая соответствует локализации дополнительного аномального пучка.
Лечение
У больных с бессимптомным течением СПВЖ лечения обычно не требуется. Исключение составляют лица, в семейном анамнезе которых были случаи внезапной смерти, спортсмены и те, чья работа связана с опасностью для самих себя и окружающих (например, водолазы и летчики).
При наличии пароксизмов наджелудочковой тахикардии лечение заключается в купировании приступов и их профилактике с помощью различных медикаментозных и немедикаментозных методов. При этом важное значение имеет характер аритмии (орто-, антидромная тахикардия, ФП), ее субъективная и объективная переносимость, ЧСЖ, а также наличие сопутствующих органических заболеваний сердца.
При ортодромной реципрокной наджелудочковой тахикардии импульс возбуждения проводится антеградно нормальным путем, поэтому ее лечение должно быть направлено на угнетение проводимости и блокаду импульсов в атриовентрикулярном узле. С этой целью используют рефлекторные вагусные пробы, которые наиболее эффективны при возможно более раннем применении.
Препаратом первого ряда для купирования ортодромной реципрокной наджелудочковой тахикардии считают аденозин, потенциальным недостатком которого является преходящее повышение возбудимости предсердий, способное провоцировать их экстрасистолию и фибрилляцию сразу же после купирования пароксизма такой тахикардии. Другим средством выбора для купирования ортодромной тахикардии при отсутствии выраженной артериальной гипотензии и тяжелой систолической сердечной недостаточности принято считать верапамил. В качестве препаратов второго ряда обычно используют b-адреноблокаторы.
При неэффективности этих средств применяют новокаинамид с целью блокады проведения через добавочный атриовентрикулярный путь. По своей безопасности и эффективности новокаинамид является препаратом выбора при лечении тахикардии с широкими комплексами QRS, когда диагноз ортодромной реципрокной наджелудочковой тахикардии вызывает сомнения.
Препаратами резерва являются амиодарон, соталол и антиаритмические препараты (ААП) 1С класса: пропафенон или флекаинид.
При антидромной реципрокной наджелудочковой тахикардии импульс проводится ретроградно через атриовентрикулярный узел, поэтому применение верапамила, дилтиазема, лидокаина и сердечных гликозидов для ее купирования противопоказано в связи со способностью данных препаратов ускорять антеградное проведение по добавочному пути и тем самым увеличивать ЧСЖ. Применение этих средств, а также аденозина может провоцировать переход антидромной наджелудочковой тахикардии в ФП. Препаратом выбора для купирования такой тахикардии является новокаинамид, при неэффективности которого используют амиодарон или ААП 1С класса.
При возникновении пароксизма ФП основной целью медикаментозной терапии является контроль частоты ритма желудочков и замедление проводимости одновременно по добавочному пути и АВ узлу. Препаратом выбора в таких случаях также является новокаинамид. Высокоэффективно и внутривенное введение амиодарона и ААП 1С класса.
Следует отметить, что применение верапамила, дигоксина и b-адреноблокаторов при ФП с целью контроля ЧСЖ у лиц с СПВЖ противопоказано из-за их способности увеличивать скорость проведения по добавочному пути. Это может перенести фибрилляцию с предсердий на желудочки.
Для профилактики пароксизмов наджелудочковых тахиаритмий, обусловленных наличием дополнительных проводящих путей, используют ААП IА, IС и III классов, обладающие свойством замедлять проведение по аномальным путям.
К немедикаментозным методам купирования приступов наджелудочковых тахиаритмий относят трансторакальную деполяризацию и предсердную (чреспищеводную или эндокардиальную) электрокардиостимуляцию, а для их профилактики – катетерную или хирургическую абляцию добавочных путей.
У больных с СПВЖ электрическую кардиоверсию применяют при всех формах тахикардии, которые сопровождаются выраженными нарушениями гемодинамики, а также при неэффективности медикаментозной терапии и в случаях, когда она вызывает ухудшение состояния больного.
Радиочастотная катетерная абляция добавочных путей является в настоящее время основным методом радикального лечения СПВЖ. Показаниями к ее выполнению являются высокий риск внезапной смерти (прежде всего наличие пароксизмов ФП), неэффективность или плохая переносимость медикаментозной терапии и профилактики приступов наджелудочковой тахикардии, а также нежелание больного принимать ААП. В случае выявления короткого эффективного рефрактерного периода аномального тракта у лиц с редкими и нетяжелыми пароксизмами аритмии, вопрос о целесообразности абляции в целях профилактики внезапной смерти решается индивидуально.
Перед катетерной абляцией выполняется ЭФИ, цель которого – подтверждение наличия дополнительного проводящего пути, определение его электрофизиологических характеристик и роли в формировании тахиаритмии.
Эффективность радиочастотной катетерной абляции высока (достигает 95 %), а летальность, связанная с процедурой, не превышает 0,2 %. Наиболее частыми серьезными осложнениями данного метода лечения являются полная атриовентрикулярная блокада и тампонада сердца. Рецидивы проведения по дополнительному пути возникают приблизительно в 5–8 % случаев. Повторная радиочастотная абляция, как правило, полностью устраняет проведение по дополнительным путям.
В настоящее время область применения хирургической деструкции добавочных путей значительно сузилась. При тех же показаниях, что и к катетерной абляции, к хирургическому лечению прибегают в случаях невозможности выполнения последней по техническим причинам или ее безуспешности, а также при необходимости проведения операции на открытом сердце в связи с сопутствующей патологией.
Литература
- Сычев О.С. Нарушения ритма сердца // Руководство по кардиологии / Под ред. В.Н. Коваленко. – К.: Морион, 2008. – С. 1059-1248, 1215-1218.
- ACC/AHA/ESC 2006 Guidelines for the management of patients with atrial fibrillation // Circulation. – 2006. – № 114. – P. 257-354.
- ACC/AHA/ESC Guidelines for the management of patients with supraventricular arrhythmias – executive summary // JACC. – 2003. – № 8. – Р. 1493-1531.
- Griffin B., Topol E. Manual of Cardiovascular Medicine. – The Lippincott Williams & Wilkins, 2004. – P. 1248.
- Hanon S., Shapiro M., Schweitzer P. Early history of the preexcitation syndrome // Europace. – 2005. – № 7. – P. 28-33.
- Keating L., Morris А., Brady W.О. Electocardiographic Features of Wolff–Parkinson–White syndrome // Emerg. Med. J. – 2003. – № 20. – Р.491-493.
Н.Т. Ватутин, Н.В. Калинкина, Е.В. Ещенко.
Донецкий национальный медицинский университет им. М. Горького;
Институт неотложной и восстановительной хирургии им. В.К. Гусака АМН Украины.
Укркардіо
Симптомы
Клиническая симптоматика наблюдается только при той форме заболевания, которая сопровождается нарушениями в работе сердечно-сосудистой системы:
- потеря сознания, обморочные состояния;
- нарушения ритма (тахиаритмия, экстрасистолия, фибрилляция желудочков);
- ваготонический, гиперамфотонический, тахикардиальный, дистрофический формируются под влиянием гуморальных факторов на гипоталамо-гипофизарную систему;
- систолическая и диастолическая дисфункция сердца, вызванная её гемодинамическими нарушениями (отёк лёгких, гипертонический криз, одышка, кардиогенный шок).
Анализы и диагностика
Главные изменения регистрируются именно на электрокардиограмме. У некоторых пациентов параллельно наблюдаются клинические симптомы заболеваний сердечно-сосудистой системы, но чаще всего пациенты чувствуют себя абсолютно здоровыми и не отмечают никаких изменений.
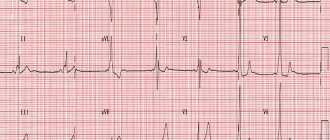
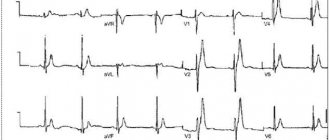
Синдром ранней реопляризации желудочков на ЭКГ:
- подъём сегмента ST над изолинией;
- выпуклость при подъёме сегмента ST обращена вниз;
- нарастание зубца R с параллельным уменьшением зубца S либо с его полным исчезновением;
- точка J находится выше изолинии, на уровне нисходящего колена зубца R;
- расширение комплекса QRS на ЭКГ;
- на нисходящем колене зубца R регистрируется «зазубрина».
Синдром ранней реполяризации желудочков у детей
Причины развития синдрома ранней реполяризации у детей могут самые разные:
- недосыпание и ненормированный режим дня;
- чрезмерная эмоциональная нагрузка;
- физические перегрузки;
- постоянная тревожность, стресс или нервное переутомление;
- замкнутость, отсутствие здорового эмоционального контакта с родителями;
- переохлаждение;
- некачественное и несбалансированное питание.
Подобный синдром может регистрироваться на ЭКГ у любого ребёнка, который слишком эмоционально реагирует на оценку своих знаний в школе, близко принимает к сердцу происходящие события, перегружается на внеклассовых занятиях. Отсутствие должного отдыха, усиленные занятия в спортивных секциях могут негативно сказаться на самочувствии ребёнка.
Прогноз. Чем опасен синдром ранней реполяризации желудочков сердца
Современные кардиологи работают на профилактику и предупреждение развития патологии, которая может привести к летальному исходу. Именно поэтому пациенты с синдромом ранней реполяризации желудочков должны регулярно наблюдаться у кардиолога для отслеживания динамики на ЭКГ и для выявления скрытых симптомов другой патологии. Опасен не сам синдром, а последствия, к которым он может привести при отсутствии должного лечения причинного заболевания.
Лицам, которые занимаются спортом, обследование рекомендуется проходить в специализированных физкультурных диспансерах, оценивая состояние до и после интенсивных тренировок, а также перед соревнованиями.
Чётких данных о переходе СРРЖ в серьёзную патологию нет. Риск летального исхода значительно возрастает при алкоголизме, злоупотреблении жирной пищей и при курении. Своевременное и полное грамотное обследование поможет выявить или исключить истинную причину и избежать проблем в будущем.