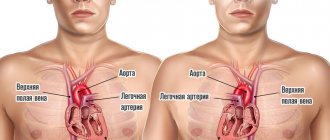
Наджелудочковая экстрасистолия (НЖЭС) – отклонение сердечного ритма от нормы, при котором возникают дополнительные сердечные импульсы. Вследствие такого процесса возникают внеочередные и неполноценные сокращения сердца. Чаще всего такая патология возникает у пациентов с проблемами сердца. В статье мы разберемся что это такое, чем опасно для жизни частое проявление и какие последствия влечет собой игнорирование симптомов.
Что собой представляет?
При наджелудочковой экстрасистолической аритмии источник распространения внеочередных сокращений локализуется над желудочками. При таком отклонении формируется очаг триггерной активности, посылающий периодические импульсы вне очереди. Код по МКБ-10 у данного нарушения 149.3.
Желудочковую и наджелудочковую экстрасистолию можно определить по выраженности симптоматики.
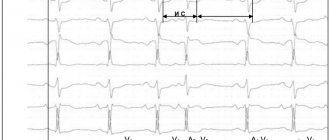
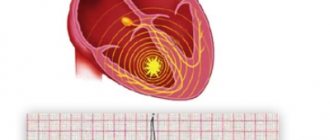
В первом случае она будет более интенсивной. Чтобы выявить характерные критерии и диагностировать признаки достаточно проведения стандартного ЭКГ (на фото). Диагностика наджелудочкового заболевания усложнена, так как на ЭКГ будет присутствовать широкий комплекс QRS.
Диагностика
Первое, на что следует обратить внимание при диагностике суправентрикулярной экстрасистолии, – это клинические признаки. Для этой патологии характерны неприятные ощущения в груди, которые вызывают существенный дискомфорт, но болью их назвать нельзя.
Чтобы подтвердить диагноз, пациент должен пройти ЭКГ и суточный мониторинг по Холтеру.
На ЭКГ суправентрикулярная экстрасистолия выглядит следующим образом:
- расширение и деформирование предсердного зубца Р раньше времени;
- вслед за зубцом Р идет нормальный желудочковый комплекс;
- компенсаторная пауза неполная;
- если происхождение экстрасистолы атриовентрикулярное, зубец Р может не определяться или наблюдаться после желудочкового комплекса.
Справка! Суправентрикулярная экстрасистолия на ЭКГ проявляется явно и не оставляет сомнений для постановки диагноза.
Классификация
Существует несколько классификаций наджелудочковой экстрасистолии. При месту нахождения очага возбуждения выделяются следующие разновидности:
- предсердные – верхние отделы сердца;
- антриовентрикулярные – перегородка между желудочками и предсердием.
В зависимости от частоты экстрасистол за 1 минуту: единичные (одиночные), множественные, групповые и парные. При единичном типе наблюдается до 5 дополнительных сокращений, при множественных – больше 5. Групповой вид предполагает сразу несколько экстрасистол, которые идут одна за другой, парный – 2 экстрасистолы идут подряд.
Можно выделить редкие и частые экстрасистолы.
Причины возникновения
Чаще всего наджелудочковая экстрасистолия возникает на фоне сердечных заболеваний. Однако, существует ряд других частых причин, которые могут спровоцировать развитие такого заболевания. К их числу относится:
- медикаментозное воздействие – не контролированный прием или передозировка мочегонных или антиаритмических лекарств;
- проблемы с электролитным обменом – низкая концентрация кальция, натрия и калия в крови;
- отравление или интоксикация – чрезмерное употребление алкоголя, негативное воздействие химикатов и курения, инфекционные болезни;
- болезни нервной системы – нейроциркуляторная дистония;
- эндокринные заболевания – сахарный диабет, повышенная или сниженная активность щитовидной железы, менопауза или начало менструации;
- неправильный образ жизни – частые стрессы, большие физические нагрузки, повышенная нервозность, низкая физическая активность.
Справка! В некоторых случаях причину развития патологического состояния установить невозможно.
Иногда экстрасистолы наджелудочкового типа возникают как самостоятельно заболевание, но это бывает очень редко – около 5-10% всех случаев. В 50% причина развития такого отклонения – присутствие сердечной патологии.
Архів
О. Й. Жарінов, В. О. Куць Національна медична академія післядипломної освіти ім. П. Л. Шупика МОЗ України
Шлуночкова екстрасистолія (ШЕ) — найбільш поширене порушення серцевого ритму, яке може істотно впливати на якість життя хворих, бути маркером структурно-функціональних змін міокарда та свідчити про небезпеку виникнення небезпечних для життя аритмій серця. Удосконалення стратегії ведення хворих із ШЕ насамперед пов’язане з розвитком концепції “стратифікації ризику”, тобто поділу пацієнтів на групи залежно від ступеня ризику смерті від усіх причин і, зокрема, раптової серцевої смерті (РСС). Крім того, активно впроваджуються сучасні інструментальні методи діагностики аритмій серця, передусім — амбулаторне моніторування ЕКГ. У клінічній практиці існує очевидна потреба у створенні узгоджених рекомендацій з ведення хворих з ШЕ, узагальненні діагностичних та терапевтичних підходів.
ЕТІОЛОГІЯ
Появу ШЕ можуть викликати будь-які структурні захворювання серця. Особливо часто її виявляють у хворих на гострий інфаркт міокарда (ІМ) та хронічну ІХС. Утім, екстрасистолія може виникати також при інших ураженнях міокарда, у тому числі субклінічних. У багатьох хворих з екстрасистолією доступними інструментальними методами дослідження не знаходять будь-яких ознак ураження серця.
Поширені причини та фактори, асоційовані з ШЕ:
- Хвороби міокарда, ендокарда та вінцевих артерій серця: ІХС, міокардити, міокардіофіброз, кардіоміопатії, вади серця, артеріальна гіпертензія або гіпотензія, серцева недостатність (СН);
- Електролітний дисбаланс (гіпокаліємія, гіперкаліємія, гіпомагніємія, гіпокальціємія), порушення кислотно-лужної рівноваги;
- Гіпоксія: захворювання легень, легенева гіповентиляція (наприклад, під час операції);
- Травматичні впливи: травма грудної клітки, операція на серці, катетеризація порожнин серця, травми головного і спинного мозку;
- Порушення вегетативної регуляції: нейроциркуляторна дистонія, неврози, діенцефаліт, симпатичні гангліоніти та трунцити, психоемоційне напруження;
- Патологічні рефлекси, зумовлені захворюваннями органів травлення (виразкова хвороба, жовчно-кам’яна хвороба, панкреатит, діафрагмальна кила, коліти й ентероколіти, особливо коли вони супроводжуються метеоризмом, запорами або порушеннями електролітного балансу); дистрофічні зміни в шийному і грудному відділах хребта (остеохондроз, спондилоартроз); хвороби бронхів та легень, особливо ті, що супроводжуються виснажливим кашлем; аденома простати;
- Діагностичні процедури: ендоскопія (бронхоскопія, гастроскопія, лапароскопія, цистоскопія, кольпоскопія, ректоскопія), пункція, масаж каротидного синуса, натискання на очні яблука, затримка дихання на глибокому вдиху;
- Алергія: харчова, медикаментозна, мікробна, професійна, побутова;
- Фармакодинамічна та токсична дія медикаментів, таких як серцеві глікозиди, хінідин, новокаїнамід, засоби для наркозу, морфін, глюкокортикоїди, препарати калію, кальцію, трициклічні антидепресанти, похідні фенотіазину, адреноміметики.
Основні електрофізіологічні механізми екстрасистолії — re-entrу (зворотний вхід збудження) та післядеполяризації. В основі виникнення екстрасистол можуть лежати також механізми асинхронного відновлення збудливості міокарда та патологічного автоматизму.
ОБСТЕЖЕННЯ ХВОРИХ
Обстеження хворих з ШЕ включає методи, які забезпечують діагностику порушення серцевого ритму, визначення клінічного та прогностичного значення аритмії, вибір лікування та оцінку його ефективності.
Анамнез.
При опитуванні хворого з’ясовують таку інформацію: суб’єктивні прояви аритмії (серцебиття, перебої в роботі серця, поштовхи або “завмирання” серця, дискомфорт у грудях, відчуття нестачі повітря, задишка, запаморочення, синкопальні стани), давність виникнення порушення ритму; фактори, що провокують аритмію (фізичне навантаження, психоемоційний стрес, певний час доби, положення тіла, прийом їжі, алкоголь, куріння); перенесені останнім часом захворювання; фонова кардіальна патологія; попередній прийом антиаритмічних препаратів (ААП).
Клінічне обстеження.
Виявлення аритмій при аускультації серця або при пальпації периферичних артерій; наявність клінічних ознак СН.
Лабораторні методи дослідження.
Визначення вмісту калію, натрію, креатиніну в сироватці крові, активності тиреотропного гормону.
ЕКГ.
Основні ЕКГ-ознаки шлуночкових екстрасистол (ШЕ):
- Передчасна поява розширеного та деформованого відносно основного ритму комплексу QRS без передуючого йому зубця Р, за винятком пізніх екстрасистол, перед якими реєструються зубці Р, що не мають електрофізіологічного зв’язку з ШЕ;
- Найчастіше — наявність повної компенсаторної паузи.
Форма ШЕ залежить не лише від локалізації джерела екстрасистолії, а й від швидкості та шляху поширення імпульсу у шлуночках. Тому ЕКГ дає змогу орієнтовно встановити розміщення ектопічного вогнища за морфологією екстрасистолічного комплексу. Якщо ШЕ має вигляд блокади правої ніжки і лівої передньої гілки пучка Гіса, її джерело міститься в системі лівої задньої гілки пучка Гіса, тобто в задній стінці лівого шлуночка; якщо ШЕ має вигляд блокади правої ніжки і задньої нижньої гілки пучка Гіса, її джерело розміщене в лівій передній гілці пучка Гіса; якщо ШЕ має вигляд повної блокади лівої ніжки пучка Гіса, то її джерело — у правій ніжці пучка Гіса. Комплекс QRS лівошлуночкової екстрасистоли у правих грудних відведеннях має моно- або біфазну форму: R, qR, RR’, RS, Rs а в лівих — rS або QS. Комплекс QRS правошлуночкової екстрасистоли у правих грудних відведеннях має форму rS або QS, а в лівих — R (табл. 1). Якщо ШЕ виникає в ділянці міжшлуночкової перегородки, як звичайно, її тривалість і форма незначно відрізняються від комплексу QRS основного ритму. Форма QRS типу rSR’ у відведенні V1 характерна для екстрасистоли з лівої половини міжшлуночкової перегородки, а тип R або qR у відведенні V6 — для екстрасистол з правої половини перегородки. Спрямованість комплексу QRS екстрасистолічного комплексу у всіх грудних відведеннях уверх дозволяє припустити локалізацію джерела ШЕ в базальних відділах серця, а спрямованість комплексу QRS униз — у ділянці верхівки. У складних для топічної діагностики випадках точне джерело екстрасистоли не вказують, обмежившись висновком про наявність ШЕ.
Таблиця 1. Характерні форми комплексів ШЕ у грудних відведеннях ЕКГ при базальній, проміжній та верхівковій їх локалізації
| Локалізація екстрасистол | Форми комплексів ШЕ у відведеннях ЕКГ | ||||||
| V1 | V2 | V3 | V4 | V5 | V6 | ||
| Правошлуночкові | Базальні | Rs, RS | RS | R | R | R | R |
| Проміжні | rS, QS | rS | rS | rS, RS | R | R | |
| Лівошлуночкові | Верхівкові | rS, QS | rS, QS | rS | rS | rS, RS | Rs, RS |
| Базальні | R | R | R | R | Rs | RS, Rs | |
| Проміжні | R, qR, RR’, RS, Rs | R, Rs | RS | RS, rS | rS | rS, QS | |
| Верхівкові | RS, Rs | rS, RS | rS | rS | rS | rS | |
| Базальні | R | R | R | R | R | R | |
| Верхівкові | rS | rS | rS | rS | rS | rS | |
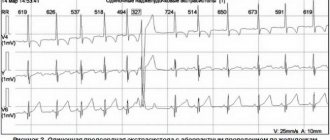
Інтервали зчеплення монотопних ШЕ однакові, незважаючи на те що їх форма може бути різною (у цьому випадку вони є поліморфними). Коливання інтервалів зчеплення монотопних екстрасистол звичайно не перевищують 0,06–0,10 с. Політопні ШЕ мають різні за тривалістю інтервали зчеплення і, як правило, різну форму комплексів QRS. Дві екстрасистоли поспіль називаються парними (рис. 1), а три–п’ять — груповими, “залповими” (рис. 2), або пробіжками шлуночкової тахікардії — ШТ. Виділяють також ранні і дуже ранні ШЕ („R на Т”) (рис. 3). Екстрасистолія може бути нерегулярною (монотопна або політопна), а її поява з певною закономірністю визначається як алоритмія (бігемінія, тригемінія, квадригемінія тощо). Інтерпольовані ШЕ реєструються між двома нормальними комплексами QRS, як звичайно, — на фоні брадикардії.
Рисунок 1.
Поодинока і парна політопна шлуночкова екстрасистолія.
Рисунок 2.
Групова політопна шлуночкова екстрасистолія.
Рисунок 3.
Рання шлуночкова екстрасистолія „R на Т”.
Шлуночкову екстрасистолію на фоні фібриляції передсердь необхідно диференціювати з аберантними шлуночковими комплексами. Вкорочений кардіоцикл при фібриляції передсердь, який закінчується аберантним шлуночковим комплексом, на відміну від передекстрасистолічного інтервалу, не супроводжується компенсаторною паузою, і йому передує подовжений інтервал RR. Аберантні комплекси QRS, як правило, мають форму блокади правої ніжки пучка Гіса різного ступеня виразності у відведенні V1 (rSR’, rSr’), а лівошлуночкові екстрасистоли — форму R, RS, Rs, qR, RR’ або Rr’ (табл. 2).
Таблиця 2. Диференціальна діагностика суправентрикулярних екстрасистол з аберацією внутрішньошлуночкової провідності і шлуночкових екстрасистол
| Ознаки | Суправентрикулярна екстрасистолія з аберацією | Шлуночкова екстрасистолія |
| Морфологія QRS у відведенні V1: | ||
| rSR’, rsR’ | Характерно | Не характерно |
| qR, R, rR’ з розщепленням на висхідному коліні | Дуже рідко | Не характерно |
| qR, R, RS, Rsr’, RR’ з розщепленням на низхідному коліні | Не характерно | Характерно |
| rS, QS | Не характерно | Характерно |
| Морфологія QRS у відведенні V6: | ||
| qRS | Характерно | Не характерно |
| rS, QS | Не характерно | Характерно |
| Переважання позитивних або негативних зубців комплексу QRS у всіх грудних відведеннях | Не характерно | Характерно |
ІНШІ МЕТОДИ ІНСТРУМЕНТАЛЬНОЇ ДІАГНОСТИКИ
Холтерівське моніторування (ХМ) ЕКГ дозволяє реєструвати ЕКГ без обмеження рухового режиму хворого протягом 24 годин і більше з наступним автоматизованим аналізом запису. Оцінюються загальна кількість екстрасистол за час спостереження, їх розподіл протягом доби, зв’язок з фізичним або емоційним навантаженням, ЧСС, прийомом їжі, зміною положення тіла, перехідними епізодами ішемії міокарда.
ХМ ЕКГ — „еталонний” метод діагностики відносно нечастої екстрасистолії, а також оцінки тяжкості ШЕ, виявлених під час реєстрації ЕКГ. ХМ ЕКГ дозволяє точніше, ніж короткочасна реєстрація ЕКГ, здійснювати якісну та кількісну оцінку порушень серцевого ритму внаслідок значно більшої кількості оцінюваних ектопічних комплексів. Поодинокі ШЕ є досить частою знахідкою при ХМ ЕКГ у практично здорових осіб.
Порівняння циркадних змін кількості екстрасистол та частоти серцевих скорочень (ЧСС) дозволяє відокремити тахі- і брадизалежні форми екстрасистолії. Одним з найбільш поширених добових типів розподілу екстрасистолії є „вагусний” (вагозалежний, або „нічний”), коли передчасні комплекси реєструються більш ніж в 1,5 разу частіше в пасивний період доби, на фоні сповільнення синусового ритму. Вагозалежна ШЕ частіше трапляється у молодих людей без ознак патології серця, нерідко вона є випадковою знахідкою і не відчувається хворими. Така форма екстрасистолії переважно не потребує антиаритмічної терапії. При „адренергічному” (симпатозалежному, або „денному” типі) середня кількість екстрасистол за годину в 1,5 разу більша в активний період доби, а екстрасистоли часто пов’язані з прискоренням синусового ритму. „Адренергічний” тип ШЕ більш характерний для літніх людей, особливо з ІХС, гіпертонічною хворобою, вадами серця, дилятаційною і гіпертрофічною кардіоміопатіями, міокардіофіброзом. На відміну від „вагусного” типу, така екстрасистолія не є доброякісною і часто потребує призначення ААП, передусім β-блокаторів і аміодарону. Дуже часто відсутній зв’язок кількості екстрасистол з періодом доби і ЧСС. Можна також спостерігати „гектичний” тип розподілу екстрасистол зі значними коливаннями їх кількості від години до години. Така висока ектопічна активність протягом короткого проміжку часу інколи може бути пов’язана з рецидивуючою ішемією міокарда. Загалом застосування ХМ ЕКГ істотно збільшує можливості виявлення екстрасистолії і парасистолії, встановлення змінності її форм і варіантів.
Метод ХМ ЕКГ дозволяє оцінювати зміни варіабельності серцевого ритму за добу. Зокрема, зниження стандартного показника варіабельності серцевого ритму — стандартного відхилення інтервалів RR протягом доби (SDNN) — нижче 50 мс свідчить про дисбаланс вегетативної регуляції серцевого ритму і є одним із предикторів виникнення РСС у хворих з післяінфарктним кардіосклерозом, систолічною дисфункцією лівого шлуночка (ЛШ) і серцевою недостатністю та збереженим синусовим ритмом. Найбільш потужним провісником ризику життєво небезпечної аритмії було поєднання низької варіабельності серцевого ритму із зниженою фракцією викиду (ФВ) ЛШ і порушеною чутливістю барорефлексу (дослідження ATRAMІ, 1998). Наголосимо, що часта ШЕ є обмеженням для оцінки часових і спектральних показників варіабельності серцевого ритму.
При ХМ ЕКГ звертають увагу також на тривалість і варіабельність інтервалу зчеплення, а також тривалість інтервалу Q-T. Привертає увагу оцінка добових коливань коригованого інтервалу QT, адже навіть при його нетривалому збільшенні може збільшуватися тривалість „вразливого” періоду серцевого циклу і схильність до виникнення пароксизмів „пірует-тахікардії”.
Повторне ХМ ЕКГ на фоні лікування дозволяє оцінити ефективність призначеної терапії. З огляду на виражені спонтанні коливання частоти виникнення аритмій серця розроблено такі критерії ефективності антиаритмічної терапії у хворих з ШЕ: а) зменшення загальної кількості ШЕ за добу більш ніж на 50–75%; б) зменшення кількості парних і ранніх ШЕ на 90% і більше; в) повне усунення епізодів ШТ; г) при поліморфній ШЕ — зменшення кількості морфологічних типів екстрасистол до 1–2. Оцінюючи адекватність лікування антиаритмічним препаратом, крім перерахованих критеріїв, потрібно також враховувати особливості його впливу на синусовий ритм, провідність, частоту ішемічних епізодів.
Інтерпретація даних ХМ ЕКГ щодо оцінки ефективності антиаритмічної терапії при ШЕ має певні обмеження. При застосуванні ААП 1-го класу за класифікацією V. Wіllіams ефективність за вказаними кількісними критеріями не дозволяє передбачити поліпшення прогнозу виживання хворих при тривалому лікуванні. Більше того, використання деяких препаратів (флекаїніду, енкаїніду) у контрольованих дослідженнях асоціювалося з істотним збільшенням імовірності РСС. Зважаючи на це, лікування пацієнтів із тяжким структурним ураженням міокарда (дисфункція ЛШ після перенесеного ІМ або при дилятаційній кардіоміопатії, з/без СН) починають із терапії етіопатогенетичного спрямування: коригують ішемію та гемодинамічні порушення. За наявності дисфункції ЛШ і частих симптомних ШЕ до базисної превентивної терапії (інгібітори ангіотензин-перетворюючого ферменту (АПФ), β-адреноблокатори, аспірин, статини) додають аміодарон або соталол — засоби з доведеною ефективністю у профілактиці злоякісних шлуночкових аритмій. Зазначимо, що β-адреноблокатори й аміодарон можна призначати емпірично з огляду на доведену здатність цих препаратів поліпшувати прогноз виживання хворих і незалежно від змін кількості порушень серцевого ритму. У цих ситуаціях ХМ ЕКГ доцільно здійснити в динаміці для оцінки перебігу порушень серцевого ритму на фоні антиаритмічної терапії. А в ситуаціях, коли застосування ААП визначається передусім клінічною вагомістю порушень ритму, а не їх прогностичним значенням, визначальним критерієм ефективності препарату є зменшення симптомів, спричинених аритмією. Наголосимо також, що найбільш ефективним засобом профілактики РСС у пацієнтів з критеріями її високого ризику є імплантація внутрішнього кардіовертера-дефібрилятора.
Проби з фізичним навантаженням
(проба Мастера, степ-тест, велоергометрія, тредміл-тест) можуть провокувати появу ШЕ під час навантаження і в ранньому відновлювальному періоді внаслідок підвищення активності симпатоадреналової системи, збільшення викиду катехоламінів, розвитку тканинної гіпоксії, ацидозу. У хворих на хронічну ІХС під час велоергометрії ШЕ виявляють у 60% обстежених, а їх частота нерідко корелює зі зміщенням сегмента ST (рис. 4). Під впливом фізичного навантаження може змінитися кількість і градація екстрасистолії: збільшення кількості екстрасистол під час навантаження при високій ЧСС або в першу хвилину після його закінчення свідчить про її можливий зв’язок з ІХС; “доброякісні” екстрасистоли звичайно зникають під час навантаження та відновлюються через 3–5 хвилин після його закінчення. Потрібно зважати на діагностичні обмеження проби з навантаженням: у частини хворих не вдається спровокувати екстрасистолію, діагностовану раніше; в 11–40% пацієнтів зі здоровим серцем при фізичному навантаженні з’являється поодинока екстрасистолія, а в 5% — парна; у деяких хворих при фізичному навантаженні можуть зникати навіть групові та ранні екстрасистоли.
Рисунок 4.
Правошлуночкова екстрасистола на фоні горизонтальної депресії сегмента ST.
Ортокліностатична проба
дозволяє уточнити характер екстрасистолічної аритмії: стабільна екстрасистолія існує у спокої та при функціональних пробах; лабільна екстрасистолія напруги з’являється або посилюється при ортостатичній пробі і стандартному навантаженні потужністю 50 Вт; лабільна екстрасистолія спокою зникає при ортостатичній пробі та фізичному навантаженні потужністю 50 Вт і з’являється після переходу в горизонтальне положення. Вважається, що лабільна екстрасистолія напруги і стабільна екстрасистолія скоріше за все пов’язані з наявністю захворювання серця і/або стійкого субстрату аритмії, а лабільна екстрасистолія спокою, як правило, є функціональною (вагусною).
Ехокардіографія
здійснюється для уточнення впливу як ШЕ, так і ААП на стан гемодинаміки. Метод дозволяє оцінити розміри порожнин серця в систолу і діастолу, фракцію викиду, товщину стінок серця, масу міокарда ЛШ, співвідношення кінцево-діастолічного об’єму і маси міокарда ЛШ, виявити зони гіпо- і акінезії, локальні гіпертрофії, клапанні вади, феномен “постекстрасистолічного підсилення”, дисплазію міокарда правого шлуночка. Зменшення ФВ ЛШ менше 40% у хворих на ІХС асоціюється з підвищенням ризику РСС. Серцевий викид можна точніше визначити з допомогою радіоізотопної вентрикулографії або коронаровентрикулографії.
Внутрішньосерцеве ЕФД
є сучасним методом діагностики порушень ритму та провідності серця, визначення показань для кардіостимуляції, радіочастотної катетерної абляції та імплантації кардіовертера-дефібрилятора. Дослідження виконується у спеціально обладнаних лабораторіях. У хворих із ШЕ абсолютних показань для проведення внутрішньосерцевого ЕФД немає. Це дослідження може бути здійснене лише при необхідності встановлення зв’язку порушень ритму серця з синкопальними та передсинкопальними станами. Хворим із безсимптомним перебігом екстрасистолії ЕФД не показане.
КЛІНІЧНЕ ТА ПРОГНОСТИЧНЕ ЗНАЧЕННЯ
Клінічне значення ШЕ в основному визначається її типом і градацією, наявністю симптомів, характером основного захворювання, ступенем ураження серця і функціональним станом міокарда.
Шлуночкові екстрасистоли в осіб без структурного ураження серця не є загрозливими для життя. Їх виявляють при ХМ ЕКГ у більшості практично здорових осіб усіх вікових груп, причому у 10% вони політопні і рідко — групові. Загалом ШЕ не обов’язково вказують на супутню кардіальну патологію, а за відсутності серцевого захворювання не є провісником підвищення захворюваності і смертності. З іншого боку, у хворих з вираженим структурним ураженням серця та дисфункцією міокарда, особливо на фоні післяінфарктного кардіосклерозу або СН, виявлення частої ШЕ є додатковим прогностично несприятливим фактором.
Ектопічна активність шлуночків відзначається у 75–90% хворих на гострий інфаркт міокарда в перші 72 години захворювання і зумовлює високу частоту РСС в цей час, але не корелює зі смертністю протягом року. Наявність ШЕ в більш пізній період захворювання вказує на несприятливий тривалий прогноз. Так, частота ШЕ менше 1 за годину спостерігається у 50% хворих при виписці зі стаціонару і вказує на дворічну смертність близько 5%. При більш частій ШЕ (1–10 за годину), що спостерігається у 20% хворих, смертність досягає 20%. Короткі пароксизми ШТ спостерігаються у 12% хворих, а смертність від усіх причин сягає до 30% протягом першого року після перенесеного ІМ. Поява життєво небезпечних аритмій серця після ІМ зумовлена поєднанням рецидивуючої ішемії з метаболічними та електролітними розладами. Важливими факторами, що сприяють аритмогенезу, є СН і стенозуючий коронарний атеросклероз.
Парні і політопні ШЕ трапляються у 70–90% хворих із СН, а короткі епізоди ШТ — у 40–80%. У цьому випадку шлуночкові порушення серцевого ритму є несприятливим прогностичним фактором, причому 33–47% усіх випадків смерті хворих із СН припадає на РСС. Аритмогенними факторами при СН є дисфункція лівого шлуночка (ФВ < 45%), ішемія міокарда, гіпоксія, електролітні розлади, а також аритмогенні ефекти застосованих терапевтичних засобів, особливо серцевих глікозидів, діуретиків і периферичних вазодилятаторів.
Дуже високою є частота ШЕ у хворих на дилятаційну кардіоміопатію. Так, часті і політопні ШЕ спостерігаються у 80–90% хворих, короткі епізоди ШТ — у 20–60%. Частота РСС сягає 10% на рік, на неї припадає половина від усіх випадків смерті. Приблизно в 50% хворих виявляють передсердні екстрасистоли. Формування аритмій пов’язане з наявністю вираженої дисфункції ЛШ і СН.
Шлуночкові екстрасистоли реєструють у 50–65% хворих на гіпертрофічну кардіоміопатію з обструкцією вихідного тракту ЛШ, у тому числі парні ШЕ — у 32%, а пароксизми ШТ — у 14–25%. Частота РСС у цих пацієнтів становить 2,5–9% на рік. Передсердна екстрасистолія трапляється рідше, ніж шлуночкові порушення ритму. Причини та фактори, які сприяють аритмогенезу: клітинна дезорганізація в різних ділянках міокарда, гіпоксія, гіпокаліємія, обструкція вихідного тракту ЛШ, діастолічна дисфункція ЛШ, СН, аритмогенні впливи препаратів, інтенсивні фізичні навантаження.
Ризик РСС внаслідок шлуночкових порушень ритму особливо зростає у хворих з аритмогенною дисплазією правого шлуночка, вродженим або набутим синдромом подовженого інтервалу QT, клапанними вадами серця (включаючи пролапс мітрального клапана), артеріальною гіпертензією.
Про ступінь небезпеки, пов’язаної з ШЕ, можуть свідчити деякі особливості ЕКГ. Як звичайно, не є загрозливими екстрасистоли з конфігурацією блокади лівої ніжки пучка Гіса і вертикальним положенням електричної осі передчасного комплексу QRS (тип Розенбаума) або коли комплекс QRS екстрасистоли у всіх грудних відведеннях спрямований уверх і нагадує графіку синдрому Вольфа-Паркінсона-Уайта типу А (тип Вольфа). Комплекс QRS таких екстрасистол не має додаткових розщеплень, його амплітуда становить 20 мм і більше, тривалість може бути до 0,12 с, а сегмент ST і асиметричний зубець Т спрямовані дискордантно до основного зубця шлуночкового комплексу. Перегородкові ШЕ з вузькими комплексами QRS частіше спостерігаються у молодих людей за відсутності структурного ураження серця і рідко є симптомними. Потенційно загрозливі ШЕ здебільшого виникають на фоні структурного ураження серця, мають форму блокади правої ніжки пучка Гіса, незначну амплітуду комплексу QRS (часто до 10 мм) з додатковими розщепленнями, а тривалість його більше 0,12–0,14 с. Можуть спостерігатися аномалії реполяризації: горизонтальна депресія сегмента ST і конкордантне спрямування симетричного, загостреного зубця Т.
КЛАСИФІКАЦІЇ ШЛУНОЧКОВОЇ ЕКСТРАСИСТОЛІЇ
Згідно з рекомендаціями Асоціації кардіологів України, створеними на основі Міжнародної класифікації хвороб Х перегляду, виділяють такі види екстрасистолії: передсердна, атріовентрикулярна, шлуночкова (поодинока — до 30 за годину, часта — 30 і більше за годину, алоритмія, поліморфна, парна, рання — типу „R на Т”).
В Україні при інтерпретації даних ХМ ЕКГ у хворих із шлуночковими порушеннями ритму традиційно використовують класифікацію B. Lown і M. Wolf (1971). Згідно з цією класифікацією розрізняють 5 класів шлуночкових екстрасистол: 1) мономорфна, <� 30 за годину; 2) мономорфна, > 30 за годину; 3) поліморфна; 4) парна (4а) і пробіжки шлуночкової тахікардії (4b); 5) рання („R на T”). Ця класифікація була розроблена для систематизації шлуночкових порушень серцевого ритму у хворих на гострий ІМ, але не відповідає потребам стратифікації ризику та вибору тактики диференційованого лікування в післяінфарктних пацієнтів. Докладніше варіанти шлуночкових порушень серцевого ритму відображені у класифікації R. Myerburg (1984), яку зручно застосовувати при інтерпретації результатів ХМ ЕКГ (табл. 3). Наголосимо, що при стратифікації ризику в післяінфарктних хворих вагомою є вже кількість ШЕ понад 10 на годину. До аритмій „високих градацій” зараховують парні ШЕ і пароксизми ШТ будь-якої тривалості. Причому стійка ШТ, незалежно від клінічних симптомів і характеру структурного захворювання серця, розглядається як злоякісне порушення ритму, тоді як прогностичне значення нестійкої ШТ сильно залежить від основного захворювання серця і функціонального стану міокарда. Морфологічний тип ШТ також визначає суттєві відмінності механізмів виникнення і тактики ведення хворих, зокрема, застосування ААП і катетерних методів лікування.
Таблиця 3. Систематизація шлуночкових порушень серцевого ритму за R. Myerburg (1984)
| Кількість екстрасистол | Форми шлуночкових аритмій | Морфологія шлуночкових тахікардій | ||
| Ступінь тяжкості | Кількість | Ступінь тяжкості | Характеристики | |
| 0 | Немає | 0 | Немає | •Мономорфна •Поліморфна •„Пірует” •З вихідного тракту правого шлуночка •Двоспрямована |
| 1 | Рідко (<1 за год.) | 1 | Поодинокі, мономорфні | |
| 2 | Нечасто (2–9 за год.) | 2 | Поодинокі, поліморфні | |
| 3 | Проміжна (10–29 за год.) | 3 | Парні, пробіжки (2 або 3–5 комплексів) | |
| 4 | Часта (30–59 за год.) | 4 | Нестійка шлуночкова тахікардія (від 6 комплексів до 29 с) | |
| 5 | Дуже часта (≥ 60 за год.) | 5 | Стійка шлуночкова тахікардія (≥ 30 с) | |
Добре відома прогностична класифікація шлуночкових аритмій, запропонована J. T. Bіgger (1993), що поділяє шлуночкові аритмії на безпечні (доброякісні), небезпечні для життя (злоякісні, летальні) і потенційно небезпечні (потенційно летальні).
- Безпечні (доброякісні) аритмії — будь-які ШЕ (рідкісні, часті, політопні, парні), а також короткі епізоди ШТ за відсутності кардіальної патології, що не викликають порушення гемодинаміки. Прогноз при цих ША такий самий, як у здорової популяції. Показань для антиаритмічної терапії немає.
- Небезпечні для життя (злоякісні) шлуночкові аритмії — епізоди ШТ, що призводять до порушення гемодинаміки або фібриляції шлуночків (ФШ). Ці аритмії, як правило, спостерігаються у хворих із вираженим структурним ураженням серця (ІХС, застійна СН, кардіоміопатії, вади серця) і порушенням скоротливості ЛШ. У цих хворих ШЕ є лише частиною спектра шлуночкових порушень ритму. Досить часто у них також виявляють нестійкі та стійкі ШТ.
- Потенційно небезпечні (потенційно злоякісні) шлуночкові аритмії — часті, політопні, парні ШЕ, короткі епізоди ШТ у хворих із структурними ураженнями серця (ІХС, СН, кардіоміопатії, вади серця), що не призводять під час порушення ритму до виражених змін гемодинаміки. Маркером більшої ймовірності виникнення життєво небезпечних аритмій серця у цих хворих є систолічна дисфункція ЛШ (ФВ ЛШ <� 45%).
ПРИНЦИПИ ВЕДЕННЯ ХВОРИХ
Тактика ведення хворих із ШЕ залежить від: а) структурного захворювання серця; б) частоти виникнення екстрасистол, наявності групових екстрасистол або супутніх пароксизмів тахіаритмії; в) клінічних симптомів, пов’язаних з аритмією. Показаннями для призначення β-блокаторів і/або інших ААП є такі клінічні ситуації: 1) прогресуючий перебіг захворювання серця з істотним збільшенням кількості ШЕ; 2) часті, політопні, парні, групові та ранні („R на T”) ШЕ, загрозливі щодо подальшого виникнення пароксизмальної ШТ і ФШ; 3) алоритмія (бі-, три-, квадригемінія), короткі пробіжки ШТ, які супроводжуються ознаками СН; 4) ШЕ на фоні захворювань, які супроводжуються збільшенням ризику життєво небезпечних аритмій (пролапс мітрального клапана, синдром подовженого інтервалу Q-T тощо); 5) виникнення або збільшення частоти ШЕ під час нападів стенокардії або гострого ІМ; 6) збереження ШЕ після припинення приступу ШТ і ФШ; 7) екстрасистоли на фоні аномальних шляхів проведення (синдромів Вольфа-Паркінсона-Уайта та Клерка-Леві-Крістеско).
Хворі з доброякісною ШЕ спеціальної антиаритмічної терапії не потребують, але необхідне динамічне спостереження, тому що в частини з них, за даними Фремінгемського дослідження, ШЕ може бути дебютом серцевого захворювання. При екстрасистолії в осіб молодого віку без структурного ураження серця, особливо тій, яка зникає під час фізичного навантаження, ААП звичайно не призначають. При суб’єктивній непереносимості екстрасистолії показані раціональна психотерапія, седативні засоби, транквілізатори або антидепресанти. Тривалість лікування залежить від медичних показань і коливається від трьох тижнів до 2–3 місяців. У випадку досягнення стійкого седативного й антиаритмічного ефекту добова доза препарату протягом кожних 6–7 днів зменшується на одну третину до повної відміни. Якщо екстрасистолія виникає на фоні вегетативної дисфункції з ознаками симпатоадреналової активації, показані β-адреноблокатори, а при домінуванні ваго-інсулярних симптомів — М-холінолітики (атропін, препарати беладони, ітроп). Хворі з захворюваннями внутрішніх органів і екстрасистолією насамперед потребують адекватного лікування основного захворювання. У всіх випадках обстеження спрямоване на виявлення та усунення потенційних провокуючих факторів екстрасистолії (таких як споживання кофеїну, певні життєві ситуації), а також супутніх порушень (артеріальна гіпертензія).
При поодиноких монофокусних ШЕ у хворих із серцево-судинними захворюваннями без порушень гемодинаміки і коронарного кровообігу призначати ААП не потрібно. Стриманий підхід до призначення ААП зумовлений тим, що ризик побічних ефектів при медикаментозному лікуванні “доброякісних” аритмій більший, ніж позитивні наслідки лікування. Ведення таких хворих полягає передусім у лікуванні основного захворювання, а також використанні седативних засобів і методів психотерапії при суб’єктивній непереносимості аритмії.
Потенційно злоякісні шлуночкові аритмії звичайно виникають на фоні структурного захворювання серця, наприклад, ІХС або після перенесеного ІМ. У таких хворих з ШЕ різних градацій існує небезпека виникнення в подальшому пароксизмів ШТ, тріпотіння або фібриляції шлуночків. Зважаючи на це, хворі з потенційно злоякісними шлуночковими аритміями передусім потребують адекватного лікування основного захворювання. З цією метою здійснюється корекція стандартних факторів ризику ІХС (артеріальна гіпертензія, куріння, гіперхолестеринемія, цукровий діабет), призначаються засоби, ефективність яких доведена у хворих з ІХС (аспірин, β-адреноблокатори, статини) і при СН (інгібітори АПФ, β-адреноблокатори, антагоністи альдостерону). При поєднанні кардіальної патології з частою ШЕ високих градацій добирають адекватну антиаритмічну терапію. Препаратами вибору найчастіше є β-адреноблокатори, особливо за наявності додаткових показань: ІХС, артеріальної гіпертензії, синусової тахікардії. Високу ефективність цих препаратів пов’язують з їх антиангінальною, антиаритмічною та брадикардитичною дією. За необхідності β-адреноблокатори поєднують з ААП І класу (пропафенон, етмозин, етацизин, дизопірамід) з урахуванням доцільності їх подальшого тривалого застосування.
Гіпотеза про профілактичну ефективність ААП І класу при ШЕ для запобігання раптовій смерті була переглянута після оприлюднення результатів дослідження CAST (1989). Прийом флекаїніду та енкаїніду в післяінфарктних хворих з безсимптомними ШЕ високих градацій супроводжувався достовірним збільшенням ризику раптової смерті порівняно з плацебо. Вказаний феномен пов’язують з аритмогенною і негативною інотропною дією ААП І класу. Водночас негативні підсумки дослідження CAST та інших досліджень ефективності ААП І класу не виключають можливості їх ефективного нетривалого використання для лікування ШЕ у хворих на ІХС, а також при інших причинах шлуночкових аритмій.
При недостатній ефективності β-адреноблокаторів і ААП І класу призначають аміодарон — найбільш потужний з існуючих антиаритмічних засобів з найнижчою ймовірністю аритмогенних ефектів. Аміодарон застосовують при резистентності до інших ААП; крім того, він є препаратом вибору у хворих з життєво небезпечними та клінічно вираженими аритміями на фоні тяжкого структурного захворювання серця. Обнадійливі результати отримано при застосуванні аміодарону у хворих з частою ШЕ після перенесеного ІМ у мета-аналізі АТМА (1997). У групах хворих, які отримували аміодарон, істотно зменшувалась імовірність РСС, але не спостерігали достовірного зменшення загальної смертності. Аміодарон — препарат вибору для лікування шлуночкових аритмій та запобігання їм у хворих із систолічною дисфункцією міокарда і СН. Використання аміодарону в малих дозах (200 мг на добу) дозволяє зменшити до мінімуму кількість некардіальних побічних ефектів. Альтернативним засобом лікування хворих із шлуночковими аритміями на фоні ІХС є соталол — ААП ІІІ класу з β-блокуючими властивостями.
Висока ефективність аміодарону і соталолу при лікуванні хворих зі злоякісними шлуночковими аритміями не свідчить про відсутність проблеми безпеки цих засобів. ААП ІІІ класу подовжують коригований інтервал Q-T, безпечна межа якого становить 440–460 мс. Якщо показники інтервалу Q-Tс перевищують вказані межі, діагностують набутий синдром подовженого інтервалу Q-T. Характерним та специфічним проявом цього стану є поліморфна ШТ (пірует-тахікардія), яка може трансформуватися у ФШ. Ризик розвитку аритмогенної дії соталолу найбільший у перші три дні прийому препарату. Загалом аритмогенні ефекти соталолу спостерігаються частіше, ніж при застосуванні аміодарону.
ПІДСУМКИ
Шлуночкова екстрасистолія — найбільш поширене у клінічній практиці порушення ритму серця. Вона може виникати при багатьох кардіальних і екстракардіальних захворюваннях, бути випадковою знахідкою у практично здорових осіб. Комплекс сучасних інструментальних і лабораторних методів обстеження пацієнтів із ШЕ спрямований на встановлення її причин та механізмів, кількості і градації, клінічного і прогностичного значення, здійснення стратифікації ризику. Загальна стратегія ведення хворих із ШЕ і, зокрема, доцільність її усунення з допомогою ААП визначаються залежно від співвідношення потенційної користі лікування для усунення аритмій, поліпшення прогнозу виживання і ризику виникнення аритмогенних та інших побічних ефектів терапії.
РЕКОМЕНДОВАНА ЛІТЕРАТУРА
- Амбулаторне моніторування ЕКГ. Сучасні технології, діагностичні можливості, показання: Метод. посібник / Бобров В. О., Жарінов О. Й., Куць В. О. та співавт. — Львів: Медицина світу, 2004. — 68 с.
- Бобров В. О., Жарінов О. Й. Шлуночкові аритмії (механізми розвитку, вплив дисфункції міокарда, прогностична оцінка, диференційоване лікування). — Львів, 1995. — 122 с.
- Дабровски А., Дабровски Б., Пиотрович Р. Суточное мониторирование ЭКГ.— М.: Медпрактика, 2000. — 208 с.
- Дослідження варіабельності серцевого ритму в кардіологічній практиці: Метод. реком. / Бобров В. О., Чубучний В. М., Жарінов О. Й. та співавт. — К: Укрмедпатентінформ, 1999. — 25 с.
- Кушаковский М. С. Аритмии сердца. — СПб.: ИКФ “Фолиант”, 1998. — 640 с.
- Орлов В. Н. Руководство по электрокардиографии. — М.: Медицинское информационное агентство, 2003. — 526 с.
- Стратифікація ризику і профілактика раптової серцевої смерті: Метод. реком. / Бобров В. О., Жарінов О. Й., Сичов О. С. та співавт. — К: Укрмедпатентінформ, 2002 . — 39 с.
- Функциональная диагностика в кардиологии / Под ред. Л. А. Бокерия, Е. З. Голуховой, А. В. Иваницкого. — М.: Изд-во НЦССХ им. А. Н. Бакулева РАМН, 2002. — Т. 1 — 427 с., т. 2 — 296 с.
Симптомы
При наджелудочковой экстрасистолии пациент ощущает “перебои” в работе сердца. Здоровый человек вообще не чувствует собственное сердцебиение. К числу других симптомов относится:
- слабость;
- головокружения;
- одышка;
- постоянное чувство беспокойства;
- чувство нехватки воздуха;
- паника;
- боязнь умереть.
Точные признаки патологического состояния будут зависеть от основного заболевания. Например, при неврозе и вегетососудистой дистонии у пациента повышается потливость и увеличивается чувство тревоги. Если причина заболевания – кардиологическая патология, то тогда наблюдаются сердечные боли.
Последствия и осложнения
При своевременном выявлении патологии, адекватной терапии и изменении образа жизни прогноз суправентрикулярной экстрасистолии благоприятный. Если у пациента нет сопутствующих недугов, смерть от экстрасистолии наступить не может. Но при игнорировании клинической картины и при отказе от лечения возможно развитие следующих осложнений – ишемическая болезнь сердца, мерцательная аритмия и другие опасные для жизни заболевания.
Важно! Несмотря на то что наджелудочковая экстрасистола, как самостоятельная патология, не представляет угрозы, консультация с врачом должна быть обязательной.
LiveJournal
Особенности у детей
Если у ребенка диагностировали наджелудочковую экстрасистолию, то следует в первую очередь следить за его образом жизни и соблюдать режим дня. Важно объяснить малышу, что если он не будет выполнять все профилактические меры, то могут возникнуть серьезные осложнения, который негативно скажутся на его здоровье.
Питание ребенка должно быть разнообразным и сбалансированным. Пища должна быть богатой на аминокислоты, витамины, белки, жиры, углеводы и минералы. В рационе должны присутствовать фрукты, овощи, молочные продукты, рыба и мясо. Следует свести к минимуму употребление сладостей и вредной пищи.
Чтобы не допустить дальнейшего развития патологического состояния необходимо, чтобы ребенок имел рациональные физические нагрузки, и как можно больше времени находился на свежем воздухе. Состояние малыша может ухудшиться вследствие простуды или инфекционного заболевания.
Важно! Если состояние ребенка ухудшилось нужно сразу же обратиться к педиатру или кардиологу. В некоторых случаях требуется госпитализация.
Лечение
Как изменить образ жизни?
При возникновении экстрасистолии наджелудочкового типа следует особенно тщательно следить за режимом дня. Для взрослых это значит, что рекомендуется иметь нормированный рабочий график, и работать не более 8 часов в сутки. Следует исключить стрессы, психоэмоциональное перенапряжение, а также работу в ночное время суток.
Необходимо отказаться от вредных привычек. Организм должен иметь полноценный отдых, поэтому спать нужно не меньше 8 часов, а время отдыха рекомендуется проводить максимально активно.
Чтобы не допустить ухудшения состояния, пациент должен пересмотреть свое питание. Рекомендуется исключить из рациона блюда с высоким содержанием холестерина и животные жиры. Основа рациона – растительная пища, диетическое мясо, орехи и сухофрукты. Особенно полезны масла: подсолнечное, оливковое и льняное.
Медикаментозная терапия
Лечить желудочковую экстрасистолию начинают с медикаментозной терапии – препараты подбираются в зависимости от присутствия дополнительных нарушений, степени отклонения от нормального сердечного ритма и типа сердечной патологии. Терапевтический эффект антиаритмических лекарств:
- профилактика возникновения органических систолических шумов;
- уменьшение уровня проводимости в отделах сердца;
- снижение силы сокращений миокарда;
- нормализация частоты сокращений сердца.
Для контроля за эффективностью и правильностью проведения терапии назначается ЭКГ. Такая процедура позволяет увидеть все изменения в организме, что дает врачу возможность своевременно корректировать курс лечения.
Антиаритмические препараты могут привести к проблемам с дыхательной системой. Поэтому лечение должно проводиться только под контролем специалиста. Чтобы минимизировать риск развития осложнений, врач периодически проводит анализ мочи и крови. Это необходимо для того, что установить концентрацию лекарственных веществ в организме пациента.
Хирургическое лечение
Хирургический метод лечения назначается только в том случае, если консервативная терапия не дала результата. Для устранения экстрасистолии наджелудочкового типа проводится радиочастотная катетерная абляция.
Такая процедура предполагает введение катетера через артерию. Врач проводит электроды по катетеру прямо к отделам сердца, из которых исходит импульс. Это закрытый тип операции, иногда проводится открытое хирургическое вмешательство.
Открытая операция назначается в том случае, если присутствует необходимость в проведении вмешательства в другие отделы сердца.
Суть оперативного вмешательства при наджелудочковой экстрасистолии сводится к устранению очага, что вырабатывает дополнительные сердечные импульсы.