Бактериоскопия – самый распространённый гинекологический анализ. Женщины и девушки разного возраста при прохождении профосмотра обязательно подвергаются такой процедуре. У 50-60% из них в мазке на флору обнаруживаются кокки. У мужчин они встречаются гораздо реже. Это связано с особенностями строения женской половой системы. Также кокки могут быть выявлены в мазке у ребёнка.
Бактерии при определённых обстоятельствах способны спровоцировать серьёзные заболевания мочеполовых и других органов, поэтому целесообразно узнать, что они собой представляют, когда угрожают здоровью и как с ними бороться.
Что такое кокки
В человеческом организме присутствует множество разных микробов. Кокки – семейство одноклеточных, названное от слова coccus, что в переводе с латыни означает – «шаровидный», а с древнегреческого – «зерно». Как и другие бактерии, кокки обладают уникальной способностью к интенсивному размножению (примерно каждые полчаса). В благоприятных условиях одноклеточные делятся надвое, т.е. дробятся, из-за чего их ещё именуют «дробянками», а далее либо существуют по отдельности, либо объединяются в группы. Кокки неподвижны, не образуют споры и являются анаэробными (могут обитать в безвоздушной среде).
Что такое гонококки?
Возбудителем гонореи выступают не окрашиваемые неподвижные бактерии, которые располагаются парно. Внешне они напоминают кофейные зерна. Бактериям не страшен фагоцитоз. Несмотря на все попытки организма, они продолжают вести активную жизнедеятельность и размножаться.
Часто в борьбе с гонококками используют антибактериальные препараты. Если неправильно их принимать, то достичь эффекта не возможно. Под воздействием средств стенки бактерий разрушаются, но способность к развитию остается. Благодаря высокой выживаемости они способны менять характеристики. При наличии углекислого газа и нормального температурного режима (37 0С) гонококки активно размножаются в искусственной питательной среде.
Нормальная микрофлора
Здоровая микрофлора женских половых органов состоит из лактобактерий – палочек Дедерлейна, бифидобактерий и незначительного (около 5%) количества кокков. За счёт этого обеспечивается нормальное течение таких процессов, как:
- обмен веществ;
- регуляция уровня кислотности;
- уничтожение болезнетворных микробов.
Само по себе присутствие кокков в мазке у женщин неопасно и естественно. Когда баланс микроорганизмов поддерживается на должном уровне, в кислой среде полезные лактобактерии размножаются и создают защиту от грибков (молочницы), кишечной палочки и других вредных микробов. Соответственно, мочеполовая система функционирует стабильно и полноценно.
Получение материала
Рак шейки матки чаще всего развивается в зоне трансформации, ему предшествуют фоновые процессы и внутриэпителиальные поражения (дисплазия эпителия), которые могут располагаться на небольших участках, поэтому важно, чтобы материал был получен со всей поверхности шейки матки, особенно из зоны стыка плоского и цилиндрического эпителия. Число измененных клеток в мазке бывает различным, и если их мало, то увеличивается вероятность, что патологические изменения могут быть пропущены при просмотре препарата. Для эффективного цитологического исследования необходимо учитывать:
- при профилактических осмотрах цитологические мазки следует брать у женщин независимо от жалоб, наличия или отсутствия изменений слизистой оболочки. Цитологическое исследование следует повторять не реже, чем раз в три года;
- желательно получать мазки не ранее, чем на 5-е сутки менструального цикла и не позднее, чем за 5 суток до предполагаемого начала менструации;
- нельзя брать материал в течение 48 ч после полового контакта, использования любрикантов, раствора уксуса или Люголя, тампонов или спермицидов, спринцевания, введения во влагалище медикаментов, свечей, кремов, в т. ч. кремов для выполнения ультразвукового исследования;
- беременность – не лучшее время для скрининга, так как возможны неправильные результаты, но, если нет уверенности, что женщина придет на обследование после родов, лучше мазки взять;
- при симптомах острой инфекции желательно получать мазки с целью обследования и выявления патологических изменений эпителия, этиологического агента; также необходим цитологический контроль после лечения, но не ранее, чем через 2 мес. после окончания курса.
Материал из шейки матки должен брать врач-гинеколог или (при скрининге, профилактическом осмотре) хорошо обученная медицинская сестра (акушерка).
Важно, чтобы в мазок попадал материал из зоны трансформации, так как около 90% опухолей исходит из зоны стыка плоского и цилиндрического эпителия и зоны трансформации и только 10% из цилиндрического эпителия цервикального канала.
С диагностической целью материал получают раздельно из эктоцервикса (влагалищной порции шейки матки) и эндоцервикса (цервикального канала) с помощью шпателя и специальной щетки (типа Cytobrush). При проведении профилактического осмотра используют Cervex-Brush, различные модификации шпателя Эйра и другие приспособления для получения материала одновременно из влагалищной части шейки матки, зоны стыка (трансформации) и цервикального канала.
Перед получением материала шейку матки обнажают в “зеркалах”, дополнительных манипуляций не проводят (шейку не смазывают, слизь не удаляют; если слизи много – ее аккуратно снимают ватным тампоном, не надавливая на шейку матки.). Щетку (шпатель Эйра) вводят в наружный зев шейки матки, осторожно направляя центральную часть приспособления по оси цервикального канала. Далее ее наконечник поворачивают на 360° (по часовой стрелке), достигая тем самым получения достаточного числа клеток из эктоцервикса и из зоны трансформации. Введение инструмента выполняют очень бережно, стараясь не повредить шейку матки. Затем щетку (шпатель) выводят из канала.
О чём говорят кокки в мазке
При нарушении микроклимата картина меняется: содержание кокков увеличивается, а полезные бактерии гибнут, поэтому если количество кокков в мазке превышает норму, это говорит о проблемах со здоровьем.
Норма: рН (уровень кислотности) – до 5. Слабокислая среда (начало воспалительного процесса): рН – до 7. Повышенная щелочная среда (активно развивается инфекция или воспаление): рН – более 7,5.
Для определения конкретного заболевания необходимо установить, какая именно разновидность шаровидных бактерий присутствует в избытке, а также выяснить наличие грамотрицательных и грамположительных кокков в мазке. Эти термины появились благодаря датскому учёному Граму и его методу выявления устойчивых к медикаментам кокков. Дело в том, что многие бактерии имеют очень прочную оболочку, непроницаемую для большинства обычных антибиотиков (грамотрицательные). Но и те микроорганизмы, чья клеточная стенка разрушается под воздействием антибактериальных препаратов (грамположительные), тоже способны вызывать серьёзные патологии, поскольку в результате продуктов их распада происходит интоксикация организма. Только благодаря крепкому иммунитету и соблюдению всех правил лечения норма бактерий восстанавливается.
На вопрос: «Что значат кокки в мазке у женщины?» можно ответить так: дисбактериоз влагалища, снижение защитных функций лактобактерий и повышенная вероятность воспалительных процессов. Кокки в мазке у мужчин также указывают на нарушение работы мочеполовой системы.
Внимание! Такое состояние требует квалифицированной медицинской помощи. Народные методы, самостоятельный приём антибиотиков и других лекарств крайне нежелательны и могут лишь усугубить ситуацию.
Для чего нужен мазок на флору
Гинекологический мазок– это то, что в первую очередь должен порекомендовать врач на первичном приеме вне зависимости от симптомов. Это исследование наряду с кольпоскопией входит в золотой стандарт профилактического ежегодного осмотра у женщин. Микроскопия мазка позволяет оценить состояние влагалища и наличие/отсутствие воспалительного процесса в органах репродуктивной системы. Лаборант увидит на предметном стекле количество лейкоцитов, эпителиальных клеток и соотношение бактерий. Если в результатах кокки преобладают над полезными бациллами или визуализируются грибы, это означает дисбактериоз, воспаление или кандидоз. При повышенном количестве лейкоцитов в мазке гинеколог может назначить дополнительные анализы на ИППП.
Разновидности кокков
Выделяют несколько разновидностей бактерий, многие из которых являются условно-патогенными:
- Диплококки (известно более 80 видов). Существуют парами, бывают грамотрицательными и грамположительными. К наиболее патогенному типу относится гонококк – возбудитель гонореи. Заболевание стоит на первом месте по распространённости в числе ИППП (инфекций, передающихся половым путём).
- Стрептококки – микробы, соединённые в цепочку. Внешне кокки в мазке выглядят, как палочки, образованные из нескольких шароподобных клеток. На сегодняшний день открыто более 100 типов стрептококков (все грамположительные). Размножаясь в половых органах, они вызывают вагинит (воспаление влагалища), цистит (воспаление мочевого пузыря), цервицит (воспаление шейки матки), эндометрит (воспаление слизистой матки) и прочие патологии.
- Стафилококки (грамположительные). Представляют собой скопления, похожие на грозди винограда. Насчитывается 27 видов возбудителей, наиболее опасный – золотистый стафилококк. Присутствие большого количества стафилококков во влагалище способствует активному размножению других болезнетворных микробов, например грибков кандида (молочница). На фоне этого нередко воспаляются слизистая и придатки матки.
- Энтерококки (кокки овальной формы, располагающиеся цепочками или парами) – условно-патогенные представители кишечной микрофлоры, которые при недостаточности гигиены способны стремительно развиваться в мочеполовой системе.
- Коккобациллы (промежуточная между бациллами и кокками форма). Гемофильная палочка, гарднерелла, хламидии обнаруживаются при наличии венерических заболеваний, бактериального вагиноза.
- Гонококки. Имеют грамотрицательную структуру и овальную форму. При поражении мочеполового тракта вызывают воспалительную реакцию с последующим развитием цервицита и сальпингита.
Коккобациллы — что это такое?
Содержание статьи
Коккобациллярная флора представляет собой наличие определенного рода бактерий, которые объединяются в 2 подвида — это бациллы и кокки. К ним можно отнести хламидии и возбудителей болезни — гарднереллеза. Нарушение баланса флоры половых органов происходит по причине увеличения количества коккобацилл. Когда это связано с бактериями, которые распространяются половым путем, то развивается бактериальный вагиноз, поражающий сотни миллион женщин на земле.Кокки до определенного момента являются полезными микроорганизмами, но если полиморфная флора нарушена, увеличена щелочная среда влагалища, то исчезает защита и болезнетворные бактерии начинают активно распространяться по половым органам, ухудшая самочувствие пациентки.Появление кокков во влагалище женщины может быть спровоцировано различными факторами, представленными:
- половыми инфекционными заболеваниями;
- игнорированием правил личной гигиены;
- ослаблением иммунной системы;
- аллергическими реакциями;
- длительными приемами антибиотиков;
- гормональными нарушениями;
- мастурбация грязными руками и прочее.
Оптимальное соотношение коккобациллярной флоры в женском организмеКонтрольный мазок берется при каждом плановом посещении гинеколога, либо же при наличии болезненных симптомов половой системы. Благодаря такому анализу определяется количество палочки кокков в выделениях.Полученные анализы можно разделить на 3 вида:
- В слабокислой среде показатели рН не превышают 5,0.
- Умеренное значение для нейтральной среды – рН 7,0.
- Щелочная среда характеризуется показателями рН более 7,5.
Если же полученные результаты не соответствуют статистическим данным, то речь идет о возникновении грамположительных кокков, которые разрушают микрофлору влагалища и ведут к ухудшению репродуктивной системы пациентки.Когда смешанная флора в мазке приближается по показателям к щелочной, тогда можно вести речь о развитии дисбактериоза, по причине запущенного воспаления половых органов.Внимание: размножение коков часто является распространенной причиной бесплодия, а потому нужно не затягивать поход к гинекологу (при появлении специфических выделений и болей в области яичников).
Причины
Факторов, провоцирующих патологию, огромное множество. Основные причины кокков в мазке:
- Неграмотное лечение. В том случае, если человек принимает антибактериальные препараты без назначения или не соблюдает дозировку, вероятность поражения патогенными микробами многократно повышается.
- Пренебрежение личной гигиеной. Игнорирование элементарных правил, неправильное выполнение процедур увеличивают риск нарушения микрофлоры влагалища. Нужно помнить, что мыло – это щёлочь, и слишком глубокие подмывания негативно влияют на кислотно-щелочной баланс. Для женщин, девушек и девочек целесообразно использовать специальные средства для интимной гигиены. Также важно совершать манипуляции от влагалища к анальному отверстию, а не наоборот.
- Ношение белья из плотных материалов или синтетики плохо сказывается на состоянии микроклимата половых органов.
- Беспорядочная сексуальная жизнь. Незащищённый контакт с носителем патогенных микробов в 99 случаев из 100 приводит к заражению. Кроме того, если не иметь постоянного партнёра и при этом регулярно заниматься сексом, микрофлора будет неизбежно подвергаться воздействию «чужих» бактерий.
- Спринцевание. Из-за частых спринцеваний полезная флора вымывается.
- Гормональные сбои. Расстройства гормонального фона вызывают бактериальный дисбаланс.
- Ослабленный иммунитет. Когда защитные функции организма снижаются, он не может противостоять опасным возбудителям.
Интеграция различных лабораторных методов
В диагностике заболеваний шейки матки важное значение имеют клинические данные, результаты исследования на микрофлору (классические микробиологические (культуральные), методы АНК (ПЦР, RT-PCR, Hybrid Capture, NASBA, и др.).
При необходимости уточнения патологического процесса (ASC-US, ASC-H) цитологическое исследование по возможности дополняют молекулярно биологическими (p16, онкогены, метилированная ДНК и др.).
Исследования для обнаружения ВПЧ имеют низкую прогностическую значимость, особенно у молодых женщин (до 30 лет), в связи с тем, что у большинства пациенток этой возрастной группы ВПЧ-инфекция имеет транзиторный характер. Однако несмотря на низкую специфичность теста в отношении интраэпителиальных опухолей и рака, именно у женщин моложе 30 лет он может использоваться в качестве скринингового с последующим цитологическим исследованием. Чувствительность и специфичность значительно увеличиваются при комплексном использовании цитологического метода и исследования для обнаружения ВПЧ, особенно у больных с сомнительными цитологическими данными. Этот тест важен при ведении пациенток с ASC-US, при динамическом наблюдении для определения риска рецидива или прогрессирования заболевания (CIN II, СIN III, carcinoma in situ, инвазивный рак).
Сопутствующие симптомы
Тревожные признаки, связанные с нарушением микрофлоры урогенитальной сферы, в 90% случаев сложно не заметить. У женщин выделения из влагалища приобретают специфический запах (кисломолочный или рыбный), становятся обильными.
Общие для мужчин и женщин симптомы кокков в мазке:
- неприятные ощущения при мочеиспускании и близости;
- зуд и жжение разной степени выраженности;
- отёчность гениталий;
- желтоватые, белые, гнойные, кровянистые выделения из половых органов.
Женщины часто жалуются на боли внизу живота, слабость, отсутствие аппетита. Это связано с тем, что в процессе жизнедеятельности патогенные клетки продуцируют токсические вещества. Также образуются очаги воспаления, из-за которых возникает ощутимый дискомфорт.
При наличии вышеперечисленных признаков следует незамедлительно показаться гинекологу, сдать анализы и пройти полный курс терапии. К самолечению прибегать запрещено!
Классификация
Существует несколько типов классификации вагинального кандидоза. В зависимости от особенностей течения выделяют острую и хроническую (рецидивирующую) формы болезни. В первом случае патология характеризуется яркими симптомами и возникает не чаще четырех раз в год. При хронизации симптоматика, как правило, менее выражена, а само заболевание рецидивирует 4 раза в год и чаще.
В зависимости от наличия осложнений выделяют неосложненный и осложненный вагинальный кандидоз. В первом случае процесс протекает относительно легко и достаточно быстро купируется при подборе адекватной терапии. Как правило, он возникает у женщин, не имеющих дополнительных факторов риска (сахарный диабет, иммунодефицитное состояние различного происхождения).
Осложненная форма вагинального кандидоза характеризуется выраженными признаками, негативным образом влияющими на повседневную жизнь пациентки. Как правило воспаление распространяется на наружные половые органы, провоцирует появление язв и трещин. Такая форма часто рецидивирует.
Локализация патологического процесса позволяет выделить три формы заболевания:
- вагинит: воспаление затрагивает только слизистую влагалища;
- вульвовагинит: поражены наружные половые органы и влагалище;
- цервицит: в процесс вовлекается шейка матки.
Осложнения
Если вовремя не обследоваться и не начать лечение, кокковые инфекции будут распространяться на соседние органы, слизистые и кожные покровы. Осложнения во многом зависят от разновидности клеток. Например, стрептококк провоцирует менингит, пневмонию, остеомиелит (поражение костных тканей). Стафилококк вызывает эндокард (воспаление внутренней оболочки сердца), пиодермию (гнойные воспалительные процессы под кожей), пневмонию, бронхит, заболевания верхних дыхательных путей (риниты, синуситы) и пищеварительного тракта. Кроме того, размножение патогенных бактерий во влагалище снижает выработку эстрогенов, что в результате становится причиной выкидышей и бесплодия.
Кокки в мазке при беременности осложняют процесс вынашивания ребёнка. Рост и развитие плода напрямую связаны с состоянием здоровья будущей матери, а воспалительный процесс может затрагивать не только прямую кишку и мочевыводящий канал, но и матку. Чтобы предотвратить опасность, следует планировать беременность заранее и при необходимости проводить терапию.
Наиболее распространённые последствия кокковых инфекций:
- эрозия шейки матки;
- эндометрит;
- пиелонефрит (поражение почек).
У мужчин при отсутствии адекватного лечения кокки приводят к простатиту (воспаление простаты), поражению яичек и семенных канальцев. Всё это грозит импотенцией и бесплодием.
Анализы на инфекции
Анализ на инфекции (ЗППП и условно-патогенную флору). Далеко не все бактерии и вирусы, обнаруживающиеся во влагалище, необходимо лечить. Например, у вас обнаружилась уреаплазма. Она относится к условно-патогенной флоре, которая имеет право находиться во влагалище. При благоприятных условиях ее наличие не вызывает воспаления и лечить её не надо (то же самое относится к другим у/п бактериям). Обязательно лечить лишь хламидии и микоплазму гениталиум. Это истинные патогены, и даже в небольшом количестве их быть не должно. А все остальное нуждается в лечении лишь при наличии воспаления и дискомфорта.
Итак: если обнаружилась условно-патогенная флора, она нуждается в лечении лишь при сопутствующем воспалении. Если воспаления нет — живите спокойно и не ешьте горстями лишние лекарства!
Яна Александровна Никитенко, врач акушер-гинеколог специалист УЗ-диагностики.
Диагностика
Диагностика представляет собой лабораторное обследование. У женщин с задней стенки влагалища, мочеиспускательного канала и канала шейки матки делают забор мазка. Мужчинам в уретру вводят специальный зонд (если воспаление уже началось, манипуляции могут быть болезненными). Далее образец биоматериала отправляется в лабораторию, где его окрашивают (метод Грама) и исследуют под микроскопом. В некоторых случаях может потребоваться дополнительная диагностика: мазок из зёва и носовой полости (при подозрении на стафилококк), общие анализы крови и мочи.
Перед проведением процедуры важно придерживаться следующих правил:
- не мочиться за 2 часа;
- не употреблять острую пищу и алкоголь за 3-5 дней;
- не принимать лекарственные препараты за 3-5 дней;
- воздержаться от близости за 2 дня;
- не использовать вагинальные свечи, не спринцеваться за 2 дня.
Внимание! Анализ сдают перед менструацией или спустя 4-5 суток после её окончания.
Микрофлора урогенитального тракта у мужчин, обследованных по поводу хронического простатита
Лечение хронической воспалительной патологии урогенитального тракта у мужчин всегда было непростой задачей в урологии. Лечение по поводу этих заболеваний, особенно осложненных нарушением фертильности, сексуальной дисфункцией, синдромом тазовых болей, может быть успешным, если производится индивидуально и базируется на знании этиологии воспалительного процесса, иммунореактивности на данный воспалительный процесс и морфо-функциональные изменений в тазовых органах.
В широкой врачебной практике в настоящее время при диагностике этиологического фактора воспалительной патологии урогенитального тракта акцент делается на выявление инфекций передаваемых половым путем. Целью данного исследования является демонстрация значимости других, не менее важных, этиологических факторов, а также места ИППП в патогенезе данной группы воспалительных заболеваний. Инфекционный воспалительный процесс в урогенитальном тракте возникает по двум механизмам.
В первом случае вирулентная ИППП вызывает клинически и лабораторно идентифицируемый уретрит, который в дальнейшем приводит к возникновению восходящего воспалительного процесса. Патогенетическая роль инфекции передаваемой половым путем в данном случае очевидна: при исследовании отделяемого из уретры, секрета предстательной железы, семенной жидкости выявляется достоверное увеличение количества лейкоцитов и ИППП; первично воспалительный процесс начинается с клиники уретрита. Пациенты с воспалительным процессом такого характера чаще всего находятся на лечении в кожно-венерологических диспансерах, когда помимо острого венерического заболевания имеется клиника простатита.
Второй механизм более сложный. Возникновению инфекционного воспалительного процесса в урогенитальном тракте в данном случае предшествуют определенные предрасполагающие факторы.
Выделим несколько основных групп:
- К первой группе факторов относятся сосудистые, трофические и морфо-фуккциональные изменения в тазовых органах, которые возникают вследствие застойных явлений в органах малого таза, привычных интоксикациях и других причин. Эти изменения хорошо известны и широко обсуждались в специальной отечественной литературе.
- Инфравезикальная обструкция также является предраспологающей причиной инфекционного воспаления. В данном случае возникает ретроградный ток мочи в ацинусы предстательной железы в момент мочеиспускания вследствие повышения внутриуретрального давления. Это может привести к инфицированию предстательной железы микрофлорой из вышележащих мочевых путей.
- Важнейшей предрасполагающей причиной воспалительного процесса урогенитального тракта является вторичный иммунодефицит, который развивается на фоне вялотекущей бактериальной внутриклеточной инфекции (хламидии, микоплазмы) и персистирующей вирусной инфекции ( урогенитальный герпес, цитомегаловирус ). Инфицирование урогенитального тракта данной микрофлорой приводит к характерному нарушению фагоцитарной активности (HCT-тест), снижению иммуноглобулинов класса А при увеличении иммуноглобулинов класса G; нарушению Т хелперного и Т супрессорного взаимодействия. Вторичный иммунодефицит, а также определенные морфо-функциональные изменения в тазовых органах открывают путь к инфицированию урогенитального тракта банальной патогенной и условно-патогенной бактериальной микрофлорой.
При развитии инфекционного процесса в урогенитальном тракте по данному механизму отсутствует какая-либо клиника уретрита, в исследованиях отделяемого из уретры будет отсутствовать достоверное увеличение количества лейкоцитов, в соскобах из уретры будет значительно реже выявляться ИППП, однако у пациентов будет присутствовать клинически и лабораторно идентифицируемый воспалительный процесс в простато-везикулярном комплексе или в органах мошонки.
При наличии вышеуказанных предрасполагающих факторов инфицирование урогенитального тракта банальной бактериальной микрофлорой принципиально возможно двумя путями: трансуретральным и гематогенным.
Гематогенным путем инфицирование чаще всего происходит из очагов хронической инфекции при сопутствующей ЛОР- патологии, заболеваниях, имеющих широчайшее распространение у населения; при заболеваниях прямой кишки с хроническими запорами, геморрое ( особенно при частых обострениях). Инфицирование по данному пути чаще всего происходит тогда, когда в предстательной железе уже имеются выраженные структурные изменения ( конгестия, кальцинаты, ДГПЖ ).
Более значим трансуретральный путь инфицирования вторичной бактериальной микрофлорой.Следует выделить 4 основных источника бактериального инфицирования.
- Широкое распространение бактериального вагиноза у женщин. По данным Преображенской клиники у женщин, обследованных по поводу воспалительных заболеваний половых органов, в 20% случаев выявлен бактериальный вагиноз. Причиной бактериального вагиноза является мелкая условно-патогенная палочковая флора, которая нередко приводит к инфицированию урогенитального тракта мужчин. Причиной бактериального вагиноза являются вялотекущие бактериальные и персистирующие вирусные инфекции, гормональные нарушения и другие причины, вызывающие вторичный иммунодефицит. В супружеских парах у женщин страдающих бактериальным вагинозом, у мужей значительно чаще выявляется хронический простатит, чем у женщин с воспалительными гинекологическими заболеваниями, но не имеющих бактериальный вагиноз.
Таблица микроорганизмов, наиболее часто встречающихся в половых органах у женщин при воспалительных заболеваниях, вызванных влагалищной гарднареллой и неспорообразующими бактериями. ( сборник трудов УрНИИДВиИ, 1985 год )
| Виды микроорганизмов. | Морфологические особенности. |
| Влагалищная гарднарелла | Коккобациллы одиночные, парные, полиморфные |
| Недифференцированные виды | Коккобациллы полиморфные |
| Коринеформы | Палочки булавовидные |
| Бифидобактерии | Палочки вариабельные, часто с раздвоенными концами. |
| Бактериоиды | Палочки, коккобациллы, часто биполярно окрашены |
| Лактобактерии | Полиморфные полочки, часто расположены длинными нитями. |
| Анаэробные кокки | Кокки, одиночные, группами или цепями. |
| Аэробные кокки | Кокки, цепочки, тетрады, скопления. |
| Пропионибактерии | Полиморфные палочки, булавовидные, кокковидные. |
| Виолонеллы | Кокки, диплококки, скопления или цепочки. |
| Фузобактерии | Палочки крупные, полиморфные, чаще длинные с заостренными концами, могут быть утолщения в центре. |
- Распространенность оральногенитальных и анальных половых сношений также является источником инфицирования урогенитального тракта мужчин. В первом случае инфицирование происходит преимущественно стрептококковой или стафилококковой микрофлорой, во втором случае — Гр- палочковой флорой ( протей, клебсиелла, кишечная палочка и т.д. ).
Клинический случай.
Пациент N13603 Игорь Николаевич, 30 лет обратился 16.05. 98 года с жалобами на тазовые боли. Обследован в УрНИИДВиИ на предмет наличия ИППП — гонорея, трихомониаз, кандидоз, гарднареллез, хламидиоз, уреаплазмоз, микоплазмоз, ВПГ не обнаружены , в секрете предстательной железы лейкоцитов 20-40-80 в п/з, данных за экстрагенитальную воспалительную патологию нет. Выполнено бактериологическое исследование секрета простаты. Выявлен стафиллококк с гемолизом и Гр+ палочка с гемолизом ОМЧ 10х9 в 1 мл отделяемого. При дополнительном расспросе выяснено, что в семье регулярно практикуется оральногенитальный секс, а супруга страдает хроническим тонзиллитом и гайморитом с частыми обострениями. Супруга ( N13784 Анна Сергеевна, 29 лет ) направлена к отоларингологу. В бактериологическом исследовании смыва с миндалин выявлен стафилококк с гемолизом, Гр+ палочка с гемолизом, ОМЧ 10х6 в 1 мл отделяемого, подтверждено наличие хронического тонзиллита и гайморита в фазе подострого течения.
- Ятрогенное инфицирование госпитальной микрофлорой при проведении уретральных лечебных или диагностических процедур широко распространенных в настоящее время.
- Инфицирование из верхних мочевых путей и мочевого пузыря, особенно при наличии инфравезикальной обструкции.
Ниже наглядно представлен механизм развития бактериального воспаления в урогенитальном тракте, когда его причиной не являются инфекции передаваемые половым путем.
Целью данной работы был анализ микрофлоры у пациентов обследованных по поводу хронического простатита. Помимо обследования на ИППП за 1996-98 годы в Преображенской клинике по различным показаниям было выполнено более 200 бактериологических посевов у мужчин.
Бактериологическое исследование секрета простаты проводится на базе бактериологической лаборатории УрНИИДВиИ. Предварительно перед забором материала пациенту предлагается опорожнить мочевой пузырь и выполнить туалет головки полового члена и препуциального мешка. Далее выполняется массаж предстательной железы, ее секрет помещается в пробирку со средой накопления — сахарным бульоном. Пробирки в термостате доставляются в бактериологическую лабораторию в течении 40-60 минут, где сразу производится рассеивание материала на 4 питательных среды: мясопептонный агар, кровяной агар, среду “Эндо” и среду Сабура. Через 24 часа для дальнейшей идентификации возбудителя производится пересеивание на соответствующие питательные среды ( например для идентификации стафилококка в желточно- солевой агар для оценки лицето-вителлазной активности, в плазму крови для оценки плазмо-коагулирующей активности ). Через 5 суток производится “считывание” результатов, чистые культуры пересеваются на среды с дисками пропитанными антибактериальными препаратами и через сутки “считывается” антибиотикограмма.
В исследуемую группу вошли только те пациенты у которых при наличии клинико-лабораторных данных за воспалительный процесс в простато-везикулярном комплексе, отсутствовали какие-либо данные за воспаление в уретре, те соблюдались следующие нижеуказанные условия.
- Минимальный объем обследования: анализ мазка, исследование секрета предстательной железы, обследование на хламидиоз, уреаплазмоз, микоплазмоз, хроническую гонорею, кровь на ВИЧ, RW, бактериологическое исследование секрета предстательной железы, УЗИ предстательной железы трансректальным датчиком.
- Весь комплекс обследования выполнен в течении не более 14 дней.
- Отсутствие клиники уретрита, а в исследовании отделяемого из уретры лейкоцитов менее 10 в поле зрения.
- Отрицательная реакция Вессермана и отсутствие ВИЧ.
Таким образом, в исследуемой группе оказалось 63 пациента в бактериологическом исследовании секрета предстательной железы которых было выделено 113 микроорганизмов. Возраст пациентов колебался от 20 до 65 лет. Отметим определенную закономерность суммарной степени лейкоцитоза в секрете предстательной железы у пациентов различных возрастных групп.
| Возраст | Количество человек | % | Количество лейкоцитов min | Количество лейкоцитов average | Количество лейкоцитов max |
| 20-29 лет | 18 | 28 | 21 | 35 | 65 |
| 30-39 лет | 25 | 40 | 34 | 58 | 101 |
| 40-49 лет | 13 | 21 | 27 | 44 | 93 |
| 50-65 лет | 7 | 11 | 24 | 44 | 83 |
В первой возрастной группе в связи с тем, что воспалительный процесс начался относительно недавно лейкоцитоз еще достаточно умеренный. Во второй группе, где анамнез воспалительного процесса уже длительный, а иммунный ответ на воспалительный процесс достаточно активный, лейкоцитоз самый высокий из представленных групп. В третьей и четвертой группе, несмотря на выраженные структурные изменения со стороны предстательной железы, лейкоцитоз вновь уменьшается. Это, возможно, происходит в связи со значительным снижением иммунного ответа при длительном хроническом воспалительном процессе.
Структура выявленной микрофлоры в бактериологическом исследовании секрета предстательной железы представлена в таблице N1.
Данные выполненного исследования необходимо оценивать с большой степенью критичности по следующим соображениям:
- В данной лаборатории отсутствует анаэростат для выполнения посева в анаэробных условиях, следовательно количество анаэробных микроорганизмов должно быть значительно больше.
- Значительный рост условно-патогенной микрофлоры подчас закрывает истинного возбудителя воспаления. При повторном бактериологическом исследовании после лечения значительно чаще высевается патогенная микрофлора. Однако данная тема выносится за рамки этой работы.
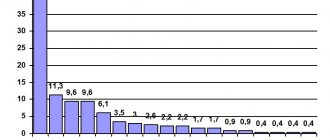
Были выявлены как патогенные, так и условно-патогенные микроорганизмы. Соотношение патогенных и условно-патогенных микроорганизмов представлено в диаграмме.
Микроорганизмы высевались как в качестве моноинфекции, так и в ассоциациях, что представлено в таблице N2.
Таким образом видно, что в 68,2% случаев в бактериологическом исследовании секрета предстательной железы высеваются ассоциации микроорганизмов. Отметим, что у 46% обследованных ( те 29 пациентов из 63 ) в секрете предстательной железы выявлены микроорганизмы вызывающие гемолиз кровяного агара, причем чем выше степень ассоциации, тем чаще в ее структуре выявляется гемолитический микроорганизм. Более чем у половины пациентов выявляются ИППП , причем их выявляемость остается практически одинаковой при любой степени ассоциации.
Эти данные представлены в таблице N2.
В таблице N3 представлена выявленная гемолитическая микрофлора:
На представленной диаграмме видно, что преобладает выявляемость стафилококкой микрофлоры, что соответствует общему раскладу выявляемой микрофлоры. Втором место занимает Грам+ палочковая флора ( неидентифицированная Гр+ палочка и коринобактерии), на третьем месте стрептококк. Отдельно отметим, что определенная часть Грам- палочковой флоры также проявляет гемолитическую активность ( 12,5% от общего количества выявленных Грам- бактерий ).
Все остальные микроорганизмы мы отнесли к условно-патогенной микрофлоре. Мы решили не выделять из данной группы микроорганизмы, которые можно рассматривать скорее как сапрофиты. По нашему мнению относить тот или иной микроорганизм в разряд сапрофитной микрофлоры необходимо индивидуально, учитывая все данные клинико-лабораторной диагностики.
Условно-патогенная микрофлора представлена в таблице N4.
По структуре патогенной и условно-патогенной микрофлоры нетрудно заметить, что выявляемая кокковая микрофлора, особенно стрептококковая, также характерна для хронических заболеваний полости рта. Гр+ и Гр- палочковая микрофлора — частый возбудитель бактериального вагиноза у женщин, кроме того Гр- палочковая — это нередко госпитальная микрофлора и инфекция, выявляемая при хронических воспалительных заболеваниях мочевыводящей системы.
У 33 пациентов т.е. у 52,4% обследованных при отсутствии клинико-лабораторных признаков воспалительного процесса в мочеиспускательном канале были обнаружены ИППП.
Выявленные ИППП представлены в таблице N5.
Гонорея идентифицировалась при исследовании соскоба из уретры PCR-методом.
Дрожжевые клетки выявлялись при бактериоскопическом исследовании отделяемого из уретры или в бактериологическом исследовании секрета простаты с идентификацией до вида. Хламидиоз идентифицировался при исследовании соскоба из уретры методом PCR или ПИФ или при наличии иммуноглобулинов класса М к инфекции. Уреаплазмоз и микоплазмоз идентифицировался при исследовании соскоба из уретры методом PCR. ВПГ и ЦМВ идентифицировались при исследовании соскоба из уретры методом PCR или при наличии иммуногобулинов класса М к инфекции.
Проведен сравнительный анализ выявляемости ИППП у пациентов в двух группах:
1 группа — в бактериологическом посеве секрета предстательной железы есть патоген, 2 группа — в бактериологическом посеве выявляется только условно-патогенная микрофлора.
Полученные данные представлены в таблице N6.
Таким образом видно, что одинаково в обеих группах выявляется кандидоз, уреаплазмоз, микоплазмоз, вирусы. Но в группе с патогенной микрофлорой значительно чаще выявляется гонорея и хламидиоз. Практически у пациентов с клинико-лабораторными данными воспалительного процесса в простато-везикулярном комплексе и при наличии хламидиоза, всегда высевается гемолитическая бактериальная микрофлора!!!
Еще одна причина по которой была выполнена данная работа демонстрируется данными следующей диаграммы.
Выводы:
- У всех пациентов, обследованных по поводу хронического простатита при отсутствии клинико-лабораторных данных острого или хронического уретрита, при бактериологическом исследовании секрета предстательной железы выявлена неспецифическая бактериальная микрофлора. У 46% пациентов ( у 29 из 63 человек ) выявлена патогенная ( гемолитическая ) микрофлора.
- У 54% пациентов выявлена условно-патогенная микрофлора, патогенность этой микрофлоры оценивается исходя из конкретной клинической ситуации с учетом всех данных обследования.
- В 68% случаев микроорганизмы высевались ассоциациями. Причем, чем выше степень ассоциации, тем чаще в ней определялся микроорганизм с гемолитической активностью.
- Структура бактериальной микрофлоры урогенитального тракта у мужчин ( как с гемолитической активностью, так и без нее ) позволяет предполагать ее возможный источник — это бактериальный вагиноз и заболевания полости рта у половых партнеров, а также, возможно, гематогенный путь инфицирования.
- У 52,4% пациентов при отсутствии клинико-лабораторных данных острого или хронического уретрита были выявлены инфекции передаваемые половым путем. Причем в тех случаях, когда в соскобах со слизистой уретры PCR — методом определялась гонококки или хламидии, при бактериологическом исследовании секрета простаты определялась гемолитическая микрофлора.
- Учитывая достаточно выраженную устойчивость выявленной микрофлоры к антибактериальным препаратам, показано включать бактериологический посев секрета предстательной железы в программу обследования пациентов с воспалительными заболеваниями урогенитального тракта.
Журавлев В.Н., Власенко Л.Ю., Панков В.И.
Лечение
Если обнаружено аномальное количество кокков в мазке, лечение нужно проводить в соответствии со всеми врачебными предписаниями. Настоятельно рекомендуется не использовать антибиотики общего назначения. Как уже упоминалось, многие кокки устойчивы к таким медикаментам, поэтому терапия может оказаться не только безрезультатной, но и опасной. Под воздействием антибактериальных средств рост патогенных клеток начнёт увеличиваться, а численность полезных бактерий – снижаться.
Для того чтобы борьба с кокками была максимально эффективной, предварительно проводится тест на чувствительность. Антибиотикограмма – бакпосев влагалища на питательную среду позволяет определить уровень восприимчивости патогенных клеток к тем или иным препаратам.
Одним из наиболее действенных препаратов против кокковых инфекций считается «Метронидазол». Его основное преимущество – отсутствие противопоказаний к применению в период беременности и кормления грудью. Совместно с антибиотиками используют лекарства, содержащие лакто-, и бифидобактерии. Для восстановления нормальной микрофлоры применяются вагинальные свечи, мази и кремы, обладающие антисептическими свойствами. Одновременно могут быть назначены иммуномодулирующие средства. Спринцевания травяными отварами нужно выполнять строго с разрешения гинеколога.
Внимание! Параллельно проходить лечение должен и постоянный половой партнёр. В это время лучше воздержаться от секса и мастурбации, использования тампонов.
После завершения курса терапии мазок на флору делают повторно. При отсутствии положительного результата подбирается другая группа антибиотиков. В 70-80% случаев госпитализация не требуется, лечение проводится в домашних условиях или амбулаторно.
Лечение вагинального кандидоза
Специфическое лечение, направленное на устранение вагинального кандидоза, проводится только после выявления возбудителя и при наличии у пациентки признаков заболевания. Основой терапии являются специфические противогрибковые средства: нистатин, клотримазол, кетоконазол, флуконазол, нитрофунгин и другие. Конкретный препарат, его доза, кратность приема и длительность курса подбираются в индивидуальном порядке в зависимости от особенностей течения заболевания, наличия сопутствующих патологий и других факторов.
Если речь идет об остром неосложненном процессе, препараты назначаются в местной форме в виде свечей, вагинальных таблеток или кремов. Они вводятся непосредственно в половые пути, где останавливают активное размножение возбудителя.
При наличии осложнений, а также при хроническом течении заболевания используются препараты системного действия в виде таблеток для приема внутрь. Схема применения подбирается в индивидуальном порядке.
До полного устранения проявлений вагинального кандидоза необходимо соблюдать половой покой, чтобы минимизировать травмирование воспаленных стенок половых путей. При хроническом течении необходимо использовать презервативы. Эффективность терапии оценивается через 14 дней после начала лечения.
Записаться на прием