Гипертиреоз – это состояние гиперфункции щитовидной железы, которое сопровождается избыточной выработкой тироксина и трийодтиронина. Повышение уровня гормонов в крови ускоряет обменные процессы в организме и оказывает негативное влияние практически на все системы органов. Симптомы гипертиреоза снижают качество жизни больного. Гипертиреоз – это состояние гиперфункции щитовидной железы, которое сопровождается избыточной выработкой тироксина и трийодтиронина. Повышение уровня гормонов в крови ускоряет обменные процессы в организме и оказывает негативное влияние практически на все системы органов. Симптомы гипертиреоза снижают качество жизни больного.
Адекватное и своевременное лечение позволяет предотвратить осложнения и замедлить патологические процессы, вплоть до полного восстановления функции щитовидной железы.
Виды гипертиреозов
Существует три формы заболевания:
- Субклиническая. Явные симптомы отсутствуют, уровень Т4 в норме, уровень трийодтиронина понижен;
- Манифестная. Проявляются характерные признаки гипертиреоза. Уровень Т4 в норме, уровень трийодтиронина низкий;
- Осложненная. Симптоматика включает сердечную недостаточность, аритмию, психоз и другие тяжелые состояния.
По уровню возникновения гипертиреоз бывает:
- первичный – патология щитовидной железы;
- вторичный – поражается гипофиз;
- третичный – процессы развиваются в гипоталамусе.
Причины гипертиреоза
К дисфункции щитовидной железы приводит ряд эндокринных заболеваний, таких как:
- Болезнь Грейвса (Базедова, Базедова-Грейвса). Синдром носит аутоиммунный характер. В организме вырабатываются антитела, которые стимулирую щитовидную железу на выработку избыточного количества гормона Т4;
- Узловой зоб, токсическая аденома. Перечисленные патологии сопровождаются формированием доброкачественных узлов в тканях железы. Образования начинают вырабатывать гормоны и вызывают гипертиреоз. Врачи пока не могут сказать точно, почему одни аденомы синтезируют Т4, а другие – нет;
- Тиреоидит. Воспалительный процесс разрушает клетки щитовидки. Гормоны попадают в кровь и вызывают гипертиреоз. Возможен аутоиммунный характер тиреоидитов. В организме вырабатываются антитела против рецепторов ТТГ. Клетки вызывают активный рост и воспаление щитовидной железы.
Заболеванию наиболее подвержены люди с наследственной предрасположенностью к эндокринным патологиям. Симптомы гипертиреоза щитовидной железы чаще наблюдаются у женщин, чем у мужчин. На развитие заболевания также влияет экологическая обстановка, хронический йододефицит, стрессы.
Симптомы гипертиреоза
Первые признаки дисфункции нехарактерные, поэтому заболевание часто путают с другими соматическими состояниями. Симптомы гипертиреоза щитовидной железы нарастают по мере нарушения обменных процессов в организме.
Основные признаки болезни:
- потеря массы тела при сохранении аппетита, объема и качества пищи;
- аритмия, тахикардия;
- тревожное состояние, депрессивность;
- повышение потливости;
- мелкий тремор пальцев и кистей рук;
- нарушение пищеварения;
- формирование видимого зоба, изменяющего контуры шеи;
- повышенная утомляемость.
Симптомом гипертиреоза у мужчин является снижение потенции, полового влечения. У женщин повышение уровня гормонов щитовидной железы вызывает нарушения менструального цикла. Беременность может закончиться самопроизвольным абортом. Симптомом гипертиреоза щитовидной железы у женщин также может являться снижение фертильности вплоть до бесплодия. В период менопаузы патология в начальных стадиях протекает бессимптомно.
Тахикардия – симптомы
Основные симптомы тахикардии таковы:
- учащение пульса (90 и больше ударов в минуту);
- учащение сердцебиения (желудочковая тахикардия);
ВАЖНО! Частота сердечных сокращений (ЧСС) и пульс в норме должны совпадать по количеству ударов в минуту. ЧСС – это количество сердечных сокращений в минуту, а пульс – количество расширений артерии за это же время, в моменты «выбросов» крови сердцем. При тахикардии и других сердечных заболеваниях показатели ЧСС и пульса могут отличаться.
- понижение артериального давления;
- ощущение тяжести в груди, вплоть до удушья;
- одышка, иногда даже при незначительных физических нагрузках или в состоянии покоя;
- влажность кожи;
- перебои и «провалы» в работе сердца;
- головокружения, темнота в глазах, предобморочное состояния (иногда обмороки, связанные с нарушением мозгового кровообращения);
- боли в области сердца – этот симптом характерен для тахикардии на фоне вегето-сосудистой дистонии (ВСД) и некоторых других патологических состояний.
Если вы обнаружили у себя один или больше из перечисленных симптомов и подозреваете, что у вас тахикардия – что делать в первую очередь? Разумеется – обратиться к кардиологу, который направит вас на определенные обследования и анализы, а затем назначит лечение. Необходимые анализы можно сдать и заранее, чтобы прийти к врачу с уже готовыми результатами.
Осложнения гипертиреоза
По мере развития болезни симптомы гипертиреоза щитовидки усиливаются, могут возникать осложнения:
- Нарушения в работе сердца. К общим симптомам гипертиреоза добавляется мерцательная аритмия. Больной плохо переносит физические нагрузки, наблюдается нарушение ритма сердца. Возможно развитие застойной сердечной недостаточности. Последствия обратимы. После устранения гипертиреоза признаки аритмии полностью излечиваются.
- Повышенная ломкость костей. В запущенной форме гипертиреоз вызывает нарушения в структуре костной ткани. Развивается остеопороз. Причина ломкости костей в том, что избыток гормонов мешает кальцию встраиваться в кость.
- Заболевания глаз. Базедова болезнь к симптомам гипертиреоза добавляет офтальмопатию Грейвса. Причина патологии в разрастании и отечности тканей, расположенных за глазными яблоками. Пациент чувствует резь в глазах, чувствительность к свету, жалуется на двоение. Острота зрения постепенно снижается. В запущенных случаях развивается слепота.
- Проблемы с кожей. Глазные симптомы при гипертиреозе часто развиваются параллельно с дермопатией Грейвса. Кожа отекает и краснеет, особенно в районе стоп и голеней.
- Тиреотоксический криз. Повышение уровня гормонов щитовидки в крови может вызывать внезапное лихорадочное состояние, усиление всех основных симптомов. Тиреотоксический криз сопровождается тахикардией. В некоторых случаях наблюдается делирий (психическое нарушение). Пациенту требуется экстренная медицинская помощь.
Виды тахикардии
Тахикардия как таковая делится на две группы:
- физиологическая, которая не считается патологией и бывает следствием физических нагрузок, а также встречается у детей-дошкольников, а затем и у подростков в период изменения гормонального фона. Кроме того, эту «безопасную» тахикардию могут вызывать и некоторые внешние факторы помимо физнагрузок – стрессы, эмоциональное возбуждение, жара, кофе, алкоголь, некоторые лекарства, резкие смены положения тела и др. Во всех этих случаях в кровь выбрасывается некоторое количество адреналина, что и служит «спусковым механизмом» для учащения сокращений сердца;
- патологическая тахикардия – это уже заболевание, причем оно может быть связано не обязательно с сердечно-сосудистой, но и с другими системами организма. Такая тахикардия при несвоевременном выявлении приводит к различным органическим патологиям, в том числе и касающимся сердечно-сосудистой системы – инфарктам, инсультам.
Патологическая форма заболевания тоже делится на виды в зависимости от частей сердца, «ускоряющих» его работу – предсердий (предсердная тахикардия) и желудочков (желудочковая тахикардия). Подвид желудочковой тахикардии – синусовая тахикардия.
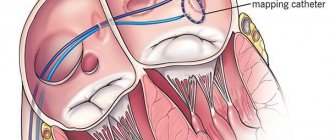
Диагностика гипертиреоза
Консультация эндокринолога
Диагностика гипертиреоза начинается с приема эндокринолога. На приеме врач задает пациенту вопросы, которые помогут в диагностике: как давно появились клинические симптомы, какая динамика болезни, нет ли в семье других больных с зобом или тиреоидитом. Обязательно проводится физикальное исследование: пальпация щитовидной железы. При явном гипертиреозе врач попытается прощупать контуры органа, определить его положение, однородность структуры, болезненность. После осмотра пациент получает направления на дальнейшие обследования для точной диагностики причины заболевания.
Лабораторные исследования
Гипертиреоз подтверждают анализы крови на уровень гормонов щитовидки. Повышенное содержание тироксина при отсутствии или минимальном количестве ТТГ указывают на гиперфункцию железы. Анализ крови особенно важен в ранней диагностике заболевания у лиц пожилого возраста. Например, симптомы гипертиреоза у женщин в менопаузе могут отсутствовать. Патологию выявляют только по результатам лабораторных исследований.
Анализ крови помогает подтвердить состояние эндокринного органа, а для определения причины гипертиреоза потребуются дополнительные обследования.
Инструментальные методы исследования
Ультразвуковое исследование. УЗИ щитовидной железы позволяет определить форму, размеры долей, оценить степень ее увеличения, обнаружить узлы, кисты, другие новообразования.
Радиоизотопная сцинтиграфия. Пациенту вводят внутривенно специальный раствор. В препарате содержатся радиоактивные изотопы йода, которые активно захватываются щитовидной железой. Через некоторое время врач оценивает степень насыщения тканей и делает вывод об их функциональности. Большое количество радиойода указывает на избыточную выработку тироксина, которая развивается, в частности, при болезни Грейвса.
Если при выраженных симптомах гипертиреоза щитовидки у женщины или мужчины наблюдается минимальное количество изотопов в железе, то вероятная причина патологии – тиреоидит. Тест на захват радиоактивного йода помогает в дифференциальной диагностике.
Тонкоигольная биопсия. Под контролем датчика УЗИ врач берет образцы тканей щитовидной железы для исследования. Материалы биопсии позволяют установить характер новообразований: доброкачественные или злокачественные. Результаты исследования также дают информацию об аутоиммунных процессах, которые могут вызывать гипертиреоз.
Лечение гипертиреоза
Подход к терапии зависит от причины гипертиреоза, возраста и состояния пациента.
Консервативные методы лечения:
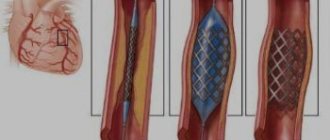
- Препараты радиоактивного йода. Изотопы накапливаются в тканях щитовидной железы, подавляя компенсаторные механизмы. Орган уменьшается в размерах, симптомы гипертиреоза постепенно ослабевают. Лечение занимает несколько месяцев. Важно, что радиоактивный йод подавляет функцию железы, поэтому со временем у пациента может развиться гипотиреоз, который восполняется гормонозаместительной терапией.
- Антитиреоидные препараты. Лекарства подавляют выработку гормонов щитовидной железой. Симптомы уменьшаются через несколько недель после приема препаратов в правильно рассчитанной дозировке. Курс лечения составляет до 1 года и дольше. В некоторых случаях гипертиреоз излечивается полностью, иногда возникают рецидивы. Важно, что антитиреоидные препараты могут вызывать аллергию, индивидуальную непереносимость, могут снижать иммунитет. Воздействием данной группы лекарств обуславливают нарушения в работе печени. Принимать препараты можно только под контролем врача.
- Симптоматическое лечение. В зависимости от тяжести проявлений гипертиреоза врач может назначить лекарства для снижения артериального давления, поддержания сердечного ритма и т. д. Симптоматическое лечение продолжают до улучшения общего самочувствия пациента.
В случае тяжелого гипертиреоза, сопровождающегося значительным увеличением щитовидной железы, множественными новообразованиями в функциональной ткани, а также при медуллярном раке показано хирургическое вмешательство. Врач частично или полностью удаляет эндокринный орган. После операции пациенту подбирают дозировку гормонов, которые принимают пожизненно.
Тиреоидные кардиопатии
Сердце при субклиническом гипотиреозе
Субклинический гипотиреоз — это патологическое состояние, характеризующееся нормальным уровнем общего и свободного тироксина (Т4) и повышенным уровнем тиреотропина (ТТГ), или гиперсекрецией ТТГ, в ответ на введение тиролиберина (ТЛГ).
Следует помнить, что в ряде случаев даже при манифестном гипотиреозе, особенно у пожилых, не наблюдается повышения уровня ТТГ. Такая особенность обусловлена экологическим неблагополучием (загрязнением окружающей среды свинцом, кадмием, оксидом углерода и т.д.), воздействием лекарств (препаратов раувольфии, клофелина и др.), дефицитом белка в пище. Также давно отмечено, что в зоне йодного дефицита снижен синтез ТТГ гипофизом.
Кардиологические «маски» субклинического гипотиреоза следующие:
- стойкая гиперхолестеринемия, атерогенная дислипидемия;
- атеросклероз;
- ИБС;
- аритмии (синусовая брадикардия или тахикардия, политопная экстрасистолия, пароксизмы мерцания и трепетания предсердий, синдром слабости синусового узла);
- цереброваскулярная болезнь;
- артериальная гипертензия;
- ПМК (и/или других клапанов), гидроперикард.
К субклиническому гипотиреозу относится эндемический зоб (ЭЗ). О том, что при ЭЗ у больных появляются кардиальные жалобы, может изменяться звучность тонов сердца, сердечный ритм, известно давно. Однако раньше считали эти изменения деятельности сердечно-сосудистой системы нерезко выраженными и обусловленными вегетативной дизрегуляцией. Широкое применение ультразвукового метода исследования сердца выявило частое развитие пролапса митрального клапана (ПМК) или других клапанов при ЭЗ и в других случаях субклинического гипотиреоза. ПМК — это систолическое выпячивание одной или обеих митральных створок в полость левого предсердия выше уровня митрального кольца. При этом нарушение смыкания створок с развитием митральной регургитации развивается не всегда. Известно более 50 заболеваний, при которых может развиться ПМК. Однако ЭЗ и гипотиреозу как этиологическим факторам ПМК должного внимания не уделено даже в литературе последних лет. Между тем даже ничтожный дефицит тиреоидных гормонов в организме обусловливает серьезные нарушения обменных процессов, в том числе дистрофические изменения в сердце, сопровождающиеся снижением интенсивности окислительного фосфорилирования, замедлением синтеза белка, уменьшением поглощения кислорода миокардом, электролитными сдвигами. Поражается как сократительный миокард, так и строма. В кардиомиоцитах откладывается креатинфосфат и возникает так называемая псевдогипертрофия миокарда. В сердце, как и в других тканях, депонируются кислые гликозаминогликаны, приводящие к слизистому отеку миокарда и стромы. При ЭЗ и гипотиреозе в 100% случаев вовлекается вегетативная нервная система. Вегетативная дистония характеризуется гипертонусом вагуса, то есть возникает парасимпатическая вегетативная дизрегуляция сердца. Как правило, ПМК у больных ЭЗ и субклиническим гипотиреозом имеет «немое» течение: количество сердечных сокращений, конфигурация сердца остаются в норме, однако в большинстве случаев наблюдается снижение одного или обоих тонов. Классические проявления ПМК — мезосистолический, реже протосистолический, или поздний систолический щелчок, прекардиальный «клик» (аускультативный феномен резонации митральной створки) не регистрируются. При анализе электрокардиограмм отклонения от нормы (синусовая брадикардия, замедление проведения импульсов в разных отделах миокарда, снижение вольтажа зубцов, особенно зубца Т) наблюдаются в 80% случаев, но не носят закономерного характера. Ультрасонографией установлено, что на фоне скрытого гипотиреоза часто встречается ПМК, в отдельных случаях сочетаясь с пролапсом трикуспидального и/или аортального (крайне редко — пульмонального) клапана. Смещение створок митрального клапана в полость предсердия достигает 3-7 мм; это I или II степень ПМК. Регургитация обнаруживается лишь в единичных случаях; диастолическое открытие митрального клапана не нарушается, объем левого предсердия в норме и, следовательно, серьезные нарушения гемодинамики не развиваются. Тем не менее ПМК можно назвать важным диагностическим симптомом ЭЗ и субклинического гипотиреоза. Пролабирование III степени, то есть более 9 мм, нехарактерно для больных субклиническим гипотиреозом. В этих случаях, даже при наличии ЭЗ, следует искать другие причины ПМК. Несмотря на отсутствие регургитации и нарушений гемодинамики у больных ЭЗ с ПМК, сохраняется опасность осложнений пролапса. Характерные осложнения ПМК — это инфекционный эндокардит, тромбоэмболии, внезапная смерть. Поэтому актуальной является разработка методов терапии ПМК у больных ЭЗ и субклиническим гипотиреозом. Известно, что для лечения ПМК используют (-адреноблокаторы с целью подавления повышенной при ПМК сократимости миокарда левого желудочка, а также для увеличения его объема и профилактики аритмий. Следует подчеркнуть, что (-адреноблокаторы противопоказаны при гипофункции щитовидной железы, поскольку оказывают антитиреоидное действие и усиливают гипотиреоз. Кроме того, парасимпатикотония также служит противопоказанием к применению этих препаратов у таких больных. Систематическая заместительная терапия препаратами тиреоидных гормонов уменьшает или полностью ликвидирует ПМК у больных ЭЗ и субклиническим гипотиреозом. Наоборот, без коррекции тиреоидной недостаточности может появиться пролапс других клапанов и нарастать регургитация.
Другой эхокардиографической находкой у больных с субклиническим гипотиреозом, в том числе у больных ЭЗ, может быть гидроперикард, который протекает бессимптомно. Обычно выпот локализуется в области верхушки и по правому контуру сердца.
Сердце при субклиническом гипертиреозе
Субклинический гипертиреоз — состояние, при котором понижается концентрация ТТГ (без гипофизарной недостаточности) в сыворотке крови, в то время как уровни тиреоидных гормонов в сыворотке остаются в пределах нормальных показателей.
Прежде чем ставить диагноз субклинического гипертиреоза, особенно у пожилых, необходимо неоднократное определение уровня ТТГ в динамике через несколько недель, поскольку снижение базального уровня ТТГ может наблюдаться при различных нетиреоидных заболеваниях, депрессии, приеме некоторых медикаментов и т.д. Истинная распространенность субклинического гипертиреоза в нашей стране пока не изучена. В Англии она составляет около 10% у женщин, в других странах варьирует от 0,5% до 11,8%.
Причины субклинического гипертиреоза различны: это эутиреоидный вариант болезни Грейвса, токсическая аденома щитовидной железы, следствие разрушения тиреоцитов при подостром или хроническом тиреоидите, а также недостаточное адекватное лечение явного гипертиреоза. Наиболее частой причиной снижения уровня ТТГ является прием тироксина (медикаментозный субклинический гипертиреоз). Нередко он возникает при беременности. Гестационный гипертиреоз, вызванный повышением уровня хорионического гонадотропина при развивающейся беременности, также часто может быть субклиническим. Йод-базедовизм, высокое йодопотребление при несовершенной массовой профилактике ЭЗ во многих случаях течет, как субклинический гипертиреоз. Для клинициста важен ответ на вопрос, влияет ли субклинический гипертиреоз на здоровье, и прежде всего на сердечно-сосудистую систему, или это лишь лабораторная находка.
Влияние тиреоидных гормонов на систему кровообращения хорошо известно. Они играют важную роль в регуляции энергетического обмена в организме. Недавно уточнено их действие на митохондриальные процессы в клетках, в том числе в кардиомиоцитах. Тиреоидные гормоны регулируют липидный состав митохондриальных мембран, содержание цитохромов и кардиолипинов в клетках и т.д., в итоге стимулируя клеточное дыхание. Эти эффекты делятся на кратковременные (несколько часов) и длительные (несколько дней). При субклиническом гипертиреозе эти процессы нарушаются. Так, при обследовании в рамках Фрамингемского исследования у пациентов с уровнем ТТГ менее 0,1 миллиед/л обнаружили, что через 10 лет у них достоверно чаще встречалась мерцательная аритмия и также достоверно возрастала смертность. Характерны следующие клинические кардиальные симптомы при субклиническом гипертиреозе: тахикардия, укорочение систолических интервалов, увеличение ударного объема левого желудочка, диастолические нарушения (снижение диастолического наполнения).
Надо ли лечить субклинический гипертиреоз? В настоящее время еще нет оценки, полученной методами доказательной медицины. Эмпирически показано, что применение (-адреноблокаторов улучшает пульс, уменьшает мерцательную аритмию, диастолическую дисфункцию у пациентов, леченных тироксином. Если субклинический гипертиреоз является вариантом болезни Грейвса, то эффективность (-адреноблокаторов в настоящее время ставится под сомнение (M. Niels, H. K. Yde, N. Soren et al., 1998). Не решен вопрос, следует ли лечить таких больных тиреостатиками. «Ждать и наблюдать», особенно если нет явных нарушений функции сердца и костного метаболизма — это одна точка зрения. Но так как субклинический гипертиреоз во многих случаях может быстро прогрессировать в явную клиническую форму, то много сторонников активного применения тиреостатиков. Очевидно, принимать решение надо индивидуально.
Сердце при манифестном гипотиреозе и манифестном тиреотоксикозе
Термины «микседематозное (гипотиреоидное) сердце» и «тиреотоксическое сердце», которые используются в настоящее время для обозначения поражения миокарда при манифестном гипотиреозе или манифестном тиреотоксикозе, предложил впервые H.Zondek еще в начале ХХ столетия. Рассмотрим патогенетические механизмы гипотиреоидного и тиреотоксического сердца.
Патогенез гипотиреоидного сердца
1.Снижение окислительного фосфорилирования и поглощения кислорода миокардом, повышение проницаемости клеточных мембран; дефицит макроэргов. 2. Замедление синтеза белка, жировая инфильтрация мышечных волокон, накопление мукополисахаридов и гликопротеидов в миокарде 3. Накопление креатинфосфата. Псевдогипертрофия миокарда 4. Усиление ПОЛ; оксидативный стресс. Повреждение клеточных мембран 5. Электрическая нестабильность миокарда. 6. Повышение натрия и снижение содержания калия в кардиомиоцитах 7. Отек мышечных волокон и интерстициальной ткани сердца; слизистый отек миокарда 8. Снижение тонуса миокарда, миогенная дилатация. Нарушение микроциркуляции 9. Слизистый отек перикарда, выпот в полости перикарда. 10. Атеросклероз коронарных сосудов 11. Анемия
Патогенез тиреотоксического сердца
1. Повышение потребности миокарда и других тканей в кислороде Стимуляция окислительных процессов тиреоидными гормонами. Оксидативный стресс 2. Повышение тонуса симпатической нервной системы и повышение чувствительности тканей к адреналину. Патологическая чувствительность тканей сердца к катехоламинам 3. Стойкая тахикардия. Укорочение диастолы. Истощение резервов 4. Уменьшение синтеза АТФ. Дефицит макроэргов 5. Повышение общего легочного сопротивления. Гипертензия малого круга 6. Катаболизм белка (миокардиального и ферментного) 7. Усиленный гликолиз, в том числе в кардиомиоцитах 8. Гипокалигистия 9. Нарушение проницаемости клеточных мембран, нарушение микроциркуляции. 10. ПМК. 11. Анемия (в ряде случаев выраженная).
Наиболее существенные осложнения, угрожающие жизни больных гипотиреозом и тиреотоксикозом, обусловлены патологическими изменениями сердечно-сосудистой системы: нарушениями ритма и проводимости, кардиалгией, артериальной гипертензией, миокардиодистрофией, недостаточностью кровообращения.
Аритмии при тиреоидной патологии
Представление о том, что при гипотиреозе неизбежна брадикардия, давно устарело. Действительно, синусовая брадикардия — характерный, но не абсолютный клинический признак гипотиреоза, в том числе микседемы: тахисистолическая форма мерцания и трепетания предсердий наблюдается часто, как правило, в виде пароксизмов. Чередование подобных пароксизмов с брадикардией ошибочно принимается за синдром слабости синусового узла как следствие ИБС. Требуется тщательное обследование больного, включая электрофизиологическое и гормональное исследование. Лечение антиаритмическими препаратами в таких случаях не только бесполезно; амиодарон, соталекс и прочие антиаритмики усугубляют гипотиреоидную аритмию. В литературе имеется интересное описание трепетания-мерцания желудочков при микседеме, устраненное гормонами щитовидной железы без антиаритмической терапии (A.Gerhard et al., 1996). Нарушения проводимости в разных отделах сердца также встречаются часто при гипотиреозе.
При тиреотоксическом сердце наблюдается стойкая синусовая тахикардия. Частота сердечных сокращений не зависит ни от эмоциональной, ни от физической нагрузки. Тахикардия не уменьшается во время сна. При тяжёлом течении заболевания у больных возникает тахисистолическая форма мерцательной аритмии. Лечение амиодароном, салуретиками провоцирует фибрилляцию предсердий. Экстрасистолия при тиреотоксикозе встречается редко. Ее появление связывают не с тиреотоксикозом, а с перенесенным до этого каким-то заболеванием сердца.
Заболевания щитовидной железы и артериальная гипертензия
Артериальная гипертензия наблюдается как при гипотиреозе, так и при гипертиреозе, но патогенетические механизмы при этом разные.
ГИПОТИРЕОЗ: повышение преимущественно диастолического АД
ТИРЕОТОКСИКОЗ: повышение систолического АД, снижение диастолического АД
1. Задержка натрия и воды в организме 2. Изменение чувствительности к циркулирующим катехоламинам 3. Нарушение секреции натрийуретического пептида
1. Увеличение сердечного выброса, увеличение минутного объема сердца 2. Активация кинин-калликреиновой системы 3. Гиперсекреция адреномедуллина 4. Функциональный гипокортицизм
Артериальную гипертензию при гипотиреозе усугубляет присоединяющийся атеросклеротический процесс. В этом случае ее течение не отличается от течения эссенциальной гипертонии, но развивается частичная или полная рефрактерность к гипотензивным препаратам. Артериальную гипертензию при тиреотоксикозе называют синдромом высокого сердечного выброса, при этом гипертрофия левого желудочка, как правило, отсутствует. Недавно открытый пептид — адреномедуллин обладает очень выраженной вазодилататорной активностью. Доказано его участие в снижении диастолического АД у больных тиреотоксикозом. Синдром высокого сердечного выброса может трансформироваться в гипертоническую болезнь. Если артериальная гипертензия у пациента сохраняется в течение нескольких месяцев после нормализации функции щитовидной железы, следует рассматривать этот случай как переход в эссенциальную гипертензию и проводить обычную антигипертензивную терапию.
Сердечная недостаточность при гипотиреоидном и тиреотоксическом сердце
При гипотиреозе, несмотря на выраженные дистрофические изменения миокарда, сердечная недостаточность проявляется крайне редко (при микседеме с большой давностью заболевания). Это объясняется прежде всего снижением потребности периферических тканей в кислороде, а также ваготонией.
При тиреотоксическом сердце снижение сократительной функции миокарда и развитие сердечной недостаточности зависит от тяжести заболевания. Укорочение диастолы приводит к истощению резервных возможностей миокарда. Мощность сокращения обоих желудочков снижается, что является результатом значительного утомления сердечной мышцы вследствие развивающейся миокардиодистрофии. При этом снижается общее периферическое сопротивление и возрастает лёгочное сопротивление. Повышение давления в легочной артерии происходит вследствие рефлекторного сужения легочных артериол (рефлекс Китаева). Расстройства гемодинамики при тиреотоксикозе приводят к тому, что левый желудочек сердца работает в условиях изотонической гиперфункции (нагрузка «объемом»), а правый — в условиях гиперфункции смешанного типа (нагрузка «объемом и сопротивлением»). Сердечная недостаточность при тиреотоксикозе развивается преимущественно по правожелудочковому типу. При этом её может усугублять формирующаяся недостаточность трехстворчатого клапана с регургитацией крови в правое предсердие. ПМК встречается при тиреотоксикозе часто, но не влияет существенно на гемодинамику, хотя в отдельных случаях на ЭКГ можно встретить признаки гипертрофии левого предсердия (С.Б. Шустов и соавт., 2000).
Изменения ЭКГ при тиреотоксикозе
ЭКГ при легком течении заболевания характеризуется:
1. Увеличением вольтажа зубцов Р, QRS, Т (особенно часто во II и III отведениях). 2. Удлинением интервала РQ до 0,2″. 3. Синусовой тахикардией. 4. Укорочением времени электрической систолы желудочков.
Для изменения ЭКГ при тиреотоксикозе средней тяжести или при большой продолжительности заболевания характерно:
1. Снижение вольтажа зубца Р, появление зазубренности зубца Р. 2. Замедление внутрипредсердной проводимости (Р>0,1″). 3. Смещение сегмента SТ книзу. 4. Снижение зубца Т или появление Т (-+), или Т(-) в большом числе отведений, особенно часто в отведениях I, II, АVL, V4-V6; 5. Удлинение электрической систолы желудочков;
Характеристика ЭКГ при тяжелом течении тиреотоксикоза.
1. Мерцательная аритмия (тахисистолическая форма). 2. Признаки относительной коронарной недостаточности.
Дифференциальная диагностика тиреотоксического сердца и ревмокардита
Опыт показывает, что нередко изменения сердца при манифестации тиреотоксикоза ошибочно трактуют как проявления первичного ревмокардита, особенно если симптомы проявились после тонзиллярной инфекции. Одышка, сердцебиение, боли в сердце, слабость, субфебрилитет, удлинение интервала PQ на ЭКГ характерны для обоих заболеваний. Ясно, что противоревматическая терапия не только не даст эффекта, но может ухудшить состояние больных. В постановке правильного диагноза помогают следующие клинические признаки: при тиреотоксикозе больные возбудимы, у них выражен диффузный гипергидроз, теплые ладони, рука «мадонны», имеется стойкая тахикардия, усиление тонов сердца, систолическая артериальная гипертензия, а при ревмокардите больные вялые, потливость локальная, кисти рук холодные, тахикардия непостоянная, усиливается после нагрузки, 1-й тон на верхушке сердца ослаблен, АД снижается.
Дифференциальная диагностика тиреотоксического сердца и митрального порока
Диастолический шум всегда свидетельствует об органическом поражении сердца. Тиреотоксикоз является исключением: систолический и диастолический шумы возникают вследствие нарушения ламинарного потока крови в полостях сердца из-за ускорения кровотока, уменьшения вязкости крови, присоединения анемии. Аускультативные изменения в сердце у больных тиреотоксикозом ошибочно трактуют как признак митрального порока. Митральная конфигурация сердца, которая появляется при тиреотоксикозе вследствие повышения давления в легочной артерии (сглаженность талии сердца за счет выбухающего пульмонального конуса) «подтверждает» диагноз. Безусловно, сонографическое исследование камер, полостей, клапанного аппарата сердца помогает избежать подобного рода диагностических ошибок. Но и у больных пороками сердца может возникнуть необходимость контроля ТТГ в крови, чтобы удостовериться в диагнозе.
Дифференциальная диагностика тиреотоксической кардиопатии и ИБС
Диагностика тиреотоксикоза бывает трудна у лиц пожилого возраста из-за клинического сходства с ИБС и атеросклерозом. Суетливость в поведении, нарушения сна, тремор рук, повышение систолического и пульсового артериального давления, пароксизмальная или постоянная форма мерцательной аритмии могут наблюдаться и при тиреотоксикозе, и при атеросклерозе. Однако при тиреотоксикозе тахикардия стойкая, тоны сердца усилены даже при мерцательной аритмии, снижается уровень холестерина и ЛПНП в крови, выражен диффузный гипергидроз, тремор рук мелкоразмашистый, могут определяться зоб, блеск глаз и другие симптомы тиреотоксикоза. Эти признаки нехарактерны для атеросклеротического поражения сердца, а ослабление 1-го тона и гиперлипидемия заставят предположить ИБС. Следует учесть, что оба заболевания нередко сочетаются, тиреотоксикоз наслаивается на уже давно текущий атеросклероз. Поскольку у пожилых лиц тиреотоксикоз может протекать без увеличения щитовидной железы, необходимо чаще контролировать у них уровень ТТГ в крови.
Лечение гипотиреоидного сердца
Устранение гипотиреоза, достижение эутиреоидного состояния дает несомненный успех в лечении гипотиреоидного сердца. Основной препарат для лечения гипотиреоза — Т4. Его средняя доза 10-15 мкг/кг у детей и 1,6 мкг/кг — у взрослых; обычно суточная доза у женщин 75-100 мкг, у мужчин 100-150 мкг. У молодых взрослых больных гипотиреозом начальная доза Т4 50 — 100 мкг/сут. Ее повышают каждые 4-6 недель на 50 мкг. У больных пожилого возраста, при ИБС и нарушениях ритма начальная доза Т4 не должна превышать 25 мкг/сут. Ее повышают осторожно под контролем общего состояния и ЭКГ через 5-6 недель. Лечение происходит под контролем ТТГ и тиреоидных гормонов в крови. Следует помнить о том, что многие препараты, такие как (-адреноблокаторы, транквилизаторы, центральные симпатолитики, амиодарон и соталол и т.д., сами могут вызывать медикаментозный гипотиреоз.
Лечение тиреотоксического сердца
Устранение тиреотоксикоза является первым условием успешного лечения тиреотоксического сердца. Существует три вида лечения болезни Грейвса: медикаментозное, хирургическое и терапия радиоактивным йодом. Из методов консервативной терапии по-прежнему применяются тиреостатические препараты (мерказолил, или его аналоги тиамазол, метимазол). Все шире входит в практику лечения тиреотоксикоза пропилтиоурацил. Хотя доза его примерно в 10 раз выше, чем доза мерказолила, тем не менее он имеет ряд преимуществ. Пропилтиурацил способен прочно связываться с белками крови, что делает его пригодным для терапии беременных и кормящих женщин. Дополнительным его преимуществом является способность ингибировать превращение Т4 в Т3. В сравнении с мерказолилом в плаценту и грудное молоко проникают меньшое количество пропилтиоурацила. Наряду с антитиреоидным действием, он обладает и антиоксидантным эффектом, что очень важно при наличии окислительного стресса у больных тиреотоксикозом.
Вопрос о схеме приема тиреостатиков при болезни Грейвса необходимо решать в два этапа: сначала добиться эутиреоидного состояния, а затем проводить поддерживающую терапию для достижения длительной ремиссии этого хронического аутоиммунного заболевания. Остается дискутабельным вопрос, с каких доз следует начинать терапию тиреостатическими препаратами — с максимальных, постепенно снижая, или с небольших. В последние годы все больше становится сторонников лечения тиреотоксикоза малыми дозами тиреостатиков. Снижение дозы тиреостатиков уменьшает число побочных эффектов и не ослабляет антитиреоидное действие. Следует отметить, что у больных с большими размерами зоба и/или высоким уровнем Т3 в сыворотке крови малыми дозами тиреостатиков не удается достичь эутиреоидного состояния и после длительного (более 6 недель) курса медикаментозного лечения. Следовательно, тактика медикаментозного лечения тиреотоксикоза должна быть индивидуальной.
Нет единой точки зрения и на тактику поддерживающей терапии. Сторонников использования высоких доз тиреостатиков в сочетании с тироксином, по принципу «блок и замещение», меньше, чем сторонников минимальных доз тиреостатиков, достаточных для поддержания эутиреоидного состояния. Проведенные проспективные исследования, в том числе европейское многоцентровое, не показали каких-либо преимуществ поддерживающего лечения большими дозами препаратов. Согласно результатам опросов как европейских, так и американских специалистов, 80-90% эндокринологов считают, что курс поддерживающей терапии должен составлять не менее 12 месяцев. Вопрос об оптимальной длительности лечения остается открытым. Полагают, что можно рекомендовать проведение лечения в течение 18 месяцев, особенно у больных, имеющих в крови антитела к рецепторам ТТГ. Проводя лечение, необходимо помнить о побочных эффектах тиреостатиков. Хотя гематологические осложнения (агранулоцитоз, апластическая анемия) развиваются редко (в 0,17% — 2,8% случаев), но являются серьезными и могут привести к летальному исходу. Необходимо отметить, что агранулоцитоз может развиться и при низкой дозе тиреостатических препаратов, и через длительный срок (12 месяцев) после начала их применения. Часто при лечении тиреостатиками наблюдается гепатотоксичность, причем частота этой патологии возрастает с увеличением дозы препаратов. У 10-25% пациентов проявляются незначительные побочные эффекты лечения, такие как крапивница, кожный зуд, артралгии, гастриты и др. Эти эффекты явно дозозависимы и требуется подбор индивидуальной дозы тиреостатика для каждого больного.
Частота рецидивов болезни Грейвса после длительного курса поддерживающей терапии тиреостатиками, по наблюдениям разных авторов, колеблется от 2 до 35%. В настоящее время мнение, что сочетанная терапия тиреостатиками и тироксином существенно снижает частоту рецидивов заболевания, пересмотрено; проспективные исследования это не подтвердили. Однако еще 78% врачей Японии продолжают применять антитиреоидные препараты в комбинации с тироксином (M. Toru et al., 1997). Пока нет четких критериев, позволяющих прогнозировать наступление ремиссии болезни Грейвса. Тем не менее на возможность неблагоприятного исхода заболевания могут указывать следующие факторы: большие размеры зоба, исходный высокий уровень тиреоидных гормонов в крови или высокий титр антител к рецепторам ТТГ. Разработан метод применения тиреостатиков в сочетании с холестирамином. Последний уменьшает тиреотоксическую интоксикацию, поглощая тиреоидные гормоны в желудке и кишечнике и препятствуя их повторному всасыванию.
Во многих странах при болезни Грейвса используют комбинированное лечение тиреостатиками с радиоактивным йодом. В настоящее время отрабатывается тактика такого лечения, поскольку неясно, оказывает ли терапия тиреостатиками неблагоприятное влияние на эффективность последующего лечения радиоактивным йодом. Нередко развивается преходящий гипотиреоз после такого лечения пациентов с болезнью Грейвса, причем заранее предсказать его развитие нельзя.
Хирургическое лечение остается наиболее быстрым методом достижения эутиреоидного состояния по сравнению с тиреостатиками или радиоактивным йодом и, кроме того, как показало рандомизированное проспективное исследование, этот вид лечения сопровождается наименьшей частотой рецидивов в течение двух последующих лет. Однако риск осложнений позволяет рекомендовать проведение струмэктомий только в тех хирургических центрах, где имеется достаточный опыт. Но и при этом условии частота отсроченного развития выраженного гипотиреоза составляет не менее 30% через 5 лет, а субклинический гипотиреоз встречается еще чаще (до 46% случаев), хотя у некоторых больных излечивается спонтанно. До настоящего времени дискутируется вопрос об оптимальном объеме оперативного вмешательства при болезни Грейвса. После субтотальной тиреоидэктомии не менее чем в 10% случаев могут развиться отсроченные (через 5-10 лет после операции) рецидивы тиреотоксикоза. Поэтому появилось немало сторонников радикального лечения болезни Грейвса — тотальной тиреоидэктомии. Необходимость постоянной заместительной терапии тиреоидными гормонами в этом случае — серьезное возражение против этого способа хирургического лечения.
Применение сердечных гликозидов у больных тиреотоксикозом даже при выраженной одышке является грубой ошибкой. Известно, что сердечные гликозиды оказывают кардиотоническое действие, вызывают усиление систолы сердца, удлинение диастолы, ваготропный эффект, замедление проводимости, в частности атриовентрикулярной. При тиреотоксикозе имеются гиперкинетический тип гемодинамики, замедление атриовентрикулярной проводимости, а поэтому применение сердечных гликозидов бессмысленно. Давно отмечена резистентность к этим препаратам при тиреотоксическом сердце. Рефрактерность к антиаритмическим препаратам у больных тиреотоксикозом — бесспорный факт. Особенно пагубно действует амиодарон, на 1/3 состоящий из йода. В литературе имеются описания случаев развития тиреотоксического криза при лечении амиодароном больных с нераспознанным тиреотоксикозом. Безусловно, при тиреотоксическом сердце необходимо назначать средства, улучшающие метаболизм в миокарде: макроэрги, витамины, антиоксиданты, препараты калия, магния.
Изменения сердца при тиреоидных кардиопатиях обратимы, если коррекция тиреоидной функции начата своевременно.
Профессор Ирина ТЕРЕЩЕНКО. Пермская государственная медицинская академия.
Профилактика гипертиреозов
Людям с отягощенной наследственностью, женщинам в период менопаузы и мужчинам пожилого возраста необходимо ежегодно проходить обследование у эндокринолога, сдавать анализ крови на уровень гормонов щитовидной железы.
Рекомендуется сбалансировать питание по БЖУ, ввести в рацион продукты, богатые витаминами А, В, С и минералами. Диета и водолечение помогают не только в профилактике гипертиреоза, но и в реабилитации пациентов после лечения. Регулярное посещение профильных санаториев помогает сохранить и улучшить здоровье эндокринной системы.
Тахикардия – какие анализы сдать?
Среди лабораторных исследований, необходимых для правильной диагностики и максимально эффективного лечения тахикардии, в первую очередь стоит упомянуть следующие:
- общий анализ крови;
- липидограмма, в которой исследуются общий холестерин и триглицериды,а также уровни «хорошего» и «плохого» холестерина – липопротеинов высокой плотности (ЛПВП), низкой плотности (ЛПНП) и очень низкой плотности (ЛПОНП);
- анализ на электролиты;
- анализы на гормоны щитовидной железы – тиреотропный гормон (ТТГ) и свободный Т4, а также анализ на антитела к тиреопероксидазе (АТПО).
Кроме того, для диагностики тахикардии кардиолог назначает и некоторые прочие обследования, не лабораторные: электрокардиографию (в том числе суточный мониторинг ЭКГ по Холтеру), эхокардиографию и др.
Если «поймать» заболевание на ранних стадиях и максимально точно установить причину его развития – тахикардию можно вылечить полностью. Поэтому ни в коем случае не относитесь безразлично к любым тревожным симптомам, связанным с сердечным ритмом, ведь в противном случае заболевание будет прогрессировать, опасность расти, а лечение в итоге будет гораздо более долгим и дорогим.
Полноценное лечение тахикардии – это не только прием лекарственных препаратов, но и пересмотр собственного образа жизни и рациона питания. Постарайтесь поддерживать нормальную физическую активность (но без переутомления), спать не менее 7–8 часов в сутки, сократить употребление животных жиров, рафинированного сахара, кофеина, алкоголя. Идеальная основа питания при тахикардии и других сердечных проблемах – молочно-растительная. По назначению врача можно пить поливитаминно-минеральные добавки с калием и магнием, или же принимать эти элементы по отдельности.