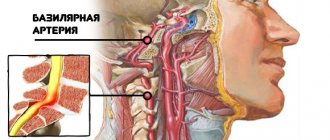
Потенциал действия (ПД) — это кратковременные амплитудные изменения мембранного потенциала покоя (МПС), возникающие при возбуждении живой клетки. По сути это электрический разряд — быстрая кратковременное изменение потенциала на небольшом участке мембраны возбудимой клетки (нейрона или мышечного волокна), в результате которого внешняя поверхность этого участка становится отрицательно заряженной по отношению к соседним участкам мембраны, тогда как его внутренняя поверхность становится положительно заряженной по отношению к соседним участкам мембраны. Потенциал действия является физической основой нервного или мышечного импульса, который играет сигнальную (регуляторную) роль.
Общая характеристика
Потенциалы действия могут отличаться по своим параметрам в зависимости от типа клетки и даже на разных участках мембраны одной и той же клетки. Наиболее характерный пример различий: потенциал действия сердечной мышцы и потенциал действия большинства нейронов. Все же, в основе любого потенциала действия лежат следующие явления:
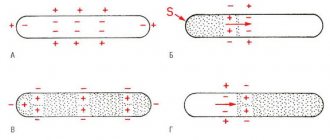
- «Мембрана живой клетки поляризована» — ее внутренняя поверхность заряжена отрицательно по отношению к наружной благодаря тому, что в растворе у ее внешней поверхности находится большее количество положительно заряженных частиц (катионов), а у внутренней поверхности — большее количество отрицательно заряженных частиц (анионов).
- «Мембрана имеет избирательную проницаемость ‘- ее проницаемость для различных частиц (атомов или молекул) зависит от их размеров, электрического заряда и химических свойств.
- «Мембрана возбудимой клетки способна быстро менять свою проницаемость ‘для определенного вида катионов, вызывая переход положительного заряда с внешней стороны на внутреннюю
Первые два свойства характерны для всех живых клеток. Третья же является особенностью клеток возбудимых тканей и причиной, по которой их мембраны способны генерировать и проводить потенциалы действия.
Основной математической моделью, описывающей генерацию и передачу потенциала действия, является модель Ходжкина-Хаксли.
Фазы
Можно четко выделить пять фаз развития ПД:
Нарастание (деполяризация)
Возникновение потенциала действия (ПД) связано с увеличением проницаемости мембраны для ионов натрия (в 20 раз по сравнению с проницаемостью для К +, и в 500 раз по сравнению с исходной проницаемостью Na +) и последующим усилением диффузии этих ионов по концентрационном градиенту внутрь клетки, приводит к изменению (уменьшение) мембранного потенциала. Уменьшение мембранного потенциала приводит к увеличению проницаемости мембраны для натрия путем открытия потенциал-зависимых натриевых каналов, а увеличение проницаемости сопровождается усилением диффузии натрия в цитоплазму, что вызывает еще более значительную деполяризацию мембраны. Благодаря наличию положительной обратной связи деполяризация мембраны при возбуждении происходит с ускорением и поток ионов натрия в клетку все время растет. Интенсивность же потока ионов калия, направленного из клетки наружу, в первые моменты возбуждения остается в начале. Усиленный поток положительно заряженных ионов натрия внутрь клетки вызывает сначала исчезновение избыточного отрицательного заряда на внутренней поверхности мембраны, а затем приводит к перезарядки мембраны. Поступления ионов натрия происходит до тех пор, пока внутренняя поверхность мембраны не приобретет положительный заряд, достаточный для уравновешивания градиента концентрации натрия и прекращение его дальнейшего перехода внутрь клетки. Натриевый возникновения ПД подтверждают опыты с изменением внешней и внутренней концентрации этого иона. Было показано, что десятикратном изменении концентрации ионов натрия во внешнем или внутреннем среде клетки, соответствует изменение ПД на 58 мВ. При полном удалении ионов натрия из окружающей клетку жидкости ПД ни возникал. Таким образом, установлено, что ПД возникает в результате избыточной, по сравнению с покоем, диффузии ионов натрия из окружающей жидкости внутрь клетки. Период, в течение которого проницаемость мембраны для ионов натрия при открытии натриевых каналов растет, является небольшим (0,5-1 мс) вслед за этим наблюдается повышение проницаемости мембраны для ионов калия благодаря открытию потенциал-зависимых калиевых каналов, и, следовательно, усиление диффузии этих ионов из клетки наружу.
Принцип «все или ничего» Согласно закону «все-или-ничего» мембрана клетки возбудимой ткани или не отвечает стимул совсем, или отвечает с максимально возможной для нее на данный момент силой. Действие раздражителя обычно приводит к локальной деполяризации мембраны. Это вызывает открытие натриевых каналов, которые чувствительны к изменениям потенциала, а через это — увеличивает натриевую проводимость, что приводит к еще большей деполяризации. Существование такой обратной связи обеспечивает регенеративную (возобновляемую) деполяризацию клеточной мембраны. Величина потенциала действия зависит от силы раздражителя, а сам он возникает только в том случае, когда деполяризация превышает некоторый определенный для каждой клетки предельный уровень. Это явление получило название «все или ничего». Однако, если деполяризация составляет 50-75% от предельной величины, то в клетке может возникнуть локальный ответ, амплитуда которой значительно ниже амплитуду потенциала действия. Отсутствие потенциала действия при пидграничному уровне деполяризации объясняется тем, что при этом недостаточно увеличивается натриевая проницаемость, чтобы вызвать регенеративную деполяризацию. Уровень деполяризации, который возникает при этом, не вызывает открытие новых натриевых каналов, поэтому натриевая проводимость быстро уменьшается, и в клетке снова устанавливается потенциал покоя.
Овершут
Деполяризация мембраны приводит к реверсии мембранного потенциала (МП становится положительным). В фазу овершута Na + -ток начинает стремительно снижаться, что связано с инактивацией потенциал-зависимых Na + -каналов (время открытого состояния — судьбы миллисекунды) и исчезновением электрохимического градиента Na +.
Рефрактерность Одним из последствий исчезновения градиента Na + является рефрактерность мембраны — временная неспособность отвечать на раздражитель. Если раздражитель возникает сразу после прохождения потенциала действия, то возбудимость не возникнет ни при силе раздражителя на уровне порога, ни при значительно более сильное раздражителю. Такое положение полной невозбудимости называется абсолютным рефрактерным периодом. За ним следует относительный рефрактерный период, когда надпороговый раздражитель может вызвать потенциал действия со значительно меньшей амплитудой чем в норме. Потенциал действия привычной амплитуды при действии порогового раздражителя можно вызвать только после нескольких миллисекунд после предварительного потенциала действия. Абсолютный рефрактерный период ограничивает максимальную частоту генерации потенциалов действия.
Реполяризация
Увеличение ионного потока калия, направленного из клетки наружу, приводит к уменьшению мембранного потенциала, в свою очередь обусловливает уменьшение проницаемости мембраны для ионов натрия, что, как указывалось, является функцией мембранного потенциала. Таким образом, второй этап характеризуется тем, что поток ионов калия из клетки наружу растет, а встречный поток ионов натрия уменьшается. Такая реполяризация мембраны продолжается, пока не произойдет восстановление потенциала покоя — реполяризация мембраны. После этого проницаемость для ионов калия также падает до исходной величины. Внешняя поверхность мембраны за счет положительно заряженных ионов калия, вышедших в среду, вновь приобретает положительный потенциала относительно внутреннего.
Следовая деполяризация и гиперполяризация
В конечной фазе происходит замедление восстановления мембранного потенциала покоя, и при этом регистрируются следовые реакции в виде следовой деполяризации и гиперполяризации, обусловлены медленным восстановлением исходной проницаемости для ионов К +.
Спонтанная диастолическая деполяризация и автоматизм
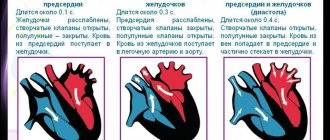
Мембранный потенциал нормальных клеток рабочего миокарда предсердий и желудочков остается постоянным на уровне потенциала покоя в течение всей диастолы (см. рис. 3.1): если эти клетки не возбуждаются распространяющимся импульсом, то потенциал покоя в них поддерживается сколь угодно долго. В сердечных волокнах другого типа, например в специализированных волокнах предсердий или в волокнах Пуркинье проводящей системы желудочков, мембранный потенциал во время диастолы непостоянен и постепенно изменяется в сторону деполяризации.
Если такое волокно не будет возбуждено распространяющимся импульсом раньше, чем мембранный потенциал достигнет порогового уровня, то в нем может возникнуть спонтанный потенциал действия (рис. 3.6). Изменение мембранного потенциала во время диастолы называется спонтанной диастолической деполяризацией, или фазой 4 деполяризации.
Обусловливая возникновение потенциалов действия, этот механизм служит основой автоматизма. Автоматизм является нормальным свойством клеток синусового узла, мышечных волокон митрального и трикуспидального клапанов, некоторых участков предсердий, дистальной части АВ-узла, а также тканей системы Гиса — Пуркинье.
В здоровом сердце частота возникновения импульсов вследствие автоматизма клеток синусового узла достаточно высока, что позволяет распространяющимся импульсам возбуждать другие потенциально автоматические клетки, прежде чем они спонтанно деполяризуются до порогового уровня. При этом потенциальная автоматическая активность других клеток обычно подавляется, хотя при целом ряде физиологических и патологических состояний она может проявляться (обсуждается ниже).
Рис. 3.6.Спонтанная диастолическая деполяризация и автоматизм волокон Пуркинье у собаки.А — спонтанное возбуждение волокна Пуркинье при максимальном диастолическом потенциале —85 мВ. Диастолическая деполяризация является следствием уменьшения во времени тока ins, или пейсмекерного тока (см. в тексте). Б — автоматическая активность, возникающая при снижении мембранного потенциала;
при большей амплитуде импульса мембранный потенциал снижается до —40 мВ, обусловливая поддерживающуюся ритмическую активность. Фрагмент Б3: усилившийся импульс тока снижает мембранный потенциал до —30 мВ, вследствие чего поддерживающаяся ритмическая активность возникает с большей частотой. Такая ритмическая активность, возникающая при менее негативных, чем —60 мВ, потенциалах, зависит, вероятно, от другого пейсмекерного тока, нежели активность, показания на фрагменте А.
Спонтанная диастолическая деполяризация является следствием постепенного изменения баланса между входящими и выходящими мембранными токами в пользу суммарного входящего (деполяризующего) тока. При исследовании пейсмекерного тока методом фиксации потенциала в волокнах Пуркинье [34—37] и клетках узла [38] была показана зависимость характеристик воротной системы как от потенциала, так и от времени.
На основании данных первоначальных исследований уровня потенциала, при котором пейсмекерный ток реверсивно меняет свое направление, предполагалось, что выходящий пейсмекерный ток, переносимый ионами K , постепенно отклоняется, позволяя тем самым направленному внутрь фоновому току деполяризовать клеточную мембрану [34—36].
Однако, согласно интерпретации результатов более поздних экспериментов, нормальным пейсмекерным током является входящий ток, переносимый преимущественно ионами Na , который с течением времени возрастает, вызывая таким образом постепенную диастолическую деполяризацию [37, 38]. Когда деполяризация достигает уровня порогового потенциала, возникает импульс, после чего пейсмекерная проводимость при деполяризации мембраны инактивируется и сможет реактивироваться лишь после реполяризации потенциала действия.
Ясно, что частота спонтанных возбуждений определяется временем, за которое диастолическая деполяризация изменяет мембранный потенциал до порогового уровня; следовательно, изменения порогового потенциала или скорости диастолической деполяризации, возникающие, например, в волокнах Пуркинье под действием адреналина, могут повлиять на частоту автоматической активности.
В клетках синусового и атриовентрикулярного узлов скорость деполяризации в нулевую фазу намного ниже (1—20 В/с), чем в нормальных волокнах Пуркинье или клетках рабочего миокарда (см. рис. 3.9). Амплитуда потенциалов действия также весьма невелика (60—80 мВ); в некоторых клетках пик потенциала действия не превышает 0 мВ [3].
По сравнению с другими сердечными клетками более низкая скорость нарастания и меньшая амплитуда потенциала действия узловых клеток отражают значительно меньшую величину входящего тока перед нулевой фазой деполяризации в этих клетках. Имеющиеся в настоящее время данные однозначно свидетельствуют о том, что меньший по величине входящий ток в клетках синусового и атриовентрикулярного узлов течет не через быстрые натриевые каналы, а через медленные каналы и переносится ионами натрия и кальция [45—47].
Такие потенциалы действия с нарастанием, зависящим от медленного входящего тока, часто называют «медленными ответами» в отличие от более обычных «быстрых ответов», нарастание в которых зависит от быстрого натриевого тока [20]. Из-за столь малой величины суммарного входящего тока и медленной деполяризации в нулевую фазу скорость проведения медленных потенциалов действия через узлы всегда низка (0,01—0,1 м/с);
именно такое медленное проведение в определенных условиях может обусловить возникновение нарушений ритма в тканях узлов. Как отмечалось ранее, медленные каналы для входящего тока имеют совершенно иные характеристики зависимости их воротного механизма от времени и потенциала по сравнению с быстрыми натриевыми каналами.
Медленный входящий ток активируется и инактивируется значительно дольше, чем быстрый натриевый ток. Поэтому после нарастания потенциала действия в узлах медленный входящий ток инактивируется только медленно, способствуя деполяризации мембраны в течение всей фазы плато потенциала действия. Активация зависимого от времени и потенциала выходящего калиевого тока вместе с инактивацией медленного входящего тока, по-видимому, вызывает реполяризацию клеток узлов, как это было описано для окончания потенциала действия в других сердечных клетках.
Рис. 3.9. Сравнение потенциалов действия синусового и АВ-узла (указаны стрелками) с потенциалами действия рабочего миокарда и волокон Пуркинье.Запись потенциалов действия произведена в следующих областях сердца (начиная сверху): синусовый узел, предсердие, атриовентрикулярный узел, пучок Гиса, волокно Пуркинье в ложном сухожилии, терминальное волокно Пуркинье и рабочий миокард желудочков.
Заметьте, что возрастание скорости и амплитуда потенциалов действия синусового и АВ-узла меньше аналогичных параметров в других клетках [3].Проводимость медленных каналов для входящего тока восстанавливается после реполяризации мембраны также гораздо медленнее, чем проводимость быстрых натриевых каналов [20, 21].
В отличие от других сердечных клеток в узловых клетках при нанесении преждевременного стимула во время конечной фазы реполяризации не отмечается возникновения потенциала действия. В действительности достаточная инактивация проводимости медленных каналов для входящего тока может сохраняться даже после полной реполяризации в клетках, ставших абсолютно рефрактерными к стимуляции [48].
Реактивация происходит постепенно в течение всей диастолы; преждевременные импульсы, вызванные вскоре после полной реполяризации, имеют более медленное нарастание, меньшую амплитуду, чем нормальные импульсы, и распространяются медленнее. Преждевременные импульсы, вызванные позднее во время диастолы, имеют соответственно более быстрое нарастание, более высокую амплитуду и, следовательно, проводятся быстрее [49].
Такое поведение отражает длительность процесса реактивации медленных каналов. Связанный с этим продолжительный рефрактерный период узловой ткани, а также значительное замедление проведения через нее преждевременных импульсов могут быть важными факторами инициации некоторых нарушений сердечного ритма.АвтоматизмКлетки синусового узла обычно являются автоматическими, так что каждый последующий потенциал действия возникает в результате спонтанной диастолической деполяризации;
клетки АВ-узла также способны возбуждаться автоматически, особенно если они не связаны с окружающим миокардом предсердий [50]. Это означает, по-видимому, что электротоническое взаимодействие клеток узла и предсердий подавляется автоматически через предсердно-узловое проведение. Автоматическая активность клеток синусового узла не может быть связана с тем же пейсмекерным током, который был ранее описан в волокнах Пуркинье.
Изменения состояния воротного механизма мембранной проводимости, ответственной за нормальный автоматизм волокон Пуркинье, происходят только в диапазоне мембранных потенциалов от —90 до —60 мВ [36]. Такие изменения проводимости вряд ли способны объяснить развитие спонтанной диастолической деполяризации в клетках синусового узла, поскольку максимальный диастолический потенциал этих клеток обычно менее отрицателен, чем —60 мВ.
Однако имеющиеся данные говорят о том, что пейсмекерный ток в синусовом узле переносится, по крайней мере частично, ионами К [38] и уменьшение этого выходящего тока при наличии постоянного фонового входящего тока приводит к постепенной деполяризации мембраны. Кроме того, важную роль играет, вероятно, входящий ток, который активируется при гиперполяризации и обозначается if [38].
https://infopedia.su/12x90c6.html
Электрический импульс, распространяющийся по сердцу и запускающий каждый цикл сокращений, называется потенциалом действия; он представляет собой волну кратковременной деполяризации, во время которой внутриклеточный потенциал поочередно в каждой клетке становится на короткое время положительным, а затем возвращается к своему исходному отрицательному уровню.
Изменения нормального сердечного потенциала действия имеют характерное развитие во времени, которое для удобства подразделено на следующие фазы [3]: фаза 0 — начальная быстрая деполяризация мембраны; фаза 1 — быстрая, но неполная реполяризация; фаза 2 — «плато», или продолжительная деполяризация, характерная для потенциала действия сердечных клеток;
фаза 3 — конечная быстрая реполяризация; фаза 4 — период диастолы.При потенциале действия внутриклеточный потенциал становится положительным, так как возбужденная мембрана временно приобретает большую проницаемость для Na (по сравнению с К ),поэтому мембранный потенциал на какое-то время приближается по величине к потенциалу равновесия ионов натрия (ENa)- ЕNаможно определить, используя отношение Нернста;
при внеклеточной и внутриклеточной концентрации Na 150 и 10 мМ соответственно он составит:Однако повышенная проницаемость для Na сохраняется лишь непродолжительное время, так что мембранный потенциал не достигает ENaи после окончания потенциала действия возвращается к уровню покоя.Указанные выше изменения проницаемости, вызывающие развитие фазы деполяризации потенциала действия, возникают вследствие открытия и закрытия особых мембранных каналов, или пор, через которые легко проходят ионы натрия.
Как полагают, работа «ворот» регулирует открытие и закрытие отдельных каналов, которые могут существовать по меньшей мере в трех конформациях — «открытой», «закрытой» и «инактивированной». Одни ворота, соответствующие активационной переменной «m» в описании Ходжкина — Хаксли [13] ионных потоков натрия в мембране гигантского аксона кальмара, быстро перемещаются, открывая канал, когда мембрана внезапно деполяризуется под действием стимула.
Другие ворота, соответствующие инактивационной переменной «h» в описании Ходжкина — Хаксли, при деполяризации движутся медленнее, и их функция заключается в закрытии канала (рис. 3.3). Как установившееся распределение ворот в пределах системы каналов, так и скорость их перехода из одного положения в другое зависят от уровня мембранного потенциала.
Поэтому для описания мембранной проводимости Na используются термины «зависимый от времени» и «потенциалозависимый».Если мембрану в покое внезапно деполяризовать до уровня положительного потенциала (например, в эксперименте по фиксации потенциала), то активационные ворота быстро изменят свое положение, чтобы открыть натриевые каналы, а затем инактивационные ворота медленно их закроют (рис. 3.3).
Слово «медленно» означает здесь, что на инактивацию уходит несколько миллисекунд, тогда как активация происходит в доли миллисекунды. Ворота остаются в указанных положениях до тех пор, пока мембранный потенциал снова не изменится, и для того чтобы все ворота вернулись к исходному состоянию покоя, мембрана должна быть полностью реполяризована до уровня высокого отрицательного потенциала.
Если мембрана реполяризуется лишь до невысокого уровня отрицательного потенциала, то некоторые инактивационные ворота останутся закрытыми и максимальное число доступных натриевых каналов, способных открыться при последующей деполяризации, сократится [14]. (Электрическая активность сердечных клеток, в которых натриевые каналы полностью инактивированы, будет обсуждаться ниже.
Распространение
Распространение в немиелинизированные волокне
В немиелинизированные (без`мякотному) нервном волокне ПД распространяется от точки к точке, поскольку возбуждение можно зарегистрировать как такое, что постепенно «бежит» по всему волокну от места своего возникновения. Ионы натрия, входящих внутрь возбуждении участка, служат источником электрического тока для возникновения ПД в прилегающих участках. В этом случае импульс возникает между деполяризована участком мембраны и ее невозбужденном участком. Разность потенциалов здесь во много раз выше, чем необходимо для того, чтобы деполяризация мембраны достигла предельного уровня. Скорость распространения импульса в таких волокнах 0,5-2 м / с
Распространение в миелинизированные волокне
Нервные отростки большинства соматических нервов миелинизированные. Только очень незначительные их участки, так называемые перехвата узла (перехват Ранвье), покрытые обычной клеточной мембраной. Такие нервные волокна характеризуются тем, что на мембране только в перехватах размещении потенциал-зависимые ионные каналы. Кроме того, эта оболочка повышает электрическое сопротивление мембраны. Поэтому при сдвиге мембранного потенциала ток проходит через мембрану перехватывающих участка, то есть прыжками (сальтаторно) от одного перехвата к другому, что позволяет увеличить скорость проведения нервного импульса, которая составляет от 5 до 120 м / с. Причем потенциал действия, который возник в одном из перехватов Ранвье, вызывает потенциалы действия в соседних перехвата за счет возникновения электрического поля, которое вызывает начальную деполяризацию в этих перехватов. Параметры ЭДС поля и дистанция его эффективного действия зависят от кабельных свойств аксона.
Типы нервных волокон, скорость проведения импульса, в зависимости от миелинизации
| Тип | Диаметр (мкм) | Миелинизация | Скорость проведения (м / с) | Функциональное назначение |
| А alpha | 12-20 | сильная | 70-120 | Подвижные волокна соматической НС; чувствительные волокна проприорецепторов |
| А beta | 5-12 | сильная | 30-70 | Чувствительные волокна рецепторов кожи |
| А gamma | 3-16 | сильная | 15-30 | Чувствительные волокна проприорецепторов |
| А delta | 2-5 | сильная | 12-30 | Чувствительные волокна терморецепторов, ноцицепторов |
| В | 1-3 | слабая | 3-15 | Преганглионарные волокна симпатической НС |
| С | 0,3-1,3 | отсутствует | 0,5-2,3 | Постганглионарные волокна симпатической НС; чувствительные волокна терморецепторов, ноцицепторов некоторых механорецепторов |
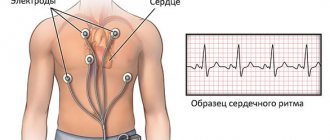
Диагностика
Для диагностики правильных процессов деполяризации и реполяризации служит электрокардиография сердца (ЭКГ).
Зубцы и интервалы ни о чем не говорят неспециалисту. Врачи функциональной диагностики знакомы с тонкими признаками и изменениями характерных зубцов, могут вычислить время реполяризации.
Увеличение времени деполяризации желудочков сердца указывает на механическое препятствие в распространении импульса. Это возможно при блокадах разной степени. Острый инфаркт чаще всего поражает левый желудочек. Здесь формируется соединительнотканный рубец, который и служит препятствием для импульса. В заключении ЭКГ врач, кроме признаков инфаркта, обязательно напишет об умеренном нарушении деполяризации.
При расшифровке учитывается форма комплексов, высота и ширина зубцов, уровень основной линии, длительность интервалов
О нарушенной реполяризации говорит снижение зубца Т. Это характерно для диффузных дистрофических изменений, кардиосклероза. В данном случае заключение ЭКГ не ставит диагноз, но помогает понять механизм образования симптомов болезни, стадию и форму.
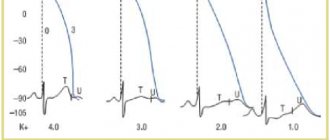
Нарушают реполяризацию гипертрофия миокарда прием некоторых медикаментов, недостаток микроэлементов и витаминов в питании, обезвоживание организма. Такого пациента следует обследовать в стационаре, провести нагрузочную пробу с хлоридом калия. После введения калия на ЭКГ фиксируется нормализация формы желудочковых комплексов.
Распространение потенциала действия между клетками
В химическом синапсе после того, как волна потенциала действия доходит нервного окончания, она вызывает высвобождение нейротрансмиттеров из пресинаптических пузырьков в синаптическую щель. Молекулы медиатора, высвобождаемых с пресинапса, связываются с рецепторами на постсинаптической мембране, в результате чего в рецепторных макромолекулах открываются ионные каналы. Ионы, начинают поступать внутрь постсинаптической клетки через открытые каналы, изменяют заряд ее мембраны, что приводит к частичной деполяризации мембраны и, как следствие, провоцирование генерации постсинаптической клетки потенциала действия.
В электрическом синапсе отсутствует «посредник» передачи в виде нейромедиатора. Зато клетки соединены между собой с помощью специфических протеиновых тоннелей — конексонив, поэтому ионные токи, с пресинаптической клетки могут стимулировать постсинаптическую клетку, вызывая зарождения в ней потенциала действия. Благодаря такому строению, потенциал действия может распространяться в обе стороны и значительно быстрее, чем через химический синапс.
- Схема процесса передачи нервного сигнала в химическом синапсе
- Схема строения электрического синапса
Нарушение реполяризации
Синдром ранней реполяризации желудочков
По каким-то причинам может иметь место нарушение процессов реполяризации. Это означает то что есть проблема с восстановлением заряда. Клетка не успевает «передохнуть» перед очередным возбуждением. Этому могут способствовать разные причины. Прием лекарственных препаратов, стимулирующих симпатическую нервную систему, может стать причиной развития синдрома ранней реполяризации желудочков. Заболевания соединительной ткани (коллагенозы), кардиомиопатия, пороки сердца, ишемическая болезнь сердца, гипертрофия миокарда и другие факторы могут приводить к нарушениям процессов реполяризации.
Клинически это может проявлять себя симптомами основного заболевания, или же регистрироваться только на электрокардиограмме. Однако, как бы не обстояли дела с Вашим самочувствием, стоит обратиться на консультацию к врачу. Будьте здоровы!
Потенциал действия в различных типах клеток
Потенциал действия в мышечных тканях
Потенциал действия в скелетных мышечных клетках аналогичный потенциала действия в нейронах. Потенциал покоя в них как правило -90мВ, что меньше, чем потенциал покоя типовых нейронов. Потенциал действия мышечных клеток длится примерно 2-4 мс, абсолютный рефрактерный период составляет примерно 1-3 мс, а скорость проводимости вдоль мышц примерно 5 м / с.
Потенциал действия в сердечных тканях
Потенциал действия клеток рабочего миокарда состоит из фазы быстрого деполяризации, начальной быстрой реполяризации, которая переходит в фазу медленной реполяризации (фаза плато), и фазы быстрой конечной реполяризации. Фаза быстрой деполяризации обусловлена резким повышением проницаемости мембраны для ионов натрия, вызывает быстрый входящий натриевый ток, при достижении мембранного потенциала 30-40 мВ инактивируется и в дальнейшем главную роль играют кальциевый ионный ток. Деполяризация мембраны вызывает активацию кальциевых каналов, в результате чего возникает дополнительный Деполяризующий входящий кальциевый ток.
Потенциал действия в сердечной ткани играет важную роль в координации сокращений сердца.
Задержанная постдеполяризация и триггерная поддерживающаяся ритмическая активность
частоты приводит к снижению амплитуды. Кроме того, если преждевременный потенциал действия при стимуляции возникает с постоянной частотой, то следующая за ним постдеполяризация имеет большую амплитуду, чем та, которая отмечается после регулярного потенциала действия. Более того, чем раньше во время основного цикла возникает преждевременный потенциал действия, тем больше амплитуда преждевременной постдеполяризации.
При достаточно высокой частоте постоянной стимуляции или после достаточно раннего преждевременного стимула постдеполяризация может достигнуть порога и вызвать нестимулированные потенциалы действия. Первый спонтанный импульс отмечается после более короткого интервала по сравнению с длительностью основного цикла, так как постдеполяризация, вследствие которой он возник, начинается вскоре после реполяризации предшествующего потенциала действия.
Следовательно, спонтанный импульс вызывает еще одну постдеполяризацию, которая также достигает порогового уровня, обусловливая появление второго спонтанного импульса (см. рис. 3.8). Этот последний импульс вызывает следующую постдеполяризацию, которая инициирует третий спонтанный импульс, и так на протяжении всего времени триггерной активности.
Триггерная активность может спонтанно прекратиться, и, если это происходит, за последним нестимулированным импульсом обычно следует одна или несколько подпороговых постдеполяризаций.Рис. 3.8. Индукция триггерной активности в предсердном волокне митрального клапана у обезьяны.На каждом фрагменте показаны лишь нижняя часть потенциалов действия.
Горизонтальные линии на фрагментах I и II проведены на уровне—30 мВ, а на фрагменте III — на уровне — 20 мВ. фрагмент IA и 1Б: триггерная активность, возникшая в результате сокращения длительности основного стимуляционного цикла. IA: продолжительность цикла стимуляции составляет 3400 мс; и за каждым потенциалом действия следует подпороговая задержанная постдеполяризация.
в озникновение триггерной активности вследствие преждевременной стимуляции. IIIA: преждевременный импульс (стрелка) вызывается во время фазы реполяризации постдеполяризации, и амплитуда последующей постдеполяризации возрастает. IIIБ: за преждевременным импульсом (большая стрелка) следует постдеполяризация, которая достигает порога (маленькая стрелка) и приводит к появлению ряда триггерных импульсов [40].
Молекулярные механизмы возникновения потенциала действия
Активные свойства мембраны, обеспечивающие возникновение потенциала действия, основанные главным образом на поведении потенциал-зависимых натриевых (Na +) и калиевых (K +) каналов. Начальная фаза ПД формируется входным натриевым током, позже открываются калиевые каналы и выходной K + -ток возвращает потенциал мембраны к исходному уровню. Начальное концентрацию ионов затем восстанавливает натрий-калиевый насос.
По ходу ПД каналы переходят из состояния в состояние: в Na + -каналов основных состояния трех — закрытый, открытый и инактивированный (в реальности все сложнее, но этих трех состояний достаточно для описания), в K + каналов два — закрытый и открытый.
Поведение каналов, участвующих в формировании ПД, описывается через проводимость и рассчитывается через коэффициенты переноса (трансфера).
Коэффициенты переноса были выведены Алан Ллойд Ходжкин и Эндрю Хаксли.
Проводимость для калия G K на единицу площади
| , |
| где: |
| an — Коэффициент трансфера из закрытого в открытое состояние для K + каналов [1 / s]; |
| bn — Коэффициент трансфера из открытого в закрытое состояние для K + каналов [1 / s]; |
| n — Фракция К + каналов в открытом состоянии; |
| (1 — n) — Фракция К + каналов в закрытом состоянии |
Проводимость для натрия G Na на единицу площади
рассчитать сложнее, поскольку, как уже было упомянуто, в потенциал-зависимых Na + каналов, кроме закрытого / открытого состояний, переход между которыми параметром, еще инактивированный / никак инактивированный состояния, переход между которыми описывается через параметр
| , | , |
| где: | где: |
| am — Коэффициент трансфера из закрытого в открытое состояние для Na + каналов [1 / s]; | ah — Коэффициент трансфера из инактивированного в не-инактивированный состояние для Na + каналов [1 / s]; |
| bm — Коэффициент трансфера из открытого в закрытое состояние для Na + каналов [1 / s]; | bh — Коэффициент трансфера из не-инактивированного в инактивированный состояние для Na + каналов [1 / s]; |
| m — Фракция Na + каналов в открытом состоянии; | h — Фракция Na + каналов в не-инактивированном состоянии; |
| (1 — m) — Фракция Na + каналов в закрытом состоянии | (1 — h) — Фракция Na + каналов в инактивированном состоянии. |
История
Основные положения мембранной теории возбуждения сформулированы немецким нейрофизиологом Ю.Бернштейном
В 1902 году Юлиус Бернштейн выдвинул гипотезу, согласно которой клеточная мембрана пропускает внутрь клетки ионы К +, и они накапливаются в цитоплазме. Расчет величины потенциала покоя по уравнению Нернста для калиевого электрода удовлетворительно совпал с измеренным потенциалом между саркоплазме мышцы и окружающей средой, который составил около — 70 мВ. Согласно теории Ю.Бернштейна, при возбуждении клетки ее мембрана повреждается, и ионы К + выходят из клетки по концентрационном градиента до тех пор, пока потенциал мембраны не становится равным нулю. Затем мембрана восстанавливает свою целостность, и потенциал возвращается к уровню потенциала покоя.
Эту модель развили в своей работе 1952 Алан Ллойд Ходжкин и Эндрю Хаксли в которой описали электрические механизмы, обусловливающие генерацию и передачу нервного сигнала в гигантском аксоне кальмара. За это авторы модели получили Нобелевскую премию в области физиологии и медицины за 1963 год. Модель получила название модель Ходжкина-Хаксли
В 2005 году Томасом Геймбургом и Анрю Д. Джексоном предложена солитонном модель, основанная на предположении, что сигнал по нейронам распространяется в виде солитонов — устойчивых волн, распространяющихся по клеточной мембране.
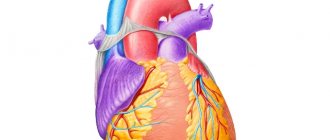
Анатомия проводящей системы
Проводящая система сердца
Довольно часто не только на слуху у медицинского работника, но и у явившегося на прием пациента встречается фраза «процессы реполяризации». А что же это такое по своей сути? Порой нехватка знаний заставляют пациента много думать, и плоды размышлений приводят его к необоснованным тревогам и печалям. А все из-за того, что отсутствует понимание простых истин электрофизиологии. Итак, наше сердце, обладая проводящей системой, имеет способность возбуждаться и возвращаться в состояние покоя. Такое определение является, конечно же, условным. Ведь этот орган работает 24 часа в сутки, а это значит, что никаких пауз в работе здорового сердца быть не должно.
Обратимся именно к его электрофизиологии. «От макушки до пят» наше сердце обеспечено проводящей системой, которая представлена узлами, пучками и волокнами. Структурной единицей этой системы является атипичная мышечная клеточка. Она содержит меньше сократительных элементов миофибрилл, но больше саркоплазмы — цитоплазмы, которая заполняет пространство между миофибриллами. Именно саркоплазма обеспечивает проведение возбуждающих импульсов внутри волокна. Даже внешне эти проводящие пути можно попытаться отличить невооруженным глазом — они немного бледнее.
Влияние некоторых веществ на потенциал действия
Некоторые вещества органического или синтетического происхождения могут блокировать образование или прохождения ПД:
- Батрахотоксин найден у некоторых представителей рода листолазов. Устойчиво и необратимо повышает проницаемость мембран для ионов натрия.
- Понератоксин был найден в муравьях рода Paraponera. Блокирует натриевые каналы.
- Тетродотоксин найден в тканях рыб семейства Скелезубови, из которых готовят японский деликатес Фугу. Блокирует натриевые каналы.
- Механизм действия большинства анестетиков (Прокаин, Лидокаин) базируется на блокировании натриевых каналов и соответственно на блокировании проведении импульсов по чувствительным нервным волокнам.
- 4-Аминопиридин — обратно блокирует калиевые каналы, удлиняет срок потенциала действия. Может использоваться в терапии рассеянного склероза.
- ADWX 1 — обратно блокирует калиевые каналы. В условиях опыта облегчал течение острого рассеянного энцефаломиелита у крыс.