Софья Касацкая «Природа» №2, 2016
Об автореСофья Алексеевна Касацкая — младший научный сотрудник лаборатории геномики адаптивного иммунитета Института биоорганической химии им. академиков М. М. Шемякина и Ю. А. Овчинникова РАН. Область научных интересов — Т-клеточный иммунитет, нейро- и онкоиммунология. Победитель конкурса «Био/мол/текст» 2015 г. в номинации «Лучшая статья по иммунологии». |
Адекватная защитная реакция организма на вторжение вирусов, бактерий и других патогенов — уничтожить пораженные клетки, не допустив распространения инфекции и гибели большого числа собственных клеток. Если инфицированная вирусом клетка его заметила, запускаются процессы врожденного иммунитета: аутофагия (утилизация внутренних компонентов клетки с помощью ферментов лизосом) и апоптоз (запрограммированная гибель клеток). Однако патогенных вирусов и бактерий очень много, к тому же они постоянно меняются до неузнаваемости. Чтобы справиться с ними, подключается система адаптивного иммунитета и его главные участники — лимфоциты. Вершиной эволюции адаптивного иммунитета стал цитотоксический Т-лимфоцит, или Т-киллер. Для распознавания фрагмента вируса (антигена) на зараженной клетке он использует Т-клеточный рецептор (T cell receptor
, TCR), случайно и независимо собирающийся на каждой Т-клетке в вилочковой железе (тимусе). Механизм сборки TCR уникален и присущ только иммунной системе позвоночных животных. Считается, что эти преимущества впервые получили примитивные рыбы около 500 млн лет назад, когда в результате ретровирусной инфекции в их гаметы внедрились гены, кодирующие особые белки (рекомбиназы), ответственные за рекомбинацию генов TCR.
Классическая иммунология человека построена на изучении иммунных клеток крови просто потому, что образец крови можно взять у любого пациента и исследовать в норме и в патологии. Именно на клетках крови была выстроена классификация Т-лимфоцитов — деление на Т-киллеры и Т-хелперы, которые проверяют антигенную специфичность Т-киллеров, выдают им «лицензию на убийство» и способны управлять всем ходом иммунного ответа через сигнальные растворимые молекулы, цитокины. Позднее из ветви Т-хелперов была выделена группа регуляторных Т-клеток, подавляющих избыточный адаптивный иммунитет.
Но, как нам напоминает реклама йогурта, значительная часть клеток иммунной системы сосредоточена вокруг слизистой оболочки пищеварительного тракта и в других тканях. В то время как в 5–6 л крови взрослого человека находится около 6–15 млрд T-лимфоцитов, в эпидермисе и коже — 20 млрд Т-клеток [], в печени — еще 4 млрд []. Достаточно ли изучения образцов крови для полного описания функций Т-клеток, если в периферических органах Т-клеток больше, чем в кровотоке? И достаточно ли классических субпопуляций, чтобы описать все типы Т-клеток, находящихся в организме человека?
Подробное описание исследования
Иммунная система (иммунитет) способствует защите организма человека от различных воспалительных (инфекционных и неинфекционных), онкологических и других заболеваний. Лимфоциты являются представителями лейкоцитов, которые ответственны за специфический иммунитет — иммунную реакцию, целенаправленно действующую на конкретный чужеродный агент — антиген.
Данный комплексный анализ определяет общее количество Т-лимфоцитов (Т-клеток) и их основных субпопуляций, а также долю активированных Т-клеток от их общего числа.
В физиологических условиях все Т-лимфоциты последовательно проходят этапы созревания и постепенно становятся зрелыми клетками, которые могут участвовать в иммунных реакциях. При контакте зрелой Т-клетки с чужеродным антигеном происходит процесс активации: Т-лимфоцит превращается в тот тип, который необходим для иммунной защиты организма в данный момент.
Выделяют следующие типы (субпопуляции) Т-лимфоцитов:
- Цитотоксические (Т-киллеры);
- Хелперы;
- Регуляторные (Т-супрессоры).
Функцией цитотоксических Т-лимфоцитов является разрушение любых чужеродных молекул: микроорганизмов, токсинов, опухолевых клеток и др. Т-хелперы усиливают степень иммунной реакции и участвуют в активации других иммунных клеток (Т-киллеры, B-лимфоциты, моноциты). Т-регуляторные лимфоциты предотвращают чрезмерную иммунную реакцию и сдерживают активность Т-хелперов.
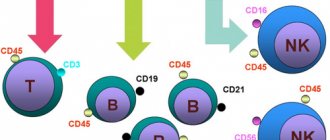
Все субпопуляции Т-клеток отличаются друг от друга набором маркеров CD (cluster of differentiation). Это хромосомные маркеры (антигены) дифференцировки, представленные в основном на поверхности Т-клеток. Каждый CD несет в себе не только опознавательную функцию, но и определенное биологическое значение. CD3-антиген (CD3+) представлен на всех зрелых Т-лимфоцитах, с помощью него можно определить абсолютное количество Т-клеток. CD4+ обнаруживается на Т-хелперах, CD8+ — на Т-киллерах.
Также есть антигены CD, которые указывают не на тип Т-клетки, а на её функциональное состояние — активирована она или нет. Их условно подразделяют на «ранние» и «поздние» CD активации. К ранним относят: CD69+, CD25+ и др.; к поздним: HLA-DR и др.
В рамках анализа оценивается общее число активированных Т-лимфоцитов с CD25+ и (отдельно) активированные Т-хелперы (CD3+CD4+CD25+) и Т-киллеры (CD3+CD8+CD25+).
Данное исследование является комплексным методом диагностики и, как правило, дополняет результаты теста иммунный статус (комплексное изучение состояния иммунной системы). Анализ может быть рекомендован для обследования пациентов с потенциальной иммунопатологической проблемой при следующих группах заболеваний:
- Инфекционные болезни любой локализации и любой природы (бактериальные, вирусные, грибковые, паразитарные);
- Аллергические патологии с тяжелым течением (бронхиальная астма, атопический дерматит, аллергический ринит и др.);
- Аутоиммунные нозологии (ревматические заболевания, аутоиммунный тиреоидит, воспалительные заболевания кишечника т др.);
- Злокачественные (преимущественно) и доброкачественные (реже) онкологические заболевания различного происхождения (кроветворной системы, внутренних органов, ассоциированных с иммунодефицитом и др.).
Состав комплекса «Ранняя активация Т-клеток и Т-регуляторные лимфоциты»:
- Т-лимфоциты;
- Т хелперы;
- Т-регуляторные клетки (CD4+CD25+CD127neg);
- Лейкоцитарная формула;
- Т-активированные клетки с маркером ранней активности (CD3+CD25+);
- Т- хелперы активированные с маркером ранней активности (CD3+CD4+CD25+);
- Т-цитотоксические активированные клетки (CD3+CD4-CD25+).
Жизненный цикл Т-лимфоцита
Каждая Т-клетка после сборки TCR проходит тестирование на функциональность случайно собранного рецептора (положительная селекция) и на отсутствие специфичности к собственным антигенам организма, т.е. на отсутствие очевидной аутоиммунной угрозы (отрицательная селекция). Этапы селекции происходят в вилочковой железе; при этом более 90% клеток-предшественников погибает, не сумев правильно собрать рецептор либо пройти селективный отбор. Выжившие Т-клетки пролиферируют и выходят из тимуса в кровоток — это наивные Т-лимфоциты, еще не встречавшиеся с антигеном. Наивная Т-клетка циркулирует в крови и периодически заходит в лимфоузлы, где в Т-клеточной зоне контактирует со специализированными клетками, которые представляют ей чужеродный антиген.
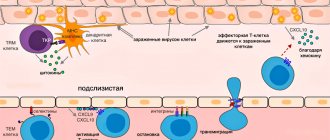
Миграция эффекторной Т-клетки в ткань при вирусной инфекции []. Сигналы воспаления от зараженных эпителиальных клеток при участии резидентных клеток передаются эндотелию сосудов, клетки которого привлекают эффекторные Т-клетки хемокинами CXCL9, CXCL10. Роллинг:
при движении по посткапиллярной венуле в ткани эффекторная клетка замедляется, образуя временные контакты с Е-селектинами и P-селектинами на клетках эндотелия.
Остановка:
эффекторная клетка плотно прикрепляется к эндотелию при взаимодействии LFA-1 и других альфа-интегринов с ICAM-1 / VCAM-1 / MAdCAM-1 (на эндотелии).
Трансмиграция:
эффекторная Т-клетка связывает эндотелиальный JAM-1 молекулами PECAM, CD99, LFA-1 и проникает через клетки эндотелия в подслизистую
После встречи с антигеном в лимфоузле Т-клетка приобретает способность снова делиться — становится предшественницей Т-клеток памяти (Stem Cell Memory T cells
, TSCM). Cреди ее потомков появляются клетки центральной памяти (
Central Memory T cells
, TCM) и эффекторные клетки-предшественники (
Effector Memory T cells
, TEM), которые при делении дают короткоживущие эффекторные клетки, осуществляющие иммунную реакцию (TEMRA-клетки) []. Все эти клетки выходят из лимфоузла и перемещаются по крови. Эффекторные клетки затем могут покинуть кровоток для осуществления иммунной реакции в периферической ткани органа, где находится патоген. Что потом — снова путешествие по крови и лимфоузлам?
Схема перехода потомков активированных Т-лимфоцитов между популяциями []. Пояснения в тексте
Клетки стромы, т.е. основы лимфоузла, выделяют сигнальные вещества (хемокины) для того, чтобы позвать Т-клетку в лимфоузел. Распознают хемокины лимфоузлов рецепторы хоминга CCR7 и CD62L. Но на эффекторных клетках оба рецептора отсутствуют. Из-за этого долгое время было загадкой, как эффекторные клетки могут попасть из периферической ткани обратно во вторичные лимфоидные органы — селезенку и лимфоузлы.
Сложный выбор эффекторной клетки.
To home
— процесс хоминга, или миграции Т-клеток, например, в наиболее привычное для наивных клеток место — лимфоузел. Альтернатива — не отправляться в путешествие по организму и превратиться в резидентную клетку ткани
В то же время стали накапливаться данные (о различиях в репертуарах TCR и профилях транскрипции между TEM в крови и в других тканях), которые никак не укладывались в концепцию постоянной миграции Т-клеток между тканями и кровью. Решено было выделить новую субпопуляцию — резидентные клетки памяти (Resident Memory T cells
, TRM), которые населяют определенный орган и не рециркулируют [].
Откуда впервые появляются резидентные клетки ткани? Это потомки эффекторных клеток, которые потеряли способность рециркулировать. Некоторые периферические для иммунной системы ткани, например слизистая тонкого кишечника и брюшная полость, позволяют эффекторным Т-лимфоцитам проникать внутрь свободно, другие — очень ограниченно. Большой поток эффекторных Т-клеток в эти ткани наблюдается только при реакции воспаления. К тканям второго типа относятся головной и спинной мозг, отделенные барьером от иммунной системы, а также многие другие ткани: периферические ганглии, слизистые половых органов и кишечника, легкие, эпидермис, глаза. Разница между двумя типами тканей — в экспрессии дополнительных молекул хоминга для эффекторных Т-клеток, например молекул адгезии MadCAM-1 для проникновения в эпителий [].
Что ещё назначают с этим исследованием?
Активированные лимфоциты (Т-лимфоциты, Т-хелперы, Т-цитотоксические клетки, иммунорегуляторный индекс, Т-активированные, NK- и B-активированные клетки)
17.54. Вен. кровь 3 дня
6 500 ₽ Добавить В корзину
Гуморальный иммунитет (иммуноглобулины IgA, IgM, IgG, IgE, циркулирующие иммунокомплексы, компоненты комплемента С3, С4)
17.51. Вен. кровь 8 дней
3 890 ₽ Добавить В корзину
Иммунный статус (скрининг) (Фагоцитарная активность лейкоцитов, клеточный иммунитет, иммуноглобулин IgE общий, иммуноглобулины IgA, IgM, IgG)
27.960. Вен. кровь 3 дня
7 640 ₽ Добавить В корзину
Иммунный статус расширенный
17.61. Вен. кровь 14 дней
22 310 ₽ Добавить В корзину
Клеточный иммунитет (Т-лимфоциты, Т-хелперы, Т-цитотоксические клетки, Иммунорегуляторный индекс, B-лимфоциты, NK-T-клетки, NK-клетки, Лейкоцитарная формула)
17.50. Вен. кровь 3 дня
5 200 ₽ Добавить В корзину
Т-киллеры:
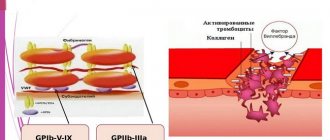
Т-киллеры – самая известная субпопуляция лимфоцитов. Они обладают способностью разрушать неполноценные клетки организма, вступая с ними в непосредственный контакт. Их еще называют цитотоксические лимфоциты: «цито» в переводе означает «клетка», значение слова «токсические» объяснять не надо.
Т-киллеры, строго осуществляющие иммунный надзор, агрессивно реагируют на чужеродный белок. Именно они вызывают реакцию отторжения трансплантата при пересадке органов. По этой причине при пересадке человеку любого органа ему некоторое время дают специальные медикаменты, которые угнетают иммунную систему: уменьшают повышенное содержание лимфоцитов и нарушают их взаимодействие. Иначе любая подобная операция заканчивалась бы отторжением нового органа или ткани, а может, даже гибелью пациента, которому такое вмешательство проводится.
Интересен механизм работы этих клеток. В отличие от фагоцитов, активно атакующих, пожирающих и переваривающих чужеродные частицы, Т-киллеры ведут себя на первый взгляд достаточно сдержанно. Своими отростками они прикасаются к объекту, а затем разрывают контакт и «уходят по своим делам». Клетка же, к которой прикоснулся лимфоцит, спустя какое-то время погибает… Отчего?
Дело в том, что во время своего «смертельного поцелуя» Т-киллеры оставляют на поверхности уничтожаемой ими клетки частицы своей мембраны. В местах контакта частицы «разъедают» поверхность объекта нападения. В результате в обреченной на гибель клетке фактически образуется сквозное отверстие. Она теряет ионы калия, внутрь нее входят ионы натрия и вода – так как клеточный барьер нарушается, ее внутренняя среда начинает напрямую сообщаться с внешней… В исходе клетка раздувается проникшей внутрь ее водой, из нее выходят белки цитоплазмы, органеллы разрушаются… Она погибает, а дальше к ней подходят фагоциты и пожирают ее остатки. Вот такое страшное наказание готовит организм всем клеткам, которые были распознаны иммунитетом как «неправильные» или чужеродные.
Использованная литература
- Литвинова, Л.С., Гуцол, А.А., Сохоневич Н.А. и др. Основные поверхностные Маркеры функциональной активности Т-лимфоцитов. Медицинская иммунология, 2014. — №1.
- Гистология (введение в патологию) / под ред. Э.Г. Улумбекова, Ю.А. Челышева, 1997. — С. 15-17, 532 -546.
- Энциклопедия клинических лабораторных тестов / под ред. Н.У. Тица. — М. : Лабинформ, 1997. — С. 214-215.
- Saraiva, D., Jacinto, A., Borralho, P. et al. HLA-DR in Cytotoxic T Lymphocytes Predicts Breast Cancer Patients’ Response to Neoadjuvant Chemotherapy. Front Immunol., 2021. — Vol. 9. — P. 2605.
Т-клетки памяти:
Справившись с очередной угрозой, лимфоциты ее запоминают. В организме человека образуется особый клон клеток, которые и хранят эти «воспоминания». Каждый клон несет в себе информацию об определенном виде угрозы. Если какой-то агрессор, с которым иммунная система уже встречалась, проникает в тело, то соответствующий клон размножается и быстро формирует вторичный иммунный ответ.
Разговор о разновидностях лимфоцитов и их функциях достаточно долгий. Здесь эта тема была представлена в максимально приемлемой и простой форме, без загрузки специфическими терминами и непонятными названиями. Будем надеяться, что любой читатель, даже не имеющий медицинского образования, примерно разобрался в том, как функционируют в его организме разные виды Т-лимфоцитов.
Из всего этого можно сделать очевидный вывод: для того чтобы жить полноценной здоровой жизнью, надо быть обладателем крепкой иммунной системы. Необходимо, чтобы процессы, о которых многие не задумываются, а еще большее количество людей даже не знает, происходили как надо.
Если природа не наградила вас устойчивым иммунитетом, вам следует задуматься о том, чтобы самостоятельно взяться за его укрепление. Для этого можно начать прием препарата Трансфер Фактор. В нем содержатся информационные молекулы, при помощи которых лимфоциты в норме общаются друг с другом, управляют различными процессами и координируют их. Восполняя недостаток естественных информационных молекул, средство является одним из самых рекомендуемых и эффективных препаратов для нормализации работы иммунитета, улучшения здоровья и профилактики заболеваний.
Клетки иммунитета обладают памятью и передают друг другу информацию