Автор Марина Лебедева
28.10.2004 13:33 (Обновлено: 05.07.2021 13:58)
Здоровье
Уровень гемоглобина у детей — один из важнейших показателей здоровья. Насколько опасны отклонения от нормы, что может быть их причиной и существуют ли способы исправить ситуацию?
В чем отличие «детского» гемоглобина от «взрослого»?
Гемоглобин начинает вырабатываться у ребенка еще в утробе на самых ранних стадиях формирования плода. Этот гемоглобин принципиально отличается от гемоглобина в крови взрослого человека и называется фетальным гемоглобином. Незадолго до рождения фетальный гемоглобин начинает заменяться «взрослой» формой этого белка — гликолизированным гемоглобином. Процесс полной замены завершается примерно в возрасте одного года.
В первые годы жизни норма гемоглобина в крови у ребенка значительно изменяется в зависимости от возраста. Этот показатель нужно тщательно контролировать, чтобы вовремя заметить критические отклонения от нормы.
Именно гемоглобин, содержащий железо, придает крови красный цвет. Но далеко не у всех существ на Земле кровь красная. Например, кровь осьминогов, омаров и крабов имеет сине-зеленый оттенок, поскольку в ней функцию гемоглобина выполняет другой белок — гемоцианин, который содержит медь, а не железо.
Железодефицитная анемия у детей грудного и младшего возраста
Анемию и анемический синдром, вызываемый многими причинами, можно упомянуть среди наиболее часто встречающихся патологических состояний, с которыми ежедневно приходится сталкиваться педиатрам общей практики. В эту группу входят различные заболевания и патологические состояния, характеризующиеся уменьшением содержания гемоглобина и/или эритроцитов в единице объема крови, приводящие к нарушению снабжения тканей кислородом. Применяются следующие лабораторные критерии анемии (Н. П. Шабалов, 2003). В зависимости от возраста детей уровень гемоглобина составляет:
- 0–1 сутки жизни — < 145 г/л;
- 1–14 дней жизни — < 130 г/л;
- 14–28 дней жизни — < 120 г/л;
- 1 мес — 6 лет — < 110 г/л.
Из всех анемий самой распространенной является железодефицитная (ЖДА), которая составляет примерно 80% от всех анемий. По данным Всемирной организации здравоохранения (ВОЗ), в мире более 500 тыс. человек страдает ЖДА. Распространенность ЖДА у детей в России и развитых европейских странах составляет: около 50% — у детей младшего возраста; более 20% — у детей старшего возраста.
ЖДА — это клинико-гематологический синдром, характеризующийся нарушением синтеза гемоглобина в результате дефицита железа, развивающегося на фоне различных патологических (физиологических) процессов, и проявляющийся признаками анемии и сидеропении.
Железо — один из основных микроэлементов в организме человека. В норме в организме взрослого человека содержится 3–5 г железа в связанной форме. 70% общего количества железа входит в состав гемопротеинов. Железо в этих соединениях связано с порфирином. Основной представитель этой группы — гемоглобин (58% железа); также железо содержится в миоглобине (8%), цитохромах, пероксидазах, каталазах — до 4%. Железо входит и в состав негемовых ферментов (ксантиноксидаза, никотинамидадениндинуклеотид (НАДН)-дегидрогеназа, аконитаза, локализующиеся в митохондриях); транспортной формы железа (трансферрин, лактоферрин). Запасы железа в организме существуют в двух формах: в виде ферритина (до 70%) и гемосидерина (до 30%). Особенность распределения железа у детей младшего возраста заключается в том, что у них выше содержание железа в эритроидных клетках и меньше железа приходится на мышечную ткань.
Всасывание железа происходит преимущественно в двенадцатиперстной кишке и проксимальных отделах тощей кишки. В суточном рационе обычно содержится около 5–20 мг железа, а усваивается только около 1–2 мг в сутки. Степень абсорбции железа зависит как от его количества в потребляемой пище и биодоступности, так и от состояния желудочно-кишечного тракта (ЖКТ).
Легче абсорбируется железо в составе гема (мясные продукты) — 9–22%. Всасывание негемового железа определяется диетой и особенностями желудочно-кишечной секреции.
Особенно активно всасывание железа происходит из грудного молока, хотя его содержание в нем невелико — всего 1,5 мг в литре; биодоступность железа грудного молока составляет до 60%. Этому способствует особая форма, в которой оно представлено, — в виде железосодержащего белка лактоферрина. В молекуле лактоферрина определены два активных центра связывания ионов Fe3+. Лактоферрин в грудном молоке содержится в виде насыщенной и ненасыщенной форм. Соотношение форм лактоферрина меняется в зависимости от периода лактации. В течение первых 1–3 мес жизни превалирует насыщенная железотранспортная форма лактоферрина. Наличие специфических рецепторов к лактоферрину на эпителиальных клетках слизистой оболочки кишечника способствует адгезии с ними лактоферрина и более полной его утилизации. Кроме того, лактоферрин, связывая лишнее, не всосавшееся в кишечнике железо, лишает условно-патогенную микрофлору необходимого для ее жизнедеятельности микроэлемента и запускает неспецифические бактерицидные механизмы. Установлено, что бактерицидная функция иммуноглобулина A реализуется только в присутствии лактоферрина.
Физиологические потери железа с мочой, потом, калом, через кожу, волосы и ногти не зависят от пола и составляют 1–2 мг в сутки, у женщин во время менструации — 2–3 мг в сутки. У детей потеря железа составляет 0,1–0,3 мг в сутки, возрастая до 0,5–1,0 мг в сутки у подростков.
Ежедневная потребность детского организма в железе составляет 0,5–1,2 мг в сутки. У детей раннего возраста в связи с быстрыми темпами роста и развития наблюдается повышенная потребность в железе. В этот период жизни запасы железа быстро истощаются из-за усиленного его потребления из депо: у недоношенных детей к 3-му месяцу, у доношенных — к 5–6-му мес жизни. Для обеспечения нормального развития ребенка в суточном рационе новорожденного должно содержаться 1,5 мг железа, а у ребенка 1–3 лет — не менее 10 мг.
Дефицит железа у детей приводит к росту инфекционной заболеваемости органов дыхания и ЖКТ. Железо необходимо для нормального функционирования структур головного мозга, при его недостаточном содержании нарушается нервно-психическое развитие ребенка. Установлено, что у детей, имевших в младенчестве железодефицитную анемию, в возрасте 3–4 лет определяются нарушения передачи нервных импульсов от центров головного мозга к органам слуха и зрения из-за нарушения миелинизации и, как следствие этого, нарушение проводимости нервов.
Причины железодефицитных состояний у детей очень разнообразны. Основной причиной ЖДА у новорожденных считается наличие ЖДА или скрытого дефицита железа у матери во время беременности. К антенатальным причинам относят также и осложненное течение беременности, нарушение маточно-плацентарного кровообращения, фетоматеринские и фетоплацентарные кровотечения, синдром фетальной трансфузии при многоплодной беременности. Интранатальными причинами дефицита железа являются: фетоплацентарная трансфузия, преждевременная или поздняя перевязка пуповины, интранатальные кровотечения из-за травматических акушерских пособий или аномалий развития плаценты или пуповины. Среди постнатальных причин сидеропенических состояний на первое место выступает недостаточное поступление железа с пищей. При этом более всего страдают новорожденные, находящиеся на искусственном вскармливании неадаптированными молочными смесями, коровьим и козьим молоком. Другими постнатальными причинами ЖДА являются: повышенная потребность организма в железе; потери железа, превышающие физиологические; заболевания ЖКТ, синдром нарушенного кишечного всасывания; дефицит запасов железа при рождении; анатомические врожденные аномалии (дивертикул Меккеля, полипозы кишечника); употребление продуктов, тормозящих абсорбцию железа.
В группе риска всегда находятся недоношенные дети и дети, родившиеся с очень большой массой, дети с лимфатико-гипопластическим типом конституции.
У детей первого года жизни к дефициту железа чаще всего приводит несбалансированная диета, в частности вскармливание исключительно молоком, вегетарианство, недостаточное употребление мясных продуктов.
К сидеропении способны приводить кровотечения различной этиологии. Источником этого могут быть: грыжа пищеводного отверстия диафрагмы, варикозное расширение вен пищевода, желудочно-кишечные язвы, опухоли, дивертикулы, язвенный колит, геморроидальные узлы, а также кровотечения из мочеполового тракта и дыхательных путей. Прием некоторых медикаментов, таких как нестероидные противовоспалительные препараты, салицилаты, кумарины, глюкокортикостероиды, также может привести к потере железа. Дефицит железа всегда сопутствует заболеваниям, сопровождающимся нарушениями кишечного всасывания (энтериты, болезнь Крона, паразитарные инвазии и др.). Дисбактериоз кишечника также препятствует нормальному перевариванию пищи и тем самым снижает способность организма усваивать железо. Кроме того, может иметь место нарушение транспорта железа из-за недостаточной активности и снижения содержания трансферрина в организме.
Распознать причину развития ЖДА в каждом конкретном случае чрезвычайно важно. Ориентация на нозологическую диагностику необходима, так как в большинстве случаев при лечении анемии можно воздействовать и на основной патологический процесс.
ЖДА проявляется общими симптомами. Один из главных и видимых признаков — бледность кожных покровов, слизистых оболочек, конъюнктив глаз. Обращают на себя внимание общая вялость, капризность, плаксивость, легкая возбудимость детей, снижение общего тонуса организма, потливость, отсутствие или снижение аппетита, поверхностный сон, срыгивание, рвота после кормления, понижение остроты зрения. Выявляются изменения со стороны мышечной системы: ребенок с трудом преодолевает физические нагрузки, отмечается слабость, утомляемость. У детей первого года жизни может наблюдаться регресс моторных навыков.
Во втором полугодии жизни и у детей старше года наблюдаются признаки поражения эпителиальной ткани — шершавость, сухость кожи, ангулярный стоматит, болезненные трещины в уголках рта, глоссит или атрофия слизистой оболочки ротовой полости, ломкость и тусклость волос, их выпадение, матовость и ломкость ногтей, разрушение зубов (кариес), отставание в физическом и психомоторном развитии.
В зависимости от степени тяжести заболевания выявляются симптомы поражения органов и систем: сердечно-сосудистой — в виде функционального шума в сердце, тахикардии; нервной системы — в виде головных болей, головокружений, обмороков, ортостатических коллапсов. Возможно увеличение размеров печени, селезенки. Со стороны ЖКТ наблюдается затрудненное глотание, вздутие кишечника, диарея, запоры, извращение вкуса — желание есть глину, землю.
Диагноз ЖДА ставится на основании клинической картины, лабораторных признаков анемии и дефицита железа в организме: гипохромная (цветовой показатель < 0,85) анемия различной степени тяжести, гипохромия эритроцитов, снижение средней концентрации гемоглобина в эритроците (менее 24 пг), микроцитоз и пойкилоцитоз эритроцитов (в мазке периферической крови); уменьшение количества сидеробластов в пунктате костного мозга; уменьшение содержания железа в сыворотке крови (< 12,5 мкмоль/л); повышение общей железосвязывающей способности сыворотки (ОЖСС) более 85 мкмоль/л (показатель «голодания»); повышение уровня трансферрина в сыворотке крови, при снижении его насыщения железом (менее 15%); снижение уровня ферритина в сыворотке (< 15 мкг/л).
Лечение ЖДА
Лечение ЖДА у детей раннего возраста должно быть комплексным и базироваться на четырех принципах: нормализация режима и питания ребенка; возможная коррекция причины железодефицита; назначение препаратов железа; сопутствующая терапия.
Важнейшим фактором коррекции железодефицита является сбалансированное питание, и в первую очередь грудное вскармливание. Грудное молоко не только содержит железо в высокобиодоступной форме, но и повышает абсорбцию железа из других продуктов, употребляемых одновременно с ним. Однако интенсивные обменные процессы у грудных детей приводят к тому, что к 5–6-му мес жизни антенатальные запасы железа истощаются даже у детей с благополучным перинатальным анамнезом и малышей, вскармливаемых грудным молоком.
Из других продуктов питания наибольшее количество железа содержится в свиной печени, говяжьем языке, телячьих почках, яичном желтке, устрицах, бобах, кунжуте, морской капусте, пшеничных отрубях, гречке, фисташках, турецком горохе, персиках, овсяных хлопьях, шпинате, лесных орехах и др. (табл.).
Абсорбцию железа тормозят танины, содержащиеся в чае, карбонаты, оксалаты, фосфаты, этилендиаминтетрауксусная кислота, используемая в качестве консерванта, антацидные препараты, тетрациклины. Аскорбиновая, лимонная, янтарная и яблочная кислоты, фруктоза, цистеин, сорбит, никотинамид усиливают всасывание железа.
Необходимы длительные прогулки на свежем воздухе, нормализация сна, благоприятный психологический климат, профилактика острых респираторных вирусных инфекций (ОРВИ), ограничение физической нагрузки. Питание ребенка должно быть сбалансированным и включать продукты, богатые железом, и вещества, усиливающие его всасывание в кишечнике. Детям, страдающим ЖДА, необходимо вводить прикорм на 2–4 нед раньше, чем здоровым. Введение мясного прикорма целесообразно начинать в 6 мес. Следует отказаться от введения в рацион ребенка таких каш, как манная, рисовая, толокняная, отдавая предпочтение гречневой, ячменной, просяной.
Однако эти меры недостаточны и не приводят к излечению ЖДА, поэтому основой терапии являются препараты железа. К основным из них, применяемым перорально, относятся: соединения трехвалентного железа — гидроксид-полимальтозный комплекс (полимальтозат железа), мальтофер, мальтофер фол, феррум лек и железо-протеиновый комплекс (железа протеин сукцинилат) — ферлатум; соединения двухвалентного железа — актиферрин, ферроплекс, тардиферон, гемофер, тотема, фумарат железа, ферронат.
Начинать терапию следует препаратами для приема внутрь и только при плохой их переносимости (тошнота, рвота, диарея), синдроме нарушенного всасывания, резекции тонкого кишечника и т. д. — препараты железа назначают парентерально. При назначении пероральных форм следует отдавать предпочтение неионным соединениям железа — протеиновый (ферлатум) и гидроксид-полимальтозный комплексы Fe3+ (мальтофер, мальтофер фол, феррум лек). Эти соединения имеют большую молекулярную массу, что затрудняет их диффузию через мембрану слизистой кишечника. Они поступают из кишечника в кровь в результате активного всасывания. Это объясняет невозможность передозировки препаратов в отличие от солевых соединений железа, всасывание которых происходит по градиенту концентрации. Взаимодействия их с компонентами пищи и лекарственными препаратами не происходит, что позволяет использовать неионные соединения железа, не нарушая режим питания и терапии сопутствующей патологии. Их применение существенно снижает частоту развития побочных эффектов, обычно наблюдаемых при назначении пероральных препаратов железа (тошнота, рвота, диарея, запоры и др.). Кроме того, у детей раннего возраста большое значение имеет лекарственная форма препарата. В этом возрасте удобно использовать капли и сиропы, что обеспечивает в том числе возможность точного дозирования препаратов и не вызывает негативного отношения ребенка.
При назначении любых препаратов железа необходимо рассчитывать индивидуальную потребность в нем для каждого пациента, исходя из того, что оптимальная суточная доза элементарного железа составляет 4–6 мг/кг. Среднесуточная доза железа при лечении ЖДА составляет 5 мг/кг. Применение более высоких доз не имеет смысла, поскольку объем всасывания железа не увеличивается.
Применение парентеральных препаратов железа показано для быстрого достижения эффекта при анемии тяжелой степени; патологии ЖКТ, сочетающейся с нарушением всасывания; неспецифическом язвенном колите; хроническом энтероколите; при тяжелой непереносимости оральных форм препаратов. На сегодняшний день в Российской Федерации для внутривенного введения разрешен только один препарат — венофер (сахарат железа), для внутримышечного может использоваться феррум лек.
Необходимо помнить, что у детей раннего возраста дефицит железа никогда не бывает изолированным и часто сочетается с недостаточностью витаминов С, В12, В6, РР, А, Е, фолиевой кислоты, цинка, меди и др. Это связано с тем, что алиментарная недостаточность и нарушенное кишечное всасывание, приводящие к дефициту железа, влияют и на насыщаемость данными микронутриентами. Поэтому в комплексную терапию ЖДА необходимо включать поливитаминные препараты.
Об эффективности терапии ЖДА можно судить уже через 7–10 дней по увеличению ретикулоцитов в 2 раза по сравнению с исходным количеством (так называемый ретикулоцитарный криз). Также оценивается прирост гемоглобина, который должен составлять 10 г/л и более в неделю. Соответственно, достижение целевого уровня гемоглобина наблюдается в среднем через 3–5 нед от начала терапии в зависимости от тяжести анемии. Однако лечение препаратами железа должно проводиться в достаточных дозах и длительно (не менее 3 мес) даже после нормализации уровня гемоглобина, с тем чтобы пополнить запасы железа в депо.
Если же в течение 3–4 нед не наблюдается значимого улучшения показателей гемоглобина, то необходимо выяснить, почему лечение оказалось неэффективным. Наиболее часто речь идет: о неадекватной дозе препарата железа; продолжающейся или неустановленной кровопотере; наличии хронических воспалительных заболеваний или новообразований; сопутствующем дефиците витамина В12; неверном диагнозе; глистной инвазии и других паразитарных инфекциях.
Противопоказаниями к назначению препаратов железа являются:
- отсутствие лабораторного подтверждения дефицита железа;
- сидероахрестические анемии;
- гемолитические анемии;
- гемосидероз и гемохроматоз;
- инфекция, вызванная грамотрицательной флорой (энтеробактерии, синегнойная палочка, клебсиелла).
При развитии тяжелых анемий, сопровождаемых угнетением эритропоэза и снижением продукции эритропоэтина, показано назначение препаратов рекомбинантного человеческого эритропоэтина (рчЭПО). Особое значение имеет применение рчЭПО при развитии ранней анемии недоношенных, которая развивается на втором месяце жизни и встречается, по данным различных авторов, в 20–90% случаев. Назначение препаратов рчЭПО (рекормон, эпрекс, эпокрин) приводит к резкой активизации эритропоэза и, как следствие, к значительному возрастанию потребностей в железе.
Поэтому применение рчЭПО является показанием к назначению препаратов железа, как правило, парентеральных. В настоящее время в Российской Федерации разрешены к применению a- и b-эпоэтины, которые вошли в список дополнительного лекарственного обеспечения. Назначeние рчЭПО позволяет в большинстве случаев избежать гемотрансфузий, при которых велика вероятность осложнений (трансфузионные реакции, сенсибилизация и пр.). Предпочтительным способом введения препаратов рчЭПО, особенно в раннем детском возрасте, является подкожный. Подкожный способ введения более безопасный и экономичный, так как для достижения эффекта необходимы меньшие дозы, чем при внутривенном введении. До недавнего времени в странах Евросоюза и в Российской Федерации для лечения гипорегенераторных анемий у детей использовались в основном β-эритропоэтины, которые при подкожном введении не вызывали значимых побочных реакций в отличие от a-эритропоэтинов, при подкожном введении которых был велик риск развития красноклеточной аплазии. Наиболее широкое распространение среди β-эритропоэтинов получил препарат рекормон (Ф. Хоффманн-Ля Рош), который удобен в применении и приводит к быстрому повышению уровня эритроцитов и ретикулоцитов, не влияя на лейкопоэз, повышает уровень гемоглобина, а также скорость включения железа в клетки.
С 2004 г. в европейских странах разрешено подкожное введение a-эритропоэтинов, среди которых в нашей стране наиболее часто используются эпрекс (Янсен-Силаг) и эпокрин (Сотекс-ГосНИИ ОЧБ).
Целью лечения рчЭПО является достижение показателей гематокрита 30–35% и устранение необходимости переливаний крови. Значения целевой концентрации гемоглобина могут варьировать в зависимости от дней и месяцев жизни ребенка, однако не могут быть ниже 100–110 г/л. В зависимости от дозы целевые значения концентрации гемоглобина и гематокрита достигаются примерно через 8–16 нед лечения рчЭПО.
С целью профилактики ЖДА рчЭПО назначается недоношенным новорожденным, родившимся с массой тела 750–1500 г до 34-й недели беременности.
Лечение эритропоэтином должно начинаться как можно раньше и продолжаться 6 нед. Препарат рекормон вводят подкожно в дозе 250 МЕ/кг 3 раза в неделю. Однако необходимо учитывать, что чем меньше возраст ребенка, тем более высокие дозы эритропоэтина ему требуются, поэтому доза может быть увеличена.
Как было сказано выше, терапия рчЭПО приводит к резкому возрастанию потребления железа, поэтому в большинстве случаев, особенно у недоношенных детей, одновременно с повышением гематокрита снижается содержание ферритина в сыворотке. Быстрое расходование запасов железа в организме может привести к ЖДА. Поэтому всем больным, получающим терапию рчЭПО, показано назначение препаратов железа. Терапия препаратами железа должна продолжаться до нормализации уровня сывороточного ферритина (не менее 100 мкг/мл) и насыщения трансферрина (не менее 20%). Если концентрация ферритина в сыворотке сохраняется стойко ниже 100 мкг/мл или есть другие признаки дефицита железа, дозу железа следует увеличить, в том числе с использованием парентеральных препаратов.
Профилактика ЖДА у детей раннего возраста включает в себя: антенатальную (правильный режим и питание беременной, своевременное выявление и лечение анемии беременной, превентивное назначение препаратов железа женщинам из групп риска по развитию ЖДА); постнатальную (соблюдение гигиенических условий жизни ребенка, длительное грудное вскармливание и своевременное введение прикормов, адекватный выбор смеси для детей, находящихся на смешанном и искусственном вскармливании, профилактика развития у ребенка рахита, гипотрофии и ОРВИ). В профилактическом назначении препаратов железа нуждаются:
- женщины репродуктивного возраста, страдающие обильными и длительными менструальными кровотечениями;
- постоянные доноры;
- беременные, особенно повторные беременности, следующие с коротким интервалом;
- женщины с дефицитом железа в период лактации.
Профилактическое назначение препаратов железа показано детям из групп риска по развитию ЖДА:
- недоношенные дети (с 2-месячного возраста);
- дети от многоплодной беременности, осложненных беременностей и родов;
- крупные дети с высокими темпами прибавки массы и роста;
- дети с аномалиями конституции;
- страдающие атопическими заболеваниями;
- находящиеся на искусственном вскармливании неадаптированными смесями;
- с хроническими заболеваниями;
- после кровопотерь и хирургических вмешательств;
- с синдромом мальабсорбции.
Доза железа, назначаемого с профилактической целью, зависит от степени недоношенности ребенка:
- для детей с массой тела при рождении менее 1000 г — 4 мг Fe /кг/день;
- для детей с массой тела при рождении от 1000 до 1500 г — 3 мг Fe/кг/день;
- для детей с массой тела при рождении от 1500 до 3000 г — 2 мг Fe/кг/день.
Значимость проблемы ЖДА у детей раннего возраста обусловлена ее большой распространенностью в популяции и частым развитием при различных заболеваниях, что требует постоянной настороженности врачей любых специальностей. Тем не менее на современном этапе в арсенале врача имеется достаточно диагностических и лечебных возможностей для раннего выявления и своевременной коррекции сидеропенических состояний.
Литература
- Анемии у детей/под ред. В. И. Калиничевой. Л.: Медицина, 1983. 360 с.
- Анемии у детей: диагностика и лечение/под ред. А. Г. Румянцева, Ю. Н. Токарева. М., 2000. 128 с.
- Аркадьева Г. В. Диагностика и лечение железодефицитных анемий. М., 1999. 59 с.
- Белошевский В. А. Железодефицит у взрослых, детей и беременных. Воронеж, 2000. 121 с.
- Борисова И. П., Скобин В. Б., Павлов А. Д. Раннее назначение рекомбинантного эритропоэтина у недоношенных детей/7-й Национальный конгресс «Человек и лекарство». М., 2000. С. 125.
- Вахрамеева С. Н., Денисова С. Н. Латентная форма железодефицитной анемии беременных женщин и состояние здоровья их детей//Российский вестник перинатологии и педиатрии. 1996. № 3. С. 26–29.
- Дворецкий Л. И., Воробьев П. А. Дифференциальный диагноз и лечение при анемическом синдроме. М.: Ньюдиамед, 1994. 24 с.
- Дворецкий Л. И. Железодефицитные анемии//Русский медицинский журнал. 1997. № 19. С. 1234–1242.
- Идельсон Л. И. Гипохромные анемии. М.: Медицина, 1981. 190 с.
- Казакова Л. М., Макрушин И. М. Иммунитет при дефиците железа// Педиатрия. 1992. № 10–12. С. 54–59.
- Казюкова Т. В., Самсыгина Г. А., Левина А. А. Дефицит железа у детей: проблемы и решения//Consilium medicum. 2002. С. 17–19.
- Малаховский Ю. Е., Манеров Ф. К., Сарычева Е. Г. Легкая форма железодефицитной анемии и латентный дефицит железа — пограничные состояния у детей первых двух лет жизни//Педиатрия. 1988. № 3. С. 27–34.
- Папаян А. В., Жукова Л. Ю. Анемии у детей: руководство для врачей. СПб.: Питер, 2001. 382 с.
- Пригожина Т. А. Эффективность рекомбинантного эритропоэтина в комплексной профилактике и лечении ранней анемии недоношенных: автореф. дис. … канд. мед. наук. М., 2001. 19 с.
- Румянцев А. Г., Морщакова Е. Ф. Павлов А. Д. Эритропоэтин. Биологические свойства. Возрастная регуляция эритропоэза. Клиническое применение. М., 2002. С. 137–144; 266–270.
- Румянцев А. Г., Морщакова Е. Ф., Павлов А. Д. Эритропоэтин в диагностике, профилактике и лечении анемий. М., 2003. 568 с.
- Сергеева А. И., Султанова К. Ф., Левина А. А. и др. Показатели метаболизма железа у беременных женщин и детей раннего возраста//Гематология и трансфузиология. 1993. № 9–10. С. 30–33.
- Тетюхина Л. Н., Казакова Л. М. Профилактика дефицита железа как мера по снижению заболеваемости детей//Педиатрия. 1987. № 4. С. 72–73.
- Dallman P. R., Looker A. C., Johnson C. L. et al. Iron Nutrition in Health and Disease. Eds. Hallberg L., Asp N. G. Libbey; London. 1996; 65–74.
- Messer Y., Escande B. Erytropoietin and iron in the anemia of prematurity. TATM 1999; 15–17.
- Ohls R. K. The use of erythropoetin in neonatoles//Clin Perinatol. 2000; 20 (3): 681–696.
- Ulman J. The role of erythropoietin in erythropoiesis regulation in fetuses and newborn infants//Ginekol. Pol. 1996; 67:205–209.
Л. А. Анастасевич, кандидат медицинских наук А. В. Малкоч, кандидат медицинских наук РГМУ, Москва
Как узнать уровень гемоглобина?
Уровень гемоглобина выявить достаточно просто — нужно только сдать кровь на общий анализ. Этот анализ включает в себя определение концентрации гемоглобина, которая измеряется в граммах на литр. Чтобы получить точную информацию, кровь нужно сдавать до кормления, желательно — утром. В течение полутора-двух часов после кормления гемоглобин понижается.
Существуют и косвенные признаки, указывающие на низкий гемоглобин у детей, в частности,
- бледная кожа
- и шелушения.
Содержание гемоглобина в капиллярной крови на 10–20% выше, чем в венозной. Это нужно учитывать при интерпретации результатов анализов.
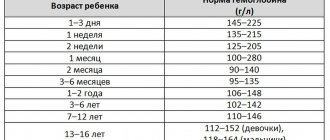
Какова норма гемоглобина в крови у ребенка?
Уровень гемоглобина у новорожденных в первые дни жизни очень высокий — 180–240 г/л. Это объясняется тем, что у малыша имеется запас железа, накопленный еще во время пребывания в утробе. У недоношенных малышей гемоглобин часто ниже нормы — 160–220 г/л. У таких деток высок риск анемии — критического понижения гемоглобина в крови.
К концу первой недели уровень гемоглобина у детей понижается до 160–200 г/л. В последующие недели и месяцы гемоглобин плавно повышается — к месячному возрасту его норма составляет уже 120–160 г/л, а к году — 110–130 г/л.
В 5 лет нормой считается 110–140 г/л, в 10 — 120–140 г/л[5].
В период полового созревания, примерно к 15 годам, уровень гемоглобина у детей достигает «взрослых» показателей — 125–165 г/л.
Гродненская областная детская клиническая больница
Подробности Опубликовано 25 Март 2015
Врач-педиатр 5 педиатрического отделения, областной внештатный детский гематолог Гузаревич В.Б.
Железодефицитная анемия у подростков
Пубертатный период — это период полового созревания, взросления, роста и развития организма подростка. Он имеет свои уникальные особенности, обусловленные мощной вегетативной, эндокринной и иммунной перестройкой организма на фоне физиологического ростового скачка, а также нарушениями психосоциальной адаптации.
Именно в это время формируются многочисленные транзиторные функциональные расстройства и проявляются ранее скрытые органические дефекты: гипоталамическая дисфункция, с широким спектром клинических проявлений (вегетососудистая дистония, метаболический синдром и пр.), врожденная неполноценность соединительной ткани (висцеро-птозы, суставная гипермобильность, остеохондроз и пр.), что способствует снижению адаптации к воздействию внешней среды. Следует отметить, что нозологические формы в этот возрастной период имеют существенные отличия. Так, у подростков доминируют заболевания эндокринной, нервной и костно-мышечной систем, тогда как инфекционные и простудные заболевания чаще регистрируются у детей младшего возраста, у взрослых возрастает частота новообразований и болезней системы кровообращения. Для этого возраста характерна полисистемность (полиморбидность) заболеваний. Например, у девушки, считающей себя практически здоровой, при тщательном обследовании диагностируются дисменорея, железодефицитное состояние, нарушение осанки, плоскостопие, нефроптоз, нестабильность шейного отдела позвоночника, хронический тонзиллит, миопия, синдром раздраженного кишечника с запором, дисфункция билиарного тракта, кристаллурия. Железодефицитное состояние относится к одной из актуальных проблем подросткового возраста. Уменьшение количества железа в организме приводит к нарушению образования гемоглобина, развитию гипохромной анемии и трофических расстройств в органах и тканях.
В настоящее время не вызывает сомнения, что главным фактором, способствующим развитию железодефицитной анемии у подростков, является несоответствие между запасами железа в организме и потребностями в нем. Дефицит железа в подростковом возрасте значительно чаще наблюдается у девушек, что может быть обусловлено обильными менструациями. Однако в тех случаях, когда потребности в железе намного превышают его поступление, железодефицитная анемия может развиться и у юношей. Наиболее частыми причинами в данном случае являются интенсивный рост подростка, занятия тяжелыми видами спорта, исходный низкий уровень железа на фоне несбалансированного питания, вегетарианства. Следует помнить, что железодефицитная анемия часто наблюдается при таких состояниях, как нервная анорексия, заболевания желудка и 12-перстной кишки, в том числе ассоциированные с Н. pylori, повторные кишечные инфекции, лямблиоз, глистные инвазии, воспалительные заболевания кишечника.
Клиническими проявлениями железодефицитной анемии являются бледность кожи и слизистых оболочек, снижение аппетита, повышенная физическая и умственная утомляемость, снижение работоспособности, раздражительность, эмоциональная неустойчивость, повышенная потливость головокружение, головные боли, шум в ушах, мелькание «мушек» перед глазами, учащение пульса, боли в сердце. Характерны сухость и шелушение кожи, дистрофические изменения ногтей, тусклость и повышенная ломкость волос, «заеды» в углах рта; жжение языка, затруднение глотания твердой пищи, извращение вкуса и запаха, мышечные боли, снижение тонуса мышц, ночное и дневное недержание мочи из-за слабости мышечного аппарата, запор. У девушек возможно нарушение менструального цикла.
Диагностика железодефицитной анемии основывается на снижении уровня гемоглобина ниже 120 г/л в общем анализе крови, а также снижение содержания ферритина (запаса железа в организме) в сыворотке крови.
Во всех случаях железодефицитного состояния необходимо установить непосредственную причину его возникновения и по возможности ее ликвидировать. Лечение должно быть комплексным и нацеленным не только на устранение анемии как симптома, но и на ликвидацию дефицита железа и восполнение его запасов в организме.
Необходимо обогатить рацион подростка продуктами — основными источниками железа, при этом имеет значение не только количество железа в конкретном продукте, но и степень его всасывания и возможность усвоения организмом.
Мясо, особенно красное (телятина, говядина, баранина, говяжий язык), является лучшим источником гемового железа, из него усваивается 20–25% железа. Железо из курицы и свинины усваиваются в меньшей степени. А в печени и рыбе железо содержится в виде ферритина и гемосидерина, поэтому усваивается еще хуже.
Негемовое железо (овощи, фрукты, орехи) усваивается плохо (1–5%), причем на его усвоение влияет много факторов, которые могут как улучшать, так и ухудшать его всасывание. Так, усиливают всасывание железа: витамин С (особенно много в цитрусовых), соляная кислота (содержится в желудочном соке), фруктоза (фрукты, мед). Ухудшают всасывание железа: препараты, снижающие кислотность желудочного сока (антисекреторные препараты, антациды), кальций (много в молочных продуктах), оксалаты (шпинат, капуста, свекла, орехи, шоколад, чай и пр.), полифенолы (какао, кофе, черный и некоторые виды травяного чая), фитиновая кислота (грецкие орехи, миндаль, бобовые, отруби)
Однако когда анемия уже развилась, ее нельзя вылечить только диетой: железодефицитная анемия лечится препаратами железа. Питание помогает поддерживать нормальный баланс железа в организме после лечения. Предпочтение отдается пероральным формам препаратов железа, так как по сравнению с парентеральным введением скорость восстановления уровня гемоглобина почти не отличается, а количество побочных эффектов резко снижено. Прием препаратов железа рекомендуется за 1 час до еды, предпочтительно в вечернее время, так как процесс всасывания железа увеличивается во второй половине суток. Терапевтический эффект при пероральном приеме железа появляется постепенно. Первым положительным клиническим признаком является исчезновение или уменьшение мышечной слабости. На 8–12 день от начала лечения повышается содержание ретикулоцитов в периферической крови. Нормализация гемоглобина происходит к 4–5 неделе от начала терапии.
В последние годы в терапии железодефицитных состояний у подростков активно применяют железосодержащие препараты нового поколения на основе полимальтазного комплекса гидроокиси трехвалентного железа – Феррум Лек, Мальтофер и Мальтофер Фол, который кроме железа содержит фолиевую кислоту, принимающую участие в выработке нуклеиновых кислот, пуринов, аминокислот, стимулирующих образование эритроцитов. Одной из привлекательных характеристик этих препаратов является их низкая токсичность. Препараты хорошо переносятся, имеют приятный вкус и форму жевательных таблеток, что, несомненно, повышает приверженность к терапии. При железодефицитной анемии детям старше 12 лет и подросткам — по 100–200 мг в сутки, а при латентном дефиците железа и в профилактических целей — по 50–100 мг в сутки. Длительность терапии, как правило, составляет не менее 2 мес, что обусловлено степенью дефицита железа в организме и истощения его запасов, скоростью кроветворения, всасываемостью. В случае клинически выраженного дефицита железа нормализация гемоглобина достигается лишь через 2–3 мес после начала лечения. После нормализации уровня гемеглобина необходимо продолжить прием препаратов железа в профилактических дозах для восстановления внутренних резервов железа в течение нескольких месяцев.
Прогноз заболевания благоприятный: излечение наступает в подавляющем большинстве случаев. Проблема дефицита железа – это, прежде всего, проблема питания, поэтому первичная профилактика железодефицитной анемии – это адекватное, сбалансированное питание человека в любом возрасте.
Причины и признаки повышения уровня гемоглобина
К повышению уровня гемоглобина у малыша могут привести разные причины. Самыми распространенными являются:
- обезвоживание — как в результате недостаточного поступления жидкости и перегрева, так и в результате диареи;
- врожденные сердечные заболевания, в том числе легочно-сердечная недостаточность;
- онкологические заболевания;
- нарушения синтеза гормона эритропоэтина;
- непроходимость кишечника;
- болезни крови.
Иногда немного повышенный уровень гемоглобина может считаться вариантом нормы. У людей, живущих в условиях высокогорья, гемоглобин немного повышен — это реакция на разреженный воздух. Также гемоглобин может быть немного выше нормы у детей, которые очень активно занимаются спортом.
Дети с повышенным гемоглобином обычно вялые и раздражительные, они страдают от сонливости и быстрой утомляемости, кожа иногда принимает красноватый оттенок.
Железодефицитные состояния у подростков: принципы коррекции
Одним из важных направлений в педиатрии является подростковая медицина, или гебиатрия, — раздел медицины, изучающий процессы полового созревания, взросления, роста и развития организма подростка, а также специфические заболевания, характерные для подросткового периода жизни.
Пубертатный период имеет свои уникальные особенности, обусловленные мощной вегетативной, эндокринной и иммунной перестройкой организма на фоне физиологического ростового скачка, а также нарушениями психосоциальной адаптации. Именно в это время формируются многочисленные транзиторные функциональные расстройства и проявляются ранее скрытые органические дефекты: гипоталамическая дисфункция, с широким спектром клинических проявлений (вегетососудистая дистония, метаболический синдром и пр.), врожденная неполноценность соединительной ткани (висцероптозы, суставная гипермобильность, остеохондроз и пр.), что способствует снижению адаптации к воздействию внешней среды. Следует отметить, что нозологические формы в этот возрастной период имеют существенные отличия. Так, у подростков доминируют заболевания эндокринной, нервной и костно-мышечной систем, тогда как инфекционные и простудные заболевания чаще регистрируются у детей младшего возраста, у взрослых возрастает частота новообразований и болезней системы кровообращения. Для этого возраста характерна полисистемность (полиморбидность) заболеваний. Например, у девушки, считающей себя практически здоровой, при тщательном обследовании диагностируются дисменорея, железодефицитное состояние, нарушение осанки, плоскостопие, нефроптоз, нестабильность шейного отдела позвоночника, хронический тонзиллит, миопия, синдром раздраженного кишечника с запором, дисфункция билиарного тракта, кристаллурия.
Железодефицитное состояние относится к одной из актуальных проблем подросткового возраста. Уменьшение количества железа в организме приводит к нарушению образования гемоглобина и снижению темпов его синтеза, накоплению свободного протопорфирина в эритроцитах, развитию гипохромной анемии и трофических расстройств в органах и тканях.
В настоящее время не вызывает сомнения, что главным фактором, способствующим развитию железодефицитной анемии у подростков, является несоответствие между запасами железа в организме и потребностями в нем.
Дефицит железа в подростковом возрасте значительно чаще наблюдается у девушек, что может быть обусловлено обильными менструациями. Однако в тех случаях, когда потребности в железе намного превышают его поступление, железодефицитная анемия может развиться и у юношей. Наиболее частыми причинами в данном случае являются интенсивный рост подростка, занятия тяжелыми видами спорта, исходный низкий уровень железа на фоне несбалансированного питания, вегетарианства. Следует помнить, что железодефицитная анемия часто наблюдается при таких состояниях, как нервная анорексия, идиопатический гемосидероз легких, синдром Гудпасчера, атрансферринемия, коллагенозы, заболевания желудка и 12-перстной кишки, в том числе ассоциированные с Н. pylori, повторные кишечные инфекции, лямблиоз, глистные инвазии, воспалительные заболевания кишечника, инфекционные заболевания (туберкулез, бруцеллез, микоз и пр.), а также при хронической почечной недостаточности и в процессе диализного лечения [1, 2].
Выделяют прелатентный дефицит железа (опустошаются запасы железа только из депо при сохранении транспортного и гемоглобинового фондов железа), латентный дефицит железа (составляет 70% от всех железодефицитных анемий) и железодефицитная анемия (составляет 30% от всех железодефицитных состояний) (табл.).
Клиническая картина железодефицитной анемии состоит из двух ведущих синдромов: анемического и сидеропенического. Для последнего характерны дистрофические изменения кожи и ее придатков; извращение вкуса и обоняния, мышечные боли (ввиду дефицита миоглобина), мышечная гипотония, изменения нервной регуляции.
Следует отметить, что клинические проявления заболевания в подростковом возрасте отличаются от проявлений у детей раннего возраста. Так, для них более характерны койлонихии, синева склер (через истонченную склеру просвечивает сосудистая оболочка), вкусовые и обонятельные нарушения, дисфагия, диспепсия.
Диагностика железодефицитных состояний основывается на определении представленных выше лабораторных показателей. Основным критерием является содержание ферритина в сыворотке крови [3]. Однако при невозможности определения данного показателя можно ориентироваться на уровень гемоглобина, определение которого доступно в любом медицинском учреждении.
Целесообразно ежегодное определение уровня гемоглобина у девушек, имеющих обильные кровопотери при менструации или иной природы, низкое потребление железа с пищей (пищевые ограничения для снижения веса, вегетарианство и пр.), железодефицитную анемию различной природы в анамнезе. Юноши нуждаются в контроле уровня гемоглобина, если интенсивно занимаются тяжелыми видами спорта (анемия атлетов).
Во всех случаях железодефицитного состояния необходимо установить непосредственную причину его возникновения и по возможности ее ликвидировать (устранить источник кровопотери, провести терапию основного заболевания, осложнившегося сидеропенией). Лечение должно быть комплексным и нацеленным не только на устранение анемии как симптома, но и на ликвидацию дефицита железа и восполнение его запасов в организме.
Необходимо обогатить рацион подростка продуктами — основными источниками железа, при этом имеет значение не только количество железа в конкретном продукте, но и степень его всасывания и возможность усвоения организмом.
Мясо, особенно красное (телятина, говядина, баранина), является лучшим источником гемового железа, из него усваивается 20–25% железа. Железо из курицы и свинины усваиваются в меньшей степени. А в печени и рыбе железо содержится в виде ферритина и гемосидерина, поэтому усваивается еще хуже.
Негемовое железо (овощи, фрукты, орехи) усваивается плохо (1–5%), причем на его усвоение влияет много факторов, которые могут как улучшать, так и ухудшать его всасывание. Так, усиливают всасывание железа: витамин С (особенно много в цитрусовых), соляная кислота (содержится в желудочном соке), фруктоза (фрукты, мед). Ухудшают всасывание железа: препараты, снижающие кислотность желудочного сока (антисекреторные препараты, антациды), кальций (много в молочных продуктах), оксалаты (шпинат, капуста, свекла, орехи, шоколад, чай и пр.), полифенолы (какао, кофе, черный и некоторые виды травяного чая), фитиновая кислота (грецкие орехи, миндаль, бобовые, отруби) [4].
Однако когда анемия уже развилась, ее нельзя вылечить только диетой: железодефицитная анемия лечится препаратами железа. Питание помогает поддерживать нормальный баланс железа в организме после лечения.
К наиболее часто применяемым соединениям железа в педиатрической практике относятся препараты железа трехвалентного гидроксид полимальтозат и соли двухвалентного железа — сульфат, фумарат, хлорид и глюконат. Для улучшения всасывания соли двухвалентного железа комбинируют с органическими кислотами, аминокислотами и другими соединениями. Предпочтение отдается пероральным формам, так как по сравнению с парентеральным введением скорость восстановления уровня гемоглобина почти не отличается, а количество побочных эффектов резко снижено. Прием препаратов железа рекомендуется за 1 час до еды, предпочтительно в вечернее время, так как процесс абсорбции железа увеличивается во второй половине суток.
Терапевтический эффект при пероральном приеме железа появляется постепенно. Первым положительным клиническим признаком является исчезновение или уменьшение мышечной слабости. На 8–12 день от начала лечения повышается содержание ретикулоцитов в периферической крови. Нормализация гемоглобина происходит к 4–5 неделе от начала терапии.
В последние годы в терапии железодефицитных состояний у подростков активно применяют железосодержащие препараты нового поколения на основе полимальтазного комплекса гидроокиси трехвалентного железа — Мальтофер и Мальтофер Фол, который кроме железа содержит фолиевую кислоту, принимающую участие в выработке нуклеиновых кислот, пуринов, аминокислот, стимулирущих эритропоэз.
Результаты применения Мальтофера различными авторами оцениваются положительно [5]. Одной из привлекательных характеристик этого препарата является его низкая токсичность. Препарат хорошо переносится, имеет приятный вкус и форму жевательных таблеток, что, несомненно, повышает приверженность к терапии. При железодефицитной анемии детям и подросткам в возрасте от года до 12 лет Мальтофер назначается в дозе 50–100 мг в сутки, при латентном дефиците и для профилактики дефицита железа — по 25–50 мг в сутки. Детям и подросткам старше 12 лет — по 100–300 мг в сутки, а при латентном дефиците железа и в профилактических целей — по 50–100 мг в сутки. Длительность терапии, как правило, составляет не менее 2 мес, что обусловлено степенью дефицита железа в организме и истощения его запасов, скоростью кроветворения, всасываемостью. В случае клинически выраженного дефицита железа нормализация гемоглобина достигается лишь через 2–3 мес после начала лечения. Для восстановления внутренних резервов железа прием в профилактических дозах должен быть продолжен в течение нескольких месяцев. При продолжающихся кровопотерях необходимо проводить профилактические курсы лечения препаратом железа (по 1 мес 2–4 раза в год).
Литература
- Коровина Н. А., Заплатников А. Л., Захарова И. Н. Железодефицитные анемии у детей (руководство для врачей). М., 1999. С. 64.
- Финогенова Н. А., Чернов В. М., Морщакова Е. Ф. и др. Анемии у детей: диагностика и лечение. М., 2000. С. 9–17.
- Финогенова Н. А., Чернов В. М., Морщакова Е. Ф. и др. Анемии у детей. Диагностика, дифференциальная диагностика, лечение. М., 2004. С. 20–64.
- Городецкий В. В., Годулян О. В. Железодефицитные состояния и железодефицитная анемия: лечение и диагностика (метод. рекомендации). М., 2006. С. 25.
- Соболева М. К. Опыт применения препаратов Мальтофер и Мальтофер Фол при лечении железодефицитной анемии у детей и подростков // Сибирский консилиум. 2003, № 1, с. 79–82.
Т. А. Бокова1, кандидат медицинских наук Г. В. Масликова, кандидат медицинских наук
ГБУЗ МО МОНИКИ им. М. Ф. Владимирского, Москва
1 Контактная информация
Чем опасен пониженный гемоглобин у ребенка?
Пониженный гемоглобин у детей встречается чаще, чем повышенный. По данным ВОЗ, нехватка гемоглобина — анемия — встречается у 47,4% детей дошкольного возраста и у 25,4% школьников.
Низкий гемоглобин у ребенка — существенный фактор риска. Он может привести к отставанию в развитии, развитию заболеваний сердца и почек (они наравне с мозгом первыми страдают от кислородного голодания), нарушению функционирования иммунной системы, заболеваниям кожи и отекам. Без лечения анемия может закончиться кардиомиопатией и сердечной недостаточностью, а эти патологии смертельно опасны. При критическом снижении уровня гемоглобина возможна даже гипоксическая кома.
Признаки низкого гемоглобина у детей многочисленны, но неспецифичны, иными словами, они сопровождают не только анемию, но и множество других заболеваний. В любом случае родителей должны насторожить такие симптомы, как слабость, вялость, плаксивость и сонливость малыша, понижение аппетита, бледность кожи. Дети постарше могут жаловаться на головокружения и головную боль. При низком гемоглобине заметно страдают когнитивные функции — память, способность к концентрации внимания, обучаемость. Множество случаев плохой успеваемости объясняется вовсе не ленью, а нехваткой железа и низким гемоглобином.
Сдавать анализ на гемоглобин нужно регулярно, как минимум раз в три месяца. Определить развитие анемии по косвенным признаком непросто, очень часто ее симптомы игнорируются или списываются на другие причины.
Делать анализ крови на гемоглобин необходимо после любых инфекционных болезней, резких изменений рациона (например, после назначения диеты при выявлении аллергии или болезней ЖКТ) и любых неожиданных переменах в поведении малыша. Если ваш ребенок из активного и жизнерадостного малыша внезапно превратился в соню и плаксу, нужно незамедлительно взять направление на анализ.
Низкий гемоглобин нередко отражается и на физическом развитии — такие детки медленно растут и отстают от здоровых сверстников по весу и росту.
Иногда анализы показывают, что гемоглобин у ребенка понижен, и это вызывает обоснованное беспокойство родителей. Чем может быть вызван пониженный гемоглобин у ребенка?
Причины пониженного гемоглобина у детей
- Инфекционные болезни и паразитарные поражения.
- Нехватка железа в питании мамы во время беременности и кормления или его недостаток в рационе самого ребенка. Нередко низкий гемоглобин наблюдается у детей женщин, придерживающихся веганской диеты. Растительная пища тоже содержит железо, но оно усваивается хуже, чем то, что присутствует в продуктах животного происхождения.
- Дефицит витаминов, необходимых для того, чтобы железо всасывалось в кровь — к ним относятся фолиевая кислота и витамин С. Важную роль в усвоении железа играет также и медь.
- Заболевания пищеварительной системы, при которых нарушается всасывание железа.
- Кровопотери после травм и операций, а также после регулярных кровотечений, например назальных.
- Нехватка физической активности и свежего воздуха.
- Врожденные патологии, в частности талассемия.
Причины анемии
Причин снижения уровня эритроцитов много, основные можно разделить на три группы:
- недостаточная выработка эритроцитов;
- преждевременное разрушение эритроцитов (гемолиз);
- кровопотеря.
Недостаточная выработка эритроцитов
Для образования гемоглобина и эритроцитов организму требуются такие микроэлементы, как железо, а также витамины В12 и фолиевая кислота. При значимом дефиците этих элементов продукция эритроцитов уменьшается и развивается железо-, В12- или фолиеводефицитная анемия. При этом дефицит железа является наиболее частой причиной анемии у детей, особенно в возрасте до 5 лет.
Эритроциты образуются из стволовых клеток-предшественниц, которые находятся в костном мозге. Уменьшение количества стволовых клеток или нарушение их функции также может приводить к снижению количества эритроцитов и возникновению анемии. Такие состояния могут быть врожденными или приобретенными.
Преждевременное разрушение эритроцитов
Анемия, возникшая вследствие гемолиза, может наблюдаться у детей при врожденных генетически-обусловленных патологиях эритроцитов, например при талассемии или сфероцитозе. В более старшем возрасте причинами гемолиза могут быть аутоиммунные заболевания, инфекции, прием некоторых лекарственных препаратов, заболевания печени и почек и ряд других болезней, например микроангиопатия.
Кровопотеря
Повышенная потеря эритроцитов может наблюдаться при явных либо скрытых кровопотерях. У детей и подростков среди явных кровопотерь чаще всего встречаются носовые и маточные кровотечения (обильные менструации). Скрытые кровопотери могут наблюдаться при заболеваниях почек, а также воспалительных заболеваниях желудочно-кишечного тракта.
Профилактика отклонений от нормы
Самая важная мера предотвращения развития осложнений, связанных с изменением уровня гемоглобина, — это регулярные анализы и осмотры у педиатра. Иногда пониженный или повышенный гемоглобин у ребенка говорит о наличии серьезных заболеваний, требующих немедленного лечения. Но многое зависит и от родителей, поскольку отклонения от нормы часто встречаются у здоровых детей из-за погрешностей в питании и режиме.
Профилактика повышенного гемоглобина
- Во время беременности и кормления грудью мамам не стоит принимать витаминные комплексы с железом без консультации с врачом. Во многих случаях дополнительные источники железа необходимы, но крайне важно не превышать рекомендованную дозировку.
- Не покупайте детские витаминные комплексы без консультации с врачом. Если ребенок получает достаточное количество железа и витаминов с пищей, добавочная порция витаминов и минералов может принести больше вреда, чем пользы.
- Пересмотрите рацион ребенка — он должен содержать мясо, овощи и фрукты, богатые железом.