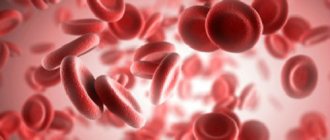
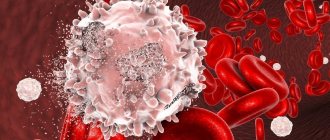
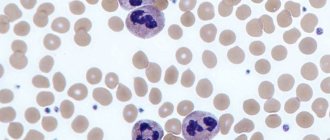
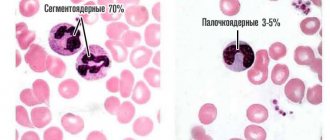
Нормобласты (нормоциты) – последняя, еще ядерная, стадия красных кровяных телец (эритроцитов) на пути к взрослому, полноценному состоянию.
На этой стадии нормобласты имеют ядро, чтобы, потеряв его, превратиться в молодую безъядерную клетку, содержащую гемоглобин и уже способную выполнять главную задачу эритроцитов (участие в дыхании).
Прежде чем стать нормобластами, будущие красные кровяные тельца проходят определенный путь.
Как известно, все элементы крови берут свое начало от стволовой клетки – она является родоначальницей будущих лейкоцитов, тромбоцитов, эритроцитов и т. д., поскольку дает несколько ростков, среди которых значится и эритроцитарный (из него произойдут клетки эритроидного ряда, в том числе, и интересующие нас – нормобласты).
Самой молодой, морфологически различимой, клеткой красного ряда является эритробласт,
который раньше называли проэритробластом. Это довольно большая по размерам (14 – 20 мк) клетка, содержащая такое же большое ядро, но не имеющая даже признаков того, за что так ценят взрослый эритроцит – в ней нет гемоглобина.
Норма в крови – ноль
В норме эти клетки в крови не встречаются,
поэтому о повышенных значениях нормобластов при исследовании препаратов речи идти не может (норма – 0). Они могут быть или не быть, а дальше уже подсчет, если их получается обнаружить.
Исключение из этих правил составляют новорожденные дети.
У ребенка первых дней жизни их присутствие в общем анализе крови не должно вызывать удивления: повышенное содержание в костном мозге и появление в крови нормобластов объясняется усиленной продукцией эритропоэтина в этот период, что ведет к увеличению красных клеток крови и гемоглобина. Спустя несколько дней, когда продукция эритропоэтина снижается, значения этих показателей тоже падают вниз.
Через некоторое время от рождения, точнее, между 2 и 3 месяцами жизни, у ребенка вновь отмечается повышенный уровень
нормобластов и ретикулоцитов и опять за счет усиленного синтеза эритропоэтина, что не вызывает беспокойства у педиатров, ведь процесс этот – физиологический.
После этого всплеска, нормы у ребенка по этим показателям с каждым месяцем все больше начнут приближаться к нормам взрослых, стало быть, в препаратах детской крови нормобласты тоже не будут встречаться, а станут обнаруживаться, как им и положено, только в миелограмме.
нормобласты, вышедшие из костного мозга в кровь
Их отсутствие в крови, между тем, не исключает их диагностическую значимость, ведь появляются они не просто так, а в силу каких-то патологических изменений, так или иначе, затрагивающих главный орган кроветворения – костный мозг.
Поскольку слово «бласт» – обозначает «росток», то все потомки бласта уже не могут считаться ростками, поэтому правильнее было бы к дальнейшим формам это название не применять, а пристроить им окончание «цит». В связи с этим, устаревшее слово «нормобласты» в лексиконе специалистов с большим стажем работы присутствует только по привычке, а молодые врачи уже называют эту клетку нормоцитом.
Гипохромная анемия — симптомы и лечение
Лечение железодефицитной анемии
Терапия ЖДА включает:
- лечение заболевания, которое вызвало анемию;
- диетотерапию;
- назначение препаратов железа: пероральных (в виде таблеток) или парентеральных (в виде внутривенных или внутримышечных инъекций);
- гемотрансфузию — переливание эритроцитарной массы.
Цели лечения ЖДА:
- купировать признаки анемии (касается острой анемии);
- нормализовать уровень гемоглобина;
- восстановить запасы железа в организме и поддерживать их нормальный уровень.
Курс терапии назначается лечащим врачом индивидуально [2].
Диетотерапия
Вылечить анемию только с помощью диеты невозможно, но всё же питание с высоким содержанием животного белка и железа будет полезно, чтобы поддержать уровень гемоглобина [37].
Для нормальной работы организма взрослым мужчинам требуется 65–117 г белка в сутки, женщинам — 58–87 г в сутки. Белки содержатся в растительной пище (бобовых, злаковых, овощах и фруктах) и в продуктах животного происхождения (молоке, молочных продуктах, яйцах, мясе, рыбе и морепродуктах). Белки и железо лучше усваиваются из продуктов животного происхождения [35]:
- из мяса и рыбы всасывается 15–35 % железа;
- из растительных продуктов — 1–5 % [24].
Яблоки, гранаты, сок красного цвета (свёклы или томатов) не могут компенсировать нехватку железа.
Питание должно быть 4–6 разовым с небольшим количеством пищи за один приём. Для нормального переваривания еда должна быть комнатной температуры: слишком холодная или слишком горячая пища раздражают слизистую желудка, что препятствует всасыванию полезных веществ. Также рекомендуется отказаться от алкоголя и курения [20].
Лечение пероральными препаратами железа
Используются две группы препаратов:
- содержащие двухвалентную форму железа (II): сульфат железа (Сорбифер Дурулес, Тардиферон, Актиферрин, Фенюльс, Максифер), фумарат железа (Ферретаб, Ранферон-12), глюконат железа (Тотема);
- содержащие трёхвалентную форму железа (III): железа гидроксид полимальтозат (Мальтофер, Феррум Лек), железа гидроксид сахарозный комплекс (Венофер), железа гидроксид декстран (Космофер, Феркайл).
Отличие групп препаратов железа
| Основные характеристики | Двухвалентная форма железа | Трёхвалентная форма железа |
| Путь введения | Перорально (через рот) | Перорально (через рот) Парентерально (инъекционно) |
| Побочные эффекты | Возникают часто при длительном применении | Возникают редко |
| Влияние пищи на всасывание | Молочные продукты, чай, кофе ухудшают всасывание железа. Продукты с витамином С улучшают всасывание | Не влияет |
| Эффект всасывания | Хорошо всасываются | Всасываются хуже |
Препараты железа не задерживаются в организме и быстро выводятся почками, поэтому быстро восполнить дефицит железа не получится. Чтобы восполнить запасы железа, доза должна составлять от 100 до 300 мг двухвалентного железа в сутки в форме таблеток. Повышать дозировку не имеет смысла, так как всасывание железа при этом не увеличивается, избыток будет уходить с калом.
На 3–5-й день от начала лечения в ОАК обычно повышается количество ретикулоцитов (незрелых эритроцитов), что говорит об эффективности терапии. Если пациент регулярно принимает препараты железа в лечебной дозировке, уровень гемоглобина нормализуется примерно через 3–4 недели от начала терапии. На этом этапе нельзя прекращать лечение. Нужно продолжить поддерживающую терапию, чтобы заполнить депо железа. Поддерживающая терапия продолжается около 6 месяцев в дозе 100 мг в сутки.
Возможные побочные эффекты. Все препараты, содержащие соли железа, могут вызывать раздражение слизистой оболочки желудка. Поэтому иногда возникают побочные эффекты в виде рвоты, диареи или изжоги. Чтобы от них избавиться, необходимо:
- снизить дозировку препарата;
- сократить сроки лечения;
- принимать препарат перед сном;
- не сочетать с несовместимыми продуктами.
Если эти меры не помогли, препарат отменяют [13].
Что влияет на всасывание железа. Витамин С помогает железу лучше усваиваться: кислота препятствует окислению железа и поддерживает его в двухвалентной форме. Поэтому рекомендуется добавить в рацион продукты, содержащие этот витамин. Дополнительный приём добавок с витамином С не требуется [36].
Беременным рекомендуется принимать препараты железа совместно с фолиевой кислотой (витамином В9), так как она участвует в процессе кроветворения [28].
Наличие в пище фитиновой кислоты (содержится в злаках, бобовых, семенах, орехах и др.), кофеина и танина (в чае, кофе), фосфатов, оксалатов (в растительных продуктах) ухудшает всасывание железа в 4–6 раз, так как они образуют нерастворимые комплексы с трёхвалентным железом и выводятся с калом [23]. Рекомендуется ограничить их потребление или употреблять за 6 часов до приёма препаратов железа.
Кальций, йод, магний, цинк, хром и селен, содержащиеся в продуктах питания и в добавках, тоже препятствуют усвоению железа, поэтому не следует принимать их вместе.
Лечение парентеральными препаратами железа
Показания к парентеральному введению препаратов железа:
- Непереносимость препаратов железа в форме таблеток.
- Нарушение всасывания железа при синдроме недостаточности всасывания, резекции тонкой кишки, энтеритах, целиакии и других заболеваниях ЖКТ.
- Обострение хронических заболеваний ЖКТ: язвенной болезни желудка и двенадцатиперстной кишки, болезни Крона, неспецифического язвенного колита.
- Тяжёлая анемия (гемоглобин 70 г/л и менее).
Препараты для парентерального введения: Феринжект, Феррактин, Феррум Лек, Фербитол, Эктофер. Препараты назначает только лечащий врач после проведённого обследования и уточнения вида анемии. Переизбыток железа в некоторых случаях ещё опаснее, чем его недостаток: портится эмаль, могут развиться тяжёлые токсические гепатиты до трансформации в цирроз и др.
Гемотрансфузия (переливание эритроцитарной массы)
Переливание эритроцитарной массы может потребоваться по индивидуальным показаниям, которые определяет лечащий врач. Показаниями могут быть:
- ЖДА тяжёлой степени;
- сопутствующие сердечно-сосудистые патологии (например, ишемическая болезнь сердца), если есть риск декомпенсации состояния на фоне анемии [38].
Лечение талассемии
Тактика лечения при различных формах заболевания отличается. Малая β-талассемия не требует лечения. При большой β-талассемии нужно начинать лечение с первых месяцев жизни: проводить гемотрансфузию и вводить хелатирующие препараты, которые удаляют избыток железа из организма (Деферазирокс).
При всех формах талассемии показан приём витаминов группы В. При развитии гиперспленизма, при котором селезёнка увеличивается и активно разрушает клетки крови, необходимо удалить селезёнку.
Одним из методов терапии талассемии является пересадка костного мозга [24].
От рождения до больших свершений
Однако, заострив внимание на названиях, мы несколько отклонились от темы. Итак, события происходят в костном мозге:
1 стадия: эритробласт
Эритробласт
– первая клетка, которую можно определить под микроскопом в препарате костного мозга. Округлое ядро, нежная сетчатая структура хроматина, несколько маленьких ядрышек (обычно 2 – 4), просветления вокруг ядра пока нет – вот такая морфология родоначальницы клеток, которые потом станут эритроцитами. В общем анализе крови здорового человека ее даже искать не нужно, поскольку ее там просто не может быть, ведь она только зародилась и до выхода «в свет» должна обзавестись новыми чертами и качествами, чтобы стать в периферической крови трудоспособной, а, стало быть, полезной.
2 стадия: пронормоцит
Пройдя стадию эритробласта, очень молодая клетка слегка уменьшает свой размер (10 – 15 мк) и начинает менять структуру ядра, чтобы потом легче было от него избавиться (ядро уменьшается и грубеет, ядрышки исчезают, вокруг ядра намечается легкое перинуклеарное просветление) – это больше не эритробласт. Новая клетка и называется по-новому пронормоцитом
, хотя некоторые продолжают именовать ее по-старому –
пронормобластом
. На этой стадии клетка эритроидного ряда очень плохо дифференцируема в миелограмме, ведь она еще не полностью утратила черты предшественника, да и новые пока не приобрела.
3 стадия: нормобласт (нормоцит)
Однако проходит совсем немного времени, как из неузнаваемой клеточной структуры, появляется «герой нашего рассказа» – нормобласт
или
нормоцит
. Он начинает насыщаться гемоглобином, который вначале концентрируется вокруг ядра (
базофильный
нормоцит), а затем распространяется на всю цитоплазму, превращая клетку в
полихроматофильный
нормобласт, то есть, клетка явно готовится к выполнению своей ответственной функции.
По мере того, как нормобласты накапливают сложный хромопротеин (Hb), необходимость в ядре отпадает, оно только мешает своим присутствием накапливаться гемоглобину. Получив достаточное количество Hb, нормоцит становится оксифильным
: цитоплазма распространяется почти все территорию, ядро теряет значимость, поэтому становится совсем маленьким (пикнотичным), огрубевшим с измененной до неузнаваемости структурой, напоминающей вишневую косточку.
4 стадия: рождение эритроцита
Нормобласт, который собирается избавиться от ненужного в дальнейшем ядра, некоторое время остается нормобластом, но в малой численности. Вытолкнув наконец-то ядро, клетка превращается в «новорожденный» полихроматофильный эритроцит
, сохраняющий небольшое количество наследственной информации (РНК), которая в течение 24 часов окончательно покинет клетку, хотя клеткой «новоиспеченную» форму назвать уже трудно (скорее, тоже по привычке).
Молодые, насыщенные гемоглобином и потерявшие последнюю связь с «родиной» эритроциты, называют ретикулоцитами
, которые в очень скором времени, после того как прибудут в кровеносное русло (до 48 часов), потеряют последнее, что подчеркивает их юный возраст – ретикулум, и превратятся в полноценные взрослые кровяные тельца –
эритроциты
. Обнаружить ретикулоциты в крови помогает специальная окраска. Весь путь, пройденный эритроцитом от эритробласта до потерявшей ядро клетки, занимает не менее 100 часов.
Очевидно, что в норме клетки красного ряда на уровне нормобласта (до того, пока он станет ретикулоцитом) у здорового человека всех возрастов в крови не появляются.
Нормобластоз – признак патологии?
Появление нормобластов в общем анализе крови (слово «повышены» как-то не подходит – об этом сказано ранее) – яркий признак патологии в организме. Эти клетки выходят в периферическую кровь при следующих обстоятельствах:
- Анемиях различной этиологии (талассемия), некоторых формах острых и хронических лейкозов. В этих случаях может доходить до нормобластоза, то есть, значения их не просто повышены – нормобластов огромное множество; Кроме этого, данные патологические состояния у взрослых людей могут вызывать образование очагов экстрамедуллярного кроветворения (печень, селезенка), которые тоже будут давать свою порцию нормоцитов.
- Массивной кровопотере – чтобы спасти организм, костному мозгу ничего другого не остается делать, как начать активную регенерацию клеточных элементов;
- Стремясь как-то восполнить недостаток в кровеносном русле, нормобласты выходят раньше времени из костного мозга при повышенном разрушении красных кровяных телец (гемолиз) без угнетения функционировании системы кроветворения;
- Остром эритролейкозе
(о. эритромиелоз, болезнь Ди Гильемо) – заболевании редком, но злокачественном. Основной характерной чертой острого эритромиелоза считают появление в периферической крови большого количества клеток эритроидного ряда, не потерявших ядро; - При распространении метастазов
злокачественных опухолей на костную систему повышенные концентрации этих клеток будут отмечаться в костном мозге, затем они начнут покидать его и выходить в периферическую кровь. Следует отметить, что в таких случаях часто не прослеживается прямой зависимости между нормобластозом и степенью анемизации (значительно повышенные количества нормобластов можно заметить при слабо выраженном малокровии);
Внезапное появление представителей молодой популяции эритроидного ряда в крови носит название кровяного криза, который характерен для злокачественной анемии.
В этом случае появление такого признака, наоборот, несколько обнадеживает, поскольку является предвестником надвигающейся ремиссии. А вот спокойная кровь при данной патологии заставляет подозревать низкую регенераторную способность органов кроветворения (апластическая анемия) и настраиваться на неблагоприятный прогноз.
Иногда клетки эритроидного ряда, не прошедшие стадию нормобласта до конца, покидают костный мозг преждевременно по причине тяжелого состояния человека, которое не обусловлено патологией системы кроветворения. Например, это может случиться при различных патологических процессах, протекающих с недостаточностью кровообращения.
Клиническое значение анализа крови (фрагмент лекции проф. Е.Б.Владимирской)
Гематология:
12.03.2009
д.м.н., проф. Е.Б.ВладимирскаяНИИ детской гематологии Минздрава России
Кровь, будучи внутренней средой организма, несет в себе стигматы жизнедеятельности различных органов и систем, изучение которых имеет несомненное клиническое значение, необходимо для диагноза, прогноза течения и контроля за терапией практически всех внутренних болезней человека.
Наиболее доступным является изучение морфологического состава крови, результаты его входят в алгоритм диагностики большинства патологических процессов.
Со времен первых исследований крови под микроскопом без использования окраски (середина прошлого века) клетки крови принято было делить на красные — эритроциты (по цвету гемоглобина) и белые — лейкоциты. Лейкоциты, в свою очередь, делятся на клетки, содержащие специфическую зернистость в цитоплазме, и по отношению этой зернистости к окраске делятся на (нейтрофилы, эозинофилы и базофилы) и не содержащие — лимфоциты и моноциты. По форме ядра первые часто называют полиморфонуклеары, а вторые — мононуклеары.
В последние годы все чаще клинический анализ крови выполняется на автоматических счетчиках, что значительно повышает точность подсчета, но, однако же, не отменяет значения данных, полученных «вручную» с помощью светооптической микроскопии. Сопоставление результатов этих двух методов, вместе с используемыми референтными значениями показателей представлено в табл.1.
Таблица 1
| Автоматический подсчет | Единицы измерения | Границы нормы | Ручной подсчет |
| hgb -гемоглобин | г/литр | М: 132 — 173 Ж: 117 — 155 | Hb |
| rbc- эритроциты | 1012 /литр | М: 4,3 – 5,7 Ж: 3,8 – 5,1 | эр. |
| hct-гематокрит | % | М: 39 – 49 Ж: 35 – 45 | ht |
| mcv- средний объем эритроцита | 1 мкм3 = 1фемтолитр | 80,0 – 95,0 | Сферический индекс (3,2-3,4) |
| mch-среднее содержание гемоглобина в эритроците | пикограммы 1 гр.=1012 пикограмм | 27,0 – 31,0 | Цветовой показатель (0,85 – 1,0) Цв.пок.= Нв (г/л) х 3_____ Эр (первые три цифры) |
| mchc– средняя концентрация Нв в 1 эритроците | г/дл | 32,0 — 36,0 | |
| rdwширина распределения эритроцитов по объему | ширина гистограммы | 11,5 – 14,5 | Нет аналога |
| plt –тромбоциты | *109 /л | 150 — 400 | Тромбоциты |
| wbc- лейкоциты | *109 /л | 4,5 –11,0 | Лейкоциты |
| neu — нейтрофилы | *109 /л % | 1,8 – 5,5 47,0 – 72,0 | Нейтрофилы |
| lym – лимфоциты | *109 /л % | 1,2 – 3,0 19,0 – 37,0 | Лимфоциты |
| mon – моноциты | *109 /л % | 0,1 – 0,9 3,0 – 11,0 | Моноциты |
| eos – эозинофилы | *109 /л % | 0,02 – 0,3 0,5 – 5,0 | Эозинофилы |
| bas – базофилы | *109 /л % | 0,0 – 0,07 0,0 –1,0 | Базофилы |
Комментируя представленные в таблице данные, необходимо отметить:
- подавляющее большинство автоматических счетчиков не определяет молодые формы лейкоцитов, нормобласты и ретикулоциты — эти данные можно получить только «вручную»;
- нормативные значения никогда не выражаются одной цифрой, существует предел допустимых колебаний (он представлен в таблице для всех показателей), в который укладывается 99,9% нормы.
Проанализируем клиническое значение отдельных показателей анализа крови.
Показатели красной крови.
Анемией называется снижение гемоглобина ниже 120 г/л: легкая степень – 110-120 г/л; средняя степень – 90-110 г/л; тяжелая степень – ниже 90 г/л.
По соотношению показателей красной крови выделяют 3 вида анемии, что является отправным пунктом для дальнейшей диагностики.
Микроцитарно-гипохромные анемии:
MCV < 80 Цв.п. < 0,85
MCH < 27; MCHC < 32
- Железодефицитная анемия
- Анемия при хроническом воспалении
- Врожденная сфероцитарная гемолитическая анемия.
- Талассемия.
Нормоцитарно-нормохромные анемии:
MCV 80 – 95
MCH = 27-31; MCHC = 32-36 Цв.п. = 0,85-1,0
Острая кровопотеря.
- Анемия при хронической почечной недостаточности
- Анемия при эндокринной патологии.
- Анемия при раке.
- Гемолитические анемии, иммунные и неиммунные.
- Апластическая анемия.
- Миелодиспластический синдром.
Гиперхромно-макроцитарная анемия.
MCV > 95
MCH > 31; MCHC = 32-36 Цв.п.> 1,0
- Мегалобластная В-12 – дефицитная (пернициозная) анемия.
- Мегалобластная фолиеводефицитная анемия.
- Аутоиммунная гемолитическая анемия.
Таким образом, при выявлении снижения гемоглобина следует прежде всего определить характер анемии: нормо-, гипо- или гиперхромный.
Остановимся подробнее на железодефицитной анемии и анемии при хроническом воспалении, диагностика и лечение которых являются прерогативой врачей-терапевтов и не требуют специальных гематологических исследований.
Железодефицитная анемия (ЖДА) выявляется у 50% женщин и 40% мужчин, представляя собою одно из самых распространенных заболеваний человека. Наиболее частой причиной ЖДА является скрытая форма кровоточивости: у мужчин – из желудочно-кишечного тракта и бронхо-легочной системы, у женщин – мено-, метроррагии. Беременность – также один из факторов развития дефицита железа у женщин. Недостаточное потребление в пище мясных продуктов является другой существенной и при этом социально обусловленной причиной развития дефицита железа. У детей, рождающихся с запасом железа, получаемым от матери в последний месяц внутриутробного развития, дальнейшее поступление железа происходит только из прикорма. Таким образом, причинами развития дефицита железа у детей раннего возраста могут быть недоношенность, многоплодная беременность, позднее введение прикорма, инфекции (повышенное потребление железа микробной флорой и нарушение всасывания).
Клиническая картина ЖДА складывается из следующих клинических синдромов:
1. Анемия: слабость, сонливость, утомляемость, одышка, сердцебиение, функциональный систолический шум, плавание мушек перед глазами.
2. Сидеропенический синдром:
· сухость, ломкость, выпадение волос, ранняя седина;
· уплощение и ломкость ногтей;
· сухость кожи, гиперкератоз;
· болезненные, незаживающие трещины в углах рта, на языке, пальцах рук, ног, пятках;
· извращение вкусовых и обонятельных пристастий;
· частые инфекции;
· нарушение глотания, мышечная слабость, слабость сфинктеров (недержание мочи при смехе, кашле)
В диагностический алгоритм ЖДА, кроме подробного клинического исследования с целью выявления скрытой кровоточивости, входит обязательное определение основных показателей обмена железа. Диагноз ЖДА подтверждают следующие значения этих показателей:
- сывороточное железо ниже 12,5 мкмоль/л
- общая железосвязывающая способность (ОЖСС) выше 64,4 мкмоль/л
- ферритин сыворотки ниже 12 мкг/л.
Коррекция ЖДА проводится длительным пероральным лечением препаратами железа (6-8 недель после восстановления гемоглобина).
Необходимо проведение дифференциального диагноза между ЖДА и анемией при хроническом воспалении.
Анемия при хроническом воспалении по показателям морфологического состава крови ничем не отличается от ЖДА и также сопровождается снижением содержания сывороточного железа. Однако в основе ее развития лежит не экзогенный дефицит железа, а невозможность его утилизации. Лечение железом при такой анемии противопоказано. Дифференциальный диагноз основан на изучении показателей обмена железа и представлен в Табл.2.
Таблица 2. Дифференциальный диагноз между ЖДА и анемией при хроническом воспалении.
| Показатели | ЖДА | Анемия при хроническом воспалении |
| Сывороточное железо | Снижено | Снижено |
| ОЖСС | Повышено | Норма или снижено |
| Ферритин сыворотки | Снижен | Норма или повышен |
Подводя итог краткому анализу клинического значения морфологических показателей красной крови, следует остановиться отдельно на ретикулоцитах и нормобластах.
Морфологическим признаком, указывающим на гемолитический характер снижения гемоглобина, является рост числа ретикулоцитов. При нормальном гемоглобине число ретикулоцитов не превышает 0,5-1,5%. Ожидаемый ретикулоцитарный ответ на гемолитическую анемию при сохранном кроветворении представлен в табл.3.
Табл.3. Ожидаемый ретикулоцитарный ответ на гемолитическую анемию.
| Гематокрит, % | 45 | 40 | 35 | 30 | 25 | 20 | 15 |
| Гемоглобин, г/л | 130 | 120 | 115 | 100 | 83 | 66 | 50 |
| Ретикулоциты, % | 0,5 | 1,5 | 5 | 10 | 15 | 20 | 30 |
Динамическое наблюдение за уровнем ретикулоцитов необходимо также и для оценки ожидаемой эффективности лечения ЖДА и пернициозной анемии. Подъем ретикулоцитов закономерно наблюдается на 5-8 день лечения железом ЖДА и особенно выражен (до 60%) на 5-8 день лечения витамином В-12 пернициозной анемии. Такая реакция кроветворения на терапию этих заболеваний может рассматриваться и как подтверждение соответствующего диагноза exjuvantibus.
Нормобластоз в периферической крови бывает редко и всегда свидетельствует о серьезной патологии. Его появление закономерно наблюдается при тяжелых формах гемолитической анемии и у пациентов, перенесших спленэктомию. Обнаружение нормобластов в крови пациентов, не страдающих этой патологией, должно явиться поводом для поиска онкологической патологии.
Об эритроцитозе можно говорить при следующих показателях крови: эритроциты выше 5,7х10*12/л у мужчин и 5,2х10*12/л у женщин, гемоглобин выше 177 г/л и 172 г/л соответственно, гематокрит выше 52% и 48% соответственно.
Первичными эритроцитозами считаются редкий генетически детерминированный семейный эритроцитоз и эритремия.
Значительно чаще встречаются вторичные эритроцитозы, обусловленные повышенным образованием эритропоэтина в ответ на артериальную гипоксию или при некоторых опухолях.
Вторичные эритроцитозы могут быть разделены на следующие группы:
1. Артериальная гипоксия
- Высотная болезнь
- Хроническая легочная недостаточность
- «Синие» пороки сердца
2. Опухоли, продуцирующие эритропоэтин
- Опухоли почек, гипернефрома
- Опухоль надпочечников
- Гемангиома мозжечка
- Рак яичников
3. Локальная ишемия почек
- Киста
- Гидронефроз
- Стеноз почечной артерии
4. Вредное производство
- Кобальтовое отравление
Лечение вторичных эритроцитозов требует устранение их причины, но может быть и симптоматическим из-за угрозы тромбозов. Симптоматическое лечение эритроцитоза – кровопускание.
Показатели белой крови.
Об увеличении или уменьшении количества различных видов лейкоцитов периферической крови можно судить только по изменению абсолютного числа этих форменных элементов.
Нейтрофилезом называется увеличение числа нейтрофилов более 6х10*9/л.
Реже нейтрофилез бывает проявлением хронического миелолейкоза, сопровождается специфическими для него клиническими и гематологическими особенностями (увеличение селезенки, лимфоузлов, омоложение крови, анемия, гипертромбоцитоз, гиперплазия костного мозга, наличие Рh-хромосомы и химерного гена c-abl-bcr).
Гораздо чаще нейтрофилез является реакцией крови на воспаление, результатом воздействия бактериального эндотоксина и выброса тканями цитокинов воспаления и хемокинов. Нейтрофильный лейкоцитоз может сопровождать любое воспаление, бактериальные, грибковые и паразитарные инфекции, некротические изменения тканей, гипоксемию, интоксикацию и опухоли различной локализации. При длительном воздействии факторов, индуцирующих нейтрофилез, происходит истощение костномозгового гранулоцитарного резерва и в кровь начинают выходить молодые клетки нейтрофильного ряда (палочкоядерные, метамиелоциты и миелоциты). Такое состояние крови носит название лейкемоидной реакции нейтрофильного ряда. Иногда возникает необходимость проведение дифференциального диагноза между такой реакцией и начальной формой хронического миелолейкоза. Отсутствие анемии, гипертромбоцитоза и высокое содержание щелочной фосфатазы в нейтрофилах характерно для лейкемоидной реакции.
Нейтропения – снижение числа нейтрофилов менее 1,8 х 10*9/л.
Агранулоцитоз — снижение числа нейтрофилов менее 0,5 х 10*9/л.
Нейтропении могут быть первичными (врожденными и приобретенными), связанными с болезнями крови (острый лейкоз, аплазия кроветворения, циклическая нейтропения), и вторичными, сопровождающими заболевания, в процессе которых происходит разрушение и повышенное потребление нейтрофилов.
Ко вторичным, реактивным, нейтропениям относятся иммунные и нейтропении при тяжелых инфекциях. Нейтропения при сепсисе сопровождается обычно омоложением лейкоцитарной формулы и является плохим прогностическим симптомом, свидетельствующим об истощении кроветворения.
Необходимо остановиться на конституциональных, так называемых, безвредных нейтропениях. Около 4% людей имеют нормальный состав крови с пониженным содержанием нейтрофилов. Эта особенность, связана с генетически детерминированым быстрым перемещением нейтрофилов в ткани, где они и осуществляют присущие им защитные функции. Люди с таким составом крови обычно меньше подвержены интеркурентным инфекциям, быстрее выздоравливают от них. Однако нередко такие пациенты, к сожалению, являются предметом пристального внимания врачей, подвергаются множеству ненужных инвазивных исследований, у них развивается ятрогенная патология. Таким образом, нейтропения, не сопровождающаяся другими изменениями крови и какими–либо клиническими симптомами, не требует немедленного вмешательства. Такие пациенты нуждаются в динамическом наблюдении.
Отдельно хочется коснуться перераспределительных нейтрофилезов и нейтропений. Циркуляция нейтрофилов имеет свои особенности: половина клеток циркулирует с кровью (эти клетки и подлежат подсчету), в то время, как другая половина находится в «краевом стоянии» у стенок сосудов. Раздражение симпатической системы, спазм сосудов увеличивают число циркулирующих клеток, а раздражение парасимпатической системы, напротив, уменьшает их число. Отсюда стрессовые состояния способствуют преходящему нейтрофилезу (например, нейтрофилез у маленьких детей при крике), а ваготония – нейтропении.
Эозинофилия – увеличение числа эозинофилов выше 0,4 х 10*9/л.
Повышенный выброс эозинофилов в кровь происходит под действием ИЛ-4 и ИЛ-5, образующихся в повышенном количестве в процессе иммунологического повреждения тканей. В последнее время доказан киллерный эффект эозинофилов при некоторых гельминтозах и паразитарных инфекциях. Эозинофилия – характерная черта коллагенозов, аллергии, многих глистных и паразитарных инвазий, иммунодефицита, особенно гипер – IG-E- синдрома, и некоторых опухолей.
Моноцитоз – число моноцитов выше 0,8 х 10*9/л.
Заболевания часто, но не всегда ассоциирующиеся с моноцитозом включают в себя:
- Инфекции (особенно туберкулез, эндокардит, сифилис).
- Лихорадка неясного происхождения
- Различные формы неоплазий и миелопролиферативных болезней.
- Хронические воспаления (особенно холецистит и ревматоидный полиартрит)
- Состояние после спленэктомии.
Лимфоцитоз – увеличение числа лимфоцитов более 4,0 х 10*9/л
Среди злокачественных лимфопролиферативных заболеваний с высоким лимфоцитозом чаще всего встречается хронический лимфолейкоз, заболевание людей старше 45-летнего возраста. Отличительной особенностью этого лимфоцитоза является его моноклоновый характер и В-клеточное происхождение.
Вторичные, реактивные лимфоцитозы, носящие поликлоновый характер, сопровождают многие вирусные инфекции, некоторые воспалительные и иммунокомплексные болезни. К ним относятся:
1. Лимфотропные вирусные заболевания:
— инфекционный мононуклеоз (атипичные мононуклеары, характерная клиника);
— инфекционный лимфоцитоз (бессимптомная эпидемическая форма у маленьких детей — до 20-30 тыс.)
2. Цитомегаловирусная инфекция (атипичные мононуклеары, характерная клиника).
3. Детские инфекции: коклюш, ветрянка, продрома скарлатины.
4. Другие вирусные инфекции: краснуха, гепатит, некоторые респираторные аденовирусные инфекции в стадии реконвалесценции.
5. Воспалительные и иммунокомплексные болезни: тиреотоксикоз, язвенный колит, болезнь Крона, васкулиты.
Лимфоцитопения — снижение числа лимфоцитов ниже 1,2 х 10*9/л.
Наблюдается относительно редко, чаще всего при кортикостероидной терапии. Может также сопровождать СПИД, лимфогрануломатоз и различные хронические инфекции (например, туберкулез, диссеминированную красную волчанку, саркоидоз).
Гипертромбоцитозом считается увеличение числа тромбоцитов более 400,0 х 10*9/л.
Первичные гипертромбоцитозы сопровождают миелопролиферативные заболевания и являются следствием опухолевой трансформации мегакариоцитарного ростка костного мозга.
Вторичные реактивные гипертромбоцитозы наблюдаются:
- После оперативных вмешательств ( около 2-х недель).
- После спленэктомии (до 1 года).
- При злокачественных опухолях
- При острой постгеморрагической и гемолитической анемиях.
- При некоторых воспалениях (туберкулез, острый ревматизм, язвенный колит, остеомиелит).
Тромбоцитопения — снижение числа тромбоцитов ниже 100,0 х 10*9/л чаще всего бывает при опухолевых заболеваниях крови, апластической анемии и иммунной тромбоцитопенической пурпуре. Тромбоцитопения входит обязательной составляющей в синдром гиперспленизма при спленомегалии. Следует иметь в виду, что серьезная угроза кровоточивости возникает при снижении числа тромбоцитов ниже 20,0 х 10*9/л.
Реактивная тромбоцитопения бывает редко, может сопровождать любую иммунную патологию и диссеминированное внутрисосудистое свертывание.
СОЭ — скорость оседания эритроцитов представляет собою неспецифическую реакцию. В норме она составляет у мужчин до 50 лет — 2-15 мм в час, а у женщин до 50 лет — 2-20 мм в час. После 50 лет у мужчин до 20 мм в час, а у женщин — до 30 мм в час.
Быстрота агрегации эритроцитов зависит от их числа (при уменьшении их количества — ускоряется) и количества крупнодисперсных белков (белки воспаления, фибриноген, антитела, гамма-глобулин и др.), адсорбированных на эритроцитах и ускоряющих их оседание. Исходя из этого, понятен широкий спектр патологии, при которой может быть выявлено ускорение СОЭ.
Таким образом, анализ морфологического состава крови имеет огромное клиническое значение, а иногда является ведущим признаком в диагностике и выборе терапии многих болезней человека.
Однако следует помнить, что важнейшим звеном в таком анализе является интегральная оценка всех показателей крови и обязательное соотнесение имеющихся в крови изменений с анамнезом и клиническими проявлениями болезни.
Литература:
1. Руководство по гематологии под ред. А.И. Воробьева, Москва, 1985 г.
2. Hematology, ed. by W.S.Beck, London, 1991
3. Manual of Clinical Hematology, ed.by J.Mazza, N.Y.,1995
Теги: Лаборатория, Кровь
« Назад к списку статей Поделиться в