Что такое «агрегация тромбоцитов»
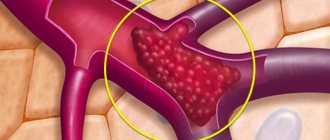
Тромбоциты представляют собой бесцветные кровяные клетки, функция которых — защита организма от кровопотерь. Когда ткани организма повреждаются, тромбоциты мгновенно устремляются к месту повреждения и блокируют его, предотвращая чрезмерную кровопотерю. Такая блокировка осуществляется за счет того, что тромбоциты мгновенно склеиваются между собой, образуют блок, который закрывает рану. Это процесс блокировки и называется агрегацией тромбоцитов. Процесс происходит в два этапа:
- Кровяные тельца слипаются между собой,
- Позже пристают к стенкам сосуда, образуется сгусток крови, тромб.
Когда организм здоров, эта функция носит защитный характер. Но если в организме пошли патологические изменения, образования тромбов способно нарушить питание в жизненно важных органах и тканях.
Индуцированная агрегация с АДФ
Описание Тромбоциты играют значимую роль в жизни человека: они предотвращают потерю крови, соединяясь друг с другом на стенке поврежденного сосуда. Этот процесс – склеивания тромбоцитов – и называется агрегацией. Важно, чтобы данный параметр не отклонялся от значений нормы, иначе это чревато кровопотерей или образованием тромба, способного перекрыть весь диаметр сосуда и привести к отмиранию тканей.
Важно, чтобы данный параметр не отклонялся от значений нормы, иначе это чревато кровопотерей или образованием тромба, способного перекрыть весь диаметр сосуда и привести к отмиранию тканей.
Агрегация тромбоцитов: что это такое?
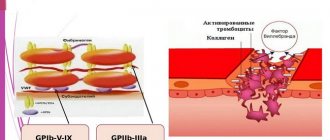
Процесс агрегации тромбоцитов в конгломераты состоит в следующем: при травме сосуда тромбоциты соединяются с фактором Виллебранда и коллагеном субэндотелиального слоя.
Агрегация тромбоцитов с коллагеном вызывает активацию красных клеток крови, причем они становятся источниками компонентов, стимулирующих агрегацию: тромбоксана и серотонина. Дезагрегация тромбоцитов – это обратный агрегации процесс.
Агрегация тромбоцитов – это защитная функция организма, но и она подвержена влиянию патологических реакций.
С одной стороны, агрегация тромбоцитов спасает нас от избыточной кровопотери, что актуально при хирургических операциях, обширных травмах и родах, с другой – гиперагрегация приводит к образованию тромба.
Тромбы очень опасны: их перемещения по кровеносной системе в сердце, головной мозг или легочную артерию могут привести к быстрой смерти. Исследование агрегации тромбоцитов учитывает их способность к соединению: при отклонениях выше нормы возможно появление инфаркта или инсульта, ниже нормы – кровопотеря, анемия, истощение.
Что такое агрегация тромбоцитов в крови? Чтобы определить значение агрегации тромбоцитов, надо сдать анализ крови из вены в пробирку, а в таком случае, когда нет раны, необходимо создать условия для объединения тромбоцитов в конгломерат.
Для этого в лаборатории внедряется индуцированная агрегация тромбоцитов.
Условия становятся максимально близкими к среде организма, в качестве индуктора агрегации тромбоцитов берутся вещества, идентичные по химическому составу человеческим, способные вызывать тромбообразование.
Индукторами могут быть:
- Серотонин.
- Коллаген.
- Адреналин.
- Арахидоновая кислота.
- Аденозиндифосфат (АДФ).
Способ измерения агрегации тромбоцитов заключается в пропускании света через плазму крови.
Различие между световой плотностью плазмы до момента свертывания крови и после образования сгустка и есть агрегационная активность тромбоцитов. Дополнительно определяют скорость агрегации тромбоцитов за 1 минуту, форму и тип волн.
Спонтанная агрегация тромбоцитов рассчитывается без использования индуктора.
Степень агрегации тромбоцитов:
- норма с АДФ – 30,7 – 77,7%
- с коллагеном – 46,4 — 93,1%
- с адреналином – 35 — 92,5%
Подготовка к сдаче анализа
Достоверная оценка результата может быть получена в случае соблюдения следующих условий: Не кушать за 12 часов до сдачи анализа. За день до забора крови не выполнять физические нагрузки и не испытывать эмоциональные потрясения.
За 7 дней до анализа остановить прием ряда лекарственных препаратов (если это невозможно, то сообщить об этом медсестре).
За день до анализа исключить алкоголь, курение, употребление чеснока и кофе. На сдачу крови приходить здоровым, без воспаления в организме.
Отклонение от нормы
Снижение агрегации тромбоцитов может происходить по следующим причинам:
- Наличием тромбоцитопатии.
- Лечением антиагрегантными средствами.
Тромбоцитопатия – заболевание, при котором нарушены функции тромбоцитов (свертываемость, тромбообразование). Проявляется болезнь наличием синяков, кровотечениями, что приводит впоследствии к малокровию.
Если агрегация тромбоцитов снижена, то назначается медикаментозное лечение, которое должен осуществлять квалифицированный специалист.
Повышенная агрегация тромбоцитов может быть при:
- Гипертонии.
- Атеросклерозе суставов.
- Инсульте и инфаркте.
- Сахарном диабете.
- Тромбозе.
Если агрегация тромбоцитов повышена, то не обойтись без консервативной терапии с применением антиагрегантных средств. Обязательно посещать врача для сдачи анализов и получения рекомендаций по лечению.
Во время беременности возможно отклонение от нормальных значений агрегации тромбоцитов.
Пониженный уровень говорит об опасности кровотечений, повышенный — проявляется при токсикозе в результате потери жидкости организмом и чреват выкидышем.
При беременности степень агрегации тромбоцитов: норма – 30-60% для любого индуктора. Анализ на агрегацию тромбоцитов назначается в случае осложненной беременности, плохого анамнеза и перед плановым зачатием.
К чему приводит нарушение агрегации тромбоцитов
Если процесс агрегации нарушен, это может привести к негативным последствиям. Так, если активность бесцветных кровяных клеток повышена, то это может привести к инсульту, инфаркту. А если выработка тромбоцитов понижена, то это может приводить к большой потере крови: человек страдает частыми кровотечениями, которые долго не прекращаются, приводят к истощению и анемии.
Именно для того, чтобы предотвратить эти последствия, проводится анализ агрегации тромбоцитов. Показанием к прохождению анализа являются:
- Частые кровотечения (носовые, маточные)
- Плохо заживающие раны.
- Синяки, которые появляются от малейшего ушиба.
- Постоянная отечность.
Для оценки тромбоцитарного компонента гемостаза подсчитывают число тромбоцитов в крови. Патология тромбоцитов является причиной кровоточивости почти в 80 % случаев. При этом тромбоцитопения – наиболее частое ее проявление. Констатировать тромбоцитопению следует в тех случаях, когда количество тромбоцитов составляет менее 150 × 109/л. Длительность кровотечения – важный скрининговый тест, основное достоинство которого состоит в том, что он позволяет одновременно качественно оценить количество тромбоцитов в крови, их адгезивные и агрегационные функции, функциональные свойства стенки кровеносных сосудов, а также выраженный дефицит плазменных факторов свертывания (например, факторов VIII и IX, недостаток которых является причиной гемофилии А и В). Удлинение времени кровотечения отражает нарушение гемостаза вследствие тромбоцитопений, тромбоцитопатий (нарушения функций тромбоцитов – адгезии и агрегации), нарушений сосудистой стенки или сочетания этих факторов. Удлинение времени кровотечения при нормальном количестве тромбоцитов в крови позволяет предположить нарушение их функций. В этом и состоит основная ценность теста, т.к. для оценки адгезивных и агрегационных свойств тромбоцитов в лабораторных условиях необходимо сложное и дорогое оборудование (агрегометр). Когда функции тромбоцитов не нарушены, время кровотечения остается в норме даже при снижении числа тромбоцитов до 100,0 x 109/л. При количестве тромбоцитов ниже этого уровня время кровотечения постепенно увеличивается в линейном соотношении с числом тромбоцитов. Спонтанные кровотечения возникают, если количество тромбоцитов становится ниже 50,0 x 109/л, смертельное кровотечение почти неизбежно, если количество тромбоцитов снижается до 5,0 x 109/л. Длительность кровотечения увеличивается при следующих состояниях:
- Выраженных тромбоцитопениях;
- Нарушении функции тромбоцитов – тромбоцитопатиях, которые бывают врожденными (синдром Бернара-Сулье) и приобретенными (пернициозная анемия, острый и хронический лейкоз, миеломная болезнь, длительный прием аспирина);
- Выраженном снижении плазменных факторов свертывания;
- При нарушении резистентности стенки капилляров (недостаток витамина С, дефектах сокращения капилляров – микроангиопатиях).
Укорочение времени кровотечения диагностического значения не имеет и чаще всего бывает следствием технической ошибки при проведении теста или свидетельствует о повышенной спастической способности капилляров. Оценить склонность к тромбообразованию по данным теста длительности кровотечения невозможно. Повышенное количество тромбоцитов в крови – тромбоцитоз, несет с собой риск повышения свертываемости и проявляется тромбозами. В клинических ситуациях риск тромбоза становится реальным, если количество тромбоцитов достигает значений 1000,0 x 109/л.
Исследование агрегационных функций тромбоцитов Процессы агрегации изучают с помощью агрегометра, отражающего ход агрегации графически в виде кривой; в качестве стимулятора агрегации часто используют АДФ, адреналин и коллаген.
Нарушения агрегации тромбоцитов при различных заболеваниях (по результатам исследований на агрегометре)
| Вид тромбоцитопатий | Стимулятор агрегации и нарушения агрегации | ||||
| АДФ | коллаген | адреналин | ристоцетин | ||
| первичная волна | вторичная волна | ||||
| Тромбастения | Патология | Патология | Патология | Патология | Норма |
| Эссенциальная атромбия | Патология | Патология | Патология | Патология | Норма |
| Аспириноподобный дефект | Норма | Патология | Патология | Патология | Норма |
| Синдром Бернара-Сулье | Норма | Норма | (+,-) | (+,-) | Норма |
| Синдром Вискота-Олдрича | Патология | Патология | Патология | Патология | Норма |
| Болезнь Виллебранда | Норма | Норма | Норма | Норма | Сниженная патологическая |
Примечание: (+,-) – диагностического значения не имеет.
Патология тромбоцитов является причиной кровоточивости почти в 80 % случаев. При этом тромбоцитопения – наиболее частое ее проявление. Констатировать тромбоцитопению следует в тех случаях, когда количество тромбоцитов составляет менее 150 × 109/л. Различают острую и хроническую тромбоцитопению. Последняя диагностируется тогда, когда продолжительность ее превышает 6 мес. У лиц с уровнем тромбоцитов выше 50×109/л редко наблюдается кровоточивость. Тем ни менее, снижение тромбоцитов ниже 100×109/л может сопровождать серьезную патологию. В связи с этим причину каждого случая тромбоцитопении необходимо выяснять. При тромбоцитопениях, тяжелых тромбоцитопатиях и при дефиците фактора Виллебранда (ФВ) значительно удлиняется время кровотечения. Кровоточивость связана с недостаточностью адгезивно-агрегационной функции тромбоцитов – нарушением образования в поврежденных сосудах тромбоцитарной пробки. Это может быть обусловлено либо значительным снижением количества тромбоцитов в крови, либо их дисфункцией, в основе которой чаще всего лежит отсутствие или блокада на мембране тромбоцитов рецепторов, взаимодействующих со стимуляторами (агонистами) агрегации этих клеток (ФВ, адреналином, АДФ, фибриногеном, арахидоновой кислотой и простагландинами), либо отсутствием в тромбоцитах или нарушением выхода из них компонентов гранул, содержащих эти стимуляторы агрегации. Современные гематологические анализаторы выводят тромбоцитометрические кривые (гистограммы распределения тромбоцитов по объему). Отмечается связь размера тромбоцитов с их функциональной активностью, содержанием в гранулах тромбоцитов биологически активных веществ, склонностью клеток к адгезии, изменениями объема тромбоцитов перед агрегацией. Наличие в крови преимущественно молодых форм тромбоцитов приводит к сдвигу гистограммы вправо, старые клетки располагаются в гистограмме слева, так как, по мере старения тромбоцитов их объем уменьшается. Увеличение содержания юных форм тромбоцитов наблюдается при кровопотере и свидетельствует об усиленной регенерации. Увеличение содержания старых форм, вакуолизированных тромбоцитов, форм раздражения и уменьшение содержания зрелых тромбоцитов, характерны для различных воспалительных процессов, интоксикаций, злокачественных новообразований.
Тромбомодулин – интегральный мембранный белок, рецептор тромбина, находящийся на клетках эндотелия кровеносных сосудов и участвующий в системе антикоагуляции. Он определяет скорость и направление процесса гемостаза, активно ограничивает и регулирует свёртывание крови. Эндотелий, образуя тромбомодулин, блокирует активные коагулянты, выделяющиеся печенью и находящиеся в плазме крови, в первую очередь — самый активный фактор свертывания — тромбин. Связанный тромбин исключается из системы свёртывания крови. Тромбин, присоединившись к тромбомодулину, приобретает новые качества: образует вместе с противосвертывающими протеинами С и S (кофактор протеина S) антиагрегантный и антитромботический комплекс, который препятствует свертыванию и тормозит фибринолиз. Таким образом система тромбомодулин-протеин С выполняет антикоагулянтную функцию. Более того, модифицированный при взаимодействии с тромбомодулином, тромбин, теряет способность превращать фибриноген в фибрин и вызывать агрегацию тромбоцитов. При повреждении сосудистой стенки тромбомодулин «отделяется» от эндотелия и поступает в кровь. Увеличение его в крови наблюдается у больных с претромботическими состояниями, васкулитами и т.д. Степень увеличения тромбомодулина в крови имеет диагностическое и прогностическое значение. Тромбомодулин значительно снижен при некоторых заболеваниях, таких как атеросклероз, что может увеличивать свёртываемость крови и повышать риск тромбоза.
Фактор Виллебранда – сложный мультимерный адгезивный гликопротеин, носитель-стабилизатор прокоагулянтного протеина F VIII:C, который является белком адгезии в процессах гемостаза. Фактор Виллебранда может связывать коллаген и, возможно, другие эндотелиальные структуры и опосредует адгезию тромбоцитов к субэндотелию через связывание поверхностного рецептора тромбоцитов гликопротеина Ib. Адгезия тромбоцитов, опосредованная Фактором Виллебранда, происходит наиболее интенсивно при высоких скоростях сдвига, т.е. в артериях. VIII-vWF является также носителем F VIII – антигемофильного глобулина А. Фактор Виллебранда у здоровых людей предотвращает рост тромба в сосудах, активируя образования плазмина. Повышенные уровни активности Фактора Виллебранда являются индикатором повреждения эндотелия при сосудистых заболеваниях, что может быть существенно для гипертензионных сосудистых осложнений. Болезнь фон Виллебранда – врождённый геморрагический диатез. В легкой форме эта болезнь является самым частым геморрагическим нарушением у мужчин, с частотой 1:100. Это заболевание гетерогенной природы, вызываемое либо дефектами структуры белка, либо снижением концентрации Фактора Виллебранда. Классификация заболевания основана на клинической картине, анамнезе и результатах лабораторного анализа, включая время свёртывания и определение антигена и активности Фактора Виллебранда. Определение уровня Фактора Виллебранда помогает в дифференциальном диагнозе двух основных типов заболевания: типа 1 и типа 2. Определение типа болезни принципиально, так как от этого зависит выбор тактики ведения больного.
Фибронектин является рецептором для фибринстабилизирующего фактора. Способствует адгезии тромбоцитов, участвуя в образовании белого тромба; связывает гепарин. Присоединяясь к фибрину, фибронектин уплотняет тромб. Под действием фибронектина клетки гладких мышц, эпителиоцитов, фибробластов повышают свою чувствительность к факторам роста, что может вызвать утолщение мышечной стенки сосудов (сужение диаметра).
Расшифровка анализа на агрегацию тромбоцитов
В анализе на агрегацию тромбоцитов о хорошем кроветворении говорят показатели 25 – 75%. Это значит, что ткани и органы нормально снабжаются кислородом, и тромбы отсутствуют.
Норма тромбоцитов
| Возраст | Показатель, х 10^9/л |
| Новорождённый | 100–420 |
| Ребёнок до года | 160–320 |
| 1–4 года | 150–300 |
| 15–18 лет | 180–340 |
| Мужчины старше 18 лет | 180–400 |
| Женщины старше 18 лет | 150–380 |
Нарушения в системе гемостаза и его коррекция у беременных с метаболическим синдромом
Частота метаболического синдрома по данным различных авторов составляет 5–20% (I. Despres, A. Marette, 1994). Следует отметить, что ожирение входит в число основных компонентов метаболического синдрома, а число женщин с ожирением, включая беременных, прогрессивно возрастает.
Имеется значительное число работ, посвященных влиянию ожирения на течение беременности и родов. Однако единичные исследования посвящены изучению некоторых метаболических показателей. Так, Г. А. Чернуха (1987) показала нарушение гормонального профиля в системе гемостаза и липидного обмена у беременных с ожирением. В. Н. Серов с соавт. (2000) отметили у беременных с ожирением и дефицитом массы тела изменения метаболических процессов, в частности гипо- и дислипидемию, снижение толерантности к глюкозе.
Важным компонентом у беременных с метаболическим синдромом является нарушение кровотока в системе матери, обусловленное ожирением, нарушенной плацентарной недостаточностью, измененный гормональный профиль: повышенный уровень лептина, измененный инсулиновый коэффициент и измененный водно-электролитный баланс.
Однако в доступной нам литературе мы не нашли работ, которые бы связывали ожирение у беременных с наличием у них метаболического синдрома.
Целью нашего исследования было изучить изменения в системе гемостаза, частоту метаболического синдрома и его коррекцию у беременных с метаболическим синдромом и определить влияние этих изменений на течение беременности и родов.
Была поставлена задача выяснить патофизиологический механизм развития гиперкоагуляции крови и повреждения эндотелия у беременных женщин с метаболическим синдромом. В исследования были включены 43 беременных с метаболическим синдромом в возрасте от 27 до 37 лет в III триместре беременности, в том числе 8 беременных, у которых развился гестоз средней степени тяжести. В качестве контроля наблюдалось 15 здоровых беременных аналогичного срока беременности. Всем беременным проведено клиническое обследование с включением перорального нагрузочного теста на толерантность к глюкозе. Критериями включения беременных основной группы были: артериальная гипертезия, висцеральное ожирение, гиперинсулинемия и гипергликемия.
Лабораторные исследования
Кровь брали из локтевой вены натощак с добавлением антикоагулянта 0,6% раствора этилендиаминтетрауксусной кислоты (ЭДТА). Определяли уровень фибриногена, антитромбина III (АТ III), толерантность плазмы к гепарину, фибринолитическую активность крови, содержание тромбоксана В2, цАМФ в тромбоцитах и простациклинах. Количественные показатели агрегации тромбоцитов оценивали по спонтанной агрегации индуцированной аденозиндифосфатом (АДФ) и коллагеном, определяли инсулин крови. Для определения агрегации тромбоцитов брали кровь в пробирки, содержащие 3,8% раствор цитрата натрия в разведении 9:1. Оценку количественных характеристик скорости и интенсивность агрегации проводили на автоматическом двухканальном лазерном анализаторе агрегации с применением программного обеспечения.
Для исследования спонтанной агрегации тромбоцитов анализировали агрегационную кривую, записанную в течение 10 минут без индуктуров. В качестве индуктора агрегации использовали раствор АДФ в концентрациях 1×10-5 М, % и 1×10-7 М, %, коллаген, фактор активации тромбоцитов, адреналин 10-4 М, аггристин. Протокол исследования агрегации тромбоцитов в богатой тромбоцитами плазме включал измерение максимальной скорости агрегации в процентах. NO определялось с помощью методики определения нитритов NO2 и нитратов как продуктов метаболизма оксида азота в сыворотке крови человека методом высокоэффективной жидкостной хромотографии на приборе Shimatsu. Сыворотка крови замораживалась и хранилась при температуре -70 градусов. При проведении анализа сыворотку размораживали, разводили эквалентным количеством, буфер и белки удаляли фильтрованием через фильтр UltraFree Units на центрифуге при 5 тысячах оборотов в минуту в течение 15 минут. Количественный анализ проводили при сравнении с внешним стандартом при длине волны 214 нм с последующим учетом разведения.
Результаты исследования
Физиологическая беременность сопровождается значительными изменениями в системе гемостаза. Для решения вопроса о развитии гиперкоагуляции крови в условиях осложненной беременности мы провели исследование системы гемостаза и функциональной активности крови у беременных основной и контрольной группы. Из табл. 1 видно, что в контрольной группе уровень фибриногена 2,36, а в основной группе 3,74, толерантность плазмы к гепарину в контрольной группе равна 948,0, а в основной группе 724,0. Очень важным показателям является уровень АТ III. В контрольной группе он составляет 37,6, а в основной группе — 27,3. Увеличение уровня фибриногена в основной группе является одним из важных звеньев нарушения микроциркуляции, которая сопровождается блокадой транспорта веществ, в частности нарушения доставки к плоду кислорода, глюкозы, липидов, белков. Нарушение проницаемости мембран сопровождается при этом изменением характера окислительных процессов, в частности повышением уровня анаэробного окисления, развитием ишемических и дистрофических изменений в тканях плода.
Клинически это проявляется снижением веса плода, асфиксией его. Большую опасность развития тромбозов во время беременности представляет собой сочетание высокого уровня фибриногена и сниженного показателя АТ III. Известно, что антикоагулянтная активность крови обеспечивается целым рядом биохимических факторов. Одним из наиболее активных антикоагулянтов является плазменный кофактор гепарина АТ III. Он является универсальным ингибитором почти всех ферментных факторов свертывания крови (особенно тромбина и фактора Ха). Критическое снижение уровня АТ III у беременных в основной группе вызывает преэкламптическое состояние. Сопоставляя количественные показатели агрегации тромбоцитов у здоровых женщин и у беременных с метаболическим синдромом, мы отметили существенные различия. С чем связаны эти изменения? Важную роль играют изменения физико-химических свойств тромбоцитов в условиях беременности и инсулинорезистентности.
Возникающая ишемия в органах и тканях нарушает энергетический потенциал тромбоцитов с развитием деполимеризации мембраны, соответствующей потерей клеткой одной из форм «свободной энергии», т. е. энергии трансмембранного потенциала. Агрегация тромбоцитов у больных с метаболическим синдромом, индуцированная АДФ, значительно повышается — до 79,1% (у здоровых лиц 61,0%). Достоверно повышается агрегация тромбоцитов, стимулированная коллагеном — до 69,0% (у здоровых лиц 57,0%). Коллаген-индуцированная агрегация очень важна, так как в случае незначительного морфологического изменения стенки сосуда возникают условия для образования внутрисосудистого тромбоцитарного тромба.
Повреждение эндотелия с обнажением коллагена является важным пусковым фактором агрегации тромбоцитов. При метаболическом синдроме у беременных значительно изменяется агрегация тромбоцитов под влиянием адреналина. Если у здоровых женщин с физиологической беременностью она составляет 13,4%, то при метаболическом синдроме она повышается до 30,2%. Адреналин-индуцированная агрегация тромбоцитов у беременных с метаболическим синдромом свидетельствует о резком повышении чувствительности рецепторного аппарата тромбоцитов к адреналину.
Из этого следует, что даже незначительные эмоциональные стрессы, умеренная физическая нагрузка могут провоцировать активацию агрегации тромбоцитов с возможным прогрессированием до развития преэкламптического состояния. Патофизиологической основой изменения агрегации тромбоцитов при гестозе является нарушение активности цАМФ клетки. Именно высокий уровень цАМФ тромбоцитов позволяет ему сохранить функциональную жизнеспособность: обмен веществ, энергии и обмен информации.
У беременных контрольной группы уровень цАМФ тромбоцитов составляет 4,1 пмоль (3×108 клеток), у женщин с метаболическим синдромом уровень цАМФ снижается до 3,0 пмоль (3×108 клеток). Гестоз характеризуется повышенным уровнем фибронектина, который постоянно взаимодействует с тромбоцитами. В норме его содержание составляет 4 мг × 109 клеток. В тромбоцитах он ассоциируется с альфа-гранулами и высвобождается из них после стимуляции тромбином или коллагеном, способствуя адгезии клеток коллагеном. Это играет важную роль при активации гемостатического процесса. Также при гестозе обнаруживается низкое содержание АТ III, на долю которого приходится около 80% всей первичной антикоагулянтной активности крови.
У беременных с гестозом обнаруживались высокие титры бета-тромбоглобулина и фактора IV тромбоцитов. Важную роль в предупреждении развития избыточной коагуляции крови при беременности клиницисты придают состоянию эндотелия. Антитромбогенные свойства стенки сосудов обеспечиваются воздействием целого ряда компонентов: 1) простациклина, являющегося ингибитором агрегации тромбоцитов и обеспечивающего выраженный эффект вазодилятации; 2) антикоагулянтов (АТ III и альфа-2 макроглобулин); 3) проактиватора плазминогена, вырабатывающегося в сосудах; 4) тромбомодулина, образующегося на поверхности эндотелиальных клеток. У здоровых лиц тромбоциты не прилипают к неповрежденному эндотелию. При повреждении же эндотелия тромбоциты легко прилипают к субэндотелию, что обусловлено снижением содержания глюкозоаминогликанов и простациклина, синтезируемого эндотелием. Уровень простациклина у здоровых лиц при беременности составляет 65,0 пг/мл, у беременных с метаболическим синдромом он снижается до 51,0 пг/мл.
Открытие продукции NO эндотелиальными клетками в 80-е годы еще раз подтвердило огромное морфофункциональное значение эндотелия, который ранее рассматривался как пассивная разделительная поверхность между кровью и экстравазальным пространством. NO обладает множеством функций, среди которых главными является поддержание нормальной функции сосудов и полноценная адаптация кардиоваскулярной системы к беременности. NO обладает вазодилятирующей антиагрегантной активностью, а также является ингибитором митогенеза.
Для выяснения значимости уровня NO у беременных в развитии гиперкоагуляции крови мы сопоставили его количественные показатели у беременных основной и контрольной группы. У лиц контрольной группы уровень NO составляет 23,2, а у лиц основной группы величина его снижается до 21,16. При этом очень важно отметить, что уровень NO повышается только через 6 месяцев после родов до 25,57. Это свидетельствует о том, что нарушение эндотелиальной функции обусловлено именно беременностью. У больных с гестозом происходит значительное повреждение эндотелия, увеличивается гипоксия и циркуляция свободных радикалов, а также агрессивных форм кислорода. При этом NO расходуется на связывание свободных радикалов, в результате чего страдает одна из важных его функций — вазодилятирующая и антиагрегантная.
Уровень АТ III значительно снижен, и это дает возможность увеличивать тромботическую активность крови (табл. 1). К этому же добавляется и снижение фибринолитической активности крови: если у контрольной группы она составляет 20,3%, то при метаболическом синдроме она снижается до 11,2%. Особую значимость приобретает повышение чувствительности тромбоцитов к различным агрегантам (коллагену, адреналину и АДФ), что при различных видах патологии, например гестозе, может приводить к тромботическим осложнениям. Имеет также важное значение сниженный у беременных с метаболическим синдромом цАМФ в тромбоцитах до 3×108 клеток пмоль, в то время как у лиц контрольной группы этот показатель составляет 4,1×108 клеток пмоль.
Важное значение в вопросах тромбоцитарной активности имеет сниженный уровень простоциклина (6-кето-PGF1-альфа в плазме — пг/мл), если у лиц контрольной группы выработка простоциклина составляет 65 пг/мл, то у беременных с метаболическим синдромом уровень простоциклина снижен до 51 пг/мл. Увеличивается в крови фактор Виллебранда, у беременных с метаболическим синдромом он составляет 2,18 ед/мл, а у лиц контрольной группы 1,04 ед/мл, усиливая таким образом агрегационную способность тромбоцитов. Таким образом, сочетанное воздействие высокого уровня фибриногена и увеличение агрегационной активности тромбоцитов, сочетающееся со сниженными такими показателями, как АТ III и простациклин, способствуют развитию тромбогеморрагического синдрома у беременных с метаболическим синдромом и является одним из пусковым механизмом присоединения гестоза.
С целью снижения перинатального риска и частоты возникновения других осложнений беременности у ряда больных метаболическим синдромом проводилась комплексная терапия, которая включала в себя:
- гипохлоридную белковую диету с включением продуктов, богатых «естественными» антиоксидантами (чернослив, изюм, черника, черная смородина);
- один из препаратов группы «синтетических» антиоксидантов: витамин Е (300 мг/сут), аскорбиновая кислота (100 мг/сут), глутаминовая кислота (3 г/сут);
- препараты группы мембранстабилизаторов, содержащие полиненасыщенные жирные кислоты: Эссенциале форте H по 2 капсулы — 3 раза, Липостабил по 2 капсулы — 3 раза и пищевую добавку Эйконол по 1 капсуле 1–2 раза в день;
- антикоагулянтную терапию (Фраксипарин 0,3 или 0,6 мл/сутки п/к в зависимости от показателей гемостазиограммы);
- антиагрегантную терапию — Кардиомагнил 75 мг/сут.
Больным проводилось лечение Кардиомагнилом 75 мг — 1 раз в день и Фраксипарином 0,3–1, 2 раза в день. В основе механизма действия ацетилсалициловой кислоты лежит необратимое ингибирование фермента циклооксигеназы (ЦОГ-1), в результате чего блокируется синтез тромбоксана А2 и подавляется агрегация тромбоцитов. Фраксипарин проявляет высокую способность к связыванию с белком плазмы крови AT III. Это связывание приводит к ускоренному ингибированию фактора Ха, чем и обусловлен высокий антитромботический потенциал надропарина. Антитромботический эффект надропарина включает активацию ингибитора превращения тканевого фактора (TFPI), активацию фибринолиза посредством прямого высвобождения активатора тканевого плазминогена из эндотелиальных клеток и модификацию реологических свойств крови (снижение вязкости крови и увеличение проницаемости мембран тромбоцитов и гранулоцитов). Надропарин кальций характеризуется более высокой анти-Ха-факторной активностью по сравнению с анти-IIa-факторной или антитромботической активностью и обладает как немедленной, так и продленной антитромботической активностью.
На фоне проводимого лечения отмечается улучшение состояния беременных и снижение показателей, представленных на гемостазиограмме, а также улучшение биохимических показателей у беременных с метаболическим синдромом на фоне проведенной терапии (табл. 2).
Таким образом, функциональная активность эндотелия при беременности (особенно при гестозе) резко нарушается. Оксидативный стресс во время беременности, особенно у женщин с метаболическим синдромом, стимулирует выработку эндотелина с соответствующим развитием гипертензии. Следовательно, дисфункция эндотелиальных клеток стимулирует выброс эндотелина, тромбоксана, ангиотензина II, тормозит продукцию оксида азота и приводит к ишемии плаценты, присоединению гестоза (табл. 1).
Исход беременности и родов прослежен у 58 женщин, поступивших в отделение патологии беременных родильного дома ГКБ № 70 г. Москвы. Контрольную группу составили данные течения беременности и родов у 15 женщин с метаболическим синдромом.
Анализ течения беременности у женщин с метаболическим синдромом свидетельствует о том, что беременность часто протекает с различными осложнениями, представленными в табл. 3.
Значительный интерес представляет анализ течения родов у женщин с метаболическим синдромом. Данные представлены в табл. 4.
Характерной особенностью течения родов у женщин с метаболическим синдромом является несвоевременное излитие околоплодных вод, аномалии родовой деятельности, крупный плод и кровотечение в третьем периоде родов.
Так, у рожениц с метаболическим синдромом средняя величина кровотечения составила 600–900 мл (у одной роженицы из этой группы кровотечение составило 1100 мл). Во всех случаях обеспечивалось использование консервативных методов лечения.
Высокий процент кровотечений у рожениц с метаболическим синдромом возможно объяснить нарушением сократительной способности матки, о чем свидетельствует значительная частота аномалии родовой деятельности.
Особый интерес заслуживает частота оперативного родоразрешения у женщин с метаболическим синдромом. Если по родильному дому № 70 частота кесарева сечения составляет по годам 22–23%, то у женщин в нашем исследовании она составила 33,6%.
Показаниями для операции кесарева сечения были: клинически узкий таз, тяжелая форма гестоза, упорная слабость родовой деятельности, не поддающаяся медикаментозной коррекции.
Таким образом, частота метаболического синдрома у женщин с ожирением составила 89,2%. Метаболический синдром неблагоприятно отражается на течении беременности и родов, что является причиной значительного увеличения частоты оперативных вмешательств, особенно родоразрешения путем операции кесарева сечения. Проведенный анализ дает основания относить беременных с метаболическим синдромом к группе высокого риска по развитию гестоза и осложнения течения родов.
Выводы
- Метаболические изменения у женщин во время беременности (повышение уровня артериального давления, гипергликемия, инсулинорезистентность) создают угрозу развития гестоза.
- В патогенезе ДВС-синдрома (диссеминированного внутрисосудистого свертывания) у беременных с метаболическим синдромом играют роль повреждение эндотелия сосудов, повышение агрегации тромбоцитов и нарушение реологических свойств крови.
- Для лечения ДВС-синдрома у беременных с метаболическим синдромом в состав комплексной терапии необходимо включать антиагреганты и антикоагулянты. Проведение комплексной терапии с включением антиагрегантов и антикоагулянтов является патогенетически обоснованной профилактикой присоединения гестоза и позволяет не допустить или отсрочить присоединение гестоза и значительно улучшить исходы беременности и родов.
Литература
- Архипов В. В., Каюпова Г. Ф., Саматова 3. А. Течение беременности и родов, состояние плода и новорожденного у женщин с ожирением // Здравоохр. Башкортостан. 1999, № 3, с. 33–34.
- Беловицкая Н. Состояние тромбоцитарно-сосудистого звена системы гемостаза у больных ИНСД с ИБС. М., 1990, с. 144.
- Бутрова С. А. Метаболический синдром: патогенез, клиника, диагностика, подходы к лечению // Рус. мед. журн. 2001, 2, 56–60.
- Василенко А. Изменение тромбоцитарного и прокоагулянтного звеньев гемостаза у больных с артериальной гипертензией // Врачебное дело. 1992, № 8, с. 65–66.
- Гинзбург М. М., Козупица Ч. С., Крюков Н. Н. Ожирение и метаболический синдром. М., 2000, с. 14–15.
- Мамедов М. Н. Клинико-биохимические особенности и пути медикаментозной коррекции метаболического синдрома. Дисс. д.м.н. М., 2001.
- Чазова И. Е., Мычка В. Б. Метаболический синдром. 2004, с. 9.
- Чернуха Г. Е. Клиническое значение нарушений показателей гомеостаза у беременных с ожирением. Дисс. к.м.н. М., 1987.
- Bernardi F., Marcheti G., Pinotti M., Arcieri P. Factor VII gene Polymorphisms Contribute About One Third of the Factor VII Level Variation in Plasma // Atherosclerosis, Thrombosis and vascular Biology. 1996, v. 16, № 1, 72–78.
- Bray G. A. Obesity. Part I. Pathogenesis//West J. Med. 1988, v. 194, № 4, p. 429–441.
- Despres J. P. The impact of overstate on the multifactorial risk profile of abdominally obese patients // Diabetes, 1998, 48, 1, 307.
- Edwards L. E., Hellerstedt W. L., Alton I. R. et al. Pregnancy compactions and birth outcomes in obese and normal-weight woman: effects of gestational weight change// Obstet. Gynec. 1996, № 87 (3), p. 389–394.
- Galtier-Derenze F., Bringer Y. Maternal overweight and pregnancy // Diabetes Metab. 1997, v. 23, № 6, p. 192–195.
- Goldenberg R. L., Tamura T. Pregnancy weight and pregnancy outcome // JAMA. 1996, № 275 (14), p. 1127–1128.
- Stico-Rahm A., Niman В., Hamsten A., Nilsson Y. Secretion of plasminogen activator inhibitor 1 from cultudef human umbilical vein endotelian cells is included by very low density lipoprotein // Atherosclerosis. 1990, 10:1067–1073.
Е. И. Соколов, доктор медицинских наук, профессор, академик РАМН И. Б. Манухин, доктор медицинских наук, профессор А. А. Мочалов О. Б. Невзоров, доктор медицинских наук, доцент
МГМСУ, Москва
Контактная информация об авторах для переписки
Использованная литература
- Клиническая лабораторная диагностика, Национальное руководство, Том 1, Долгов В.В., Меньшиков В.В., 2012, стр 761-765
- Козловский В. И., Ковтун О. М., Сероухова О. П., Детковская И. Н., Козловский И. В. Методы исследования и клиническое значение агрегации тромбоцитов. Фокус на спонтанную агрегацию // Вестник ВГМУ. 2013. №4.
- Puri RN, Colman RW.ADP-induced platelet activation.Crit Rev BiochemMol Biol. 1997;32(6):437-502. doi: 10.3109/10409239709082000. PMID: 9444477.
- Murugappa S, Kunapuli SP. The role of ADP receptors in platelet function.FrontBiosci. 2006 May 1;11:1977-86. doi: 10.2741/1939. PMID: 16368572.
- Barbara Lunghi, Anna Lecchi, Rosa Santacroce, Mariangela Scavone, Rita Paniccia, Andrea Artoni, Christian Gachet, Giancarlo Castaman, Maurizio Margaglione, Francesco Bernardi, Marco Cattaneo. Severe bleeding and absent ADP-induced platelet aggregation associated with inherited combined CalDAG-GEFI and P2Y12 deficiencies.Haematologica 2020;105(7):e361-e364
Тромбоцитарный гемостаз
Исследование агрегационной способности тромбоцитов
Обследование пациентов с кровотечением требует тщательного анамнеза, в том числе семейного, сведений о приеме лекарственных препаратов, физикального обследования, и только после этого лабораторного исследования.
Количественные и функциональные нарушения тромбоцитов часто встречаются у пациентов с кровотечениями.
Типы нарушений функции тромбоцитов:
| Нарушение функции тромбоцитов | Вероятный диагноз |
| Нарушение адгезивной функции тромбоцитов | Синдром Бернара-Сулье Велокардиофасциальный синдром Тромбастения Гланцманна Врожденная афибриногенемия Болезнь фон Виллебранда (возможно — тромбоцитарный тип болезни фон Виллебранда) Дефекты рецепторов коллагена |
| Аномалии тромбоцитарных рецепторов | Дефекты рецепторов TxA2 Дефект α-адренергических рецепторов Дефект P2Y12 рецепторов Антитромбоцитарные препараты (например, клопидогрель) |
| Аномалии тромбоцитарных гранул | Дефицит плотных гранул — дефицит α-гранул — синдром серых тромбоцитов |
| Аномалии секреции содержимого гранул тромбоцитов, либо нарушение передачи сигнала в тромбоцитах | Первичные дефекты секреции Дефекты агрегации, которые аналогичны тем, которые наблюдаются при расстройствах пула хранения тромбоцитов, но с нормальным содержанием гранул и ТхА2 Дефекты агонистов рецепторов на поверхности тромбоцитов — адреналина — тромбоксана — АДФ — коллагена Дефекты в активации белка G (дефекты внутриклеточной передачи сигнала) |
| Нарушение метаболизма арахидоновой кислоты | Дефекты циклооксигеназы Дефицит тромбоксансинтазы Прием наркотических препаратов |
| Нарушение прокоагулянтного механизма тромбоцитов | Синдром Скотта |
| Дефекты цитоскелета тромбоцитов | Расстройства, связанные с MYH9 Синдром Вискотта-Олдрича |
До проведения специфических анализов, исследующих функциональные свойства тромбоцитов, рекомендуется выполнить следующие лабораторные тесты:
- Общий анализ крови с определения количества тромбоцитов и среднего объема тромбоцитов. Это имеет значение при наследственной макротромбоцитопении (синдроме Бернара-Сулье), микротромбоцитопении (синдроме Вискотта-Олдрича), при некоторых заболеваниях костного мозга.
- Изучение мазка крови и морфологии тромбоцитов. Необходимо для установления таких диагнозов, как псевдотромбоцитопения, синдром серых тромбоцитов. В некоторых случаях, например, при тромбоцитопении Хегглина мазок крови может показать наличие телец Деле (светло-серо-голубых овальных базофильных лейкоцитарных включений, расположенных в периферической цитоплазме нейтрофилов).
Специфические лабораторные тесты для определения функциональных свойств тромбоцитов включают в себя такие обследования как:
— скрининговые тесты, отражающие функциональную активность тромбоцитов, например, активированное время свертывания (АСТ), время кровотечения (ВК) и PFA-100, — агрегометрия например, классическая агрегометрия по Борну, — проточная цитометрия для количественной оценки наличия или отсутствия мембранных гликопротеинов тромбоцитов, — специализированные исследования, применяемые в научно-исследовательских лабораториях.
Принцип метода агрегатометрии по Борну:
Метод измерения агрегации тромбоцитов турбидиметрическим методом по Born (по Борну) основан на регистрации изменений светопропускания в суспензии тромбоцитов. Эти изменения обусловлены снижением светорассеивания и увеличением светопропускания (прозрачности) суспензии в процессе образования тромбоцитарных агрегатов.
В классической агрегометрии по Борну используется плазма, богатая тромбоцитами (БТП). В агрегометре БТП перемешивается в кювете при температуре 37°С. При добавлении агониста образующиеся агрегаты тромбоцитов поглощают меньше света, что регистрируется фотоэлементом.
ОТП – обедненная тромбоцитами плазма, БТП – богатая тромбоцитами плазма.
Наглядно принципы агрегометрии по Борну можно увидеть на анимационной англоязычной презентации, любезно предоставленной авторами научного сайта https://www.platelet-research.org — https://www.platelet-research.org/3/aggregometry.htm.
Преаналитическая вариабельность
Препараты, блокирующие функции тромбоцитов, включают в себя НПВП (нестероидные противовоспалительные препараты), специфические антитромбоцитарные препараты, такие как клопидогрель, а также некоторые антибиотики, антидепрессанты, бета-блокаторы и пр. На функцию тромбоцитов могут влиять также такие продукты, как чеснок, куркума и кофеин, продукты с высоким содержанием жиров (они могут привести к появлению хиломикронов в плазме, что препятствует нормальному светопропусканию в процессе проведения тестирования агрегации тромбоцитов). Ряд факторов может влиять на правильность результатов агрегации тромбоцитов:
— очень высокое или низкое количество тромбоцитов;
— температура — образцы крови для тестирования агрегации тромбоцитов следует хранить при комнатной температуре;
— рН — агрегацию тромбоцитов следует проводить при физиологическом значении рН;
— концентрация фибриногена.
Агонисты тромбоцитов:
Добавление агониста тромбоцитов к ОТП приводит к активации тромбоцитов, изменению их формы от дискоидной до сферической, которая связана с увеличением оптической плотности в процессе активации тромбоцитов. Единственным исключением из этого являются адреналин (эпинефрин), который не приводит к изменению формы тромбоцитов, и ристоцетин, который вызывает не агрегацию, а агглютинацию тромбоцитов.
Существуют два типа агонистов:
— сильные агонисты — коллаген, тромбин, ТхА2, арахидоновая кислота — непосредственно вызывают агрегацию тромбоцитов, синтез и секрецию ТхА2 гранул тромбоцитов.
— слабые агонисты — АДФ и адреналин — вызывают агрегацию тромбоцитов, не вызывая секреции.
Сильные агонисты при низких концентрациях могут действовать как слабые агонисты, но слабые агонисты, даже при высоких концентрациях, не будут действовать в качестве сильных агонистов.
С некоторыми слабыми агонистами (АДФ и адреналин) кривая агрегации тромбоцитов может иметь двухфазный вид — начальную волну агрегации (первичную волну), а затем вторичную волну агрегации, которая, как правило, необратима. При более высоких концентрациях АДФ две волны агрегации сливаются и двухфазный сигнал отсутствует.
Реакция агрегации к агонисту усиливается при высвобождении ТхА2 из фосфолипидов мембран и секреции АДФ из плотных гранул. АДФ и ТхА2 являются агонистами, которые, взаимодействуя с их специфическими рецепторами, усиливают реакцию агрегации тромбоцитов.
Рабочие концентрации используемых агонистов и механизм их действия:
| Агонист | Рабочая концентрация (С) | Механизм действия |
| АДФ | Низкая –1.0 μM, 2.5 μM, 5.0 μM Высокая – 10.0 μM | АДФ связывается со своим рецептором на поверхности тромбоцитов. Первоначальное связывание приводит к высвобождению внутриклеточного кальция и изменению формы тромбоцита, ведущее к образованию первичной волны агрегации. Вторичная волна отражает высвобождение АДФ из гранул хранения тромбоцитов. Низкая доза АДФ вызывает лишь первичную агрегацию и ее эффект является обратимым. АДФ связывается с двумя G-белками рецепторов P2Y1 и P2Y12. Связывание АДФ с рецептором P2Y1 вызывает изменение формы и инициирует агрегацию тромбоцитов (первичную волну) за счет мобилизации кальция. Рецептор P2Y12 считается основным АДФ-рецептором и ответственным за полную агрегацию тромбоцитов через ингибирование аденилциклазы. Рецептор P2Y12 является также мишенью для клопидогреля. Вторая волна АДФ-индуцированной агрегации подавляется аспирином и НПВС. |
| Адреналин | 5 μM, 10μM | Адреналин связывается с α2-адренергическим рецептором на поверхности тромбоцитов, что приводит к ингибированию аденилциклазы и высвобождению ионов кальция. Агрегация тромбоцитов с адреналином визуально аналогична агрегации с АДФ с наличием начальной первичной волной агрегации, высвобождением сохраненного АДФ из тромбоцитов и второй волной необратимой агрегации. Как и с АДФ, эта вторая волна агрегации подавляется аспирином и НПВС. Адреналин, как и АДФ считается слабым агонистом. |
| Ристоцетин | Низкая –0.5 mg/mL Высокая –1.5 mg/mL,5 mg/mL | Ристоцетин в высоких концентрациях вызывает агглютинацию тромбоцитов через фактор Виллебранда и комплекс GPIb-IX-V. |
| Коллаген | 1, 4μg/mL | Коллаген связывается с рецепторами GРVI и GРIa / IIa, индуцируя высвобождение содержимого гранул, пул TXA2, а затем приводит к устойчивой активации GPIIb-IIIa.Рецептор GРIa / IIa участвует в адгезии тромбоцитов. Рецептор GРVI участвует в передаче сигналов тромбоцитов и генерации TхA2. Лаг-фаза формируется после добавления коллагена к ОТП обычно меньше, чем за 1 мин. |
| Арахидоно-вая кислота | 500μg/mL | Арахидоновая кислота является предшественником TхA2 в тромбоцитах. Арахидоновая кислота превращается в TхA2 при участии циклооксигеназы и тромбоксан-синтетазы. ТхА2 является мощным индуктором агрегации тромбоцитов, вызывая высвобождение гранул, образование еще большей генерации TхA2 и затем устойчивой активации рецепторов GРIIb-IIIа. |
| Тромбин | Низкая –50 nmol/L Высокая – 100 nmol/L | Тромбин является самым мощным физиологическим активатором тромбоцитов, действующим на рецепторы PAR1 и PAR4.Тромбин вызывает агрегацию тромбоцитов даже при низких концентрациях, это не приводит к полной агрегации, однако при меняет форму тромбоцитов. При более высокой концентрации тромбин индуцирует полную агрегацию тромбоцитов. |
Используемая аббревиатура: БТП – бедная (обедненная) тромбоцитами плазма, ОТП – обогащенная тромбоцитами плазма, TхA2 — тромбоксан А2, С – концентрация, GP – гликопротеид.
Вид классической двухфазной кривой агрегации тромбоцитов:
При введении адреналина и низких доз АДФ обычно образуется двухфазная кривая агрегации, в то время как при введении других агонистов, либо при высоких концентрациях индукторов, возможно слияние первой и второй волн. При двухфазной агрегации вторая волна связана с реакцией высвобождения гранул тромбоцитов.
Параметры агрегатограммы.
Основные параметры агрегатограммы можно интерпретировать только после предварительной оценки активности тромбоцитов по типам кривых агрегатограммы (обратимая, двухфазная, необратимая и отсутствие агрегации тромбоцитов).
Основными параметрами агрегатограммы являются интенсивность первичной (Тпа), вторичной (Тва), максимальной агрегации (Тма) и дезагрегации (Тда). О динамике процесса агрегации на графике следует судить по углам наклона кривой агрегатограммы на этапе первичной агрегации (α1), вторичной агрегации (α2) и дезагрегации (β). Характеристикой динамики реакции высвобождения эндогенных стимуляторов агрегации тромбоцитов является время латентного периода для коллаген-индуцированной агрегации (tлп) и время начала вторичной агрегации (tва) в норме для двухфазных кривых агрегатограммы (высоких доз АДФ и адреналина).
Для агрегации, индуцированной коллагеном важно также оценить укорочение или удлинение латентного периода (tлп) по сравнению с величиной этого показателя у здоровых людей.
Качественная оценка агрегатограммы позволяет не только диагностировать гипер- или гипореактивность тромбоцитов, но и предположить причины их возникновения. Для количественной регистрации различных типов агрегатограмм следует вычислять следующие показатели:
— при необратимой агрегации – Тма, Тпа, Тда, Tва, α1, α2, из которых самыми информативными являются Тва, α2 и Tва;
— при обратимой агрегации – Тма и Тда.
Диапазон колебаний основных показателей агрегатограммы:
| Параметры агрегатограммы | Диапазон изменений | Параметры агрегатограммы | Диапазон изменений |
| Тма | 30-50% | Tва | 30-45 с |
| Тва | 30-40% | α1 | 60-75 º |
| Тда | 60-80% (от величины Тпа) | α2 | 60-75 º |
| Тпа | 10-20% | β | 30-45 º |
| tлп | 25-30 с | ||
Референсные значения
Агрегационная активность в норме составляет при использовании индукторов:
- Агрегация тромбоцитов с АДФ (5,0 мкмоль/мл): 60-90%
- Агрегация тромбоцитов с АДФ (0,5 мкмоль/мл): 1,4-4,3%
- Агрегация тромбоцитов с адреналином: 40-70%
- Агрегация тромбоцитов с коллагеном: 50-80%
Интерпретация данных
| Ориентировочный диагноз | Изменения на агрегатограмме |
| Тромбастения Гланцманна или афибриногенемия | Отсутствие или значительное снижение агрегации при стимуляции любыми агонистами, кроме ристоцетина |
| Синдром Бернара-Сулье или болезнь фон Виллебранда | Отсутствие или значительное снижение агрегации с ристоцетином |
| Нарушение пула хранения | Первичная волна агрегации только с АДФ, адреналином и коллагеном. |
| Действие аспирина или аспириноподобный эффект | Отсутствие агрегации с арахидоновой кислотой. Присутствие первичной волны только с АДФ. Снижение или отсутствие агрегации с коллагеном. |
| Действие клопидогреля | Отсутствие агрегации с АДФ |
| 2В тип болезни фон Виллебранда (БВ) или тромбоцитарный тип БВ | Агрегация с низкой дозой ристоцетина (0,5 мг/мл) |
Ссылка на методическое пособие «Клинико-лабораторная диагностика нарушений функции тромбоцитов». Васильев С.А., Берковский А.Л., Мелкумян А.Л., Суворов А.В., Мазуров А.В., Козлов А.А. ФГБУ Гематологический научный центр, МЗ РФ, Москва, 2013 г.
При подготовке раздела использованы данные научного сайта www.practical—hemostasis.com.
Когда нужно сдавать анализ Агрегация тромбоцитов с АДФ (4 концентрации с аденозиндифосфатом)?
- Перед назначением препаратов, оказывающих влияние на систему свёртывания.
- Дифференциальная диагностика заболеваний, сопровождающихся патологическими кровотечениями.
- В рамках комплексной оценки тромбоцитарного звена гемостаза у пациентов перед (обширной) операцией, а также у беременных женщин с высоким риском развития акушерских осложнений.
- Определение резистентности к лекарственным средствам из группы антиагрегантов.
- Выявление наследственных и приобретенных тромбоцитопатий.