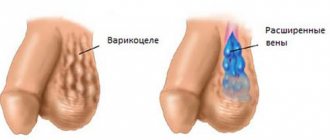
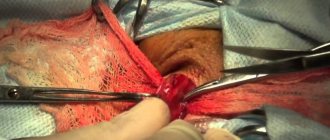
Варикозное расширение вен яичка, или варикоцеле, — проблема, с которой сталкиваются многие мужчины. Часто болезнь возникает еще в подростковом возрасте и обнаруживается на урологическом осмотре. Согласно статистике, от варикоцеле страдают 5-7% молодых людей 18-20 лет и 15-17% мужчин до 40 лет. В 80-98% случаев наблюдается левостороннее расширение вен.
Варикоцеле характеризуется скрытым течением и долгое время никак не проявляет себя. Обнаружить заболевание в начальной стадии удается только с помощью специальных тестов. Визуализировать патологически расширенные вены помогает проба Вальсальвы при варикоцеле. Что это за исследование и в чем его преимущества?
Историческая справка
Сегодня пробу Вальсальвы при варикоцеле применяют для оценки увеличения венозной сети семенного канатика при задержке дыхания и натуживании. Аналогичным приемом с небольшими изменениями пользовались более 100 лет назад, но с другой целью.
Еще в ХХ веке активно практиковали метод, названный в честь хирурга Антонио Марии Вальсальвы. Итальянский специалист изучал анатомию уха и сделал вывод, что главная функция слуховой трубы заключается в проветривании среднего уха для поддержания оптимального давления по обе стороны барабанной перепонки. В нормальном состоянии труба закрыта. При погружении под воду давление сильно возрастает. Чтобы нормализовать его, нужно сделать выдох.
Первоначально методику, основанную на этом открытии, практиковали для очищения среднего уха, диагностики болезней мозга и сердца. Позже область применения стала шире: видоизмененную пробу Вальсальвы стали активно использовать в урологии для диагностики варикоцеле.
Алгоритм и необходимость ультразвукового сканирования
Тогда как физикальные способы позволяют только выявить наличие варикоцеле в семенном канатике, ультразвуковое сканирование информирует о типе болезни и нарушениях в сперматогенезе, которые успел нанести недуг, дает информационную базу для назначения адекватной тактики лечения. В качестве подтверждения эффективности ультразвукового сканирования целесообразно ознакомиться с результатами одного из исследований. Работа проводилась в период 1998-2006 гг в отделении хирургии сосудов ГУ СККБ. Были обследованы и прооперированы мужчины с варикоцеле (101 пациент) в возрасте 6 — 35 лет.
Для оценки морфологического состояния ренокавальной зоны и сосудов гроздевидного сплетения применялась комплексная флебография, эхография и флеботензиометрия. Диагностика позволила выявить 3 вида гемодинамически значимого рефлюкса в вены гроздьевидного сплетения по Coolsaet, причем у 89 пациентов обнаружен первый реносперматический тип без рефлюкса, у 7 мужчин диагностирован второй илеосперматический тип и третий смешанный тип наблюдался у 5 больных.
В ходе ультразвукового исследования ренокавальной зоны пристальное внимание было уделено признакам аорто-мезентериальной компрессии левой почечной вены. На основании обследования удалось сформулировать показания к проведению реконструктивного вмешательства на левой яичковой вене.
Наряду с пробой Вальсальвы и способами ультразвуковой диагностики одной из обязательных процедур, которые проходит пациент на этапе диагностики, является анализ спермограммы. Такое исследование направлено на определение объема эякулята, процента малоподвижных, неподвижных и мертвых сперматозоидов, скорости их движения и прочих параметров, влияющих на репродуктивную функцию.
Методика выполнения пробы Вальсальвы
Пробу Вальсальвы широко используют в диагностике варикоцеле на ранних стадиях, когда выраженных клинических симптомов еще нет. Методика применяется в качестве самостоятельного способа исследования или в сочетании с УЗИ.
Пациентам с подозрением на варикоцеле пробу Вальсальвы проводят при первом осмотре. Мужчина делает глубокий вдох и задерживает дыхание. Уролог в это время пальпирует мошонку и яички. При наличии патологических изменений становится заметным даже незначительное расширение вен.
Для оценки кровотока в пораженных сосудах пробу Вальсальвы также выполняют во время УЗИ. Специалист просит мужчину глубоко вдохнуть и сильно напрячь мышцы живота. Признаки заболевания — расширение семенных канатиков и появление эластичных узелков.
Пройти диагностику и оперативное лечение варикоцеле приглашает наша клиника. Медицинское учреждение оснащено необходимым оборудованием, прием ведут опытные урологи-андрологи. Запись на консультации — по телефонам.
Antonio Maria Valsalva был выдающимся анатомом, физиологом и профессором хирургии в Университете Болоньи. В 1704 г. он опубликовал свою самую известную работу «De Aure Humana Tractatus», которая более столетия служила справочником по лечению заболеваний среднего уха. В нескольких параграфах своей книги А. М. Valsalva в деталях описал терапевтический прием «для выталкивания инородных тел и жидкостей из среднего уха», при котором больной делал попытку выдоха в течение нескольких секунд при закрытом рте и носе. Много лет спустя (1851 г.) в Германии физиолог Edward Weber детализировал ассоциированные с этим приемом изменения в сердечно-сосудистой системе, позволяющие его использовать для определения автономной (вегетативной) регуляции сердца. Исторически, отдавая должное обоим авторам, в мировых источниках литературы такой прием часто называют пробой Вальсальвы-Вебера (ПВВ) [1].
Проба позволяет количественно и комплексно оценивать вклад симпатической и парасимпатической частей вегетативной нервной системы (ВНС) в осуществление регуляции функций сердца и сосудов [2].
В происхождении вазовагальных обмороков (ВВО) широко обсуждается роль вегетативных нарушений. Возможности применения ПВВ у больных с ВВО не изучались, что определило актуальность настоящего исследования.
Материалы и методы
В исследование включили 12 здоровых лиц (все мужчины, средний возраст 31±7 лет) и 30 больных с ВВО (12 (40%) мужчин, средний возраст 32±14 лет). Больные имели достоверно меньшие рост и массу тела по сравнению с группой здоровых лиц, вероятно, в связи с преобладанием в последней мужчин. Вазовагальный генез обмороков у больных во всех случаях подтвержден данными клинического опроса с использованием специально разработанной анкеты [3]. При этом иные (метаболические, неврологические, кардиальные и ортостатические) причины приступов потери сознания исключены результатами предварительного инструментального обследования.
У больных также отсутствовали клинически значимые заболевания соматической, эндокринной, нервно-психической природы и прием лекарственных препаратов.
Всем лицам, включенным в исследование, выполнена ПВВ. Пробу проводили с использованием специализированного комплекса Task Force Monitor («CNSystem», Австрия), который давал возможность синхронно с мониторированием электрокардиограммы (ЭКГ) и частоты сердечных сокращений (ЧСС) — интервалов R-R
неинвазивно в режиме «от удара к удару» контролировать артериальное давление (АД) на пальцах правой руки фотокомпенсационным методом (по изменениям пульсового кровенаполнения) в сочетании с периодической калибровкой сигнала с учетом АД, измеренного осциллометрическим методом на плече левой руки.
Первоначально пациенту в покое лежа на спине в течение 20 мин проводили запись исходных показателей.
В это время испытуемому объясняли порядок проведения пробы и обучали приему Вальсальвы, включая короткое пробное его выполнение. Затем выполняли ПВВ в соответствии с рекомендациями P. Novak [2].
При выполнении пробы обследуемый брал в рот загубник (одноразовый пластмассовый шприц емкостью 10 мл, к разъему для иглы которого подсоединялся входной шланг манометра; на расстоянии 10 мм от этого места в теле шприца иглой №0740 выполнялись 4 отверстия для обеспечения небольшой утечки воздуха при усиленном выдохе, что предотвращало «некорректное» выполнение пробы пациентом с закрытой голосовой щелью). Пациент делал глубокий вдох и затем усиленный выдох в загубник. Ориентируясь на показания подключенного к загубнику манометра, он поддерживал давление 40 мм рт.ст. в течение 15 с. Затем обследуемый отпускал загубник и выполнял обычный вдох. Для облегчения выполнения пробы использовали специальный носовой зажим.
Пробу повторяли трижды с 3-минутным интервалом между тестами. Для последующего расчета выбирали один из тестов с минимальным количеством артефактов на трендах АД и ЧСС. Для углубленной обработки результатов исследования и расчета дополнительных показателей проводили экспортирование данных трендов АД и ЧСС в электронные таблицы формата Excel с последующим обсчетом с использованием возможностей программы Exсel.
Анализ результатов ПВВ для выявления нарушений ВНС и определения степени их выраженности включал визуальную оценку кривых изменений АД и ЧСС, а также расчет параметров, которые в настоящее время используют ведущие лаборатории, занимающиеся диагностикой и лечением патологии ВНС [2, 4-6]. Полный перечень таких показателей приведен в табл. 1
, а схематическое изображение фаз пробы — на
рис. 1
.
Рисунок 1. Динамика среднего АД и интервалов R-R
во время ПВВ у здорового добровольца. Объяснения в тексте.
Статистическую обработку и анализ полученных данных проводили с использованием непараметрических методов. Для оценки межгрупповых сравнений показателей использовался критерий Манн-Уитни, а для исследования достоверности изменения показателей в каждой из исследуемых групп во время проб — метод Вилкоксона. Для оценки частот качественных признаков использовали непараметрический метод Фишера. Все различия считали достоверными при р
<0,05.
Результаты и обсуждение
При анализе изменений показателей функции сердечно-сосудистой системы при выполнении ПВВ выделяют 4 фазы (см. рис. 1; рис. 2)
[1, 2, 4-7].
Рисунок 2. Динамика среднего АД и интервалов R-R
во время ПВВ у больного с ВВО. АДср в позднюю II фазу не достигает исходного уровня (нормальный вариант реакции для сравнения см. рис. 1). В I фазе, когда испытуемый делает усиленный вдох и начинает экспираторное усилие, наблюдается повышение АД, обусловленное усиленным выбросом крови из сердца, при этом может отмечаться некоторое снижение ЧСС (увеличение длительности интервалов
R-R
). II фаза по времени соответствует экспираторному напряжению и характеризуется быстрым первоначальным снижением АД (ранний период). Это вызвано падением возврата венозной крови и сердечного выброса на фоне высокого внутригрудного давления, а затем постепенным повышением АД, часто превышающим исходный его уровень (поздний период), под действием компенсаторных барорефлекторных механизмов. Результатом являются возбуждение симпатической части ВНС и вазоконстрикция, а также ослабление вагусных влияний и синусовая тахикардия (уменьшение длительности интервалов
R-R
). Однако если непосредственно перед проведением пробы испытуемый делал глубокие дыхательные движения, то во II фазу может наблюдаться брадикардия, связанная с усиленным действием блуждающего нерва [7]. Внезапное прекращение экспираторного усилия через 15 с от начала проведения пробы приводит к падению внутригрудного давления и АД (III фаза). В дальнейшем при возобновлении дыхательных движений возврат венозной крови к сердцу увеличивается и на фоне сохраняющегося повышенного уровня вазоконстрикции (как результат симпатической активации во II фазе) отмечается подъем АД, превосходящий исходный его уровень («овершут»), ЧСС замедляется.
При недостаточности компенсаторных физиологических механизмов регуляции АД и ЧСС описанная стадийность при выполнении ПВВ может быть нарушена, а реакции гемодинамических показателей извращены, что наблюдается при различной патологии ВНС.
Анализ параметров, характеризующих различные фазы ПВВ (см. табл. 1)
, не выявил достоверных различий между здоровыми лицами и больными с ВВО по большинству из них, за исключением индекса «2» давления на пробе
(см. табл. 1; табл. 2)
.
У больных с ВВО значение индекса «2» (т.е. прироста АД в «поздний период» II фазы) в среднем по группе оказалось меньше, чем у здоровых лиц (см. рис. 1, 2)
.
При визуальном анализе существенное изменение формы кривой среднего АД, состоящее в том, что к концу II фазы пробы АД не достигало исходного уровня, зафиксировано у 10 из 30 больных с ВВО (т.е. у 33%) (см. рис. 2)
, и ни у одного здорового лица. Различия по частоте выявления данного феномена между двумя группами достоверны
(см. табл. 2)
.
Проанализированные нами индексы используются для выявления поражения симпатической части ВНС и степени его выраженности [4]. Величина снижения среднего АД (индекс «1»), возможность восстановления этого показателя к концу II фазы ПВВ (индекс «2»), остаточная величина, необходимая для достижения исходного его уровня (индекс «3»), приняты в качестве количественных и качественных критериев оценки «симпатической недостаточности». По результатам исследования P. Novak [4], индекс «3» из всех изучавшихся показателей при анализе ПВВ являлся оптимальным для оценки симпатического звена регуляции АД, так как позволял четко отличать здоровых лиц от больных с «симпатической недостаточностью» и был взаимосвязан с ортостатической гипотонией, а также со степенью ее выраженности.
В нашей работе по индексу «3» достоверные различия между больными с ВВО и здоровыми лицами не обнаружены. Возможно, это связано с тем, что в отличие от исследования P. Novak, в нашем исследовании у больных отсутствовали признаки классической ортостатической гипотонии (снижение систолического АД >20 мм рт.ст.) при активной ортостатической пробе.
Имеются расхождения во мнениях относительно наличия вегетативной патологии у больных с ВВО. Считается, что у лиц, подверженных ВВО, отсутствует истинное поражение ВНС при использовании традиционных критериев оценки ее функции, а имеющаяся симптоматика объясняется с позиций гиперболически выраженного рефлекторного ответа, приводящего к брадикардии и артериальной гипотонии [8]. В то же время ряд клинических и экспериментальных работ [9-15] показывает, что с применением других способов оценки регуляторных возможностей ВНС (анализ показателей вариабельности ритма сердца, микронейрографическое исследование симпатической активности перонеальных мышц, импедансная кардиография, сцинтиграфия миокарда с метайодбензилгуанидином, меченным радиоактивным йодом) могут выявляться признаки, которые указывают на недостаточный вклад симпатического звена в осуществление регуляции деятельности сердца и сосудов.
Для истинного суждения о степени тяжести поражения ВНС необходим комплексный анализ функционирования ее двух частей — симпатической и парасимпатической. По результатам нашей работы между больными с ВВО и здоровыми лицами в параметрах, характеризующих «вагусную» регуляцию сердца (чувствительность артериального барорефлекса, коэффициент Вальсальвы — см. табл. 1
), не получено достоверных межгрупповых различий. В то же время у 9 (30%) из 30 больных при индивидуальном анализе коэффициента Вальсальвы с поправкой на пол и возраст [2] выявлено его снижение
(см. табл. 2)
. Результаты, полученные в настоящей работе, отличаются от данных литературы [13, 15], которые указывают на сохранность «вагусных» влияний на синусный узел у больных с ВВО и даже на их усиление как в положении покоя лежа, так и особенно при развитии синкопе. Причиной подобных различий могут служить как методические особенности оценки функции ВНС (анализ вариабельности ритма сердца), использованные в данных исследованиях, так и факторы, принимающие участие при формировании разных выборок больных.
Для выявления вегетативных нарушений обычно используют комплексный подход — проводят несколько тестов (пробу с глубоким дыханием, пробу Вальсальвы, пробу с активным или пассивным ортостазом и судомоторный тест), а при определении выраженности обнаруженной патологии принято использовать специальные шкалы. ПВВ — единственная из перечисленных, оценка результатов которой позволяет сделать заключение о возможных нарушениях как в симпатической, так и парасимпатической частях ВНС.
В целом у 16 (53%) из 30 больных с ВВО определены признаки вегетативных нарушений либо в симпатической (измененная форма кривой АДср.), либо в парасимпатической (индивидуально измененный коэффициент Вальсальвы) части ВНС. Совпадение по вовлечению в процесс обоих ее частей констатировано в 3 случаях. Используя шкалы оценки степени вегетативной недостаточности [2], выявленные нарушения у больных, включенных в настоящее исследование, можно расценивать как легкие.
Заключение
При выполнении дозированной ПВВ признаки симпатической недостаточности (нарушение адренергической регуляции АД) выявляются у 33% больных с ВВО, парасимпатической недостаточности (нарушение «вагусной» регуляции кардиохронотропной функции) — у 30%.