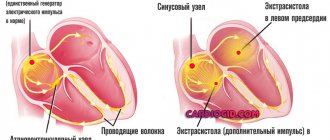
Среди заболеваний сердца эндокардит – одно из наиболее коварных. Под воздействием различных инфекций (всего насчитывают около 130 возбудителей данного заболевания) воспаляется внутренняя оболочка сердца. Опасность состоит в том, что симптомы инфекционного эндокардита проявляются не сразу, поэтому пациенты не всегда обращаются за помощью своевременно. Также болезнь нелегко поддается диагностике, из-за чего лечение может быть начато позже положенного срока. Вот почему кардиологи рекомендуют регулярно проходить обследование в медицинских центрах, оснащенных современной аппаратурой, имеющей широкие исследовательские возможности.
Что такое эндокардит
Симптомы болезни возникают у людей различного возраста, в том числе детей с диагнозом «врожденные пороки сердца» (тетрада Фалло, дефекты единственный желудочек и др). Спровоцировать ее могут:
- пролапс митрального клапана;
- гипертрофическая кардиомиопатия;
- оперативное вмешательство на клапанах сердца;
- деффекты сердечных перегородок;
- ишемическая болезнь сердца (особенно после операции).
Заболевание имеет прежде всего инфекционную форму. Воспаление, вызванное микроорганизмами, затрагивает не только сам эндокард – внутренние ткани сердечной мышцы, — но и сердечные клапаны, расположенные рядом сосуды. Нередко инфекция проникает в печень, почки, селезенку.
Чаще всего патология становится следствием других заболеваний. Предпосылками возникновения инфекционного эндокардита является бактериологическое заражение организма при различных условиях. Также инфекция поражает сердце при травмах его клапанов вследствие установки протезов, кардиостимуляторов, на поверхности которых могут развиваться микроорганизмы. Встречаются атеросклеротические формы, вызванные дистрофическими изменениями сердечных тканей, и ревматические формы – при ревматизме клапанов сердца.
ИНФЕКЦИОННЫЙ ЭНДОКАРДИТ: диагностика, клиническое течение, лечение
Инфекционный эндокардит (ИЭ) относится к числу тяжелых заболеваний с высоким уровнем летальности. В отсутствии лечения смертность при ИЭ составляет 100%. В последние годы отмечается значительный рост числа больных эндокардитом в нашей стране и за рубежом. По данным различных авторов, сегодня выросла заболеваемость в пожилом и старческом возрасте, а также среди лиц в возрасте до 30 лет, использующих внутривенное введение наркотиков [1, 2].
Известно, что ИЭ представляет собой заболевание инфекционной природы с первичной локализацией возбудителя на клапанах сердца, пристеночном эндокарде, протекающее с проявлениями системной инфекции, сосудистыми осложнениями и иммунной реакцией [3, 4, 5].
Традиционно развитие ИЭ связывают с наличием «внутрисердечных» факторов риска, к которым относят врожденные и приобретенные пороки сердца, наличие протезированных клапанов, пролапсов клапанов и другие аномалии [6]. В последние годы к категории лиц повышенного риска отнесены больные с очаговой инфекцией, а также лица, у которых применялись инвазивные методы исследования, включая установку подключичного катетера [7]. Особую группу риска составляют наркоманы, практикующие внутривенное введение наркотиков, у которых ИЭ протекает с поражением интактных клапанов сердца.
В данной работе обобщен опыт диагностики и ведения больных ИЭ на базе общетерапевтического отделения Александровской больницы Санкт-Петербурга за период 1998–2003 гг. Диагностика заболевания осуществлялась в соответствии с критериями Duke [8]. Диагноз ИЭ оценивался как достоверный при наличии двух главных критериев, а именно:
- при выделении типичного для ИЭ возбудителя при посевах крови больного;
- при определении эхокардиографических признаков поражения эндокарда — подвижные вегетации на клапанах сердца, абсцессов в области протеза клапана; образования внутрисердечных фистул и др., в сочетании с тремя или/и пятью вспомогательными критериями, к которым относились сосудистые осложнения (эмболии крупных артерий, септические инфаркты легких, внутричерепные кровоизлияния и др.), иммунологические феномены (гломерулонефрит, узелки Ослера, геморрагический васкулит и др.), а также фебрильная лихорадка, гепато-спленомегалия и другие проявления системной инфекции.
Нами было проведено обследование 105 больных ИЭ, из них у 80 человек в возрасте от 18 до 30 лет (первая группа) основным фактором риска заболевания являлась инъекционная наркомания.
Во второй группе больных (25 чел.) основными предрасполагающими факторами развития ИЭ были врожденные и приобретенные пороки сердца, а также протезированные клапаны.
У лиц старшей возрастной группы дополнительным фактором риска являлись дегенеративно-дистрофические изменения клапанов сердца.
Взаимосвязь характера поражения клапанов сердца и факторов риска ИЭ представлена в таблице 1.
По данным эхокардиографического исследования, у 100% больных первой группы были выявлены подвижные вегетации на створках трикуспидального клапана (ТК), что сопровождалось формированием его недостаточности I—III степени.
Во второй группе больных ИЭ отмечалось поражение левых камер сердца с образованием вегетаций на створках аортального и митрального клапанов. Изолированное поражение митрального клапана наблюдалось у двух человек с ревматическим пороком сердца (митральный стеноз), у одной больной с врожденным дефектом межжелудочковой перегородки и в единственном случае обструктивной формы гипертрофической кардиомиопатии.
Среди лиц пожилого и старческого возраста у девяти человек (36%) определялось изолированное поражение аортального клапана в отсутствии признаков аортального стеноза. Наряду с этим, у пяти больных (20%) в возрасте от 72 до 87 лет ИЭ развился на фоне аортального порока атеросклеротического генеза, причем у всех пятерых было выявлено сочетанное поражение аортального и митрального клапанов. Дегенеративно-дистрофические изменения других клапанов сердца определялись у 100% больных старшей возрастной группы.
Образование вегетаций на створках аортального клапана наблюдалось у двух больных с третичной формой сифилиса на фоне имеющегося аортального порока, связанного со специфическим процессом в аорте.
В двух случаях мы наблюдали развитие эндокардита протезированных клапанов.
При сопоставлении результатов посевов крови в двух группах больных определялись существенные различия как в частоте выделения микробной флоры, так и в видовом составе возбудителей эндокардита. По нашим данным, возбудителем ИЭ у больных-наркоманов в 71,3% наблюдений (57 чел.) являлся золотистый стафилококк, тогда как во второй группе, наряду с кокковой флорой, чаще обнаруживались грамотрицательные микроорганизмы (28%). Отрицательные результаты посевов крови значительно реже наблюдались в первой, чем во второй, группе больных ИЭ: 18,7% и 56% — соответственно. Данные относительно этиологической структуры ИЭ в обследуемых группах больных представлены в таблице 2.
Клиническая характеристика и особенности течения ИЭ
Клиническое течение и характер осложнений инфекционного эндокардита во многом зависят от локализации клапанных вегетаций — в правых или левых камерах сердца, а также степени вирулентности возбудителя заболевания.
Течение ИЭ у больных-наркоманов отличалось особой тяжестью и полисиндромностью. Причиной госпитализации у большинства больных были острые осложнения основного заболевания. Значительная часть больных поступала в реанимационное отделение стационара с клиническими симптомами одно- или двухсторонней многофокусной пневмонии, причиной которой являлась септическая тромбоэмболия ветвей легочной артерии (72% больных). Течение пневмонии сопровождалось тяжелой дыхательной недостаточностью, нередко с развитием респираторного дистресс-синдрома (РДСВ) и очагами деструкции в легких (12%). Проявления вторичной нефропатии, которые обнаруживались у 100% больных в первой группе, иногда ошибочно трактовались как обострение хронического гломеруло- или пиелонефрита, мочекаменной болезни, что служило поводом для госпитализации этих больных в урологическое и нефрологическое отделения.
Во второй группе больных основной причиной госпитализации была длительная фебрильная лихорадка в сочетании с анемией и гепатолиенальным синдромом. Наряду с этим, у пяти человек (20%) поводом для госпитализации послужила прогрессирующая сердечная недостаточность.
Основные клинические синдромы, наблюдаемые у больных ИЭ первой и второй групп, представлены в таблице 3.
По нашим наблюдениям, характерной особенностью клинического течения ИЭ у больных-наркоманов являлась высокая частота септической ТЭЛА с формированием множественных очагов инфильтрации в легких. У многих больных легочные тромбоэмболии носили рецидивирующий характер (31,3% больных) и нередко осложнялись развитием деструктивных очагов в легких.
Образование вегетаций у 100% больных первой группы сопровождалось недостаточностью трехстворчатого клапана I—III степени с формированием потоков регургитации. Вместе с тем, у большинства пациентов не определялось тяжелых нарушений центральной гемодинамики, связанных с дисфункцией ТК. В данной группе больных характерной клинической особенностью был обратимый характер нарушений гемодинамики на фоне проводимой терапии. Острая сердечная недостаточность с дилятацией полостей сердца и снижением фракции выброса до 40% и ниже наблюдалась у 28 больных (35,3%) в связи с присоединением острого миокардита или на фоне сочетанного поражения клапанов сердца.
Вторичная нефропатия являлась одним из самых распространенных синдромов в первой группе больных ИЭ. Острая почечная недостаточность наблюдалась у 16 больных, причем у 10 из них она носила обратимый характер и была связана с острым ДВС-синдромом, а также с острой сердечной недостаточностью с отеками. Инфекционно-токсическая нефропатия регистрировалась в 73,8% наблюдений и сопровождалась мочевым синдромом — гематурией, протеинурией, лейкоцитурией — при достаточном уровне клубочковой фильтрации.
Характерной особенностью ИЭ во второй группе было подострое течение заболевания с длительным периодом лихорадки на догоспитальном этапе, причем в пожилом и старческом возрасте лихорадка носила субфебрильный характер с редкими подъемами температуры до фебрильных цифр.
Большинство больных подострым инфекционным эндокардитом (ПИЭ) поступали в стационар в стадии развернутой клинической картины заболевания с клиническими признаками тромбоэмболии сосудов большого круга кровообращения. В данной группе больных наиболее распространенными следует признать такие осложнения, как церебральные эмболии с развитием ишемических и геморрагических инсультов, эмболии почечных сосудов с болевым синдромом и гематурией, а также формирование острых очаговых изменений в миокарде, связанных с эмболией коронарных сосудов или прикрытием устьев коронарных артерий вегетациями [9].
Септические тромбоэмболии церебральных сосудов нередко сопровождались развитием гнойного менингоэнцефалита с летальным исходом. Вместе с тем, при посевах крови у 56% больных второй группы не получено роста микробной флоры. Обращает на себя внимание тот факт, что септицемия у больных с положительными результатами посевов крови в 28% наблюдений была обусловлена грамотрицательной микрофлорой. В этой категории больных источником бактериемии являлись очаги хронической инфекции в мочеполовой системе, а у двух больных (по данным аутопсии) был выявлен двухсторонний апостематозный нефрит.
У значительного числа больных ПИЭ (62%) определялись признаки острой недостаточности кровообращения с застойными хрипами в легких, легочной гипертензией, увеличением полостей сердца и периферическими отеками.
В этой группе больных чаще, чем в первой, наблюдалась преренальная азотемия и ОПН, связанные с развитием острой недостаточности кровообращения.
Острый диффузный миокардит, типичными проявлениями которого были различные нарушения ритма, диагностирован у 27% больных второй группы.
Анемия со снижением уровня гемоглобина до 80 г/л и менее выявлена у 100% больных второй группы. Значительное увеличение СОЭ (более 45 мм/ч) наблюдалось у 85,8% больных подострым ИЭ.
Кожные изменения в виде геморрагических высыпаний, пурпуры Шенлейн-Геноха, а также другие проявления иммунного воспаления в обеих группах больных встречались нечасто — 6,3 и 4% в первой и второй группах, соответственно.
Лечение больных ИЭ
Консервативная терапия больных ИЭ проводилось с использованием антибиотиков широкого спектра действия в сочетании со средствами дезинтоксикационной, антикоагулянтной и метаболической терапии. В составе антибактериальной терапии больные получали цефалоспорины III-IV поколений в комбинации с аминогликозидами и метронидазолом. Из группы цефалоспоринов назначались: цефтриаксон (лонгацеф) 2 г в сутки внутривенно (в/в), или цефотаксим (тальцеф) 2 г в сутки в/в, или цефепим (максипим) 2 г в сутки в/в в сочетании с аминогликозидами (амикацин в суточной дозе 1,5 г в/в) и метронидазолом по 1,5-2 г в сутки в/в. В случае, если такая терапия оказывалась неэффективной или существовали противопоказания к вышеперечисленным препаратам, применялись антибиотики группы линкозаминов: клиндамицин 1,2 г в сутки в/в или линкомицин 3 г в сутки в/в в сочетании со фторхинолонами (ципрофлоксацин 400 мг в сутки в/в). В условиях отделения реанимации в течение пяти–семи дней проводилась терапия имипинемом (тиенамом) в дозе 2—4 г в сутки в/в или рифампицином в суточной дозе 0,45—0,6 г в/в. Средняя продолжительность курса антибиотикотерапии в обследуемой группе больных составила 28 + 3,5 дней.
Дезинтоксикационная терапия включала в себя внутривенные инфузии реополиглюкина, гемодеза, поляризующих смесей в сочетании с петлевыми диуретиками. Объем вводимой жидкости составлял в среднем 2-2,5 л в сутки. В течение всего периода инфузионной терапии осуществлялся контроль за функциональным состоянием почек, электролитным составом крови, суточным диурезом. В условиях отделения реанимации у всех больных осуществлялся мониторинг ЦВД. Инфузионная терапия проводилась в течение всего острого периода заболевания до купирования проявлений интоксикационного синдрома. Средняя продолжительность курса составила 22 + 4,5 дня.
Развитие легочной эмболии, особенно в сочетании с признаками острого ДВС-синдрома в стадии гиперкоагуляции, служило основанием для назначения антикоагулянтной терапии. Начальная доза гепарина составляла 10 тыс. ЕД внутривенно, струйно, за-тем — по 1000 ЕД в час внутривенно, капельно с переходом на подкожное введение до 30 тыс. ЕД в сутки. Введение гепарина осуществлялось под контролем показателей коагулограммы и времени свертывания крови. Одновременно проводились внутривенные трансфузии свежезамороженной плазмы по 300 мл в сутки с добавлением 2500–5000 ЕД гепарина. Анемия тяжелой степени (Нb менее 80 г/л, Ht ≤25) корригировалась переливаниями эритроцитарной массы (пять–семь доз). При наличии гипопротеинемии использовалось введение растворов аминокислот, альбумина или нативной плазмы. Выявление клинических и рентгенологических признаков отека легких на фоне рецидивирующего течения септической ТЭЛА служило показанием для назначения кортикостероидов (преднизолон от 120 до 200 мг в сутки внутривенно капельно). Терапия антикоагулянтами прямого действия в сочетании с трансфузиями криоплазмы проводилась до стойкого улучшения показателей гемостаза. Критериями нормокоагуляции являлись уровень фибриногена в плазме 3-4 г/л, отсутствие тромбоцитопении, нормализация ВСК, АЧТВ, тромбинового времени, а также отрицательные паракоагуляционные тесты. По нашим данным, купирование проявлений острого ДВС-синдрома на стадии гиперкоагуляции у 75% больных отмечалось на седьмой–десятый день от начала комплексной терапии.
У части больных формировалась резистентность к проводимой антибактериальной терапии, которая характеризовалась нарастанием интоксикации, фебрильной лихорадкой, прогрессирующей анемией, а также высевами из крови возбудителя ИЭ – золотистого стафилококка — в 65% наблюдений. При рентгенологическом обследовании данной категории больных с большой частотой определялись очаги деструкции легочной ткани, а у трех больных гнойный выпот в плевральной полости.
Длительное применение антибиотиков широкого спектра действия у 70,3% больных (38 чел.) сопровождалось развитием побочных эффектов антибактериальной терапии. Кандидоз полости рта глотки, пищевода, а также кишечный дисбактериоз III-IV стадии был выявлен у 36 больных (66,7%). Применение антибиотиков с гепатотоксическими свойствами (цефалоспорины, линкозамины, метронидазол) у двух больных (3,7%) с хроническим гепатитом С и В приводило к прогрессированию печеночной недостаточности, которая сопровождалась высокой ферментемией (АЛТ 1500 ЕД, АСТ 1000 ЕД) и желтухой.
Развитие застойной сердечной недостаточности с появлением акроцианоза, влажных хрипов в базальных отделах легких, периферических отеков в сочетании с кардиомегалией и падением фракции выброса до 50—45% наблюдалось у пяти больных (9,3%) на фоне массивной инфузионной терапии.
Длительная антикоагулянтная терапия в 20,4% (11 чел.) наблюдений сопровождалась повышением толерантности плазмы к гепарину, что клинически выражалось в развитии периферических флеботромбозов, в то время как гепарининдуцированной тромбоцитопении в обследуемой группе больных мы не наблюдали.
Положительные результаты консервативной терапии были получены у 70,2% больных (56 чел.) с поражением ТК и лишь у 32% пациентов (6 чел.) из второй группы. Исходом ИЭ в обеих группах больных являлось формирование недостаточности клапанов сердца.
Госпитальная летальность при ИЭ у наркозависимых лиц составила 29,4% (24 чел.), тогда как у больных с поражением левых камер сердца (вторая группа) уровень смертности составил 68% (19 чел.).
По данным аутопсии, основными причинами смерти больных ИЭ были:
- септикопиемия с формированием гнойных очагов в печени, почках селезенке, головном мозге с развитием полиорганной недостаточности (46,2%);
- сердечная недостаточность на фоне полипозно-язвенного эндокардита с разрушением клапанов сердца, а также острый миокардит с дилятацией полостей сердца (39,4%);
- вторичная нефропатия с развитием почечной недостаточности, отеком легких, отеком головного мозга (14,4%).
Таким образом, характерные особенности ИЭ у лиц с наркотической зависимостью — это острое течение заболевания с поражением правых камер сердца и рецидивами септической ТЭЛА. Возбудителем ИЭ у инъекционных наркоманов в 71,3% является высоковирулентный золотистый стафилококк. Формирование недостаточности трехстворчатого клапана I—III степени стало самым распределенным осложнением ИЭ у наркоманов. При этом у большинства больных не наблюдается тяжелых нарушений центральной гемодинамики, приводящих к развитию острой недостаточности кровообращения.
Подострый ИЭ у больных с предрасполагающими заболеваниями сердца, а также у лиц пожилого и старческого возраста протекает с преимущественным поражением левых камер сердца, причем в старшей возрастной группе преобладает моноклапанное поражение. Наличие сопутствующей патологии у лиц старше 60 лет маскирует течение основного заболевания, чем и обусловлены поздняя диагностика и высокая смертность больных. Для затяжного течения ИЭ характерна низкая высеваемость возбудителя, по сравнению с острыми формами заболевания. Развитие тромбоэмболий сосудов большого круга кровообращения является характерной клинической особенностью подострого ИЭ.
Положительный эффект от проводимой консервативной терапии наблюдается у большинства больных ИЭ с поражением ТК, тогда как при подостром эндокардите левых камер сердца консервативная терапия является малоэффективной у большинства больных.
Госпитальная летальность в обеих группах больных обусловлена диссеминацией возбудителя с формированием гнойных очагов и полиорганной недостаточностью, а также развитием острой недостаточности кровообращения и вторичной нефропатии.
Литература
- Буткевич О. М., Виноградова Т. Л. Инфекционный эндокардит. — М., 1997.
- Симоненко В. Б., Колесников С. А. Инфекционный эндокардит: современное течение, диагностика, принципы лечения и профилактики. — Клин. мед., 1999. — 3. — С. 44-49.
- Тазина С. Я., Гуревич М. А. Современный инфекционный эндокардит. — Клин. мед.,1999. — 12. — С. 19-23.
- Bansal R. C. Infective endocarditis. Med Clin North America 1995; 79 (5): 1205-1239.
- Bayer A. S., Bolger A. F., Taubert K. A. et al. Diagnosis and management of infective endocarditis and its complications. Circulation 1998; 98: 2936-2948.
- McKinsey D. S., Ratts T. E., Bisno A. I. Underlying cardiac lesions in adults with infective endocarditis. The changing spectrum. Amer J Med 1987; 82: 681-688.
- Lamas C. C. Eykyn S. J. Suggested modifications to the Duke criteria for the clinical diagnosis of native valve and prosthetic valve endocarditis: analysis of 118 pathologically proven cases. Clin Infect Dis 1997; 25: 713-719.
- Durack D. T., Lukes A. S., Bright D. K. et al. New criteria for diagnosis of Infective Endocarditis Utilization of Specific Echocardiographic Finding. Amer J Med 1994; 96: 200-209.
- Тюрин В. П., Дубинина С. В. Инфекционный эндокардит у лиц пожилого и старческого возраста. — Клин. мед., 2000. — 4. — С. 53-56.
В. И. Уланова В. И. Мазуров, доктор медицинских наук, профессор Медицинская академия последипломного образования, Санкт-Петербург
Классификация и причины эндокардита
В соответствии с причинами и клиническими проявлениями заболевание классифицируют следующим образом.
Инфекционный (бактериальный) эндокардит чаще всего проявляется в острой форме. На клапанах сердца или в сердечных тканях образуются язвы, полипы, которые приводят к функциональным нарушениям.
Хроническую или подострую форму обычно вызывают стрептококки. Заболевание проявляется изъязвлением и изменением формы сердечных клапанов, образованием тромбов в сосудах с последующей закупоркой. Следствиями могут стать воспаления почек, инфаркты других органов.
Заболевание неинфекционного характера возникает на фоне общего ослабления организма, при различных интоксикациях, у пожилых людей при развитии маразма. Среди форм – дегенеративная бородавчатая, абактериальная и др. Чаще всего проявляется в виде тромботических наложений на ткани клапанов.
Ревматический эндокардит, как следует из самого названия, возникает из-за ревматизма. При этом воспаление распространяется на сердечные клапаны и становится причиной пороков сердца. Различают 4 его формы: диффузный, острый бородавчатый, возвратно-бородавчатый, фибропластический.
Эндокардит Леффлера характеризуется увеличением эозинофилов крови и уменьшением объемов сердечных камер из-за фиброзных изменений эндокарда, а затем и миокарда. Выделяют три его стадии: острая (отмирание клеток в течение 5-6 недель), тромботическая (образование тромбов и атрофия части тканей), фиброз (склероз и утолщение эндокарда).
Воспалительные заболевания сердца — перикардит
Перикардит — что это? Воспаление околосердечной сумки (перикарда) — серозной оболочки сердца; возникает чаще всего как осложнение того и или иного заболевания, реже, как самостоятельное заболевание. Причины развития перикардита также разнообразны, как и при других воспалительных заболеваниях сердца. Принципиально выделяют инфекционные (бактерии, вирусы, простейшие и даже некоторые виды грибов) и неинфекционные (заболевания соединительной ткани, опухоли, травмы, послеоперационные). По форме — острые (сухой, экссудативный, с тампонадой сердца или без) и хронические. Проявляется перикардит увеличением объема жидкости в полости околосердечной сумки или образованием фиброзных стриктур, затрудняющих работу сердца.
Перикардит: симптомы
Специфические симптомы перикардита отсутствуют, при остром процессе развивается сердечная недостаточность. Перикардит обычно дает болевой синдром в грудной клетке, левой руке, отдаленно напоминающий инфаркт миокарда, но на ЭКГ при перикардите сохраняется достаточная амплитуда R, отсутствует патологический зубец Q, изменения касаются конечной части желудочкового комплекса (сегмента ST и зубца Т). Помимо боли, появляются жалобы на одышку, сердцебиение, общую слабость, похудение, может развиваться сухой кашель, в тяжелых случаях — кровохарканье, чувство тяжести в правом подреберье, увеличение окружности живота (следствие прогрессирования сердечной недостаточности). Острый сухой перикардит чаще возникает внезапно — с резкого повышения температуры, болей колющего характера в области сердца, ощущения перебоев сердца. Экссудативный перикардит может развиваться постепенно, чем больше скопилось жидкости в околосердечной сумке, тем ярче проявляются симптомы перикардита: набухание шейных вен, отеки на ногах, синюшность (цианоз) лица, удушье, расстройства глотания, асцит (скопление свободной жидкости в брюшной полости), тахикардия.
Перикардит: диагностика
При любых подозрениях на нарушения работы сердца необходимо срочно проконсультироваться со специалистом. Врач-кардиолог
может поставить предположительный диагноз уже при физикальном осмотре. Аускультативным подтверждением диагноза станут отсутствие или смещение верхушечного толчка и перкуторное расширение границ сердца, приглушение тонов сердца или шум трения перикарда (при сухом перикардите). Инструментальная диагностика —
ЭКГ
,
эхокардиография
— позволит верифицировать диагноз. Заболевания перикарда опасны, поэтому недопустимо заниматься самолечением, пить «что-нибудь от сердца». Без правильной и быстрой диагностики заболевания, возможны тяжелые последствия.
Перикардит: лечение
Лечение воспалительных заболеваний сердца проводится под наблюдением врача, как правило в стационаре. Только в некоторых легких случаях, допустимо амбулаторное лечение. Приоритетное направление терапии при перикардите — лечение основного заболевания. Для уменьшения объема жидкости в перикарде могут быть назначены мочегонные препараты. При угрозе тампонады (сдавления полостей сердца) выполняют чрескожную пункцию и эвакуируют содержимое. Лечение сдавливающего (констриктивного) перикардита только оперативное.
Факторы риска развития перикардита
Развитие воспалительных заболеваний серозной оболочки сердца провоцируют:
- ревматизм;
- системные аутоиммунные заболевания;
- тяжёлые пневмонии;
- хроническая почечная недостаточность;
- туберкулез, бруцеллез;
- склонность к аллергическим реакциям.
Профилактика воспалительных заболеваний сердца
Первичная профилактика большинства воспалительных заболеваний сердца заключается в двух простых правилах:
- повышение сопротивляемости организма к инфекциям (закаливание, здоровый образ жизни);
- своевременное лечение очаговой инфекции (тонзиллиты, кариес, гаймориты, фурункулез и т.д.).
Вторичная профилактика воспалительных заболеваний сердца заключается в предупреждении рецидивов заболевания, мероприятия по диспансерному учету пациентов, соблюдение рекомендаций лечащего врача по лечению основного заболевания (если оно имеется).
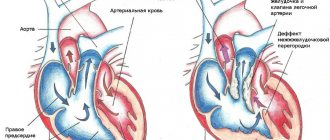
Инфекционный (бактериальный) эндокардит
При острой форме симптомы бактериального эндокардита развиваются достаточно быстро. Обычно инфекция поражает оболочку сердечных клапанов, на тканях створок появляются язвы 2-10 мм, а сами створки набухают – накапливаются тромбоциты и фибрин, образуются аневризмы. В итоге один из крупных сосудов может оказаться закупоренными тромбом, а частицы клапана могут оторваться. В ряде случаев не исключен септический инфаркт.
Если вовремя не обратиться за квалифицированной помощью и не начать лечение:
- развивается сердечная недостаточность;
- деформируется структура клапанов и створок;
- появляются аритмические явления;
- нарушается гемодинамика.
Для пациентов с подострым септическим эндокардитом характерны те же проявления патологии, однако в данном случае чаще всего ткани поражаются тромботическими образованиями, которые рано или поздно закупоривают один из важнейших сосудов.
Причины
Существует множество причин возникновения эндокардита:
- инфекции;
- травмы;
- аллергические заболевания;
- интоксикации;
- поражения соединительной ткани.
Нередко эндокардит развивается не как самостоятельная болезнь, а как следствие других патологий в организме. Заболеванию в равной степени подвержены как мужчины, так и женщины. Возникнуть он может в любом возрасте. На сегодняшний момент известно около 130 видов микроорганизмов, способных спровоцировать эндокардит.
Эндокардит у детей
У детей наиболее часто встречается бактериальный вид данного заболевания. Патология выражается поражением митрального и аортального клапанов, а затем распространяется на внутренние сердечные ткани:
- ребенок ощущает острый токсикоз;
- ткани эндокарда воспаляются;
- происходит поражение миокарда;
- сосуды могут закупориваться;
- нарушается кровоток.
Инфекционный эндокардит у детей обычно развивается более быстрыми темпами, воспаление может охватить другие внутренние органы и привести к печеночной, почечной недостаточности. Поэтому за профессиональной кардиологической помощью в данном случае необходимо обратиться в кратчайшие сроки.
Симптомы эндокардита
Для заболевания характерно бессимптомное протекание на ранней стадии, а также внезапное обострение на фоне относительно здорового состояния. Симптомы эндокардита у взрослых пациентов обычно проявляются спустя 10-14 дней после инфицирования:
- лихорадка с ознобом, обильным выделением пота;
- на нескольких дней может повышаться температура;
- появляются признаки интоксикации: головная боль, слабость, истощение;
- кожа может приобретать бледный, желтоватый оттенок;
- на слизистых, ступнях, ладонях могут наблюдаться высыпания.
Эти признаки свидетельствуют о наличии в организме инфекции, поэтому следует незамедлительно обратиться к врачу и начать лечение.
Их дополняют более характерные симптомы инфекционного эндокардита у взрослых, которые свидетельствуют о развитии именно этого заболевания:
- артритные изменения суставов;
- поражение сердечных клапанов;
- тромбоз и закупорка крупных артерий;
- увеличение лимфоузлов;
- инфаркт почки и другие поражения;
- тремительно развивающаяся сердечная недостаточность;
- перикардит.
Данные симптомы эндокардита выявляются в ходе диагностических процедур.
Воспалительные заболевания сердца: симптомы
Клиническая картина воспалительного заболевания сердца зависит от того, какие ткани оказались задействованы в патологическом процессе: воспаление непосредственно сердечной мышцы (миокардит), воспаление внутренней оболочки сердца (эндокардит) или воспаление околосердечной сумки (перикардит). Общим симптомами могут быть длительные боли в сердце, одышка, сердцебиения, нередко (при инфекционном процессе), повышение температуры тела до фебрильных цифр. При первых же подозрениях на проблемы с сердцем на фоне любого инфекционного заболевания необходимо обратиться к Врач-кардиолог
. Некоторые формы воспалительных заболеваний сердца протекают остро и приводят к очень тяжелым последствиям.
Диагностика эндокардита
Квалифицированная диагностика инфекционного эндокардита – это целый комплекс обследований. Пациенту назначается программа кардиоскрининга, в которую входят:
- различные виды электрокардиограммы (суточное мониторирование, стресс-эхокардиография);
- УЗИ сердца и сосудов;
- компьютерная сфигмоманометрия.
Также применимы современные диагностические методы: кардиоритмография, допплерография. Обязательно проводятся анализы крови и посевы на стерильность – одни из важнейших обследований при инфекционном эндокардите.
Лечение эндокардита
На ранней стадии лечение инфекционного эндокардита заключается в антибактериальной терапии и поддержании сердца лекарствами. Если же септический эндокардит уже проявил себя значительными изменениями в тканях сердца (поражение клапанов, аорты, миокарда), возможно оперативное вмешательство.
- Антибактериальное лечение при симптомах эндокардита предусматривает использование современных антибиотиков (бензилпенициллин, пенициллины, амфотерицин и др.), вводимых внутривенно.
- Проводится пассивная иммунизация с целью нейтрализовать бактерии в организме. Для этого чаще всего используют внутривенно специальные антитоксические сыворотки (иммуноглобулин, гипериммунная плазма).
- Хирургическое вмешательство проводится в случаях, когда необходимо удалить очаги инфекции в тканях сердца и восстановить измененные болезнью сердечные структуры. Услуги кардиохирурга необходимы, если у пациента прогрессирует сердечная недостаточность, наблюдается тромбоэмболия сосудов и т.д.
Воспалительные заболевания сердца — миокардит
Миокардит — что это? Воспалительное поражение сердечной мышцы, которое проявляется нарушением сердечной деятельности (возбудимости, проводимости и сократимости). Чаще всего имеет вирусную природу (половина всех случаев миокардита). Заболеванию подвержены люди среднего возраста (30–40 лет, немного чаще — женщины). По происхождению миокардиты бывают:
- ревматические;
- инфекционные (вирусный, бактериальный и др.);
- аллергические (лекарственный, поствакцинальный, трансплантационный);
- при диффузных заболеваниях соединительной ткани;
- вследствие воздействия физических факторов (травмы, ожоги, воздействии ионизирующей радиации);
- идиопатический (невыясненной природы) миокардит Абрамова – Фидлера.
Течение миокардита может быть острым, подострым, хроническим (рецидивирующим).
Миокардит: симптомы и диагностика
Симптомы миокардита часто связаны с инфекционным заболеванием – ОРВИ, ангины, и т.п. (на фоне или вскоре после него). Наиболее часто встречающиеся признаки заболевания — недомогание, слабость, утомляемость, одышка, сердцебиение, нарушения ритма сердца, иногда — дискомфорт и боли в грудной клетке, редко — болезненность в суставах. При инфекционном миокардите обычно доминируют симптомы инфекционного заболевания (лихорадка, повышение температуры тела, общие признаки интоксикации). Начало миокардита может протекать бессимптомно, с субфебрильной или нормальной температурой, часто отмечаются сердцебиения, «перебои» в работе сердца, одышка. Степень выраженности симптомов зависит от распространенности и остроты воспалительного процесса. При отсутствии терапии будут нарастать признаки сердечной недостаточности. Необходимо срочно проконсультироваться с врачом-специалистом! Своевременно проведенные диагностические исследования (УЗИ сердца
,
ЭКГ
, рентгенография) могут выявить:
- увеличение размеров сердца;
- нарушения сердечного ритма (тахикардию, реже брадикардию, различные аритмии);
- нарушения внутрисердечной проводимости.
Диагностика миокардита часто требует комплексного подхода. Помимо физикального исследования, обычно используются:
- клинический и биохимический анализ крови;
- электрокардиографию
(ЭКГ); - эхокардиографию
(УЗИ сердца); - рентгенографию органов грудной клетки
; - изотопное исследование сердца;
- МРТ сердца;
- эндомиокардиальную биопсию;
- посевы крови и других биологических жидкостей;
- комплексное исследование иммунологических показателей.
Обратившись за помощью в клинику «Энерго», Вы получите возможность в одном месте пройти все необходимые для правильной диагностики воспалительных заболеваний сердца исследования. Записаться на прием в клинику «Энерго» можно через форму на сайте или по телефону, указанному на странице.
Как лечить миокардит?
Вылечить миокардит легкой степени, протекающий без осложнений, можно в амбулаторных условиях. При более тяжёлом течении требуется госпитализация, обязательный постельный режим, этиотропная, противовоспалительная и симптоматическая терапия. Этиотропная терапия — лечение инфекции, ставшей причиной миокардита (вирусной, бактериальной, грибковой и пр.), и поддерживающая терапия первичного заболевания (ревматизма, СКВ, тиреотоксикоза и т.д.).
Факторы риска развития миокардита
Развитие воспалительных заболеваний сердца провоцирует:
- снижение иммунитета;
- вирусные инфекции и острые инфекционные заболевания (ОРВИ, ангины);
- очаги хронической инфекции (кариес, тонзиллит);
- наследственная предрасположенность к воспалительным заболеваниям сердца;
- паразитарные и грибковые заболевания.