Введение
Определение
Резистентная гипертензия
Резистентная гипертензия — это повышение артериального давления (АД), требующее терапии более чем 3 препаратами (один из них диуретик).
- В официальном отчете Американской Кардиологической Ассоциации, опубликованном в 1988 году, определение расширили, включив пациентов, у которых АД, в конечном счёте, контролировалось, но требовалось 4 или более препарата, чтобы сделать это, т.н. «контролируемая резистентная гипертензия».
Рефрактерная гипертензия
- Термин «рефрактерная гипертензия» использовался с упоминанием о подгруппе пациентов с неэффективной антигипертензивной терапией в четырёх отдельных научных публикациях.
- В течение короткого отрезка времени между этими публикациями, определение рефрактерной гипертензии всё более раскрывалось.
- Термин использовался для определения артериальной гипертензии (АГ) у пациентов, с неэфффективной максимальной антигипертинзивной терапией. При первом использовании термина, рефрактерная гипертензия была определена, как неконтролируемая гипертензия при использовании 5 и более антигипертензивных препаратов из различных классов.
- Большинство недавних использований в литературе термина «рефрактерная гипертензия» подчеркивало неэффективность оптимального контроля давления крови 5 или более антигипертензивными препаратами, включая длительно действующие тиазидные диуретики и антагонистов минералкортикоидных рецепторов (МРА).
Эпидемиология
Резистентная гипертензия
- Сведения, полученные из поперечных исследований, сходятся в том, что резистентная гипертензия определяется исключительно по числу препаратов, необходимых для 10-20 % пациентов с АГ для ее коррекции.
- Например, в анализе исследований большой этнически-разнороднойкогорты в Соединенных Штатах, Sim с соавт. оценивали лиц, зарегистрированных в системе здравоохранения Южной Калифорнии. Более 470 тыс. человек были исследованы, из них по определению Американской Кардиологической Ассоциации 15,3 % имели резистентную гипертензию.
- Из 68045 пациентов, включенных в анализ, приблизительно 15% имели резистентную гипертензию (по определению Американской Кардиологической Ассоциации), т.е. АД > 140/90 мм рт. ст. при использовании 3 и более антигипертензивных препаратов, включая диуретики,
Длительные исследования показывают, что распространенность резистентной гипертензии резко увеличилась в несколько последних десятилетий.
- Используя сведения непрерывных Исследований Национального Здоровья и Питания Населения, Roberie и Elliot предположили, что распространенность явной резистентной гипертензии в Соединенных Штатах повысилась с 8,8% в 1988-1994 гг. до 14,5% в 1999-2004 гг., и до 20,7% в 2005-2008 гг.
- Быстрое увеличение предполагаемого уровня распространённости заставляет задуматься о том, что резистентная гипертензия может представлять собой один из быстро растущих видов гипертензии.
- Причина увеличения уровня резистентной гипертензии не совсем понятна, но нет сомнений в связи общих факторов риска развития АГ, таких как пожилой возраст,
- ожирение,
- хроническая болезнь почек (ХБП).
Рефрактерная гипертензия
- Среди четырёх ныне опубликованных исследований по рефрактерной гипертензии предположительный уровень распространенности этого состояния варьировал приблизительно от 5 до 30 %.
- В начальных изучения рефрактерной гипертензии ретроспективный анализ более чем 300 пациентов, проведенный Алабамским Университетом в Бирмингеме в клинике по изучению резистентной гипертензии показал, что приблизительно 10 % пациентов с достаточной терапией никогда не могли достичь контроля над давлением крови, несмотря на использование 5 или более антигипертензивных препаратов.
- Позднее, когда та же самая группа исследователей опубликовала проспективный анализ более чем 700 пациентов с резистентной гипертензией, в результате которого выяснилось, что только у 29 или приблизительно у 4 % была установлена рефрактерная гипертензия.
- Существуют важные различия между определениями рефрактерной гипертензии, которые давали разные исследования. Ранее, в ретроспективном анализе определение рефрактерной гипертензии было основано только на потребности в 5 и более антигипертензивных препаратов, без разделения используемых препаратов на классы. Позже, в проспективном анализе определение рефрактерной гипертензии стало более строгим и заключалось в нерегулярном приеме лекарств, объединяющих 5 и более препаратов, включающих хлорталидон и спиронолактон.
- В исследовании Modolo с соавт. рефрактерная гипертензия определялась только количеством препаратов, т.е. 5 и более. В поперечном анализе 116 человек с резистентной гипертензией, 31 % имел такое повышенное давление, которое не контролировалось 5 и более препаратами. Все рефрактерные пациенты получали диуретики и большинство получало спиронолактон (76%).
- Еще одно исследование рефрактерной гипертензии, представляло собой поперечную оценку участников исследования «Причины географических и этнических отличий в течение инсульта» (REGARDS), крупного (n=30239) когортного исследования. В этом анализе, рефрактерная гипертензия была определена как неконтролируемая гипертензия, несмотря на приём 5 или более различных классов препаратов. Использование диуретиков, включая конкретно хлорталидон и спиронолактон, было не обязательной частью определения. Частота рефрактерной гипертензии составляла 3,6 % от пациентов с резистентной гипертензией (не контролируется 3 или более препаратами или контролируется 4 и более препаратами) и 0,5% от всех пациентов с гипертензией. Все участники «Причин географических и этнических отличий в течение инсульта» (REGARDS), отнесенные к группе рефрактерной гипертензии, получали диуретики (любой из двух – гидрохлортиазид (ГХТЗ) или фуросемид), никто не получал хлорталидон и спиронолактон.
В настоящее время опубликованы исследования по рефрактерной гипертензии, определяющие её различную распространенность от низкой 5% до высокой 30% среди пациентов с истинной резистентной гипертензией.
Широкое расхождение, несомненно, связано ссущественными различиями в анализируемых когортах и определением рефрактерной гипертензии. По определению, прежде чем диагностировать рефрактерную гипертензию, необходимо использовать хлорталидон и спиронолактон.
Лечение резистентной артериальной гипертонии: новые перспективы
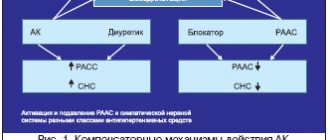
В фокусе внимания находится резистентная, или рефрактерная, артериальная гипертония (АГ) как одна из причин плохого контроля АД. Под резистентной АГ, в соответствии с рекомендациями РМОАГ/ВНОК [5], Европейского общества по АГ/Европейского общества кардиологов (ESH/ESC), а также Американской коллегии кардиологов (АСС) и Американской ассоциации сердца (AHA) [6,7], понимают превышение целевого уровня АД несмотря на лечение тремя гипотензивными препаратами, один из которых – диуретик. Резистентная АГ может быть контролируемой в том случае, если контроль АД достигается при назначении большего количества препаратов. В противном случае АГ является резистентной неконтролируемой. Также выделяют псевдорезистентную АГ, обусловленную неправильным измерением АД, низкой приверженностью к лечению и «офисным» повышением АД. В большинстве случаев резистентной является нераспознанная вторичная АГ: связанная с синдромом обструктивного апноэ во время сна (СОАС), первичным альдостеронизмом, феохромоцитомой, гиперкортицизмом, паренхиматозными заболеваниями почек, стенозом почечных артерий, часто плохо контролируемая АГ встречается при сахарном диабете. Кроме того, к резистентности могут приводить чрезмерное потребление соли, алкоголя и некоторые лекарства (нестероидные противовоспалительные препараты (НПВП), слабительные, амфетамины, производные эфедрина, эстрогенсодержащие оральные контрацептивы, лакрица, глюкокортикостероиды, эритропоэтины). Выраженность гипертензивного действия указанных средств индивидуальна, однако доказано, что его проявлению способствуют пожилой возраст, сахарный диабет, снижение почечной функции. Особой формой АГ является злокачественная гипертония. Злокачественная АГ характеризуется значительным повышением АД (более 180/120 мм рт.ст.) с развитием тяжелых изменений сосудистой стенки (фибриноидный некроз), что приводит к кровоизлияниям и/или отеку соска зрительного нерва, ишемии тканей и нарушению функции различных органов. Переход АГ в злокачественную возможен при всех ее формах, однако чаще это происходит у пациентов со вторичной или тяжелой АГ. При отсутствии эффективного лечения 50% пациентов умирают в течение первого года. Наличие злокачественной АГ оценивается как тяжелое неотложное состояние и требует снижения ДАД до 100–110 мм рт. ст. в течение 24 ч. Пациентам со злокачественной АГ показана трехкомпонентная гипотензивная терапия. Предикторами недостаточного контроля АД являются пожилой возраст (старше 75 лет), гипертрофия левого желудочка (ГЛЖ), ожирение (индекс массы тела более 30 кг/м2), высокое исходное АД (систолическое АД более 160 мм рт.ст.), хроническая почечная недостаточность (ХПН) с креатинином более 1,5 мг/дл, сахарный диабет, а также, по результатам исследования ALLHAT, принадлежность к негроидной расе и женский пол. Наряду с этим представляют несомненный интерес обнаруженные в исследовании ASCOT данные о снижении риска развития резистентности у больных, получающих лечение антагонистами кальция (АК) (амлодипином) с последующим присоединением ингибитора ангиотензинпревращающего фермента (иАПФ) периндоприла [8] (табл. 1). Способы преодоления резистентной АГ, рекомендованные для клинической практики Непременными условиями успешного лечения АГ являются снижение веса, ограничение потребления соли, употребления алкоголя, регулярные физические нагрузки умеренной интенсивности, диета с ограничением животных жиров и употреблением большого количества полиненасыщенных жиров, грубой клетчатки, овощей, фруктов (DASH–diet: Dietary Approaches to Stop Hypertension), по возможности, отмена препаратов, способствующих повышению АД или уменьшающих эффективность гипотензивной терапии, выявление и лечение вторичной АГ, а также наблюдение у специалиста по АГ. Очень важно, чтобы врач и пациент проявляли настойчивость в снижении повышенного АД и достижении его целевого уровня. Для достижения эффективного контроля АД от пациента требуется приверженность к лечению, а она во многом зависит от того, насколько добросовестно врач будет проводить разъяснительную работу и сможет убедить больного в необходимости лечиться. Зачастую АГ бывает формально признана резистентной, хотя средства фармакотерапии не выбраны, дозы препаратов не доведены до максимальных терапевтических, не использованы рациональные комбинации гипотензивных средств и т.д. Для наиболее эффективного лечения резистентной АГ целесообразно воздействие на разные звенья патогенеза. Огромное значение придается назначению блокаторов ренин–ангиотензин–альдостероновой системы (РААС). Доказана эффективность комбинации блокаторов РААС с АК как при гипо–, так и при гиперрениновой форме АГ за счет прямого и ренин–опосредованного механизма вазодилатации. При комбинированном применении препаратов этих групп потенцируются органопротективные эффекты (регресс ГЛЖ, протеинурии, антиишемическое, антиатеросклеротическое, натрийуретическое действие). Кроме того, при совместном назначении иАПФ либо блокатора рецепторов ангиотензина (БРА) с АК нейтрализуются контррегуляторные механизмы, снижающие эффективность каждого из препаратов в монотерапии: в противовес АК иАПФ и БРА подавляют активность РААС и симпатической нервной системы (СНС); в свою очередь АК усиливают экскрецию натрия, что повышает эффективность иАПФ/БРА. Благодаря этому частота таких нежелательных эффектов, как тахикардия и отеки голеней, значительно снижается. Большая эффективность комбинации АК с блокаторами РААС в снижении АД и предотвращении осложнений АГ подтверждается результатами как российских, так и зарубежных исследований: АSCOT–BPLA (комбинация АК + иАПФ сравнивалась с комбинацией β–блокатор + диуретик), ACCOMPLISH (комбинация иАПФ + АК сравнивалась с комбинаций иАПФ + диуретик), HAMLET (комбинация амлодипина и лизиноприла сравнивалась с монотерапией), EMEA (комбинации амлодипина с валсартаном 5/160 мг и 10/160 мг сравнивались с монотерапией валсартаном 160 мг). В российском исследовании ПРОРЫВ [9] была показана высокая эффективность фиксированной комбинации периндоприла с амлодипином у 4115 больных с неконтролируемой АГ в достижении целевого уровня АД (рис. 1). При резистентной и тяжелой АГ с целью повышения приверженности к лечению и экономической эффективности рекомендованы их фиксированные комбинации. В то же время двойная блокада РААС (одновременное назначение иАПФ и БРА или присоединение к одному из них прямого ингибитора ренина алискирена) себя не оправдала из–за развития нежелательных эффектов. В большинство схем лечения резистентной АГ входят мочегонные средства. Учитывая имеющуюся у больных с резистентной АГ скрытую (как правило, отеки отсутствуют) перегрузку объемом даже при лечении мочегонными в стандартных дозах, последние должны назначаться в максимально переносимой/эффективной дозе. Доза диуретика постепенно увеличивается до максимально допустимой. В этой ситуации необходимо помнить о возможности появления клинических признаков чрезмерной дегидратации, таких как слабость, ортостатическая гипотония, снижение перфузии тканей (повышение креатина, не объясняющееся другими причинами). Чрезмерная терапия мочегонными препаратами может приводить к избыточному выведению натрия с последующей активацией РААС и повышением АД. Начинать лечение мочегонными препаратами рекомендуют с тиазидных диуретиков (гидрохлоротиазид, в некоторых случаях – сульфонамидное производное тиазидов индапамид, а также препараты, отсутствующие на территории РФ: бендрофлуазид, хлорталидон, метолазон). Наиболее эффективно в этой группе снижает АД хлорталидон (доступный на территории РФ только в виде фиксированных комбинаций с атенололом). Хлорталидон имеет большую продолжительность действия и более выраженный гипотензивный эффект, чем гидрохлоротиазид, его назначение в меньших дозировках приводило к сопоставимому снижению АД. В исследовании ALLHAT показана способность хлорталидона снижать риск сосудистых событий. При ХПН могут применяться петлевые диуретики (фуросемид, торасемид, буметанид, этакриновая кислота). За рубежом при АГ в сочетании с ХПН преимущество имеет тиазидное производное метолазон и его усовершенствованная формула микрокс в дозе 0,5–1,0 мг/сут. (в настоящее время не продается в РФ), однако его недостатком является вариабельная абсорбция. Основным побочным эффектом мочегонных средств является гипокалиемия, поэтому в течение первых 10–14 дней, пока не установится новый баланс калия, необходим контроль его уровня в плазме. Полезны могут быть калийсберегающие агенты и их комбинации с тиазидами. В рекомендациях РМОАГ/ВНОК по диагностике и лечению АГ [4] говорится о целесообразности назначения при резистентной АГ тройной полнодозовой гипотензивной терапии; рациональными признаны следующие трехкомпонентные комбинации: иАПФ + дигидропиридиновый АК + β–адреноблокаторы (β–АБ); БРА + дигидропиридиновый АК + β–АБ; иАПФ + АК + диуретик; БРА + АК + диуретик; иАПФ + диуретик + β–АБ; БРА + диуретик + β–АБ; дигидропиридиновый АК + диуретик + β–АБ. Из представленных комбинация блокатора РААС с АК и мочегонным средством представляется наиболее эффективной, именно ее рекомендуют и американские эксперты (резистентная АГ). При наличии специальных показаний (ИБС, ХСН) оправданно присоединение к этой схеме β–блокатора, предпочтительно с вазодилатирующими свойствами. В последние годы возобновился интерес к антагонистам альдостерона, давно известному спиронолактону и относительно недавно вошедшему в клиническую практику селективному антагонисту минералокортикоидных рецепторов эплеренону. При резистентной АГ эффективность антагонистов альдостерона доказана вне зависимости от наличия или отсутствия гиперальдостеронизма. В одном из крупнейших исследований – ASCOT – был проведен анализ, включивший 1411 человек, соответствующих критериям резистентности [10]. К проводимой терапии у больных, не достигших целевого уровня АД, присоединялся спиронолактон в средней дозе 25 мг/сут., который способствовал дополнительному снижению систолического/диастолического АД на 22/10 мм рт.ст. через год лечения (рис. 2). В этом и в ряде других исследований показано увеличение риска гиперкалиемии у больных с ХПН, а также при одновременном назначении других препаратов, повышающих концентрацию калия в плазме: иАПФ или БРА, НПВП. В недавно завершившемся рандомизированном исследовании ASPIRANT (включено 117 больных) спиронолактон или плацебо были присоединены к терапии в среднем четырьмя гипотензивными средствами, была показана эффективность спиронолактона в снижении систолического АД при резистентной АГ. В другом рандомизированном исследовании 42 пациента с избыточным весом или ожирением в дополнение к исходной терапии, включавшей БРА или иАПФ и еще 3 препарата, получали иАПФ или БРА либо спиронолактон (25–50 мг/сут.); было показано, что при резистентной АГ эффект спиронолактона выше, чем при двойной блокаде РААС. Эплеренон отличается значительно более редкой частотой развития таких нежелательных эффектов спиронолактона, как гиперкалиемия и гинекомастия. Эффективность эплеренона при резистентной АГ изучалась в одном из исследований, включавшем 52 больных с резистентной АГ, избыточным весом/ожирением и разным состоянием почечной функции. При добавлении эплеренона в дозе 50–100 мг/сут. к терапии от 3 до 7 гипотензивных средств (в том числе иАПФ или БРА) происходило достоверное снижение АД вне зависимости от исходного уровня альдостерона и активности ренина плазмы, а также уменьшалась потребность в назначении других средств, снижающих АД. Только у 2 пациентов было в общей сложности 3 случая умеренной гиперкалиемии (калий плазмы менее 6, но более 5,5 ммоль/л). Эти исследования, несмотря на относительно небольшую выборку участников, свидетельствуют о целесообразности включения спиронолактона или эплеренона в схему лечения больных с резистентной АГ. Имеются данные об эффективности при резистентной АГ сочетания амилорида с гидрохлоротиазидом, особенно при невозможности применения антагонистов минералокортикоидных рецепторов. В резерве фармакотерапии препараты, назначение которых ограничено побочными эффектами и требует врачебного контроля: гипотензивные средства центрального действия (клонидин, гуанфацин), миотропные периферические вазодилататоры (гидралазин, миноксидил, отсутствующие на данный момент на территории РФ), симпатолитики (резерпин, гуанетидин), α1–блокаторы (доксазозин, теразозин). Новые гипотензивные средства в стадии разработки В последнее десятилетие предпринимаются попытки поиска новых фармакологических мишеней и воздействия на них с целью более эффективного снижения АД и уменьшения частоты побочных эффектов. С этой точки зрения привлекательной представлялась блокада РААС на уровне ренина, однако преимущество его прямого ингибитора алискирена при резистентной артериальной гипертонии не доказано. Кроме того, существуют данные о негативных эффектах алискирена в определенных группах больных. Так, по результатам исследования ALTITUDE одновременное назначение прямого ингибитора ренина алискирена с иАПФ или БРА у больных с сахарным диабетом 2 типа приводит к нарушению почечной функции, гипотонии и гиперкалиемии. Также на фоне лечения этой комбинацией было отмечено увеличение смертности и частоты инсультов, в связи с чем исследование было досрочно прекращено. Одновременное назначение алискирена с иАПФ или БРА при сахарном диабете и почечной недостаточности (скорость клубочковой фильтрации (СКФ) – менее 60 мл/мин.) не рекомендуется. В настоящее время можно выделить следующие классы новых фармакологических средств на разных этапах разработки: препараты, воздействующие на РААС (блокаторы рецептора проренина, двойные и тройные ингибиторы вазопептидаз – АПФ, неприлизина, эндотелинпревращающего фактора; антагонисты альдостероновой синтазы; полимеры – ионообменники калия, созданные для предотвращения гиперкалиемии 39; антагонисты рецепторов альдостерона, отличные от спиронолактона и эплеренона, например нестероидные гибриды со свойствами антагонистов кальция; препараты, воздействующие на систему реналазы); селективные антагонисты рецепторов эндотелина–А; донаторы оксида азота (препараты, высвобождающие оксид азота: нитрозил–кобаламид, NO–высвобождающие гибриды лозартана и телмисартана, непептидные нитропроизводные ингибиторов ренина, напроксинод – донатор NO со свойствами НПВП (для лечения АГ с артритом); агонисты натрийуретических пептидов, агонисты рецепторов к АТ–2 типа 2. В лабораторных экспериментах на крысах показана эффективность методов генетической терапии с внедрением на вирусных и других векторах генов, ответственных за экспрессию веществ, способствующих снижению АД. Также ведется работа над созданием вакцины против АТ–2. Интерес представляют молекулы, направленные на борьбу с клеточным старением, т.е. ингибиторы (аминогуанидин, пиридоксамин) и лидазы (алагебриум и структурные аналоги пиридина) конечных продуктов гликирования, которые способствуют повышению жесткости артерий и формированию изолированной систолической АГ. Эндоваскулярное лечение резистентной АГ Наличие резистентной АГ стимулирует разработку методов нелекарственного воздействия на патогенетические механизмы заболевания. Перспективным методом в лечении резистентной артериальной гипертонии в настоящее время считается катетерная аблация симпатического сплетения почечной артерии, или почечная денервация [11,12]. В начале XX века R. Smithwick, возглавлявший отделение хирургии в Бостонском университете (США), предложил операцию для лечения АГ, во время которой выполнялась билатеральная люмбодорсальная симпатэктомия и спланхникэктомия с резекцией симпатических ганглиев в нижнегрудном отделе. Частым осложнением была симптоматическая ортостатическая гипотензия, но, несмотря на это, многие пациенты с тяжелой АГ чувствовали себя после вмешательства лучше. В дальнейшем данный хирургический метод не получил развития ввиду появления гипотензивных средств. Сегодня метод Smithwick переживает свое второе рождение. Патофизиология. При АГ практически любого генеза имеет место повышение тонуса симпатической нервной системы (СНС). Гиперактивация СНС и прогрессирующее повышение АД взаимно усиливают друг друга и участвуют в формировании порочного круга. Повышенная активность СНС больше всего затрагивает почки. При гиперактивации СНС в почке происходит вазоконстрикция, снижаются кровоток и фильтрация, усиливается секреция ренина, увеличивается реабсорбция натрия и воды. Афферентная импульсация от почек по афферентным нервным волокнам поступает сначала в боковые рога спинного мозга, а затем в сосудистый центр в центральной нервной системе, способствуя повышению АД. Она усиливается при растяжении механорецепторов, ишемии почек, под воздействием гипоксии. В эксперименте показано, что электрическая стимуляция афферентных нервных волокон почек повышает АД и вызывает спазм сосудов. Денервация этих волокон, наоборот, способствует снижению АД. Процедура. Система для денервации Medtronic Ardian Sympicity Catheter System состоит из генератора радиочастотных волн и одноразового катетера с механизмом управления кончиком. Генератор вырабатывает радиочастотные волны мощностью 5–8 Вт и постоянно контролирует температуру и импеданс на кончике катетера. При превышении или недостижении необходимых параметров либо через 2 мин. эффективного воздействия система автоматически отключается. Кончик катетера представляет собой платиновоиридиевый электрод, он рентгеноконтрастен и благодаря этому выполняет также функцию метки при катетеризации. При эндоваскулярной почечной денервации после ангиографии почечной артерии в ее устье устанавливается направляющий катетер 6F, затем под ангиографическим контролем катетер для радиочастотной аблации (РЧА) подводится до уровня бифуркации и подключается к генератору (рис. 3). После этого с помощью специального механизма, позволяющего ориентировать катетер для РЧА в нужном направлении, он продвигается проксимально (от почки к аорте). При этом выполняется 4–6 радиочастотных воздействий по 2 мин. с шагом не менее 5 мм и углом вращения 45° по окружности сосуда. Катетер воздействует на симпатические волокна через всю толщу почечной артерии. Аблация приводит к определенному повреждению эндотелия, однако пока по результатам контрольных ангиограмм не выявлено клинически значимых последствий этого повреждения. В литературе встречаются попытки объяснить отсутствие значимого повреждения эндотелия его меньшей чувствительностью к выбранному воздействию, а также охлаждающим действием крови, омывающей внутреннюю стенку артерии. Доказательная база В настоящее время эффективность и безопасность эндоваскулярной денервации почек активно изучается во всем мире. К данному моменту завершены исследования Symplicity HTN–1,2; проводятся исследования HTN–3 и Duration of Renal Sympathetic Activation and Hypertension [12–14]. В проведенных исследованиях показана эффективность метода в снижении АД при резистентной АГ, а также его безопасность. Максимальная длительность наблюдения составила 2 года, к концу этого срока снижение АД составило в среднем около 30/10 мм рт.ст. По данным Symplicity HTN–1, после почечной денервации уровень САД ниже 140 мм рт.ст. был достигнут у 39%, ниже 160 мм рт.ст. – у 82% оперированных. При высокой эффективности процедуры осложнения имели место в небольшом количестве случаев и успешно излечивались. Среди осложнений была 1 псевдоаневризма, 1 диссекция, успешно устраненная стентированием, 1 эпизод послеоперационной гипотензии, 1 случай инфекции мочевых путей, 1 случай болевого синдрома в спине, у 7 человек из 52 оперированных во время процедуры отмечалась преходящая брадикардия, в части случаев потребовавшая введения атропина, у 2 больных имело место усугубление атеросклероза почечной артерии, эндоваскулярного лечения не потребовалось (в частности, в HTN –1 был случай прогрессирования стеноза почечных артерий в сегменте, удаленном от места воздействия). Случаев нарушения азотовыделительной функции почек не было (оценивались через 6 мес. по креатинину, СКФ, цистатину С). Впервые в России эта процедура была осуществлена в 2011 г. в РКНПК. Опубликованы данные о 5 успешно проведенных операциях [15]. При контроле через 1 мес. сохранялся стойкий эффект от процедуры, АД продолжало снижаться, побочных эффектов, а также ранних и поздних осложнений не отмечалось. Симпатическая денервация почечных артерий пока является недостаточно изученным методом, поэтому эксперты ESH/ESC рекомендует прибегать к ней только при наличии строгих показаний. Показанием к процедуре является резистентная неконтролируемая эссенциальная АГ (систолическое АД при измерении у врача и самоконтроле – более 160 мм рт.ст. или 150 мм рт.ст. – у больных сахарным диабетом), несмотря на проводимое специалистом по АГ трехкомпонентное лечение и удовлетворительную приверженность пациента к лечению. Противопоказаниями к процедуре являются: почечные артерии менее 4 мм в диаметре и менее 20 мм в длину, манипуляции на почечных артериях (ангиопластика, стентирование) в анамнезе, стеноз почечных артерий более 50%, почечная недостаточность (СКФ менее 45 мл/мин./1,75 м2), сосудистые события (ИМ, эпизод нестабильной стенокардии, транзиторная ишемическая атака, инсульт) менее 6 мес. до процедуры, любая вторичная форма АГ. Метод электрической стимуляции барорецепторов каротидного синуса Еще один метод воздействия на активность СНС на стадии клинических испытаний заключается в электрической стимуляции барорецепторов каротидного синуса (БКС) с целью рефлекторного снижения АД. БКС, расположенные в области бифуркации сонных артерий, принимают участие в регуляции АД. При его повышении происходит растяжение рецепторов, далее импульсация от них поступает в сосудистый центр головного мозга, что приводит к снижению АД. При АГ чувствительность барорецепторов снижается. Схема БКС предсталена на рисунке 4. При электрической стимуляции электроды стимулятора каротидного синуса Rheos (CVRx, Minneapolis, MN, USA) подводятся к сонным артериям и соединяются с генератором, который вшивается под кожу передней грудной стенки. Имплантация стимулятора проводится сосудистым хирургом, кардио– или нейрохирургом. Перед внедрением электрода в толщу стенки сонной артерии проводится выбор наиболее чувствительной к стимуляции зоны каротидного синуса: генератор подает на электрод небольшой разряд (для терапии ВАТ используется ток под напряжением 1–6 В); через 30 с после воздействия на данный участок каротидного синуса измеряется АД. Электрод оставляется в том месте, где снижение АД в ответ на разряд заданной силы максимально. Сила подаваемого на электроды разряда регулируется компьютерной программой, по аналогии с тем, как это происходит при настройке электрокардиостимулятора; генератор и компьютер находятся в радиочастотном сопряжении. Данные первого рандомизированного двойного слепого плацебо–контролируемого исследования по оценке клинической эффективности стимуляции БКС – Rheos Pivotal Trial опубликованы в 2011 г. [16]. В ходе исследования у 265 пациентов с резистентной АГ была показана эффективность метода стимуляции БКС. При контроле через год снижение систолического АД составило в среднем 35 мм рт.ст.; у половины испытуемых были достигнуты значения АД менее 140 мм рт.ст. Максимальная длительность наблюдения составила 53 мес., в течение всего этого срока гипотензивный эффект сохранялся. Основные осложнения были связаны с инфицированием операционной раны и повреждением нерва, однако их частота была значительно меньше, чем при хорошо отработанной операции эндартерэктомии, и в большинстве случаев эти осложнения были обратимыми, а резидуальные эффекты – незначительными. Важно отметить, что для достижения полного эффекта необходимо продолжительное время, т.к. перестройка сосудистого тонуса является по своей природе длительным процессом. В другом недавно опубликованном исследовании Barostim neo (30 пациентов) изучался прибор 2–го поколения, значительно меньших размеров для односторонней стимуляции. Барорецепторная стимуляция показала свою эффективность даже у тех 6 больных, у которых в анамнезе были ранее выполненная безуспешная катетерная денервация почечных артерий и более высокий исходный уровень АД [17]. Полученные результаты свидетельствуют о перспективности метода. В настоящее время продолжается его совершенствование. Возможно, в недалеком будущем начнется внедрение электрической стимуляции БКС в клиническую практику. В РФ клинические испытания данного метода не проводились. Таким образом, создается впечатление, что в арсенале специалистов по АГ скоро появятся новые способы нелекарственного лечения – денервация почечных артерий и электрическая стимуляция БКС. Помимо оценки эффективности этих методов остаются неясными разные аспекты лечения: предикторы успеха и критерии эффективности процедур, длительность эффекта, возможность повреждения эндотелия сосудов, риск развития нежелательных эффектов. Тем не менее успех их первых клинических испытаний позволяет рассчитывать на их применение в ближайшем будущем. Процедуры и аппаратные методы лечения АГ на этапе научной разработки Интерес представляет метод нейроваскулярной декомпрессии ствола мозга. Есть данные о том, что повышенное АД может быть связано с его сдавлением извитыми артериями, в основном задней нижней мозжечковой артерией. В небольших работах (рандомизированные исследования в этой области еще не проводились) отмечено стойкое снижение АД в результате хирургической декомпрессии мозга, однако, в соответствии с данными Norman Kaplan, не любая извитость артерий патогенетически обусловлена АГ и хирургическая декомпрессия помогает не всем больным с АГ. Пока неизвестно, как определить, связана ли АГ у конкретного больного с нейроваскулярной компрессией, но описаны синдромы, при которых эта связь достоверно существует (брахидактилия, гипертония, нейроваскулярная компрессия). Замечено, что глубокая стимуляция головного мозга, используемая при синдроме хронической боли, болезни Паркинсона и др., может приводить к снижению АД при сопутствующей АГ, но пока она не применяется в клинической практике. Обсуждается также возможность разработки нового метода лечения АГ с помощью аппаратного контроля функции дыхания, основанного на связи дыхательного и сосудодвигательного центров. Заключение Эффективное лечение АГ относится к приоритетным направлениям в медицине. «Преодоление резистентности» при лечении больных с АГ во многом базируется на соблюдении всех рекомендуемых принципов ведения данной категории пациентов, включая рациональный подбор комбинированной терапии. В случаях истинной резистентности к терапии существуют методики лечения с помощью аппаратов, позволяющих достичь контроля АД с приемлемой степенью безопасности.
Литература 1. Kearney P.M., Whelton M., Reynolds K. et al. Global burden of hypertension: analysis of worldwide data // Lancet. 2005. Vol. 365. P. 217–233. 2. Guidelines for the management of arterial hypertension. The Task Force for the Management of Arterial Hypertension of the European Society of Hypertension (ESH) and of the European Society of Cardiology (ESC) // Eur. Heart J. 2007. Vol. 28. P. 1462–1536. 3. Оганов Р.Г., Тимофеева Т.Н., Колтунов И.Е. и др. Эпидемиология артериальной гипертонии в России. Результаты федерального мониторинга 2003–2010 гг. // Кардиоваск. терапия и профилактика. – 2011. – Т. 10(1). – С. 8–12. 4. Российское медицинское общество по артериальной гипертонии (РМОАГ)/Всероссийское научное общество кардиологов (ВНОК). Диагностика и лечение артериальной гипертензии. Российские рекомендации (четвертый пересмотр) // Системные гипертензии. – 2010. – № 3. – С. 5–26. 5. The 7th report of the Joint National Committee on prevention, detection, evaluation, and treatment of high blood pressure // JAMA. 2003. Vol. 289. P. 2560–2572. 6. Calhoun D.A., Jones D., Textor S. et al. Resistant hypertension: diagnosis, evaluation, and treatment. A scientific statement from the American Heart Association Professional Education Committee of the Council for High Blood Pressure Research // Hypertension. 2008. Vol. 51. P. 1403. 7. Acelajado M.C., Pisoni R., Dudenbostel T. et al. Refractory hypertension: definition, prevalence, and patient characteristics // J. Clin. Hypertens. (Greenwich). 2012. Vol. 14(1). P. 7–12. 8. Gupta A.K., Nasothimioua E.G., Changa C.L. et al. Baseline predictors of resistant hypertension in the Anglo–Scandinavian Cardiac Outcome Trial (ASCOT): a risk score to identify those at high–risk // J. Hypertens. 2011. Vol. 29. 9. Карпов Ю.А., Деев А.Д. от имени врачей–участников программы ПРОРЫВ. Неконтролируемая АГ – новые возможности в решении проблемы повышения эффективности лечения // Кардиология. – 2012. – № 2. – С. 29–35. 10. Chapman N., Dobson J., Wilson S. et al. Anglo–Scandinavian Cardiac Outcomes Trial Investigators. Effect of spironolactone on blood pressure in subjects with resistant hypertension // Нypertens. 2007. Vol. 49. P. 839–845. 11. Schmieder R.E., Redon J., Grassi G. et al. ESH Position Paper: renal denervation – an interventional therapy of resistant hypertension // J. Hypertens. 2012. Vol. 30(5). 12. Krum H., Schlaich M., Whitbourn R. et al. Catheter–based renal sympathetic denervation for resistant hypertension: a multicentre safety and proof–of–principle cohort study //Lancet. 2009. Vol. 373. P. 1275–1281. 13. Symplicity HTN–1 Investigators. Catheter–based renal sympathetic denervation for resistant hypertension: durability of blood pressure reduction out to 24 months // Hypertens. 2011. Vol. 57. P. 911–917. 14. Symplicity HTN–2 Investigators. Renal sympathetic denervation in patients with treatment–resistant hypertension (The Symplicity HTN–2 Trial): a randomized controlled trial // Lancet. 2010. Vol. 376. P. 1903–1909. 15. Данилов Н.М., Матчин Ю.Г., Чазова И.Е. Эндоваскулярная радиочастотная денервация почечных артерий – инновационный метод лечения рефрактерной артериальной гипертонии. Первый опыт в России // Ангиол. и сосуд. Хирургия. – 2012. – № 18(1). – С. 51–56. 16. Burke S.L., Evans R.G. et al. Levels of renal and extrarenal sympathetic drive in angiotensin–2–induced hypertension // Hypertens. 2008. Vol. 51. P. 878–883. 17. Bisognano J.D., Bakris G., Nadim M.K. et al. Baroreflex activation therapy lowers blood pressure in patients with resistant hypertension: results from the double–blind, randomized, placebo–controlled rheos pivotal trial // JACC. 2011. Vol. 58. P. 765.
Видимость против истины
Резистентная гипертензия
- Оценка уровня распространенности резистентной гипертензии основывается на вышесказанном и базируется исключительно на уровне клинического измерения АД и количестве прописанных антигипертензивных медикаментов.
- Не берутся в расчет общие причины так называемой псевдотерапевтической резистентности, включающей эффект «белого халата»,
- низкую приверженность к терапии,
- неполное соблюдение терапевтического режима.
- Коррекция этих факторов приведёт к уменьшению оцениваемого уровня гипертензии и к лучшей приблизительной оценке частоты «правдивой» резистентной гипертензии.
- Например, в исследовании de la Serra с соавт. обсуждалось, что в анализе испанского Реестра амбулаторного мониторинга АД учитывались отдельные факторы риска. Примечательно, что почти 38% пациентов с диагностированной резистентной гипертензией имели гипертензию «белого халата» (т.е. АД повышалось в клинике, но контролировалось вне клиники).
- Например, Jung с соавт. недавно сообщили, что из 76 пациентов, направленных в специальную клинику резистентной гипертензии, 53 % не регулярно принимали своих антигипертензивные препараты (данные были получены на основании анализов мочи и крови с определением соответствующих метаболитов препаратов). Как выяснилось, из этих пациентов, с низкой приверженностью к лечению, 30% не принимали ни одного препарата.
- В оценке более 200 клинических общественных организаций на юго-востоке Соединенных Штатов, Egan с соавт. выявили 44684 пациента, у которых АД оставалось неконтролируемым, несмотря на то, что им было прописано 3 и более антигипертензивных препарата.
- Авторы сделали ретроспективную оценку пациентов, которые были выбраны полностью рандомно, в многопрофильном исследовании, направленном на оценку клинической неэффективности терапии либо контроля кровяного давления.
- 91% пациентов получал диуретики (либо ГХТЗ, либо фуросемид), никто не получал хлорталидон и антагонистов минералкортикоидных рецепторов.
В целом, данные Grigoryan и других недавних исследований показывают, что частота истинной резистентной гипертензии, вероятно, меньше чем 50% от частоты диагностируемой резистентной гипертензии.
Рефрактерная гипертензия
- Определение диагностируемой, в сравнении с истинной рефрактерной гипертензией, пока ещё систематически не проработано.
- Строгие определения приверженности терапии базируются на измерении уровней лекарственных препаратов в сыворотке крови и моче.
- Возможно, распространенность не приверженцев терапии среди пациентов с рефрактерной гипертензией будет выше, чем при резистентной гипертензии.
- Два из опубликованных исследования по рефрактерной гипертензии сообщают об эффекте «белого халата», установленном при 24-часовом амбулаторном мониторировании АД. Modolo с соавт. говорят, что пациенты с рефрактерной гипертензией имели, возможно, более заметный «белый эффект» (≥20/10 мм рт. ст. при сравнении уровней амбулаторного и офисного кровяных давлений), чем пациенты с контролируемой или неконтролируемой резистентной гипертензией, но не имеется точно определенного числа или процентного соотношения пациентов с рефрактерной гипертензией.
- Dudenbostel с соавт. в своём исследовании сообщают, что за 24-часа амбулаторного мониторирования уровни АД были значительно выше у пациентов с рефрактерной гипертензией, в сравнении с контролируемой резистентной, но без сообщения о степени эффекта «белого халата» или его распространенности.
Таким образом, пока множество исследований показывают, что причины псевдорезистентности общие у пациентов с резистентной и рефрактерной гипертензией, однако степень, с которой эти самые факторы обнаруживаются у пациентов с рефрактерной гипертензией, всё ещё не определена.
Резистентная артериальная гипертензия – возможные пути преодоления проблемы
Конради А.О. выступила с докладом на Интернет конгрессе.
00:00
Григорий Павлович Арутюнов, доктор медицинских наук, профессор:
— Мы передаем слово Александре Олеговне.
Александра Олеговна Конради, доктор медицинских наук, профессор:
— Я рада приветствовать вас из морозного Петербурга.
Тема моего сегодняшнего выступления «Резистентная артериальная гипертензия». Сегодня мы традиционно стали заниматься этой проблемой. Постараемся поделиться с нашими слушателями программы современными представлениями по резистентной гипертонии.
Короткий план. Сегодня мы обсудим вопрос, что мы подразумеваем под понятием резистентной гипертонии, как часто она встречается, каковы ее причины, как ее реально выявить и как реально лечить.
Согласно последнему определению (с 2007-го года не выходило каких-то обновлений) под резистентной гипертензией (или рефрактерной к терапии) мы можем понимать такое состояние, когда лечение пациента включает изменение образа жизни и назначение не менее трех антигипертензивных препаратов в адекватных дозах. Но при этом систолическое и/или диастолическое артериальное давление (АД) не снижается должным образом.
В этом определении есть два достаточно важных момента, а именно о трех лекарственных препаратах. В Европейских рекомендациях не оговаривается, каких именно. Понятие «адекватной дозы» растяжимое. В данном случае, по-видимому, следует подразумевать большую полную терапевтическую дозу препарата. Если препарат недодозированный, то мы не можем считать такого больного резистентным.
Американцы всегда идут немножко дальше, поэтому в их рекомендациях имеются некоторые примечания. Препараты должны использоваться в рациональных рекомендациях, но включать в свой состав диуретики. Здесь уже становится более понятным, в каком случае, если есть три препарата, мы можем считать пациента резистентным к терапии.
Снижение АД необходимо до целевого уровня. Для всех больных – это 140 и 90. Для больных высокого риска – это 130 и 80. Изолированная артериальная гипертензия (АГ) – это, как минимум, меньше 160-ти. Должно быть соблюдено условие реального приема препаратов, то есть больные должны быть привержены к лечению.
Согласно современным данным, что мы можем сказать о распространенности АГ и ее контроле. Несмотря на большие наши государственные вложения и реализацию федеральных программ (по борьбе с АГ, социально значимыми заболеваниями), все равно сегодня доля больных, которые имеют должный уровень АД в процессе терапии, чуть более превышает 20% по самым оптимистичным прогнозам.
02:47
Неконтролируемая гипертония не означает еще резистентную. Подумаем, сколько таких пациентов сегодня в мире.
Если мы представим, согласно данным о распространенности, что 40% жителей России (взрослого населения) страдают повышением АД, то это примерно 60 миллионов человек, проживающих на территории Российской Федерации. Примерно 20 миллионов в России не знают, что у них повышенное АД. Только 12 миллионов получают лечение. Из них только 6-7 миллионов людей имеют целевой уровень АД. Если мы говорим о больных с сахарным диабетом, то это еще меньше.
Таким образом, по самым скромных подсчетам около 6-7 миллионов больных, ходящих по улице и ходящих на наш прием сегодня, имеют неконтролируемый уровень АД по различным причинам.
Неконтролируемый уровень АД даже у больных, получающих лечение, всегда резистентен с проводимой терапией. Очень часто это, к сожалению, низкая приверженность и наш не совсем адекватный подбор лечения.
Мы проанализировали обычную среднестатистическую Петербургскую поликлинику в случайной выборке пациентов. Обратили внимание, что на сегодняшний день на стандартном терапевтическом участке примерно 63 – 64% пациентов имеют неконтролируемый уровень АД, несмотря на то, что регулярно посещают своего врача.
Если посмотрим на тех пациентов, которые находились на стационаре и получали лечение, при выписке имели целевой уровень АД, то эффект ускользает через какое-то время по различным причинам. Практически те же самые 60% находятся вне целевых уровней АД. Примерно у 2/3 пациентов эта проблема касается и после стационарного подбора терапии.
Таким образом, это тоже не дает существенного прогресса.
В чем причина. Отчасти это может быть связано с тем, что мы переоцениваем свои собственные возможности. Мы провели большой опрос среди врачей Санкт-Петербурга, Иркутска, Ленинградской области и других регионов. Как они сами оценивают результаты своего лечения. В частности, доля больных, которые реально достигают целевого уровня АД.
05:06
Сегодня мы можем видеть, что большинство врачей считают, что у них до 50 – 60% пациентов имеют целевой уровень АД. На самом деле в реальной ситуации это примерно 5-10% пациентов. Эта переоценка наших возможностей приводит к тому, что мы не долечиваем реально наших пациентов.
По современным данным истинная резистентность к терапии встречается не так часто – от 1-го до 11% в специализированных отделениях. Не более чем в 5% среди всей популяции больных АГ. Чаще она встречается у больных, имеющих тяжелые органные поражения, у больных со значимой гипертрофией левого желудочка, с поражением глазного дна, почек.
Ее распространенность нарастает с возрастом. Чаще всего наблюдается у больных с диабетом (СД) и метаболическим синдромом (МС).
Любое органное поражение (будь то гипертрофия левого желудочка, утолщение комплекса интима медиа, наличие бляшек в сонных артериях, выраженная ретинопатия) чаще встречается у больных, имеющих резистентность к терапии, чем у среднестатистического больного с повышением АД.
Эта проблема, к сожалению, будет актуализироваться еще больше. Ожидается увеличение продолжительности жизни населения. Данные по США и по всему миру. Мы ожидаем увеличение доли лиц, которым будет старше 60-ти лет. Благодаря успехам здравоохранения, продолжительность жизни в России тоже нарастает. Особенно пожилое население в Петербурге, где мы трудимся.
Проблема пожилого возраста становится актуальной. Таких больных все больше. Практически любой врач знает, что достичь целевого уровня АД у пожилого человека сложнее.
Если посмотрим статистические данные, то обращаем внимание, что с возрастом нарастает распространенность изолированной систолической АГ и доля больных, имеющих недостаточный контроль АД.
Такая же проблема связана с ростом распространенности ожирения и СД. США подсчитали ожидаемое увеличение роста распространенности ожирения. С 1991-го по 2001-й год почти в 2 раза увеличилась распространенность и того и другого состояния в США.
То же касается ожидаемой частоты СД, распространенность которого считается, что возрастет, чуть ли не в 25 раз к 2005-му году. Мы хорошо знаем, что снизить АД тяжело.
07:41
Если посмотреть на все крупные рандомизированные исследования, то систолическое АД вообще редко снижается ниже уровня 140, установленного как целевой уровень АД. Но если мы выделим больных с СД, для которых целевой уровень давления является 130, то ни одно из исследований, на которые мы ссылаемся, когда обсуждаем вопрос антигипертензивной терапии, вообще не достигло этого уровня среднестатистических популяций.
Связано это именно с тем, что вылечить такого пациента до целевого уровня крайне тяжело. Организм больного СД упорно сопротивляется назначаемой ему терапии.
Сегодня мы должны констатировать тот факт, что распространенность АГ, резистентной к терапии, будет только расти. Это связано с тем, что мы имеем дело с:
- — стареющей популяцией;
- — ростом распространенности ожирения;
- — снижением физической активности;
- — недостаточным вниманием вообще к систолическому АД;
- — ростом потребления разного рода эндогенных стимуляторов (в том числе лекарственных препаратов, препятствующих адекватному снижению АД);
- — более жесткими целями самого лечения.
Мы сегодня вспоминали современные целевые уровни АД.
Согласно толковому словарю, что такое цель. Это результат, на который направлены наши усилия. Но стопроцентное попадание в цель бывает далеко не всегда, даже в спорте. Реальный результат достигается, в частности, в баскетболе, примерно в половине случаев. То же самое мы можем сказать сегодня и об успехе лечения АГ.
09:11
Успех терапии очень строго зависит от того, какую цель мы сегодня себе поставим. Если когда-то для нас целевой уровень АД был 160 и 95, то очень легко 40% больных мы могли контролировать. Как только мы поставили себе целевой уровень, благодаря 140 и 90, то сразу снизилась доля контроля до 10%.
Сегодня некоторые честные исследования, которые изучают больных с СД, и ставят целевой уровень 130 и 80, говорят о том, что результат в популяции достигаем примерно в 1% случаев.
(Демонстрация слайда).
Я покажу это на наших собственных данных по скринингу больных с АГ в Санкт-Петербурге. Это данные настоящего эпидемиологического исследования на репрезентативной выборке. Вы можете видеть, что и осведомленность лечения очень низкая. Доля больных, получающих лечение и доля больных, имеющих контроль АД, к сожалению, составляет лишь 2%, а даже не 20%, которые дают нам официальные данные мониторинга гипертонии.
Классификация резистентной гипертонии. Одной из частых причин является не сама резистентность, а ошибки в измерении АД и использовании понятия резистентности. Существуют специфические причины. В частности, вторичная гипертензия, которую мы иногда не диагностируем, несмотря на наши знания в этом вопросе.
Экзогенные воздействия, среди которых мы еще не упомянули сегодня злоупотребление солью. Это одна из частых причин – недостаточное ограничение потребления натрия. Злоупотребление алкоголем.
Сопутствующие факторы. Синдром обструктивного апноэ во сне, метаболический синдром. Очень важно в деятельности врача – несовершенство назначенной терапии и нарушение приверженности со стороны пациента.
Что касается сонного апноэ, буквально очень коротко покажу. Среди больных, которые получают три и более антигипертензивных препарата в максимальных дозах, то есть истинно являются резистентными. У мужчин распространенность сонного апноэ достигает 97%, у женщин 65%.
Женщины – это тот контингент, у которых эта проблема вообще недооценивается, мало обсуждается. Эти данные действительно впечатляют и показывают, что это очень важная ситуация. Недаром в Американских рекомендациях синдром сонного апноэ считается одним из вариантов вторичной АГ.
11:35
Сегодня благодаря этому исследования 2007-го года была показана связь нарушения дыхания во время сна любого происхождения с резистентностью к терапии.
Существует миф, что целевое АД очень сильно зависит от приверженности к лечению. Конечно, это так. Чем ниже приверженность к лечению, тем хуже возможность достичь целевого уровня АД.
Мы очень часто ищем причины вторичной АГ у лиц молодого возраста. В целом, в рекомендациях всегда записано, что чем моложе пациент, чем выше у него уровень АД, тем более активен должен быть наш поиск в отношении причины вторичной гипертонии.
Однако хочется обратить ваше внимание на то, что вероятность вторичной гипертонии с возрастом не снижается, а лишь нарастает. В возрасте 70-ти лет она достигает 17,5%. Это достаточно значимое число. Хотя в среднем мы считаем, что только 10% больных имеют вторичную АГ.
В настоящее время, к сожалению, благодаря введению строгих стандартов лечения гипертонии, наши диагностические возможности в поиске вторичной гипертензии несколько даже снижаются.
Хочу обратить ваше внимание на такую важную причину резистентности к терапии, как первичный альдостеронизм. На сегодняшний день это одно из самых недодиагностированных состояний АГ. Чем выше степень повышения давления (особенно у больных с резистентной гипертонией), тем выше распространенность первичного альдостеронизма в популяции больных с гипертензией. Она достигает 20%. Это практически каждый пятый пациент.
Лишь у 20% больных с первичным альдостеронизмом по современным данным наблюдается такой симптом как гипокалиемия. Он может нас насторожить в отношении наличия альдостеронизма у пациентов.
13:33
Сегодня определение активности ренина в плазме концентрации альдостерона считается обязательным исследованием, которое должно проводиться в случае трудности подбора терапии. Наличие значимого образования, визуализирующегося в надпочечниках, совсем не обязательно присутствует при этом состоянии. Очень часто у этих пациентов имеется доброкачественная двусторонняя гиперплазия коры надпочечников, которая никак не визуализируется и может быть диагностирована только благодаря гормональным исследованиям.
В различных клиниках в меру проводились исследования. В Сиэтле, в Бермингеме, в Норвегии и в Чехии. Практически все эти исследования дают одну и ту же двадцатипроцентную распространенность альдостеронизма у больных с резистентной гипертонией.
Если мы в целом посмотрим на пациентов, у которых наблюдается рефрактерная гипертония, то большинство из них говорит о том, что 60% – это лекарственные причины. Наша терапия несовершенна. Мы сами создаем проблемы резистентности к лечению.
Другое исследование «Rush». Те же самые 58% – это причины, связанные с несовершенством самой терапии. Среди этих 58 процентов 94% занимает неоптимальный режим терапии. Только небольшая доля может быть отнесена к лекарственным взаимодействиям и каким-то прочим лекарственным несовершенствам.
Мы попытались провести такое же исследование в России на нашей Петербургской популяции среди пациентов, которые находятся на лечении в нашей поликлинике. Получили абсолютно такой же показатель, но отличающийся лишь на 1% (59% пациентов). Причина резистентности к лечению – это так называемые лекарственные причины. Но даже на обычном терапевтическом участке чуть меньше (где-то 46%).
Одна из основных причин – клиническая инертность, то есть отсутствие действия врача в отношении интенсификации лечения при наличии такой необходимости. Это связано с тем, о чем я уже говорила. Мы переоцениваем успех проводимого лечения. Иногда мы сознательно используем различные предлоги для того, чтобы не интенсифицировать лечение.
В частности, что пациент пожилой, он может его не перенести и так далее. Тем самым оставляем больного на недостигнутом целевом уровне АД.
15:57
Для того чтобы вылечить больного с тяжелой гипертензией, необходимо учитывать три момента:
- — приверженность пациента;
- — бороться с собственной некомпетентностью в этом вопросе, а именно с инертностью врача (хотя это абсолютная норма человеческого поведения):
- — преодолевать различные механизмы повышения АД;
- — иметь хорошую организацию помощи для подобных пациентов.
Проблема терапевтической инертности существует абсолютно везде. Здесь даже проблема не в стоимости проводимого лечения. Четко было показано, что это проблема, характерная даже в таких исследованиях, где лекарство предоставляется пациентам бесплатно.
На сегодняшний день нужно сменить собственную установку в этом лечении, чтобы понять, что целевой уровень АД должен быть достигнуть у пациента любой ценой. Было проведено интересное исследование, опубликованное в 2002-м году, по сравнению двух стратегий.
Пациенты были сначала вылечены по обычным рекомендациям. Затем была применена стратегия достичь целевого уровня абсолютно любой ценой, в том числе комбинацией четырех, пяти, шести и более лекарственных препаратов. Преодолеть резистентность к терапии в большинстве случаев все-таки оказалось возможным.
В сегодняшний алгоритм лечения больных с резистентной гипертонией входит обязательная оценка собственной адекватности режима терапии и оценка приверженности к лечению. Обязательная диагностика ожирения и синдрома сонного апноэ. Обязательный анализ сопутствующей терапии и анализ правильности измерения АД и точности.
Для того чтобы установить причину повышения АД, необходимо обязательно оценить домашний уровень АД. Уровень АД измерить другим лицом, чтобы исключить гипертонию «белого халата». При необходимости провести его суточное мониторирование.
Проанализировать всю терапию, которую пациент получает. Отменить препараты, которые могут способствовать повышению АД, если это возможно. Изучать побочные эффекты терапии. Провести скрининг наличия синдрома сонного апноэ (хотя бы при помощи опросников). Углубленно обследовать пациента на предмет вторичной гипертензии. Добиться соблюдения пациентом диеты, режима физических нагрузок и обязательно ограничение поваренной соли.
Если есть необходимость, то консультироваться с психологом, даже психиатром. Обязательно должны быть исключены панические атаки как причина кризового нарушения АД. Важно также обращать внимание на показатели гемодинамики. В частности, периферического сопротивления и сердечного выброса.
18:31
Современные рекомендации по лечению резистентной гипертонии, как ни странно, достаточно скудны. Одни из наиболее удачных были опубликованы в 2006-м году (хотя есть и международные рекомендации). Там записано, что если пациент получает три препарата, включая диуретики, целевое АД по-прежнему не достигнуто, то нам необходимо обязательно снизить потребление соли, скорректировать лечение диуретиками с учетом функции почек.
Если у вас креатинин нормальный, в основном это тиазидные диуретики. При превышении креатинина используются петлевые диуретики. Обязательно используются вазодилататоры альтернативного класса и так далее. Если только нет эффекта, то больной госпитализируется в специализированную клинику.
Современные комбинации в лечении включают комбинации многих препаратов (диуретики, бета-блокаторы, антагонисты кальция, длительно действующие препараты). Желательно фиксированные комбинации. Оригинальные препараты с доказанной эффективностью обязательно должны использоваться.
Даже в структуре одного класса нужно стараться использовать препараты, наиболее эффективно в режиме каждого класса доказавшие свою эффективность в ряде клинических исследований. При недостаточном эффекте используются низкие дозы спиринолактона или «Верошпирона» («Verospiron»). Центральные препараты также могут быть эффективны.
Если мы говорим об антагонистах кальция, без которых невозможно лечение больного с резистентной гипертонией, то, допустим, более современные антагонисты кальция уже третьего поколения, такие как препарат «Лерканидипин» («Lercanidipine»), обладают очень длительным эффектом. Они препятствуют проблемам утреннего подъема АД, что обеспечивает более плавный антигипертензивный эффект и может способствовать преодолению резистентности к лечению.
При применении такого препарата отсутствует симпатическая стимуляция, связанная с вазодилатацией. Отсутствует эффект, который обладает прогипертензивным действием и активирует другие прогипертензивные пути в процессе лечения. Это очень важно.
20:32
Если мы берем класс блокаторов рецепторов ангиотензина II, которые используем у наших пациентов, то тоже в структуре этого класса, помимо всяких органно-протективных эффектов (о которых нет сегодня времени говорить, и вы о них хорошо знаете), нужно обращать внимание на силу антигипертензивного эффекта. Не совсем она однозначна у представителей одного и того же класса.
Один из новых препаратов «Олмесартан» («Olmesartan») или «Кардосал» («Cardosal»), который сегодня появился и на российском рынке, дает достаточно значимое снижение АД, более выраженное при использовании стандартных терапевтических доз, чем некоторые другие представители этого класса.
Добавление «Верошпирона» эффективно в определенной степени у большинства больных (и не только у пациентов, имеющих вторичный или первичный гиперальдостеронизм). В данном случае не следует использовать тест назначения «Верошпирона» для диагностики альдостеронизма. В целом добавление этого препарата в качестве четвертого препарата обеспечивает дополнительные преимущества.
Очень коротко о новых стратегиях в лечении таких пациентов. Сегодня используются более сильные натрийуретики, симпатолитические препараты, новые вазодилататоры. Кроме того, используются немедикаментозные подходы. Такие как устройства, влияющие на барорецепторы (постоянная стимуляция барорефлексов).
Система управляемого дыхания. СРАР, специфичная для лечения синдрома сонного апноэ. Некоторые препараты с альтернативными механизмами действия. В частности, блокаторы эндотелина. Достаточно много данных по «Дарузентану» («Darusentan»).
22:06
(Демонстрация слайда).
Таким образом имплантируется система для стимуляции барорефлекса, с двусторонней имплантацией специальных электродов. Она со временем обеспечивает значимое снижение систолического и диастолического АД и числа сердечных сокращений.
(Демонстрация слайда).
Так выглядит рентгенограмма пациента с имплантируемым устройством. С двух сторон.
Сегодня этой компанией созданы уже электроды с односторонней имплантацией, значительно меньшего размера. Эта техника очень активно развивается. Допустим, у экспериментального животного резко снижается АД. Сегодня уже более двух тысяч пациентов в мире ходят с подобными имплантируемыми устройствами.
(Демонстрация слайда).
Так выглядит аппарат для СРАР-терапии. Это назальная маска. Она обеспечивает достаточно значимое снижение АД на фоне приема антигипертензивных препаратов.
Еще один новый подход. Процедура аблации почечных симпатических нервов. Она выполняется как стандартная ангиография почечных артерий. Процедура похожа на стентирование. Наносится от 4-х до 6-ти аппликаций на каждую почечную артерию. После этого с течением времени обеспечивается значимое снижение спилловера регионального и общего норадреналина.
В течение года значимое снижение АД, до 25 – 30 мм рт. ст. в среднем по группе, что позволяет у ряда больных даже отменить терапию.
Развиваются и новые генные технологии. В частности, «Antisence» технология. Сегодня экспериментальные работы уже говорят, что блокирование РНК ряда рецепторов, белков приводит к снижению АД.
Проблемы генной терапии достаточно большие. Но в перспективе это тоже есть. Самая большая проблема – безопасность такого лечения. В противном случае, наверное, мы сегодня уже подошли бы к генной терапии в отношении, в первую очередь, гена NO-синтазы, о которой так подробно рассказывала Оксана Михайловна.
24:06
Большой бум в литературе вызвала вакцина против АГ. Несмотря на то, что она не имела больших побочных действий, наблюдение за этими пациентами не привело к широкому внедрению вакцины. Затраты и сложность этого лечения не окупались результатом, который мы имели.
Резистентная гипертония. Как нам улучшить результат. Первое, что бы мне хотелось сказать. Никогда не миритесь с недостигнутым целевым уровнем АД. Если вы не будете с этим мириться и пытаться улучшить прогноз пациента, то и пациенты будут более привержены к лечению.
Всегда нужно убедиться в правильности измерения АД. Всегда думать о том, что пациент может быть не полностью привержен к лечению. Необходимо всегда исключить вторичную гипертензию у таких больных согласно существующим рекомендациям. Старайтесь изменять терапию, сделайте ее более рациональной. Никогда не бойтесь большого числа препаратов, если они назначаются в рациональных комбинациях.
Используйте фиксированные комбинации для повышения приверженности и уменьшения полипрагмазии. Не стесняйтесь посоветоваться со специалистом, если у вас есть такая необходимость.
Основной принцип сегодня – агрессивная терапия против агрессивной гипертензии. В такой ситуации я думаю, что гипертензия обязательно сдастся под нашим напором.
Спасибо за внимание.
Григорий Арутюнов: Александра Олеговна, большое спасибо за этот прекрасный эмоциональный и очень глубокий доклад. На ваше имя пришло несколько вопросов. Если позволите, я их озвучу.
Вопрос: Когда можно сделать вывод о том, что АГ резистентная? Через какое время?
Спрашивает доктор, который работает в поликлинике.
Александра Конради: На сегодняшний день разные специалисты отводят разное количество времени нашим пациентам. В целом мы можем подозревать эту проблему через месяц. Но стопроцентно выставить такой диагноз – нам все равно потребуется от трех до шести месяцев.
Для разворачивания полного эффекта всех препаратов и отработки терапии необходимо время.
26:12
Григорий Арутюнов: Спасибо большое. Второй вопрос.
Вопрос: Какая терапия систолической гипертонии пожилых наиболее эффективна?
Александра Конради: Наиболее эффективно все равно сегодня применение дигидроперидиновых антагонистов кальция и тиазидных диуретиков. Изолирован систолической гипертонией.
Проблема может быть только в том, что не всегда эта терапия хорошо переносится. Завоевывают свои позиции блокаторы рецепторов ангиотензина II при систолической гипертензии. Хотя победить антагонисты кальция, по-моему, еще ни один препарат не смог у этой категории больных.
Григорий Арутюнов: Вопрос из реальной жизни.
Вопрос: В вашей личной практике была такая ситуация, когда резистентность преодолеть не удалось? Что вы сделали?
Александра Конради: Конечно, была. У нас таких больных очень много. Организован целый центр резистентной гипертонии. Мы начали процедуру радиочастотной аблации почечных артерий. Под нашим наблюдением находится 5 пациентов. В ближайшее время их будет 10. Мы с удовольствием поделимся этими данными.
Проблемой все равно всегда останутся больные, которые не поддаются терапии. Именно для них и разрабатываются альтернативные подходы. Мы должны искать другой выход. Медикаментозная терапия за счет выраженного ремоделирования и проблем, имеющихся у пациента, не может обеспечить у всех больных.
27:38
Григорий Арутюнов: Спасибо большое за очень честный и профессиональный ответ.
Но есть еще вопрос.
Вопрос: Есть ли какие-то биохимические маркеры резистентной гипертензии?
Александра Конради: К сожалению, нет. Я даже сегодня не стала останавливаться на тех исследованиях, которые проводились в отношении того, какие существуют предикторы, как ответит на терапию пациент и так далее.
Очень часто использовались алгоритмы. Допустим, высокий ренин, низкий ренин. В зависимости от этого подбирать терапию. Они клинически себя не оправдывают. Эффект лечения зачастую бывает непредсказуем.
Единственный подход, который более или менее работает, гемодинамический. Если мы определим уровень сердечного выброса и уровень периферического сосудистого сопротивления, то там, где последний повышен, добавление большого количества вазодилататоров, вплоть до нужного эффекта.
Там, где есть больные с высоким выбросом, необходимо давать бета-адрено-блокаторы. Хоть это теперь и не модно в лечении АГ. Это обеспечивает у них дополнительный антигипертензивный эффект.
Что касается биохимических маркеров, чем отличается больной с резистентной гипертонией от обычного. Клинически надежного не существует.
Григорий Арутюнов: Спасибо. Последний маленький вопрос.
Вопрос: Как отличить гипертонию «белого халата» от того, о чем говорили вы – от резистентной?
Александра Конради: В реальной жизни самое простое – попросить больного принести дневник самоконтроля АД, посмотреть, какое давление у него дома. Если вы не доверяете, что кто-то правильно измеряет, вы можете попросить даже вашу медсестру измерить давление вне врача. Это в меньшей степени вызывает эффект «белого халата».
В трудных случаях – суточное мониторирование АД. Там же тоже есть свои проблемы. Больной на процедуру мониторирования тоже реагирует. Все по-разному. Этот метод, несмотря на то, что его так хвалят, не идеален в диагностике гипертонии «белого халата».
Григорий Арутюнов: Спасибо большое, Александра Олеговна, за эти глубокие исчерпывающие ответы. Спасибо за вашу лекцию и ваши ответы.
До новых встреч.
29:55
Характеристики пациента и сопутствующие заболевания
Резистентная гипертензия
Крупный анализ, подходящий для оценки, — это исследование Sim с соавт. более чем 470 тыс. пациентов с гипертензией, зарегистрированных в системе здравоохранения Южной Калифорнии между 1 января 2006 года и 31 декабря 2007 года.
- В целом, 60327 пациентов с гипертензией подходило под критерии резистентной гипертензии. Это составляет 12,8% всех пациентов с гипертензией и 15,3% из получающих препараты.
- более старшего возраста,
- сахарный диабет,
Рефрактерная гипертензия
- В поперечном анализе когорты исследования «Причины географических и этнических отличий в течение инсульта» (REGARDS), обсуждаемом выше, сильнейшим предиктором рефрактерной гипертензии была афроамериканская раса с коэффициентом распространенности 4,88 (95% доверительный интервал – 2.79-8.72). Принадлежность к африканской расе была также сильным независимым фактором риска развития рефрактерной гипертензии в исследовании Modolo с соавт.
- В исследованиях Университета Алабамы рефрактерная гипертензия была более широко распространена у афроамериканцев, чем у белых.
В целом, эти исследования показывают, что как и при резистентной гипертензии, сильными независимыми факторами риска для развития рефрактерной гипертензии являются ожирение и африканское происхождение. Также подобно резистентной гипертензии, коморбидность, ассоциированная обычно с рефрактерной гипертензией, включает диабет, хроническую болезнь почек, болезни сердца, инсульты.
Прогноз
Резистентная гипертензия
Увеличивающееся количество продольных и проспективных исследований явно демонстрируют, что пациенты с резистентной гипертензией имеют повышенный риск кардиоваскулярных и почечных осложнений и общей смертности, в сравнении с пациентами с более легко контролируемой гипертензией.
- Например, исследователи, оценивали риск возникновения инсульта и коронарной болезни сердца, а также общую смертность среди 2043 участников REGARDS с резистентной гипертензией относительно 12279 участников REGARDS с контролируемой гипертензией, лечимой <4 классами антигипертензивных препаратов либо с неконтролируемой гипертензией, лечимой 1 или 2 классами антигипертензивных препаратов.
- Резистентная гипертензия была разделена на 2 подгруппы, включающие участников с контролируемой гипертензией с помощью ≥4 классов антигипертензивных препаратов (т.е. контролируемая резистентная гипертензия) и неконтролируемой гипертензией с помощью ≥3 классов антигипертензивных препаратов (т.е. неконтролируемая резистентная гипертензия).
- В течение среднего периода наблюдений, равного 5,9 лет и после многовариабельных корректировок, выяснилось, что риск возникновения инсульта увеличивается на 25% (коэффициент риска 1,25; 95% доверительный интервал 0,94-1,65) в сравнении с участниками без резистентной гипертензии.
- В течение среднего периода наблюдений 4,4 года выяснилось, что риск развития коронарной болезни сердца увеличивается на 69% (1,69; 1,27-2,24) и общая смертность на 29% (1,29; 1.14-1,46) в течение среднего периода наблюдений, равного 6 годам.
- В сравнении с контролируемой резистентной гипертензией, неконтролируемая резистентная гипертензия была ассоциирована с увеличенным риском развития коронарной болезни сердца (2.33; 1,21-4,48), но не инсульта или смерти.
- Имея контролируемую резистентную гипертензию, не повышается риск инсульта, коронарной болезни сердца или смерти относительно участников без резистентной гипертензии.
При анализе гипотензивного и гиполипидемического лечения для попытки предупредить инфаркт миокарда исследователи определили, что риск инсульта, коронарной болезни сердца, болезни периферических артерий, терминальной стадии болезни почек и общей смертности у участников с контролируемой резистентной гипертензией (n=1870) относительно участников без резистентной гипертензии (n=12814) определялся контролем АД с помощью ≤3 антигипертензивных препаратов. Средний срок наблюдения составил 4,9 лет.
- Частота всех исходов так же, как и общая смертность, возрастает у пациентов с резистентной гипертензией.
- Значительно увеличивается риск развития терминальной стадии болезни почек (95%), застойной сердечной недостаточности (88%) и инсульта (57%).
- Риск развития хронической болезни сердца и болезней периферических артерий возрастает на 44% и 23% соответственно.
- Общая смертность увеличивается на 30% в сравнении с участниками исследования без резистентной гипертензии.
- Интересно, что примерные скорости развития хронической болезни сердца, застойной сердечной недостаточности, болезней периферических артерий и конечной стадии болезни почек были в каждом случае выше среди пациентов с контролируемой резистентной гипертензией относительно участников без резистентной гипертензии, оставляя остаточный риск развития кардиоваскулярных и почечных болезней даже после установления контроля над давлением крови, при использовании 4 и более препаратов.
- Эти два исследования так же, как и проспективные исследования, ясно показывают, что гипертензия, которая требует назначения 4 и более препаратов, в основном, увеличивает риск кардиоваскулярных и почечных осложнений и так же риск смерти, в сравнении с гипертензией, которая контролируется использованием 3 или менее препаратов.
Рефрактерная гипертензия
Последствия, включая общую смертность, пока что ещё не оценены для пациентов с рефрактерной гипертензией.
- Учитывая историю длительной, неконтролируемой и часто тяжёлой гипертензии, можно предположить, что увеличивается риск внезапных кардиоваскулярных осложнений, таких как инсульт и застойная сердечная недостаточность.
- Кажется интуитивно понятным, что у пациентов с рефрактерной гипертензией, больший риск кардиоваскулярных осложнений и смерти относительно пациентов с контролируемой гипертензией, однако доказательство такого высокого риска с настоящее время отсутствует.
Механизмы резистентной гипертензии в сравнении с рефрактерной
- Большинство литературных данных сходятся на том, что постоянное внутрисосудистое удерживание жидкости – это общая причина, лежащая в основе резистентной гипертензии. Например, Taler с соавт. продемонстрировали, что пациенты с истинной резистентной гипертензией характеризуются увеличением растяжения стенки сосудов, оцениваемого по жидкости в грудной клетке.
- В свою очередь, многочисленные исследования указывают, что в стойком удержании жидкости играет роль повышение уровня альдостерона.
- Дополнительные факторы также способствуют несоответствующему скоплению жидкости. Это известные факторы риска развития резистентной гипертензии: повышенная чувствительность к соли, афроамериканская раса, пожилой возраст, хроническая болезнь почек и диабет. Высокая концентрация соли, характерная для большинства стран во всем мире, доказано содействует непосредственному удержанию жидкости и развитию резистентной гипертензии, хотя избыточное удержание жидкости не всегда ассоциируется с большим потреблением соли в моделях на животных с гипертензией и обобщенных когортах с гипертензией.
- Этиология рефрактерной гипертензии может быть совсем иной, не зависеть от объёма внутрисосудистой жидкости.
- Ретроспективный анализ Acelajado с соавт. показал, что стойкое внутрисосудистое удержание жидкости вряд ли объясняет неэффективность антигипертензивной терапии, которая имела место у всех пациентов с рефрактерной гипертензией, которых лечили в том числе комбинацией хлорталидона и спиронолактона вместе со многими другими классами препаратов.
- Кроме того, несмотря на значительно высокие базальные уровни АД, антигипертензивный ответ в отношении спиронолактона был намного меньше у пациентов с рефрактерной гипертензией относительно лиц, у которых АД могло контролироваться (<140/90 мм рт. ст.). Такой незначительный эффект был замечен ещё при использовании высоких доз спиронолактона при сравнении с контрольной группой.
- Неэффективность такой интенсивной диуретической терапии, включающей высокие дозы спиронолактона, предполагает что механизм неэффективной терапии не связан с несоответствующим удержанием жидкости.
- Если это правда, то такая особенность имеет важное клиническое значение, дополнительное усиление диуретической терапии вряд ли обеспечит хоть какое-то улучшение контроля АД, пока будет возрастать риск развития связанных с диуретиками неблагоприятных событий.
- Эти данные основаны на наблюдении за предварительно измеренным, высоким в покое уровнем частоты сердечных сокращений у лиц с рефрактерной гипертензией по сравнению с лицами с контролируемой резистентной гипертензией.
- В этом исследовании снова наблюдали за высокой офисной частотой сердечных сокращений у пациентов с рефрактерной гипертензией, как в сообщении Acelajado. Высокие уровни частоты сердечных сокращений были подтверждены амбулаторным мониторированием с большим различием ночью (72,7±9 уд./мин. при рефрактерной гипертензии против 65,6±9уд./мин. при контролируемой резистентной гипертензии).
Резистентная артериальная гипертония
Артериальная гипертония (АГ) определяется как резистентная (рефрактерная), если на фоне приема трех и более антигипертензивных препаратов различных классов (один из которых диуретик) в дозах, близких к максимальным, не удается достичь целевого артериального давления (АД) < 140/90 мм рт. ст. у большинства пациентов с АГ (или < 130/80 мм. рт. ст. у пациентов с сахарным диабетом и почечной недостаточностью).
По результатам исследования ALLHAT, было выявлено, что около 47% пациентов остались резистентными к антигипертензивной терапии спустя год после рандомизации, несмотря на жесткую схему титрации и комбинации препаратов, предусмотренную в данном исследовании. Сходные результаты (43% резистентных пациентов) были получены в Syst-Eur Study. По данным Yakovlevitch and Black, субоптимальный режим приема препаратов является наиболее частой причиной резистентности (43%), следующая по частоте причина — толерантность к лекарственным препаратам (22%), далее — вторичная АГ (11%), низкая комплаентность (10%).
Рефрактерная АГ (РАГ) может быть разделена на две большие категории: истинная РАГ и псевдорезистентная АГ.
ПСЕВДОРЕЗИСТЕНТНАЯ АГ
Проблемы, связанные с измерением АД
Основным правилам измерения АД, а также техническим факторам, влияющим на уровень АД, посвящено большое количество публикаций в медицинской печати и методических рекомендаций. Однако врачи общей практики зачастую пренебрегают существующими правилами измерения АД, что влечет за собой целый ряд ошибок:
- использование маленькой манжетки;
- измерение АД без предварительного отдыха;
- быстрое выпускание воздуха из манжетки:
- измерение АД на одной руке;
- аускультация до пальпаторного измерения АД.
Псевдогипертония диагностируется достаточно редко: в том случае, когда АД, измеренное по методу Короткова, не соответствует истинному (внутриартериальному) уровню АД. Этот феномен, связанный с выраженным атеросклерозом и кальцификацией плечевой и лучевой артерий, наблюдается у пожилых пациентов. Утолщение и уплотнение стенки артерий с возрастом приводит к тому, что для достижения компрессии ригидной артерии требуется более высокое давление (выше истинного) в манжетке, что приводит к завышению цифр АД. Наличие у пациента псевдогипертонии можно заподозрить при наличии следующих признаков:
- отсутствие поражений органов-мишеней;
- кальцификация плечевой и других артерий по данным исследований (рентген, УЗИ);
- АД в плечевой артерии выше, чем на ногах (что лишний раз иллюстрирует необходимость полного пропедевтического осмотра пациента);
- симптомы гипотензии на фоне антигипертензивной терапии при отсутствии выраженного снижения АГ (обычно трактуется у пожилых пациентов как усугубление неврологической симптоматики дисциркуляторной энцефалопатии в вертебро-базиллярном бассейне);
- тяжелая систолическая АГ.
Существование псевдогипертонии может быть верифицировано при наличии симптома Ослера — пальпация плечевой артерии даже когда внутриманжеточное давление превышает систолическое АД. Окончательное подтверждение диагноза возможно лишь при внутриартериальном измерении АД.
Низкая комплаентность
Комплаентность (приверженность пациентов к терапии) определяется как способность пациента точно следовать клиническим назначениям по приему лекарственных препаратов и модификации образа жизни. Прием лекарственных препаратов в соответствии с врачебными назначениями как минимум в 80% является наиболее общей характеристикой медикаментозной комплаентности. Низкая комплаентность встречается у более чем 50% пациентов, в том числе включенных в клинические исследования. Примечателен факт уменьшения количества пациентов с низкой приверженностью к терапии до 10% среди больных, наблюдающихся у специалистов по лечению АГ (США), что демонстрирует значение квалификации специалиста и дефицита временного фактора в общении с пациентом, который присутствует у врачей общей практики.
Многочисленные факторы, такие, как стоимость медикаментов, низкий интеллектуальный уровень пациента, сложности режима приема и дозирования и др., должны анализироваться врачом при диагностике РАГ и подозрении на низкую приверженность к терапии. Тщательный расспрос остается одним из наиболее оптимальных методов определения нарушений приверженности пациента к лечению. Врач должен устанавливать реалистичные краткосрочные цели для всех специфических компонентов лечения (контроль веса, снижение употребления соли, физическая активность, снижение употребления алкоголя и, по возможности, одно- либо двукратный режим дозирования препаратов) и максимально индивидуализировать свои рекомендации, исходя из конкретной клинической ситуации, социальных и семейных особенностей пациента.
Ошибки в назначении препаратов
Подобные ошибки представляют собой частую причину развития псевдорезистентной АГ. Несмотря на огромное количество клинических исследований, постоянную публикацию исследовательских и методических материалов в медицинской печати, широкое обсуждение правил назначения и комбинации препаратов среди врачей общей практики и кардиологов, ошибки в дозировании и комбинировании антигипертензивных препаратов встречаются достаточно часто.
Современная тактика медикаментозной гипотензивной терапии предусматривает возможность выбора между монотерапией и комбинированной терапией. Для получения целевых показателей АД у большинства пациентов, особенно с I–III степенью повышения АД, требуется назначение комбинированной терапии.
Среди преимуществ комбинированной антигипертензивной терапии можно выделить следующие:
- использование препаратов с различными механизмами действия позволяет контролировать несколько патогенетических звеньев АГ;
- входящие в комбинацию препараты используются в более низких дозах, что снижает вероятность развития побочных эффектов;
- при назначении фиксированных комбинаций (два препарата в одной таблетке) улучшается приверженность к терапии.
Эффективными и хорошо переносимыми считаются следующие лекарственные комбинации:
- диуретики и β-блокаторы (атенолол, бисопролол);
- диуретики и ингибиторы АПФ (каптоприл, лизиноприл, эналаприл) или антагонисты рецепторов к ангиотензину II (валсартан, лозартан);
- антагонисты кальция (дигидропиридины: амлодипин, нифедипин) и β-блокаторы;
- антагонисты кальция и ингибиторы АПФ или антагонисты рецепторов к ангиотензину II;
- антагонисты кальция и диуретики;
- α-блокаторы (доксазозин, теразозин) и β-блокаторы.
Могут использоваться и другие комбинации с препаратами центрального действия (α2-агонисты, агонисты имидазолиновых I2-рецепторов), а также трех- и более компонентная схема.
Рекомендуется использование длительно действующих препаратов, обеспечивающих эффект в течение 24 ч и требующих однократного приема в течение суток, что значительно улучшает приверженность к терапии.
Под неадекватным режимом использования препаратов подразумевается назначение гипотензивных препаратов в низких дозах, использование патогенетически неграмотных комбинаций (препараты одного класса, например верапамил и дигидропиридин, или препараты со сходным механизмом действия — ингибитор АПФ и антагонист рецепторов к ангиотензину II — или сходными побочными эффектами).
Алгоритм оптимизации антигипертензивной терапии приведен на рисунке 1.
| Рисунок 1. Алгоритм оптимизации лекарственной терапии |
Таким образом, в случае резистентной АГ клиницист должен тщательно проанализировать назначенную схему антигипертензивной терапии: убедиться в адекватности назначенных доз и патогенетической оправданности применяемых комбинаций, а также в правильности назначенного режима терапии (соотнесение длительности действия и кратности назначения препаратов). При необходимости следует добавить к используемой схеме еще один препарат, учитывая при этом индивидуальные особенности пациента (поражение органов-мишеней, ассоциированную и сопутствующую патологию).
ИСТИННАЯ РЕЗИСТЕНТНАЯ АГ
Повышенная вариабельность и реактивность АД
Гипертония «белого халата» («офисная гипертония», «кабинетная гипертония») определяется как состояние стабильного повышения АД во время измерения на приеме у врача при нормальных значениях вне лечебного учреждения. Рассматривается как проявление стресс-индуцированной гипертонии. По данным Brown и соавторов, 2–3 из каждых 10 пациентов с резистентной АГ при суточном мониторировании АД имеют хороший контроль АД (среднее значение менее 135/85 мм рт. ст.). Пациенты с данным феноменом часто демонстрируют повышенную чувствительность к антигипертензивным препаратам, которые значительно снижают «нестрессорное» АД и могут вызывать симптомы гипотензии. Пациенты в этом случае самостоятельно отменяют гипотензивные препараты или начинают принимать их хаотично, что значительно затрудняет ведение этих пациентов, снижает комплаентность.
В данном случае рекомендуется проведение внеофисного измерения АД (суточное мониторирование и дневники самоконтроля АД) до коррекции схемы антигипертензивной терапии. Несмотря на достаточную простоту диагностики данного феномена, клиницисты часто недооценивают его распространенность и значимость, что приводит к ошибкам в подборе схем лекарственной терапии и снижению комплаентности.
Барорефлекторная недостаточность
Нестабильность АД с периодами значительного повышения и снижения встречается у пациентов с повреждением барорефлекторной функции. Данное состояние встречается достаточно редко и очень трудно диагностируется.
Физиологическая резистентность (перегрузка объемом)
Наиболее частой причиной физиологической резистентности АГ является перегрузка объемом. Чрезмерное употребление соли может служить причиной развития РАГ у леченых пациентов. Использование прямых вазодилататоров (миноксидил, гидралазин), адреноблокирующих препаратов (α-блокаторы и β-блокаторы) и больших доз сильнодействующих диуретиков может приводить к увеличению задержки жидкости и формированию РАГ. Наиболее частой причиной персистирующей гиперволемии является назначение ежедневного однократного приема фуросемида. За снижением внутрисосудистого объема в течение нескольких часов после приема фуросемида следует активация ренин-ангиотензин-альдостероновой системы (РААС) с включением механизмов задержки натрия, которые восстанавливают весь потерянный натрий во время краткого интервала натрийуреза. При сохраненной функции почек назначение утренней дозы длительно действующего гидрохлортиазида (12,5–25 мг) способно разорвать этот порочный круг. Все препараты, снижающие АД, снижают также почечное перфузионное давление и клубочковую фильтрацию, что приводит к задержке натрия и жидкости.
К сожалению, многим пациентам с РАГ, которые получают несколько гипотензивных препаратов, не назначаются диуретики в адекватных дозах. Ограничение употребления соли само по себе приводит к адекватному контролю объема циркулирующей плазмы, снижению АД, улучшению переносимости лечения, уменьшению количества применяемых антигипертензивных препаратов. На фоне снижения употребления соли эффективность всех антигипертензивных препаратов повышается, за исключением антагонистов кальция.
При подозрении на перегрузку объемом необходимо определение количества натрия в суточной моче. При этом часто обнаруживается неадекватность в выполнении диетических рекомендаций у пациентов, которые утверждают, что соблюдают низкосолевую диету. У больных, не соблюдающих низкосолевую диету, экскреция натрия увеличивается.
Лекарственные взаимодействия
Идентификация лекарственных препаратов, снижающих эффективность антигипертензивной терапии, крайне важна, так как помогает индивидуально оптимизировать терапию у пациентов с учетом механизма действия применяемых препаратов. Остановимся лишь на наиболее часто применяемых.
Стероиды. АГ регистрируются у более чем 20% пациентов, принимающих синтетические кортикостероиды. Прием данных препаратов также может быть причиной резистентности АГ. Фактором риска развития РАГ является пожилой возраст. Такие лекарственные субстанции, как натуральная лакрица, фенилбутазон, карбеноксолон, препараты преднизолона, кортизола обладают минералокортикоидной активностью. Прием этих препаратов в средних дозах может приводить к псевдогиперальдостеронизму (задержка натрия, гиперволемия, гипокалиемия с метаболическим алкалозом и подавление плазменного ренина и альдостерона). Мази, антигеморроидальные препараты, глазные капли, ингаляционные бронходилататоры, назальные антиаллергические спреи могут содержать субстанции со значительной минералокортикоидной активностью. Некоторые из этих препаратов могут содержать симпатические амины. Для снижения АД и преодоления рефрактерности необходим отказ от применения этих препаратов. В случаях, когда терапия стероидами является обязательной, эффективными препаратами являются диуретики. В процессе терапии диуретиками необходим мониторинг калия, так как данные препараты способны усиливать гипокалиемию при стероидзависимой АГ.
Половые гормоны. Пероральные контрацептивы способны индуцировать АГ приблизительно в 5% случаев при использовании высокодозовых комбинаций эстрогенов и прогестинов. Фактором риска возникновения и усугубления АГ являются курение, ожирение, раса (афроамериканцы), диабет, почечная патология. Описаны случаи развития злокачественной АГ на фоне приема оральных контрацептивов. Следующей группой риска возникновения РАГ являются мужчины, принимающие эстрогены с целью лечения рака предстательной железы. Даназол, полусинтетический андроген, используемый для лечения эндометриоза, наследственного ангионевротического отека, может приводить к гиперволемии и усугублению АГ.
Препараты, влияющие на симпатическую нервную систему. Фенилэфрин, назначаемый в виде глазных капель, адреналоподобные вещества, используемые топически при глаукоме, могут приводить к росту АД у нормотоников и пациентов с АГ. Присоединение к антигипертензивной схеме α-блокаторов, α- и β-блокаторов нивелирует данные эффекты.
Большинство аноректиков, нежелательных для применения, состоят из комбинации антигистаминоподобных веществ и адренергических агонистов (обычно фенилпропаноламин, эфедрин, псевдоэфедрин или кофеин). α-адренергическая интоксикация, индуцированная назальными и пероральными деконгестантами и противокашлевыми препаратами, содержащими большие дозы оксиметазолина, фенилэфрина, эфедрина, может индуцировать АГ или усугублять уже имеющуюся патологию. Препараты выбора — α-блокаторы, α- и β-блокаторы.
Нестероидные противовоспалительные препараты. НПВС могут потенцировать повышение АД и конкурировать с антигипертензивными препаратами. НПВС повышают на 40% риск развития АГ. НПВС взаимодействуют с некоторыми антигипертензивными препаратами, такими, как диуретики, β-блокаторы, ингибиторы АПФ, но не с антагонистами кальция — препаратами центрального действия, антигипертензивная эффективность которых не связана с продукцией простагландинов. Индометацин, пироксикам, напроксен вызывают значительное повышение АД, тогда как сулиндак и полные дозы аспирина оказывают наименьшее воздействие на уровень АД. Минимальные дозы аспирина не влияют на показатели АД у пациентов с АГ. Селективные препараты-ингибиторы циклооксигеназы-2 (целекоксиб, рофекоксиб) не приводят к повышению АД и не оказывают дозозависимых эффектов на АД. Метаанализы показали, что НПВС приводят к увеличению среднего АД на 4–5 мм рт. ст. Они являются причиной задержки натрия, повышения чувствительности к прессорным гормонам. Принимая во внимание широкую распространенность заболеваний суставов и позвоночника среди пожилых пациентов, клиницисты должны отчетливо осознавать возможные взаимодействия НПВС с антигипертензивными препаратами.
Трициклические антидепрессанты. Трициклические антидепрессанты препятствуют гипотензивным эффектам адреноблокаторов, таких, как гуанетидин, что может приводить к значительному повышению АД. Эти препараты предупреждают накопление антигипертензивных препаратов в адренергических нервных окончаниях, где они блокируют передачу нервного возбуждения. Подобные взаимодействия описаны и для других гипотензивных препаратов (метилдопа, клонидин).
Ассоциированные состояния
Метаболический синдром и ожирение. Распространенность метаболического синдрома в настоящее время приобретает характер эпидемии и в некоторых странах, в том числе и России, достигает 25–35% среди взрослого населения.
У пациентов с метаболическим синдромом эффективность антигипертензивных препаратов снижается, и двухкомпонентная схема, как правило, не позволяет достичь целевого АД. Это связано с патогенетическими особенностями АГ при метаболическом синдроме.
В норме инсулин обладает сосудистыми протективными эффектами и вызывает инсулинобусловленную вазодилатацию. Но при хронической гиперинсулинемии и инсулинорезистентности запускаются другие патофизиологические механизмы, приводящие к АГ: стимуляция симпатико-адреналовой системы (САС), РААС; повышение содержания внутриклеточного Na+ и Са2+, уменьшение К+ с увеличением чувствительности сосудистой стенки к прессорным воздействиям; повышение реабсорбции Na+ в проксимальных и дистальных канальцах нефрона (задержка жидкости с развитием гиперволемии). Особое значение приобретает стимуляция пролиферации гладкомышечных клеток сосудистой стенки под действием гиперинсулинемии (сужение артериол и увеличение сосудистого сопротивления).
Неудачи в лечении АГ при метаболическом синдроме обусловлены, как правило, фокусировкой терапевтической тактики только на АГ. В основе успешной терапии лежит принцип одновременной коррекции всех звеньев патогенеза метаболического синдрома, всестороннее воздействие на причины и следствия инсулинорезистентности: изменение образа жизни, лечение ожирения, терапия нарушений углеводного обмена, лечение дислипидемии. При подборе антигипертензивной терапии следует учитывать следующие особенности: метаболические эффекты гипотензивных препаратов (влияние на липидный спектр, инсулинорезистентность, уровень глюкозы и мочевой кислоты); необходимость более частого использования 3-, 4-компонентной схемы терапии с воздействием на различные звенья патогенеза АГ, характерные для метаболического синдрома.
Курение приводит к транзиторному повышению АД, увеличению вариабельности АД. При большом количестве выкуриваемых сигарет продолжительность эпизодов гипертонии растет. Антигипертензивная эффективность β-адреноблокаторов у курящих больных АГ снижается.
Алкоголь. Злоупотребление алкоголем (хроническая алкогольная интоксикация) приводит к повышению АД у нормотоников и индуцированию резистентности к антигипертензивным препаратам. Существуют дозозависимые гипертензивные эффекты алкоголя. Основным видом лечения является прекращение или уменьшение употребления спиртных напитков. В некоторых случаях прекращение приема алкоголя не улучшает контроля АД.
Генетические особенности
Полигенный синдром эссенциальной гипертонии включает широкий спектр гемодинамических и нейроэндокринных особенностей. Так, плазменная активность ренина частично определяет индивидуальную чувствительность к β-блокаторам, ингибиторам АПФ, антагонистам рецепторов к ангиотензину II. Широко известна связь изменений гена ангиотензиногена с сольчувствительностью. Описаны генетически детерминированные изменения в метаболизме лекарственных препаратов, такие, как ускоренный метаболизм (гидралазин), но для основных классов гипотензивных препаратов значимые генетические особенности метаболизма не подтверждены. Общепризнана высокая чувствительность к диуретикам и относительно низкая к ингибиторам АПФ, β-блокаторам, антагонистам рецепторов к ангиотензину II у пациентов негроидной расы.
Вторичные формы АГ
Прогрессирование почечной недостаточности представляет собой наиболее частую и легко диагностируемую причину резистентности АГ. Реноваскулярные болезни широко распространены среди пациентов с ранее контролируемой АГ, особенно если атеросклеротические поражения присутствовали в других сосудистых бассейнах. В течение последних лет представление о влиянии первичного гиперальдостеронизма (ПГА) на распространенность РАГ серьезно изменилось. Исследователи отмечают большую частоту ПГА. Многие эти пациенты имеют нормальный уровень калия в плазме при повышенном уровне альдостерона плазмы относительно ренина. У большинства из них диагностируется билатеральная гиперплазия коры надпочечников, при которой не показано оперативное лечение. Препаратом выбора в данном случае является спиронолактон.
Синдром обструктивного апноэ сна (СОАС). По данным H. Issakson и соавторов, среди пациентов с рефрактерной в 56% случаев выявляется СОАС.
Обусловленная СОАС типичная «утренняя» АГ, преимущественно диастолическая, плохо поддается коррекции обычными гипотензивными препаратами. Клиницисты часто недооценивают значение этого состояния и не включают в традиционную схему сбора анамнеза вопросы, касающиеся храпа пациента, наличия остановок дыхания во сне. А это необходимо особенно у пациентов с ожирением.
Существуют достаточно противоречивые данные относительно эффективности и безопасности антигипертензивных препаратов различных групп у больных с СОАС. Так, выявляется ряд побочных эффектов при лечении некоторыми антигипертензивными препаратами, в частности угнетение тонуса мышц верхних дыхательных путей при лечении β-адреноблокаторами, α-метилдопой, а также в результате метаболического алкалоза, вызванного диуретиками. В других работах подтверждаются положительные эффекты диуретиков в виде уменьшения количества эпизодов дыхательных нарушений во время сна. Однозначно положительные данные получены при использовании антагонистов кальция и ингибиторов АПФ.
Однако для успешной терапии АГ при СОАС необходимо проведение комплекса лечебных мероприятий, направленных на устранение СОАС. Наиболее эффективными в настоящее время являются увулопалатофарингопластика, СРАР-терапия (постоянное положительное давление в дыхательных путях).
Алгоритм диагностики РАГ представлен на рисунке 2.
Необходимо помнить, что причиной резистентности АГ может быть сочетание нескольких экзогенных факторов и также вторичных форм АГ. Лечение РАГ предполагает элиминацию экзогенных факторов и использование максимально переносимых доз препаратов в многокомпонентной схеме терапии, включающей длительнодействующие диуретики. Многие исследования доказывают необходимость и целесообразность присоединения спиронолактона к 3- или 4-компонентной схеме терапии у пациентов с РАГ.
Литература
- Oparil S., Michael A. Weber. Hypertension: A Companion to Brenner and Rector’s The Kidney, 2000.
- Erdine S. Resistant hypertension. ESH. Scientific Newsletter, 2003; 4: N15.
- Hypertension Primer, Third Edition, 2003 American Heart Association.
- Европейские рекомендации по диагностике и лечению артериальной гипертонии, 2003.
Т. В. Адашева, кандидат медицинских наук, доцент МГМСУ, Москва