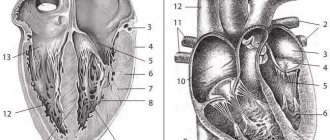
Антиангинальные препараты – это группа лекарственных средств, которые применяют для лечения ишемической болезни сердца – стенокардии и инфаркта миокарда.
Ишемическая болезнь сердца (ИБС) – это патологическое состояние, связанное с кислородным голоданием сердечной мышцы (миокарда) из-за недостаточного поступления крови к сосудам сердца.
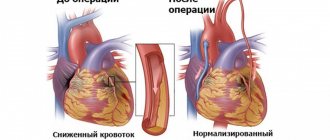
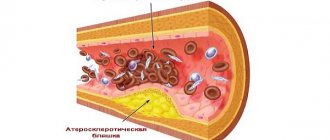
Хроническая ишемическая болезнь сердца проявляется стенокардией. Причинами стенокардии обычно является сужение просвета коронарных (сердечных) сосудов атеросклеротической бляшкой (стенокардия напряжения) или спазмом сосудов (вазоспастическая стенокардия).
Острая ишемическая болезнь сердца проявляется нестабильной стенокардией и инфарктом миокарда. Причиной острой ИБС является частичная или полная закупорка просвета сосудов тромбом.
Нестабильную стенокардию рассматривают как предынфарктное состояние. Чаще всего она переходит в острый инфаркт миокарда, однако в случае быстрого распознания и оказания помощи нестабильная стенокардия способна разрешиться вполне благополучно.
Сужение просвета коронарных сосудов приводит к снижению доставки крови (а вместе с кровью – кислорода и питательных веществ) к миокарду, что проявляется кислородным голоданием сердечной мышцы, болью при физической нагрузке или психоэмоциональном стрессе.
Полная же закупорка просвета коронарных сосудов приводит к резкому дефициту кислорода в питаемых этими сосудами участках сердца и, при отсутствии лечения, их гибели – некрозу.
Лекарственные препараты, применяемые при стенокардии, называют антиангинальными средствами (от старого латинского названия стенокардии: angina pectoris – грудная жаба).
Сложности при стратификации риска как фактор, затрудняющий выбор терапии
Хорошо известно, что степень интенсивности превентивной медикаментозной терапии пациентов с ишемической болезнью сердца (ИБС) должна напрямую определяться уровнем сердечно-сосудистого риска. К сожалению, несмотря на множество разработанных для этой цели шкал, оценка риска для больных ИБС без острого инфаркта миокарда (ОИМ) в анамнезе сегодня сильно затруднена. В большинстве случаев существующие шкалы занижают степень риска для пациентов группы высокого риска и завышают – в группе низкого риска [1].
Наиболее значимой практической сложностью здесь представляется невозможность получения реальной информации о степени стабильности атеросклеротических бляшек в коронарных сосудах пациента с ИБС, обладающей первостепенной прогностической ценностью. По всей видимости, крупные, но имеющие плотную фиброзную покрышку атеросклеротические бляшки разрываются реже, но при этом обусловливают выраженную клиническую симптоматику (в частности, ангинозные боли). В то же время при их разрыве и высвобождении внутрь сосуда огромного количества прокоагулянтного тканевого фактора вероятно развитие тромботической окклюзии крупного сосуда, клиническим эквивалентом которого служит обширный инфаркт миокарда с формированием зубца Q [2].
Небольшие бляшки реже приводят к значимому снижению коронарного кровотока, что определяет более редкие и менее интенсивные приступы ангинозной боли. Но при этом бляшки небольшого размера могут быть значительно менее стабильными, эрозии или разрывы их тонкой фиброзной покрышки могут приводить к развитию ОИМ, как правило, без формирования зубца Q (рис. 1). В качестве наглядного примера можно привести истории болезни пациентов с плохо компенсируемым сахарным диабетом 2 типа, в анамнезе часто имеющих несколько мелкоочаговых инфарктов и эпизодов нестабильной стенокардии.
По новым данным, при нестабильной стенокардии внутри коронарных артерий возможно формирование своеобразного динамического равновесия, при котором в течение достаточно длительного времени на поверхности интимы происходят небольшие надрывы или образуются эрозии интимы, но формирования тромба удается избежать за счет активации антитромботической системы. Использование методов прямой визуализации структуры атером in vivo, таких как оптическая когерентная томография/спектроскопия, позволяет выявить такие бляшки [3].
В рамках данной концепции несложно объяснить результаты исследования COURAGE (Clinical Outcomes Utilizing Revascularization and Aggressive Drug Evaluation), в котором стентирование коронарных артерий не приводило к улучшению прогноза, но значительно улучшало клиническую симптоматику. По всей вероятности, несмотря на то что ангинозные боли у данных пациентов были связаны с крупными, с успехом стентированными бляшками, прогноз в данном случае определялся мелкими нестабильными бляшками, стентирования которых, по понятным причинам, не выполнялось.
Сегодня оценка степени стабильности атеросклеротических бляшек и вмешательства, направленные на их стабилизацию, в т. ч. через “упрочнение” фиброзной покрышки, становятся новой парадигмой превентивной кардиологии. По сути, все традиционные шкалы, разработанные для больных ИБС, решают задачу оценки риска посредством анализа факторов, опосредованно характеризующих именно стабильность атером.
Основы лечения ишемической болезни сердца
Антиангинальные препараты используют как для купирования (устранения) приступа стенокардии, так и для профилактики возникновения приступов систематически.
Помимо антиангинальных препаратов в лечении стабильной и вазоспастической стенокардии применяют средства для лечения атеросклероза (антиатеросклеротические), профилактики тромбообразования (антиагреганты).
Для лечения нестабильной стенокардии и острого инфаркта миокарда применяют в первую очередь не антиангинальные средства, а фибринолитики (препараты, растворяющие тромбы) и антикоагулянты и антиагреганты (препараты, препятствующие повторному тромбообразованию).
Новые неинвазивные диагностические опции
Одним из основных направлений развития современной кардиологии является поиск минимально инвазивных методов прямой или косвенной оценки стабильности атеросклеротических бляшек, что позволит более точно предсказывать риск развития острого коронарного синдрома (ОКС). Их практическое применение представляется особенно важным при ведении пациентов со средним риском, выбор оптимального лечения которых часто затруднен. Сегодня на Западе с этой целью наиболее широко используется такой интегральный показатель масштаба поражения коронарного русла, как кальциевый индекс, который рассчитывается при проведении мультиспиральной компьютерной томографии (МСКТ) [4].
Другим подходом, который также может быть реализован при проведении МСКТ, служит оценка распределения плотности контраста в коронарном русле, что позволяет определять участки коронарных артерий с низким напряжением сдвига, где ожидаемо могут формироваться нестабильные атеромы [5].
Сегодня появляется все больше экспериментальных неинвазивных методик, призванных фокусно определять состояние атеросклеротических бляшек.
К ним относятся следующие методы диагностики:
• МР-визуализация с применением внутрисосудистых катушек и новых контрастов (например, ультрамалых частиц оксида железа, которые накапливаются макрофагами);
• совмещенные технологии МСКТ/МРТ (магнитно-резонансная томография), ПЭТ/КТ (позитронно-эмиссионная томография/компьютерная томография), КТ/сцинтиграфия;
• молекулярная лучевая диагностика (например, сцинтиграфия с 99Tc-аннексином 5, 99Tc-IL-2, с меченными тромбоцитами и липопротеидами низкой плотности).
Среди перспективных биохимических маркеров нестабильности атеросклеротических бляшек можно обозначить липопротеин-ассоциированную фосфолипазу А2, матриксную металлопротеиназу 9, растворимый лиганд CD40, неоптерин, а также широко доступный для практического определения высокочувствительный С-реактивный белок [6].
Основные принципы фармакотерапии
ИБС – хроническое “доброкачественное” заболевание, в связи с чем основными задачами ее лечения служат уменьшение числа, продолжительности и тяжести приступов ангинозных болей и улучшение прогноза, который определяется риском развития таких сердечно-сосудистых осложнений, как ОИМ, жизнеугрожающие нарушения ритма и хроническая сердечная недостаточность (ХСН).
В настоящее время влияние на прогноз пациентов с ИБС доказано только для статинов, ингибиторов ангиотензинпревращающего фермента – иАПФ (рамиприла и периндоприла), антитромбоцитарных препаратов и β-адреноблокаторов (после перенесенного ОИМ). В данном обзоре мы сосредоточимся на терапии, способной в первую очередь облегчать состояние больных стенокардией напряжения.
Антиангинальная и антиишемическая терапия хронической ИБС
Бета-адреноблокаторы (БАБ) по праву считаются краеугольным камнем лечения ИБС. В отсутствие абсолютных противопоказаний селективные β1-адреноблокаторы в обязательном порядке следует назначать всем пациентам с ОИМ в анамнезе ввиду их способности повышать выживаемость таких пациентов и снижать частоту развития повторных ОИМ.
Кардиоселективные БАБ служат основным инструментом лечения стенокардии напряжения, и прибегать к антиангинальным препаратам других групп следует только после того, как потенциал БАБ максимально задействован [7].
Крайне важно добиваться целевых значений частоты сердечных сокращений (ЧСС, 55–60 ударов в минуту), без достижения которых антиангинальная терапия не может быть признана оптимальной. В том случае когда на фоне применения БАБ у пациента со стабильной стенокардией продолжают отмечаться приступы ангинозных болей, следует предпринять попытку снизить ЧСС до 50 ударов в минуту, если на этом фоне не развивается атриовентрикулярная (АВ)-блокада [7]. При этом измерять ЧСС следует утром до приема очередной дозы препарата.
Сегодня нередко можно встретить больных, принимающих большие дозы нитратов в связи с выраженной ангинозной болью, но не получающих оптимальной терапии БАБ.
В большинстве случаев это связано со следующими факторами:
• неоправданными опасениями в отношении развития побочных эффектов, которые редко встречаются (в первую очередь различных блокад и бронхообструктивного синдрома);
• желанием назначить низкую дозу БАБ в рамках комбинированной антиангинальной терапии (реальная эффективность которой может значительно уступать терапии БАБ в полной дозе);
• трудностями при сопоставлении дозировок различных БАБ (сегодня врачи часто используют бисопролол в дозе 10 мг, но избегают применения метопролола в дозах выше 150 мг/сут, в связи с чем пациенты, получающие метопролол, часто имеют более высокую ЧСС);
• сложностями, связанными с титрованием БАБ (особенно это относится к липофильному карведилолу, обладающему труднопредсказуемой зависимостью между дозировкой и эффективностью);
В случае непереносимости БАБ их можно заменить на блокаторы кальциевых каналов (БКК). Следует особо отметить, что ни в одном из контролируемых исследований БКК не было показано их влияния на выживаемость пациентов со стенокардией.
У пациентов с бронхиальной астмой препаратом выбора можно считать верапамил пролонгированного высвобождения, обладающий пульсурежающим эффектом. При этом следует помнить, что по сравнению с БАБ его применение пожилыми пациентами сопряжено с более высоким риском развития АВ-блокады II–III степеней. При появлении значимого замедления АВ-проведения на фоне применения верапамила оправданно проведение холтеровского мониторирования ЭКГ, в т. ч. для исключения АВ-блокады II степени в ночные часы.
Дигидроперидиновые БКК обладают более слабым антиангинальным эффектом, нежели недигидроперидиновые, но могут с успехом применяться пациентами с нарушениями проводимости. Ряд больных эти препараты могут приводить к развитию субэндокардиальной ишемии [7].
В случае наличия противопоказаний к назначению БАБ, в первую очередь при наличии блокады АВ-проведения ΙΙ степени или бронхиальной астмы, в качестве пульсурежающего препарата может использоваться ингибитор If-каналов ивабрадин. Антиангинальный эффект ивабрадина реализуется только за счет урежения ЧСС, ввиду чего он “по силе” уступает БАБ, обладающим многогранным механизмом антиишемического и кардиопротективного действий. Следует отметить, что в крупном клиническом исследовании, включившем более 10 тыс. пациентов с ИБС и ХСН, ивабрадин не показал влияния на сердечно-сосудистую смертность и частоту госпитализаций, обусловленных ОИМ и ХСН [8].
Классификация антиангинальных препаратов
В зависимости от механизма действия антиангинальные препараты классифицируют на:
- препараты, повышающие доставку кислорода к сердцу: ментол, валидол (ментол в ментиловом эфире изовалериановой кислоты), дипиридамол;
- препараты, понижающие потребность сердца в кислороде: β-адреноблокаторы (пропранолол, метопролол, атенолол, бетаксолол, бисопролол, небиволол, карведилол);
- брадикардитические средства (ивабрадин);
- органические нитраты и нитратоподобные средства – сиднонимины (нитроглицерин, изосорбида мононитрат, изосорбида динитрат, пентаэритритила тетранитрат, молсидомин);
Комбинированная антиангинальная терапия
Наличие жалоб на ангинозные боли пациентов с ИБС, получающих терапию первой линии, диктует необходимость подключения дополнительных антиишемических лекарственных средств. Алгоритм их применения представлен на рис. 2.
До инициации комбинированной антиангинальной терапии следует удостовериться, что целевая ЧСС достигнута с применением БАБ. В случае непереносимости БАБ, не связанной с наличием блокад, следует предпринять попытку назначения верапамила или дилтиазема в режиме монотерапии.
Добавление к БАБ препарата ивабрадин оправданно, только если ЧСС на фоне максимальной дозы БАБ (20 мг биспопролола или 400 мг метопролола) превышает 70 ударов в минуту либо если титрование дозы БАБ невозможно (например, в связи с хронической обструктивной болезнью легких или клинически выраженным атеросклерозом сосудов нижних конечностей). Применение ивабрадина совместно с малыми дозами БАБ с целью урежения ЧСС у больных, которые хорошо переносят БАБ, ввиду отсутствия доказательной базы следует отнести к нерациональным назначениям.
В том случае если на фоне целевой ЧСС больного продолжают беспокоить ангинозные боли, в качестве “второго” препарата оптимально назначать БКК [11], в ряде случаев можно также использовать длительно действующие нитраты/донаторы NO или никорандил.
Жалобы на наличие ангинозной боли у пациентов с ИБС, получающих терапию двумя антиангинальными препаратами, служат прямым показанием к проведению коронарографии с последующим решением вопроса о тактике реваскуляризации. В настоящее время ежедневная комбинированная терапия тремя и более антиангинальными препаратами может считаться оправданной только для тех пациентов, у которых по какой-либо причине проведение реваскуляризации невозможно.
Результаты
Исследование А
Полностью закончили исследование 28 пациентов. Двое больных выбыли из исследования в связи с неявкой на обследование. Перекрестный дизайн исследования обеспечил полную идентичность групп по возрасту (в среднем 47 [41–54] лет), полу (12 мужчин и 16 женщин), длительности АГ (2 [0–6] года) и индексу массы тела (29 [25–32] кг/м2). В табл. 1 представлена исходная характеристика гемодинамики в группах по данным офисного, “домашнего” и мониторного измерения АД.
. Исходная характеристика центральной гемодинамики (Me [ИИ]).
Выделенные группы были сопоставимыми по исходным параметрам гемодинамики и суточного профиля АД. Через две недели терапии доза бисопролола была увеличена до 10 мг 14 пациентам в группе Конкора (50,0 %) и 15 – в группе Бидопа (53,6 %). Доли пациентов с увеличенной дозой препарата в группах не различались (рχ2 = 0,79). В течение последующих четырех недель терапии 2 (7,1 %) пациентам, принимавшим оригинальный бисопролол, доза последнего была уменьшена до 5 мг в связи с развитием брадикардии < 55 уд./мин. К окончанию исследования средняя доза Конкора составила 7,0 ± 2,5 мг, Бидопа – 7,8 ± 2,5 мг (р = 0,25).
Динамика АД и ЧСС по данным офисного измерения на фоне приема исследуемых препаратов представлена в табл. 2.
. Динамика офисного АД и ЧСС на фоне лечения бисопрололом (Me [ИИ]).
Прием обоих препаратов в течение 2 и 6 недель приводил к статистически значимому снижению клинического АД и ЧСС по сравнению с исходными значениями. Средняя ЧСС к 6-йнеделе исследования в группе оригинального препарата была ниже, чем в группе генерика.
Динамика АД и ЧСС по данным самостоятельного контроля на фоне приема изучаемых препаратов представлена в табл. 3.
. Динамика домашнего АД и ЧСС на фоне лечения бисопрололом (Me [ИИ]).
АД и ЧСС достоверно уменьшались в обеих группах начиная со 2 недели приема препаратов. В группе Конкора отмечено дальнейшее снижение ДАД в интервале 2–6 недель. Средний уровень ДАД ко 2-й неделе исследования был ниже в группе Бидопа (на границе достоверности).
СМАД проведено двукратно на фоне первого этапа лечения. Пригодными для анализа оказались данные 12 пациентов первой группы и 13 –второй. В табл. 4 приведена динамика параметров СМАД на фоне приема препаратов бисопролола.
. Динамика показателей СМАД на фоне лечения бисопрололом (Me [ИИ]).
Данные, представленные в табл. 4, свидетельствуют о достоверном снижении среднесуточных АД и ЧСС на фоне лечения обоими препаратами. Прием генерического бисопролола в отличие от оригинального также приводил к уменьшению временных индексов гипертензии и росту индекса времени гипотензии по ДАД. На рис. 1–3 отображена степень гипотензивного и пульсурежающего эффектов Конкора и Бидопа. При офисном и мониторном измерении АД и ЧСС препараты оказа- лись одинаково эффективными как по гипотензивному, так и по пульсурежающему действию. При домашнем контроле АД степень снижения САД к 6-й неделе и ЧСС ко 2-й неделе лечения была бóльшей в группе Бидопа.
Целевое АД < 140/90 мм рт. ст. по окончании 6-недельного курса приема было достигнуто 20 пациентами первой группы (71,4 %) и 18 – второй (64,3 %; рχ2 = 0,57). Двоим пациентам группы Конкора (7,1 %) на дозе 10 мг/сут. была зарегистрирована брадикардия < 55 уд./мин, что не сопровождалось клиническими симптомами, однако потребовало снижения дозы препарата. Другие побочные нежелательные реакции, связанные с приемом исследуемых препаратов, не зафиксированы.
Исследование Б
Завершили исследование все включенные в него пациенты (18 больных). При рандомизации последовательности назначения препаратов для 10 больных первым препаратом был Конкор, вторым – Бидоп, для 8, наоборот, первым Бидоп, вторым –Конкор. Для 11 пациентов доза бисопролола составляла 10 мг, для 6 – 20 и для 1 – 5 мг (13,5 ± 2,8 мг). Анализ количества приступов стенокардии в контрольном периоде и на фоне приема Конкора и Бидопа показал существенное снижение приступов на фоне применения обоих препаратов. Общее количество приступов в контрольном периоде составило 3,8 ± 1,1, на фоне приема Конкора – 1,2 ± 0,3 (p < 0,01), на фоне приема Бидопа – 1,0 ± 0,2 (p < 0,01), количество приступов на фоне каждого из препаратов не различалось (p = 0,21).
На фоне приема Конкора и Бидопа САД, ДАД и ЧСС в покое достоверно уменьшилась по сравнению с данными показателями в контрольном периоде. Между группами достоверных различий этих показателей не отмечено (р > 0,05; табл. 5).
. Уровни АД и ЧСС в покое в контрольном периоде и на фоне лечения бисопрололом (Me [ИИ]).
При проведении исходного нагрузочного теста у всех пациентов зарегистрирована ишемическая депрессия сегмента ST. При проведении нагрузочного теста на фоне приема Конкора и Бидопа ишемическая депрессия сегмента ST также была зарегистрована для всех обследованных больных. При этом отмечено достоверное (р < 0,001) уменьшение степени депрессии сегмента ST на той же минуте нагрузки по сравнению с тестом, проведенным во время контрольного периода. На фоне приема Конкора степень депрессии сегмента ST уменьшилась в среднем на 29 %, на фоне приема Бидопа – на 34 %;различие между этими показателями недостоверно (р > 0,05). Увеличение продолжительности нагрузки на фоне приема Конкора и Бидопа более чем на 2 минуты наблюдалось у всех больных. При применении Бидопа увеличение нагрузки составило 186 ± 12 секунд, на фоне приема Конкора – 179 ± 11 секунд (р > 0,05).
Несмотря на увеличение продолжительности физической нагрузки и выполненной работы индекс пульсдавление на высоте нагрузки не изменялся. В контрольном периоде он соcтавил 18612 ± 87 ЕД, на фоне приема Конкора – 18423 ± 98, на фоне приема Бидопа – 18512 ± 85 ЕД (р > 0,05).
Ведение пациентов с рефрактерной стенокардией при невозможности проведения реваскуляризации
Концепция рефрактерной стенокардии включает три следующих фактора:
1. Ишемию миокарда;
2. Ангинозную боль;
3. Невозможность проведения реваскуляризации [12].
“Неподходящими” кандидатами для проведения реваскуляризации обычно считаются такие категории пациентов [12]:
• больные вазоспастической стенокардией;
• пациенты с подозрением на микрососудистую дисфункцию (с объективными признаками ишемии миокарда в отсутствие значимых стенозов коронарных артерий или с нормально функционирующими шунтами);
• больные, обладающие небольшим объемом ишемизированного миокарда, при невозможности проведения ангиопластики (например, с гемодинамически значимым симптом-связанным дистальным однососудистым поражением), стратифицированные в группу низкого риска;
• пациенты с диффузным, “нитевидным” коронарным атеросклерозом (характерно поражение двух и более коронарных артерий, захватывающее дистальное русло с артериями < 1 мм в диаметре);
• лица с очень высоким периоперационным риском (ввиду тяжелых сочетанных заболеваний, часто к этой группе относятся пожилые люди с многососудистым поражением).
Необходимо подчеркнуть, что заключение о невозможности проведения реваскуляризации должно приниматься полидисциплинарной командой и этот статус может быть пересмотрен с учетом изменения состояния больного, возможности привлечения опытной хирургической бригады, способной оперировать пациентов высокого риска.
Далее мы рассмотрим препараты, которые могут использоваться в схемах “максимизированной” антиангинальной терапии таких пациентов.
Одним из высокоэффективных антиангинальных препаратов является никорандил – активатор АТФ-зависимых калиевых каналов плазматической и митохондриальных мембран с нитратоподобными свойствами. Обычно к никорандилу прибегают в случае непереносимости БАБ и БКК, но он может использоваться и в составе комбинированной терапии. В двойном слепом исследовании, включившем больных стабильной стенокардией, было показано, что никорандил приводил к значимому увеличению толерантности к физической нагрузке, времени до появления ангинозной боли и депрессии ST ≥ 1 мм [13]. В рандомизированном клиническом исследовании (РКИ) IONA, включившем более 5000 больных хронической ИБС, никорандил, назначенный в дозе 20 мг 2 раза в сутки, продемонстрировал превосходство над плацебо в плане влияния на частоту госпитализаций, что было расценено как снижение риска развития нестабильной стенокардии. Примерно в трети случаев в первые дни после приема никорандила может отмечаться головная боль [13], также существует риск развития толерантности к его действию.
Другим перспективным лекарственным средством является ранолазин, частично ингибирующий окисление жирных кислот и блокирующий поздние натриевые каналы (работающие в диастолу). Ранолазин способен нивелировать индуцированную ишемией натриевую и кальциевую “перегрузку” кардиомиоцитов, улучшая перфузию и диастолическую функцию миокарда. Кроме того, он обладает антиаритмическим действием и способен снижать уровень гликозилированного гемоглобина у пациентов с сочетанием ИБС и СД.
В нескольких рандомизированных двойных слепых исследованиях (MARISA, ERICA, CARISA) показано, что ранолазин снижает частоту эпизодов стенокардии, потребление нитратов и повышает толерантность к физической нагрузке без клинически выраженного влияния на ЧСС и АД [14]. При этом в исследовании MERLIN TIMI 36 (Metabolic Efficiency With Ranolazine for Less Ischemia in Non-ST Elevation Acute Coronary Syndromes), в рамках которого пациенты с ОКС наблюдались в течение года, ранолазин не показал влияния на риск развития ОИМ и сердечно-сосудистую смертность. При лечении стенокардии у лиц с микрососудистой дисфункцией возможно также использовать препараты с анальгетическими свойствами, такие как ингибитор фосфодиэстеразы аминофиллин, антидепрессант имипрамин. Можно также применять методы психотерапии и кардиореабилитации [15].
Среди нелекарственных методов, которые могут облегчать состояние ряда пациентов с рефрактерной стенокардией, можно указать усиленную наружную контрпульсацию, ударно-волновую терапию и электростимуляцию спинного мозга [16]. Такая инвазивная процедура, как трансмиокардиальная лазерная реваскуляризация, согласно мета-анализу 7 исследований (n = 1137), не может быть признанной эффективным методом лечения рефракторной стенокардии [17].
В настоящее время уточняется эффективность таких экспериментальных методик лечения резистентной стенокардии, как клеточная терапия и применение факторов роста, активирующих ангиогенез, в т. ч. гранулоцитарно-макрофагального колониестимулирующего фактора, способного “мобилизовать” стволовые клетки костного мозга для участия в ангиогенезе коронарного русла.
Современные подходы к антиангинальной терапии при ишемической болезни сердца: в фокусе сиднонимины
Гиппократ указывал, что «боль в области сердца, которая появляется с определенной частотой у старых людей, является предзнаменованием внезапной смерти». Бартолетти (1576–1630), Гарвей (1527–1658), Морганьи (1684–1771) описывали случаи возникновения у пожилых и старых людей сильных острых болей в левой половине грудной клетки, сопровождавшихся беспокойством, страхом, удушьем, обмороком во время приступа. Первое описание классической стенокардии принадлежит У. Гебердену (1772), который для ее обозначения в своем докладе Лондонскому Королевскому обществу впервые применил термин «angina pectoris» и подробно и точно охарактеризовал клиническую картину грудной жабы («геберденова грудная жаба»). Parry (1799) первым указал на связь стенокардии с изменением структуры сердца и поражением коронарных артерий. Он же первым высказал предположение, что ангинозная (стенокардитическая) боль возникает вследствие уменьшения снабжения сердца кровью. В 1909 г. на первом съезде российских терапевтов было дано классическое описание клинической картины инфаркта миокарда в основополагающем труде В.П. Образцова и Н.Д. Стражеско «К симптоматологии и диагностике тромбоза коронарных артерий». (Страже́ско Николай Дмитриевич – впоследствии видный советский терапевт, организатор науки, академик АН СССР и академии наук Украины, Герой Социалистического Труда). В настоящее время сердечно–сосудистые заболевания прочно удерживают 1–е место среди всех причин смертности в экономически развитых странах, являясь одной из наиболее распространенных патологий среди хронических неинфекционных заболеваний. Несмотря на это, начиная со второй половины XX в. странах Западной Европы и Северной Америки наблюдается устойчивое снижение смертности от сердечно–сосудистых заболеваний. Эта тенденция отмечается в последние годы и в странах Восточной Европы [1,2]. В Российской Федерации от сердечно–сосудистых заболеваний умирают более 1 млн человек, т.е. примерно 700 человек на 100 тыс. населения. ИБС часто развивается у трудоспособных, творчески активных лиц, существенно ограничивая их социальную и трудовую активность, усугубляя социально–экономические проблемы в обществе [1–4]. Основой снижения заболеваемости и смертности при ИБС является борьба с управляемыми факторами риска заболевания. Так, еще в классическом Фрамингемском исследовании, начатом в США в 1949 г., показано, что риск развития ИБС связан с повышенным артериальным давлением, высоким уровнем холестерина, курением, нарушением толерантности к глюкозе и гипертрофией левого желудочка (результаты Фрамингемского исследования см. на интернет–сайте Национального сердечного института США – www.nhlbi.nih.gov/about/framingham, 1998). 1. Немодифицируемые (неизменяемые) факторы риска (ФР) ИБС [5–7]: • возраст старше 50–60 лет; • пол (мужской); • отягощенная наследственность. 2. Модифицируемые (изменяемые) ФР [5–7]: • дислипидемии (повышенное содержание в крови холестерина, триглицеридов и атерогенных липопротеинов и/или снижение содержания антиатерогенных ЛВП); • артериальная гипертензия (АГ); • курение; • ожирение; • нарушения углеводного обмена (гипергликемия, сахарный диабет); • гиподинамия; • хронический стресс; • нерациональное питание; • гипергомоцистеинемия и др. Сочетание у одного человека нескольких факторов риска значительно повышает опасность заболевания ИБС и, как правило, отягощает ее течение. Фармакотерапия ИБС предусматривает обязательное проведение профилактических мероприятий, направленных на устранение модифицируемых факторов риска ИБС. Важная роль при этом отводится коррекции АГ, нормализации уровня глюкозы у больных с сахарным диабетом, отказу от курения, комплексной модификации диеты, борьбе с избыточным весом, физическим тренировкам [1–3]. Лечение стенокардии напряжения предусматривает использование различных групп лекарственных средств, воздействующих на те или иные звенья патогенеза ИБС [3]. Основным патогенетическим фактором ИБС является нарушение кровотока в коронарных артериях, приводящее к дисбалансу между перфузией и метаболическими потребностями миокарда. Потребность миокарда в кислороде определяется напряжением миокардиальной стенки, частотой сердечных сокращений и сократимостью миокарда и зависит от метаболических процессов, связанных в том числе и с трансмембранными токами ионов кальция, от объема желудочков сердца и от величины систолического АД. Сократимость зависит от характера органического поражения сердца. Снабжение сердечной мышцы кислородом напрямую связано с состоянием коронарного кровотока, а величина последнего зависит и от коронарного сопротивления, и от активности симпатической нервной системы, и от уровня перфузионного давления, и от гемореологических свойств крови, в частности от уровня агрегации тромбоцитов [3,8–11]. Основными целями лечения больных ИБС являются: улучшение качества жизни пациента за счет снижения частоты приступов стенокардии и других актуальных для больного симптомов; профилактика острого инфаркта миокарда; улучшение выживаемости. Препараты, используемые для лечения ИБС: • Антиангинальные средства: – донаторы оксида азота – нитраты (нитроглицерин, изосорбида динитрат, изосорбида–5–мононитрат); – сиднонимины (молсидомин (Сиднофарм)); – β–адреноблокаторы (атенолол, бисопролол, пропранолол и др.); – антагонисты кальция (верапамил, дилтиазем и др.). • Противоатеросклеротические (гиполипидемические) средства. • Антитромбоцитарные препараты (ацетилсалициловая кислота, клопидогрел). • Метаболические средства (триметазидин). Целью антиангинальной терапии при ИБС является уменьшение числа приступов стенокардии в течение суток вплоть до полного их устранения. Это дает возможность больному быть в повседневной жизни достаточно активным, не чувствовать жизненного дискомфорта в связи со многими ограничениями, предшествовавшими лечению. Подобные изменения физического и психологического статуса больного объективно приводят к существенному улучшению качества его жизни. Кроме того, во многих случаях симптоматическая терапия позволяет больному продолжать профессиональную деятельность, если она не сопряжена с тяжелым физическим трудом. Успешным антиангинальное лечение считается в случае полного или почти полного устранения приступов стенокардии и возвращения больного к нормальной активности (стенокардия не более I функционального класса – ФК, когда болевые приступы возникают только при значительных нагрузках) и при минимальных побочных эффектах терапии [13–15]. Нитраты. Препараты нитратов при «грудной жабе» применяются уже около полутора столетий. Нитроглицерин был открыт Асканио Собреро в 1847 г. в Турине. Собреро также первым обратил внимание на сильную головную боль, вызываемую при пробе на язык малых количеств нитроглицерина. В 1849 г. К. Геринг, исследуя на добровольцах фармакологическое действие нитроглицерина, подтвердил, что его применение достаточно закономерно вызывает головную боль. В 1851 г. Уильям Меррелл (William Murrell) впервые использовал нитроглицерин при стенокардии в 1876 г., хотя в то время нитроглицерин был занесен в Британскую фармакопею лишь как лекарственное средство от повышенного кровяного давления. Меррелл, врач–практик, работавший в двух лондонских госпиталях одновременно, экспериментально определил оптимальную дозировку из соотношения эффективности и безопасности: 1%–ный спиртовый раствор нитроглицерина по 3 капли с пол унцией воды трижды в сутки. В таком виде препарат действовал значительно дольше, нежели амилнитрит, и более мягко. Публикация Меррелла, подводившая итоги нескольких лет исследований сначала на себе, а потом на пациентах со стенокардией, вошла в золотой фонд медицины. Год спустя фармацевтом Уильямом Мартиндейлом (William Martindale) была разработана твердая форма препарата: 1/100 грана нитроглицерина в шоколаде – которая, помимо удобства в использовании, имела лучшую усвояемость. В 1882 г. в США известная фирма Parke, Davis & Co. стала производить нитроглицерин уже в пяти различных дозировках. Индустрия производства нитроглицерина пережила расцвет в 1900 г., при этом рабочие данных предприятий подвергались значительному воздействию паров органических нитратов. Результаты воздействия проявились в виде явлений привыкания к нитратам (о чем свидетельствовали симптомы «болезни понедельника», «Monday disease», исчезающие к концу недели) и синдрома отмены (воскресные сердечные приступы, «Sunday Heart Attacks»). Механизм антиангинального действия нитратов заключается в уменьшении потребности миокарда в кислороде, что обусловлено снижением напряжения стенки желудочков, систолического артериального давления и объема желудочков. Кроме того, антиангинальное действие реализуется путем улучшения снабжения миокарда кислородом: за счет увеличения коронарного кровотока, снижения коронарного сопротивления, уменьшения спазма коронарных артерий и увеличения коллатерального кровотока. Они обладают также ингибирующими адгезию и агрегацию тромбоцитов и, очевидно, антитромботическими свойствами. Антиагрегационные эффекты нитратов могут рассматриваться как важное дополнение их антиишемического действия [1,2,12,14,15]. Нитраты легко проникают через все слизистые оболочки, а также через кожу, поэтому они доступны в многочисленных лекарственных формах. Эти лекарственные формы можно подразделить на следующие (табл. 1) [2]: 1. Всасывающиеся через слизистую оболочку рта. К ним относятся: а) Классические таблетки нитроглицерина для приема под язык, так называемые буккальные (т.е. предназначенные для аппликации на слизистую оболочку щеки или десны) лекарственные формы нитроглицерина и изосорбита динитрата. б) Аэрозоли нитроглицерина и изосорбита динитрата, которые способны оказывать столь же быстрое действие, как и сублингвальные таблетки нитроглицерина (эффект начинается в течение 60–90 с), но значительно более удобны в применении. 2. Для приема внутрь. Это различные таблетки и капсулы изосорбита динитрата, изосорбита мононитрата и нитроглицерина. Таблетки могут быть обычными либо специальными, сделанными таким образом, чтобы продлить действие препарата. 3. Для накожного применения. Мази нитроглицерина и специальные наклейки (пластыри) нитроглицерина для аппликации на кожу. Такие пластыри рассчитаны на действие в течение 24 ч. 4. Для внутривенного введения. Ампулы с раствором нитроглицерина и изосорбита динитрата. β–адреноблокаторы. Препараты этой группы применяются в лечении больных ИБС на протяжении более сорока лет. β–блокаторы являются препаратами первого выбора для лечения стенокардии, особенно у больных, перенесших инфаркт миокарда, так как они оказывают быстрый антиангинальный эффект и к тому же приводят к уменьшению смертности и частоты повторного инфаркта при длительном применении [1–3,14–15]. β–адреноблокаторы вызывают антиангинальный эффект путем снижения потребности миокарда в кислороде (за счет урежения частоты сердечных сокращений – ЧСС, снижения АД и сократительной способности миокарда), увеличения доставки к миокарду кислорода (в силу усиления коллатерального кровотока, перераспределения его в пользу ишемизированных слоев миокарда – субэндокарда), антиаритмического и антиагрегационного действия, снижения накопления кальция в ишемизированных кардиомиоцитах. Блокаторы кальциевых каналов (антагонисты кальция). Основной точкой приложения препаратов данной группы на уровне клетки являются медленные кальциевые каналы, по которым ионы кальция переходят внутрь гладкомышечных клеток кровеносных сосудов и сердца. В присутствии ионов кальция происходит взаимодействие актина и миозина, обеспечивающих сократимость миокарда и гладких мышечных клеток. Кроме того, кальциевые каналы «задействованы» в генерации пейсмекерной активности клеток синусового узла и проведении импульса по атриовентрикулярному узлу. Установлено, что вазодилатирующий эффект, вызванный антагонистами кальция, осуществляется не только посредством прямого действия на гладкую мускулатуру сосудистой стенки, но и опосредованно – через потенцирование высвобождения NO эндотелием сосудов. Этот феномен был обнаружен у большинства дигидропиридинов и исрадипина, в меньшей степени – у нифедипина и негидропиридиновых препаратов. Для длительного лечения стенокардии из производных дигидропиридинов рекомендуется использовать только пролонгированные лекарственные формы или длительно действующие препараты антагонистов кальция. Блокаторы кальциевых каналов – мощные вазодилататоры, они снижают потребность миокарда в кислороде, расширяют коронарные артерии. Препараты могут применяться при вазоспастической стенокардии, сопутствующих обструктивных легочных заболеваниях [1–2,15] Любой практикующий врач хорошо знает о высокой эффективности нитратов при стенокардии. В то же время нитраты нередко вызывают различные побочные эффекты – головную боль (иногда непереносимую), тошноту, гиперемию лица, артериальную гипотензию, сердцебиение; при регулярном приеме возможно развитие толерантности к данной группе препаратов. Кроме того, установлено, что применение нитратов показано далеко не всем больным ИБС. Согласно результатам исследований ISIS–4 и GISSI–3 (58 050 и 19 394 пациентов соответственно) применение нитратов у пациентов с инфарктом миокарда не приводит к улучшению их прогноза. Более того, менее представительные, но более длительные исследования MSMI (1072 пациента) и MDPIT (1779 пациентов) продемонстрировали, что длительный прием нитратов после инфаркта миокарда приводит к существенному ухудшению прогноза у этих больных. В последние годы появилось еще одно обстоятельство, затрудняющее применение органических нитратов у мужчин, страдающих ИБС: они несовместимы с приемом ингибиторов фосфодиэстеразы 5–го типа (ФДЭ5), к которым относятся силденафил, тадалафил и варденафил, применяемые при часто сочетающейся с ИБС эректильной дисфункции [16]. В качестве серьезной альтернативы нитратам могут рассматриваться, пожалуй, только препараты из группы сиднониминов; первый и типичный представитель – Сиднофарм, один из широко применяемых препаратов молсидомина, его отличительной характеристикой является соотношение стоимость–эффективность. Молсидомин является антиангинальным средством из группы сиднониминов. Не являясь нитратом по химическому строению, Сиднофарм (молсидомин) оказывает схожее с ними действие, поскольку способен отщеплять молекулу оксида азота – NO; сиднонимины и нитраты в настоящее время нередко объединяют в группу антиангинальных препаратов – донаторов оксида азота. При попадании в организм молсидомин метаболизируется в печени, превращаясь в активное производное – SIN–1. Последний, попадая в кровь, активируется (SIN–1A), и от него отщепляется NO–группа, воздействующая на процесс активации гуанилатциклазы. В результате ГТФ превращается в цГМФ, что приводит к расслаблению клеток мышечной оболочки сосудов и вазодилатации. Таким образом, вазодилатирующий эффект Сиднофарма близок к эффекту эндотелиального расслабляющего фактора. В коронарной системе расширяются главным образом эпикардиальные артерии. В венозной системе молсидомин расширяет преимущественно мелкие и средние сосуды, что способствует депонированию крови в ней, уменьшает приток крови к сердцу и преднагрузку на сердце. В больших дозах молсидомин оказывает расширяющее действие на артерии и артериолы, что способствует снижению периферического сопротивления, АД и посленагрузки. В отличие от органических нитратов, активирующих гуанилатциклазу лишь после образования S–нитрозотиола, Сиднофарм стимулирует образование цГМФ без предварительного взаимодействия с SH–группами. Поскольку действие молсидомина не зависит от SH–групп, толерантность к нему не развивается, в то время как истощение SH–групп является причиной развития толерантности к нитратам. Снижается сопротивление коронарных артерий и на 20% увеличивается кровоток, что улучшает кровоснабжение ишемизированных участков миокарда. При этом не наблюдается феномена обкрадывания миокарда. Снижается агрегация тромбоцитов, уменьшается образование тромбоксана, подавляется адгезия тромбоцитов к сосудистой стенке, увеличивается синтез простагландина (простациклина), который ингибирует агрегацию тромбоцитов и оказывает сосудорасширяющее действие [2,3]. Гемодинамические эффекты SIN–1 включают уменьшение систолического и конечного диастолического давления в левом желудочке, ударного объема, среднего артериального давления и системного сосудистого сопротивления, увеличение частоты сердечных сокращений и диастолического коронарного кровотока [17]. Кроме того, SIN–1 ингибирует внутрикоронарную агрегацию тромбоцитов in vitro [18] и при внутрикоронарном введении [19], а также способствует высвобождению простациклина, также препятствующего тромбообразованию [20]. В то же время прием молсидомина внутрь в дозе 8 мг 3 раза/сут. значимо не влиял на реологию крови у пациентов с ИБС [21]. Возможно также, что метаболит молсидомина SIN–1C обладает иммуномодулирующими свойствами, что может благоприятно влиять на течение иммунных процессов в очаге некроза при инфаркте миокарда. При длительном использовании сиднониминов толерантность к ним или к нитратам не развивается [16,22]. Действие молсидомина проявляется через 15–20 мин., продолжительность действия – от 1 до 6 ч (в среднем 4 ч). Для профилактики приступов стенокардии таблетки по 2–4 мг принимают 2–3 раза/сут. после еды либо применяется форма пролонгированного действия – таблетка 8 мг (ретард) 1 раз/сут. В более тяжелых случаях можно применять таблетку по 4 мг (форте) 3 раза/сут. или по 8 мг (ретард) 2 раза/сут. Для купирования приступов стенокардии при плохой переносимости нитроглицерина можно принять сублингвально 1–2 мг молсидомина (1/2–1 таблетку по 2 мг). Биодоступность препарата при приеме внутрь составляет 44–59%, концентрация в плазме достигает максимума в течение 1–2 ч, дальнейший метаболизм с высвобождением оксида азота и образованием метаболитов идет быстро; период полувыведения (Т1/2) SIN–1 составляет 1–2 ч. Препарат не выделяется в неизмененном виде, 90% метаболитов выводятся из организма с мочой. В пожилом возрасте при печеночной и сердечной недостаточности эффект первого прохождения через печень уменьшается, а период полувыведения увеличивается [23]. При тяжелой печеночной недостаточности (увеличение бромсульфалеиновой пробы до 20–50%) отмечено замедление выведения и увеличение концентрации молсидомина в плазме крови. Препарат не кумулирует (в т.ч. у больных с почечной недостаточностью). Молсидомин расширяет периферические венозные сосуды, оказывает антиагрегантное, аналгезирующее и антиангинальное действие. Его венодилатирующая активность обусловлена выделением после ряда метаболических превращений оксида азота (NО), стимулирующего растворимую гуанилатциклазу, в связи с этим молсидомин рассматривается как донатор NО. В результате этого происходит накопление цГМФ, который способствует расслаблению гладких мышц стенки сосудов (в большей степени – вен). Снижение преднагрузки даже без прямого влияния на сократимость миокарда приводит к восстановлению нарушенного при ИБС соотношения между потребностью миокарда в кислороде и его поступлением (на 26% уменьшается потребность в кислороде). Препарат снимает спазм коронарных артерий, улучшает коллатеральное кровообращение, увеличивает переносимость нагрузок, уменьшает число приступов стенокардии при физической нагрузке, подавляет раннюю фазу агрегации тромбоцитов, снижает выделение и синтез серотонина, тромбоксана и других проагрегантов. У больных с хронической сердечной недостаточностью молсидомин, снижая преднагрузку, способствует уменьшению размеров камер сердца. Он снижает давление в легочной артерии, уменьшает наполнение левого желудочка и напряжение стенки миокарда, ударный объем крови. Клиническая эффективность молсидомина при ИБС оценена в ряде клинических исследований. В частности, Messin R. и соавт. [24] провели многоцентровое рандомизированное двойное слепое плацебо–контролируемое 6–недельное исследование эффективности обычной (4 мг) и ретардированной (8 мг) форм препарата у 90 больных стабильной стенокардией напряжения. На фоне терапии выявлены достоверные повышение толерантности к нагрузке и уменьшение депрессии сегмента ST во время нагрузочных проб, уменьшение частоты ангинозных приступов и потребности в нитроглицерине, причем пролонгированная форма оказалась несколько эффективнее. В 1997 г. во Франции было проведено исследование ACCORD, в котором изучалось влияние сиднониминов на просвет коронарных артерий и прогноз у 700 больных, перенесших баллонную транслюминальную ангиопластику . Препаратом сравнения был дилтиазем. В качестве первичной точки отслеживалась шестимесячная летальность в группах сравнения, вторичными точками были частота рестенозов и изменение просвета коронарных артерий при повторной коронарографии через полгода. В исследовании установлено, что линcидомин и молсидомин в большей степени увеличивают просвет коронарных артерий, уменьшают частоту рестенозов по сравнению с дилтиаземом, но не влияют на прогноз жизни коронарных больных. Этим данным отчасти противоречат результаты двойного слепого плацебо–контролируемого исследования, проведенного Wohrle J., Hoher M. и соавт. [25]. Исследование включало 166 пациентов после коронарной ангиопластики, получавших в течение 6 мес. молсидомин 8 мг/сут. или плацебо. На фоне фармакотерапии частота рестенозов оказалась такой же, как в группе плацебо, однако функциональный класс стенокардии заметно снижался. Наряду с нитратами, сиднонимины могут использоваться у больных сердечной недостаточностью. Так Spring A. и соавт. изучали динамику изменения фракции выброса у 30 пациентов с сердечной недостаточностью. На фоне базовой терапии (ингибиторы АПФ, диуретики, сердечные гликозиды) фракция выброса составляла 33,8%, а через 3 мес. после добавления к терапии молсидомина (6 мг/сут.) она значимо увеличилась (до 44,8%). Проведенное сравнение влияния 24–часовой инфузии молсидомина и изосорбида 5–мононитрата (IS–5–MN) на уровень давления в легочной артерии в рандомизированном двойном слепом плацебо–контролируемом перекрестном исследовании у 15 пациентов с NYHA II–III показало, что молсидомин в большей степени снижает давление в легочной артерии. Интересное наблюдение сделали Lee S.–D. и соавт. (2001), описавшие трех пациентов с неспецифическим аортоартериитом и легочной гипертензией, у которых ингаляция оксида азота эффективно снижала давление в легочной артерии и легочное сосудистое сопротивление. Молсидомин (в отличие от нифедипина) в дозе 4 мг оказывал такой же эффект, на длительное время снижая одышку, улучшая гемодинамические параметры и увеличивая толерантность к нагрузке. В последнее время появились также данные о возможности применения молсидомина при лечении первичной легочной гипертензии у новорожденных. Также одним из показаний для применения молсидомина может быть цирроз печени с явлениями портальной гипертензии. Известно, что применение нитратов и b–блокаторов позволяет уменьшить давление в системе воротной вены. Hori N. и соавт. в 1996 г. были опубликованы результаты экспериментального исследования на крысах, в ходе которого было показано, что молсидомин эффективнее, чем пропранолол, снижает давление в воротной вене у экспериментальных животных, а комбинация этих препаратов имеет полный аддитивный эффект. Полученные данные создают предпосылки для продолжения исследования эффективности молсидомина (Сиднофарма) при легочной и портальной гипертензии. Таким образом, Сиднофарм (молсидомин) может применяться при следующих клинических состояниях. – Стабильная стенокардия напряжения – при стенокардии напряжения II ФК препарат может применяться эпизодически в дозе 2–4 мг за 30–60 мин. до физической нагрузки (или иной ситуации, стереотипно вызывающей приступ стенокардии). При стенокардии напряжения III–IV ФК препарат может назначаться в суточной дозе 16 мг (4 мг 4 раза/сут.). – Острый коронарный синдром – применение Сиднофарма целесообразно в случаях непереносимости органических нитратов или быстрого развития толерантности к ним. Не следует применять Сиднофарм при наличии нестабильной гемодинамики. – Ранняя постинфарктная стенокардия – Сиднофарм не менее эффективно, чем органические нитраты, уменьшает количество приступов стенокардии в суточной дозе 16 мг (простая или ретардная формы). – Застойная сердечная недостаточность – Сиднофарм может использоваться как дополнение к стандартной терапии (иАПФ, диуретики, сердечные гликозиды, b–адреноблокаторы) в случаях ее недостаточной эффективности. Кроме того, Сиднофарм (молсидомин) может назначаться на ночь при развитии ночных приступов сердечной астмы. На фоне терапии молсидомином возможно развитие побочных явлений, включая артериальную гипотензию (особенно при одновременном приеме алкоголя), головную боль в начале лечения; редко наблюдаются головокружение, тошнота, аллергические реакции в виде кожных высыпаний, бронхоспазма. Возможны головная боль, замедление скорости психомоторных реакций, тошнота, потеря аппетита, диарея. Противопоказаниями к применению препарата являются кардиогенный шок; артериальная гипотония; глаукома (особенно закрытоугольная); I триместр беременности и период лактации; понижение центрального венозного давления; повышенная чувствительность к компонентам препарата. Одновременное применение Сиднофарма с сосудорасширяющими, антигипертензивными средствами и этанолом увеличивает выраженность гипотензивного эффекта. При одновременном применении Сиднофарма с ацетилсалициловой кислотой усиливается ее антиагрегантное действие. Таким образом, к преимуществам препарата относятся доказанная эффективность при ишемической болезни сердца, стенокардии напряжения и застойной сердечной недостаточности, лучшая по сравнению с нитратами переносимость и отсутствие толерантности к препарату при регулярном приеме в течение длительного времени. Все это определяет широкие перспективы применения в широкой клинической практике антиангинального препарата молсидомина (Сиднофарм), особенно в условиях роста заболеваемости сердечно–сосудистой патологией, роста резистентности к нитратам и зачастую их плохой переносимости.
Литература 1. Щукин Ю.В., Рябов А.Е. Хроническая ишемическая болезнь сердца в пожилом и старческом возрасте. Пособие для врачей. — Самара: Издательство «Волга–Бизнес», 2008. — 44 с. 2. Косарев В.В., Бабанов С.А. Клиническая фармакология лекарственных средств, применяемых при сердечно–сосудистых заболеваниях.–Самара.–«Офорт».–2010.–140с. 3. Косарев В.В., Бабанов С.А., Астахова А.В. Фармакология и лекарственная терапия. Под ред. В.К.Лепахина. М.: Эксмо, 2009. 4. Шальнова С.А., Деев А.Д., Оганов Р.Г. Факторы, влияющие на смертность от сердечно–сосудистых заболеваний в российской популяции. Кардиоваск. тер. и проф. 2005; 4 (1): 4–9. 5. Российские рекомендации «Диагностика и коррекция нарушений липидного обмена с целью профилактики и лечения атеросклероза». Секция атеросклероза ВНОК // Кардиоваскулярная терапия и профилактика.2004. № 2(приложение).36 с. 6. The Cholesterol and Recurrent Events Trail Investigators. The 14. effect of pravastatin on coronary events after myocardial infarction in patientd with average cholesterol levels. N Engl J Med 1998; 335: 1001–9. 7. Athyros 15. VG, Papageorgiou AA, Mercouris BR. The Greak Atorvastatin and acoranary heart disease Evaluation (GREECE) Study. Curr Med Res Opin 2002; 18: 220–8. 8. Serruys PW, de Feuter P, Macaya C et al. Intervention Prevention 16. Study (LIPID) Investigators. Fluvastatin for prevention of cardiac events following successful first percutaneous coronary intervention: a randomized controlled trail. JAMA 2002; 287: 3215–2. 9. Shepherd J, Cobbe SM, Ford I et 17. al., for the West of Scotland Coronary Prevention Study Group. Prevention of coronary heart disease with pravastatin in men with hypercholesterolemia. N Engl J Med 1995; 333: 1301–7. 10. Downs JR, Clearfield M, Weis S et al., for the 18. AFCAPS/TexCAPS Research Group, (1998). Primary Prevention of Acute Coronary Events With Lovastatin in Men and Women With Average Cholesterol Levels: Results of AFCAPS/TexCAPS. JAMA 279: 1615–22. 11. Kleemann R., Kooistra T. HMG–CoA Reductase Inhibitors: Effects on Chronic Subacute Inflammation and Onset of Atherosclerosis Induced by Dietary Cholesterol. Curr Drug Targets Cardiovasc Haematol Disord. 2005 Dec;5(6):441–53. 12. Оганов Р. Г., Масленникова Г. Я. Сердечно–сосудистые заболевания в Российской Федерации во второй половине ХХ столетия: тенденции, возможные причины, перспективы. – Кардиология, 2000. – №6. – С. 4–8. 13. Ольбинская Л. И., Лазебник Л. Б. Донаторы оксида азота в кардиологии. – М., 1998. – 172 с. 14. Аронов Д.М., Лупанов В.П. Диагностика и лечение хронической ишемической болезни сердца. Качество жизни. Медицина. 2003; 2: 16–24. 15. Лупанов В.П. Стабильная стенокардия: тактика лечения и ведения больных в стационаре и амбулаторных условиях. Рус. мед. журн. 2003; 11 (9): 556–63. 16. Agvald P, Adding LC, Gustafsson LE, Persson MG. Nitric oxide generation, tachyphylaxis and cross–tachyphylaxis from nitrovasodilators in vivo. Eur J Pharmacol. 1999. 1999; 385(2–3):137–45. 17. Arkonac BM, Kersten JR, Wynsen JC, Nijhawan N, Warltier DC. Differential hemodynamic effects of the nitric oxide donor pirsidomine in comparison to SIN–1, nitroprusside, and nitroglycerin. Pharmacology. 1996; 52:92–100. 18. Darius H, Ahland B, Rucker W, Klaus W, Peskar BA, Schror K. The effects of molsidomine and its metabolite SIN–1 on coronary vessel tone, platelet aggregation, and eicosanoid formation in vitro: Inhibition of 12–HPETE biosynthesis. J Cardiovasc Pharmacol. 1984; 6:115–121. 19. Ovize M, Lorgeril M, Cathignol D, Delaye J, Renaud S. Inhibition of coronary artery thrombosis by SIN–1, a donor of nitric oxide. J Cardiovasc Pharmacol. 1990; 16:641–645. 20. Salvemini D, Currie MG, Mollace V. Nitric oxide–mediated cyclooxygenase activation: A key event in the antiplatelet effects of nitrovasodilators. J Clin Invest. 1996; 97:2562–2568. 21. Wohrle J, Nusser T, Hoffmeister A, Kestler HA, Grebe OC, Hoher M, Hombach V, Koenig W, Kochs M. . Dtsch Med Wochenschr. 2003; 128(24):1333–7. 22. Schror K, Forster S, Woditsch I. On–line measurement of nitric oxide release from organic nitrates in the intact coronary circulation. Naunyn–Schmiedeberg’s Arch Pharmacol. 1991, 344:240–246. 23. Rosenkranz B, Winkelmann BR, Parnham MJ. Clinical pharmacokinetics of molsidomine. Clin Pharmacokinet. 1996; 30(5):372–84. 24. Messin R, Karpov Y, Baikova N, Bruhwyler J, Monseu MJ, Guns C, Geczy J. Short– and long–term effects of molsidomine retard and molsidomine nonretard on exercise capacity and clinical status in patients with stable angina: a multicenter randomized double–blind crossover placebo–controlled trial. J Cardiovasc Pharmacol. 1998; 31(2):271–6. 25. Wohrle J, Hoher M, Nusser T, Hombach V, Kochs M. No effect of highly dosed nitric oxide donor molsidomine on the angiographic restenosis rate after percutaneous coronary angioplasty: a randomized, placebo controlled, double–blind trial. Can J Cardiol. 2003; 19(5):495–500. 26. Lee S.–D., Kim D.–S., Shim T.–S., Lim C.–M., Koh Y., Kim W.–S., Kim W.–D. Nitric Oxide and Molsidomine in the Management of Pulmonary Hypertension in Takayasu’s Arteritis. Chest, 2001; 119(1): 302 – 307.
Метаболическая и антиоксидантная терапия
“Антиоксидантная терапия” гармонично вписывается в традиционные схемы лечения ИБС благодаря использованию таких препаратов, как статины, иАПФ, карведилол, обладающих выраженным антиоксидантным действием. При этом благоприятные антиишемические, кардиопротективные и антиатеросклеротические эффекты “чистых” антиоксидантов (биофлавоноидов, полифенолов, витаминов, глутатиона, эмоксипина, этилметилгидроксипиридина), показанные на различных биологических моделях, в настоящее время не были продемонстрированы ни в одном крупном клиническом исследовании. В нескольких проспективных плацебо-контролируемых РКИ были показаны нейтральные и даже негативные эффекты витаминов [18]. Недавно обнаружилось, что ряд экспериментов, в которых было показано положительное действие кверцетина, проведен с грубейшими нарушениями биомедицинской этики [19]. Таким образом, использование больными ИБС антиоксидантов, в т. ч. в составе БАД, не оправданно.
Метаболические препараты также имеют достаточно скудный доказательный базис. В связи с этим Европейское агентство по оценке лекарственных средств сократило спектр показаний к применению препарата триметазидин, который может использоваться лишь в качестве дополнительного антиангинального средства в случае непереносимости или недостаточной эффективности терапии первой линии [20]. В качестве сферы рационального применения триметазидина в составе комплекс ной антиангинальной терапии можно указать стенокардию, обусловленную микрососудистой дисфункцией.
В России при лечении пациентов с ИБС также применяется препарат мельдоний – аналог γ-бутиробетаина. Мельдоний ингибирует фермент γ-бутиробетаин-гидроксилазу, что приводит к замедлению биосинтеза карнитина и транспорта длинноцепочечных жирных кислот через митохондриальную мембрану in vitro (при этом β-окисление жирных кислот замедляется, происходит “переключение” внутриклеточного метаболизма на гликолиз). Обратным действием обладает препарат L-карнитин, ускоряющий транспорт длинноцепочечных жирных кислот в митохондрии, β-окисление которых значительно более выгодно энергетически, но и требует бoльших количеств кислорода. Вопрос о том, какая из данных стратегий может считаться оптимальной в условиях клинической практики, когда длительно существующая хроническая ишемия миокарда может смениться острой при развитии ОКС, остается открытым.