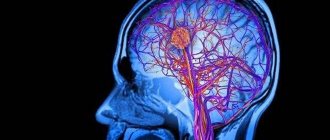
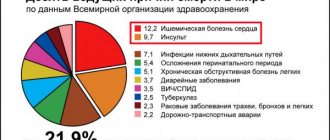
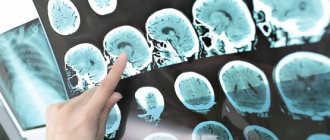
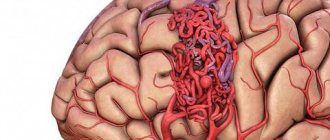
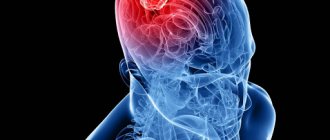
Инсульт мозжечка до сих пор относится к наименее изученным заболеваниям центральной нервной системы. Вариабельность клинических проявлений, их сходство с симптомами поражения полушарий головного мозга и другие особенности значительно затрудняют диагностику. Возникает эта патология относительно редко: приблизительно 2% пациентов с острыми нарушениями церебрального кровообращения имеют локализацию очага в мозжечке. Страдают чаще мужчины среднего и пенсионного возраста. Какие характерные симптомы заболевания и как лечить такой инсульт? Ответы на эти вопросы — в нашей статье.
Виды мозжечкового инсульта
По стандартной классификации на основе патогенеза выделяют два вида мозжечкового инсульта:
- ишемический;
- геморрагический.
По статистике, значительно преобладает первый вид. На долю ишемического поражения мозжечка, по данным различных источников, приходится от 80 до 90 процентов случаев. Однако по прогнозам специалистов, уже через 50 лет ожидается удвоение числа заболеваний с геморрагической природой — результат старения и изменения расового состава населения планеты.
Ишемический мозжечковый инсульт
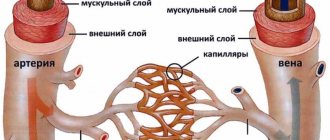
В основе развития ишемического поражения мозжечка лежит частичная или полная закупорка тромбом сосудов, приносящих артериальную кровь. В связи с этим нервные клетки перестают получать кислород, а также питательные вещества. Как известно, нервная ткань очень чувствительна к гипоксии, и если кровоток не нормализовать, то нейроны начинают гибнуть.
Геморрагический мозжечковый инсульт
При геморрагической природе заболевания происходит резкое нарушение кровоснабжения мозжечка вследствие разрыва артерии или капилляра, питающего эту структуру. В связи с анатомическими особенностями кровообращения последствия сосудистой катастрофы очень тяжело спрогнозировать, так как в патологический процесс часто вовлекается ствол головного мозга.
Диагностика
С целью подтверждения диагноза мозжечковый инсульт проводят УЗИ. Исследование позволяет определить смещение, увидеть область отеков, обнаружить поврежденную артерию.
Информативным методом диагностики является магнитно-резонансная томография или компьютерная томография. Оба способа дают точную картину изменений, размер повреждений, глубину, обнаружить причину заболевания.
Берется анализ крови на общую формулу и биохимию. Данные позволят выявить уровень содержания сахара, холестерина, других веществ, которые являются признаками болезней, спровоцировавших удар.
Симптомы инсульта мозжечка
Клиническая картина как ишемического, так и геморрагического нарушения кровоснабжения мозжечка разнообразна, но имеются характерные симптомы, позволяющие заподозрить поражение кровеносных сосудов именно в этой зоне. К ним относится мозжечковая атаксия. Этот синдром связан с функциональной деятельностью мозжечка и включает:
- Нарушение равновесия. Пациент не может устойчиво стоять, при ходьбе раскачивается в разные стороны.
- Изменения в речи. Нарушение поступления артериальной крови в мозжечок сопровождается скандированной речью. Пациент громко пытается произнести обычные слова.
- Потеря точности в движениях. Больному трудно контролировать мелкую моторику, движения становятся размашистыми.
- Тремор. Появляется дрожание конечностей, головы, туловища.
- Нистагм. Глазные яблоки совершают непроизвольные колебательные движения. Их частота может достигать нескольких сотен в минуту.
Среди общих симптомов, характерных для острого нарушения церебрального кровообращения, можно выделить головную боль, головокружение, спонтанную рвоту, лихорадку, утрату сознания, нарушение глотания, паралич мускулатуры.
Ишемический инсульт в бассейне задних мозговых артерий: проблемы диагностики, лечения
И.А. ХАСАНОВ, Э.И. БОГДАНОВ
Республиканская клиническая больница МЗ РТ, г. Казань
Казанский государственный медицинский университет
Хасанов Ильдар Акрамович
врач неврологического отделения для больных с острыми нарушениями мозгового кровообращения
420064, г. Казань, ул. Оренбургский Тракт, д. 138, тел. (843) 237-35-47, e-mail
В статье в свете современных данных рассматриваются проблемы диагностики и лечения ишемических инсультов в бассейне задних мозговых артерий (ЗМА) с учетом особенностей их этиологии, клинической картины и данных нейровизуализации.Парные задние мозговые артерии, формирующиеся путем бифуркации базилярной артерии и являющиеся ее терминальными ветвями, служат основными источниками кровоснабжения верхней части среднего мозга, таламусов и задне-нижних частей полушарий головного мозга, включая затылочные доли, медиобазальные отделы височных долей и нижнемедиальные отделы темени.Ишемические инсульты в бассейне задних мозговых артерий составляют, по разным данным, от 5-10 до 25% случаев всех ишемических инсультов.Наиболее частой причиной изолированных инфарктов в бассейне ЗМА является эмболическая окклюзия ЗМА и ее ветвей, которая имеет место примерно в 82% случаев.В 9% случаев в ЗМА выявляется тромбоз in situ, еще в 9% случаев причиной инсульта служат вазоконстрикция, связанная с мигренью, и коагулопатии.Очень редкой причиной инфаркта в данном бассейне может быть и артериальная диссекция, затрагивающая ЗМА.Наиболее частыми и характерными признаками инфарктов в бассейне ЗМА являются зрительные нарушения (гомонимная гемианопсия), центральный парез лицевого нерва, головная боль, нарушения чувствительности, афатические нарушения, гемипарез и ниглект.
Ключевые слова:
ишемический инсульт, инфаркт мозга, задняя мозговая артерия, нейровизуализация, тромболитическая терапия
I.A. KHASANOV, E.I. BOGDANOV
Kazan State Medical University
Republican Clinical Hospital of the Ministry of Health of the Republic of Tatarstan, Kazan
Ishemic stroke in a system of posterior cerebral arteries: problems of diagnosis and treatment
In the article on the basis of present knowledge are considered the problems of diagnosis and treatment of ishemic strokes in a system of posterior cerebral arteries (PCA) taking into account their causation, clinical presentation and neuroimaging data.Paired posterior cerebral arteries, which are shaped by basilar artery bifurcation and are its terminal branches, are the main sources of blood supply of the upside of midbrain, thalamus and back and bottom parts of cerebral hemispheres, including occipital lobes, mediobasal branches of temporal lobes and lower medial crown branches.Ishemic strokes in a system of posterior cerebral arteries amount to 5-10% or up to 25% of all ishemic strokes.The most common cause of isolated heart attacks
in a system of PCAistheembolic occlusionof PCAand its branches, which occurs in about 82% of cases.In 9% of cases in PCAisrevealed thrombosis, inother9% of cases the cause of stroke are vasoconstriction associated with migraine, and coagulopathy.A very seldom reason for a heart attack in this system can be artery dissection which affects PCA.The most frequent and characteristic features of heart attacks in a system of PCA are visual impairments (equilateral hemianopsia), central paresis of facial nerve, headache, sensation disorders, aphatic disorders, hemiparesis and neglect.
Key words:
ischemic stroke, cerebrovascular accident, posterior cerebral artery, neuroimaging, thrombolytic therapy.
Ишемические инсульты в бассейне задних мозговых артерий (ЗМА) составляют, по разным данным, от 5-10 до 25% случаев всех ишемических инсультов [1-4]. Они могут явиться причиной целого ряда клинических симптомов, далеко не всегда своевременно и адекватно распознающихся самими пациентами, их родственниками и врачами, ведь остро возникший грубый моторный дефицит, с которым обычно ассоциируется инсульт, в этом случае может быть невыраженным или вовсе отсутствовать. Отсрочка в своевременной диагностике или некорректный диагноз ставят под сомнение возможность проведения больному адекватной терапии (прежде всего тромболизиса), что в свою очередь не может не влиять на исход болезни [5]. Большую роль в постановке диагноза играет возможность использования нейровизуализации, правильный выбор метода и грамотная интерпретация результатов [2]. Видится важным представление и анализ особенностей клинической картины, нейровизуализации и лечения ишемических инсультов в бассейне задних мозговых артерий в свете современных данных.
Наиболее частой причиной изолированных инфарктов в бассейне ЗМА является эмболическая окклюзия ЗМА и ее ветвей, которая имеет место в 82% случаев. При этом кардиогенный генез наблюдается в 41% случаев, в то время как артерио-артериальная эмболия из позвоночных и базилярной артерий — лишь в 32% случаев. У 10% пациентов источник эмболии установить не удается. В 9% случаев в ЗМА выявляется тромбоз in situ. Вазоконстрикция, связанная с мигренью, и коагулопатии являются причинами инфаркта мозга в 9% случаев [6]. Если изолированные инфаркты в бассейне ЗМА в большинстве случаев имеют кардиоэмболическую природу, то вовлечение ствола мозга и/или мозжечка в сочетании с инфарктом в бассейне ЗМА наиболее часто связано с атеросклеротическим поражением сосудов вертебробазилярного бассейна [7, 8]. Очень редкой причиной инфаркта в данном бассейне может быть и артериальная диссекция, затрагивающая ЗМА [9]. Вне зависимости от причины инфаркта обычно он лишь частично захватывает бассейн ЗМА [10, 11].
Парные задние мозговые артерии, формирующиеся путем бифуркации основной артерии и являющиеся ее терминальными ветвями, служат основными источниками кровоснабжения верхней части среднего мозга, таламусов и задне-нижних частей полушарий головного мозга, включая затылочные доли, медиобазальные отделы височных долей и нижнемедиальные отделы темени [10, 12, 13].
На ранних стадиях развития организма человека задняя мозговая артерия представляет собой ветвь внутренней сонной артерии (ВСА) и кровоснабжается из системы каротид, при этом задняя соединительная артерия (ЗСА) исполняет роль ее проксимального сегмента. В последующем кровь в задние мозговые артерии начинает поступать из основной артерии, а ЗСА, являясь ветвью внутренней сонной артерии, становится наиболее значимым анастомозом между каротидным и вертебробазилярным бассейнами. По разным данным, от 17 до 30% взрослых людей имеют фетальный (эмбриональный) тип строения ЗМА, при котором ВСА в течение всей жизни остается основным источником кровоснабжения ЗМА. Фетальный тип строения ЗМА в большинстве случаев наблюдается унилатерально, при этом противоположная ЗМА обычно начинается от асимметрично расположенной, изогнутой базилярной артерии. В случаях, когда обе задние мозговые артерии являются ветвями внутренних сонных артерий, как правило, наблюдаются хорошо развитые крупные задние соединительные артерии, а верхний сегмент базилярной артерии бывает короче, чем обычно (базилярная артерия заканчивается отходящими от нее двумя верхними мозжечковыми артериями). Примерно в 8% случаев обе ЗМА исходят из одной и той же ВСА [7, 8, 12, 14, 15].
ЗСА впадает в ЗМА примерно на 10 мм дистальнее места бифуркации базилярной артерии. Каждую ЗМА условно можно разделить на 3 части: предкоммуникационная часть, или Р1-сегмент по Фишеру, — участок ЗМА проксимальнее места впадения в нее ЗСА, посткоммуникационная часть, или Р2-сегмент, расположенный дистальнее места впадения ЗСА в ЗМА, и конечная (корковая) часть, отдающая ветви к соответствующим областям коры головного мозга [12, 16]. От предкоммуникационной части отходят парамедианная мезенцефалическая, задняя таламоперфорирующая и медиальная задняя хороидальная артерии, участвующие преимущественно в кровоснабжении вентролатеральных ядер таламуса и медиального коленчатого тела. Левая и правая задние таламоперфорирующие артерии могут отходить от общего ствола, называемого артерией Першерона; подобный вариант строения обычно встречается в сочетании с односторонней гипоплазией Р1-сегмента и фетальным строением ЗМА. Ветвями посткоммуникационной части являются педункулярные перфорантные, таламо-геникулятная и латеральная задняя хороидальная артерии, кровоснабжающие латеральное коленчатое тело, дорсомедиальные ядра и подушку таламуса, часть среднего мозга и латеральную стенку бокового желудочка [2, 12, 17]. Основными корковыми ветвями ЗМА являются передняя и задняя височные, теменно-височная и шпорная артерии [10]. Границы водораздела бассейнов средней и задней мозговых артерий значительно колеблются. Обычно границей бассейна ЗМА служит сильвиева борозда, но иногда средняя мозговая артерия кровоснабжает и наружные отделы затылочной доли вплоть до затылочного полюса. При этом ЗМА всегда снабжает кровью участки коры головного мозга в области шпорной борозды, а зрительная лучистость в ряде случаев получает кровь из средней мозговой артерии, соответственно, гомонимная гемианопсия не всегда подразумевает инфаркт в бассейне ЗМА [12].
При ишемических инсультах в бассейне ЗМА в зависимости от локализации окклюзии сосуда, а также от состояния коллатерального кровоснабжения в клинической картине могут выявляться симптомы поражения среднего мозга, таламусов и полушарий головного мозга. В целом до 2/3 всех инфарктов в бассейне ЗМА являются корковыми, таламусы вовлекаются лишь в 20-30% случаев, а средний мозг менее чем в 10% случаев [7, 18, 19]. Соответственно наиболее частым вариантом ишемического инсульта в бассейне ЗМА является изолированный инфаркт полушарий большого мозга, в первую очередь затылочных долей, реже встречается сочетанное поражение таламусов и мозговых полушарий, в небольшом проценте случаев — изолированный инфаркт таламуса и, наконец, комбинация поражения среднего мозга, таламуса и/или гемисфер является наиболее редким вариантом [2].
Иногда наблюдается билатеральное поражение областей мозга, кровоснабжаемых из ЗМА. Это имеет место в первую очередь при синдроме верхушки базилярной артерии (top of the basilar syndrome), который представляет собой эмболическую окклюзию дистального отдела основной артерии и характеризуется угнетением сознания, зрительными нарушениями, глазодвигательными и поведенческими расстройствами, часто без моторной дисфункции [2].
По данным ряда авторов, наиболее частыми и характерными признаками инфарктов в бассейне ЗМА являются зрительные нарушения (до 95% случаев), гомонимная гемианопсия (66,7% случаев), центральный парез лицевого нерва (52% случаев), головная боль, преимущественно в затылочной области (50 случаев), нарушения чувствительности (40% случаев), афатические нарушения (38% случаев), гемипарез (18% случаев) и ниглект (10% случаев). Пациенты обычно имеют комбинацию симптомов [2, 7, 8, 11].
Гомонимная гемианопсия возникает с контрлатеральной стороны при инфарктах в зонах кровоснабжения полушарных ветвей ЗМА вследствие поражения стриарной коры, зрительной лучистости или латерального коленчатого тела. В отсутствие вовлеченности затылочного полюса макулярное зрение остается сохранным. Дефект полей зрения может ограничиваться лишь одним квадрантом. Верхнеквадрантная гемианопсия возникает при инфаркте стриарной коры ниже шпорной борозды или нижней части зрительной лучистости в височно-затылочной области. Нижнеквадрантная гемианопсия — следствие поражения стриарной коры выше шпорной борозды или верхней части зрительной лучистости в теменно-затылочной области. Окклюзия шпорной борозды также может быть ассоциирована с болями в ипсилатеральном глазу. Нарушения зрения могут иметь и более сложный характер, особенно при двустороннем поражении затылочных долей, включая зрительные галлюцинации, зрительную и цветовую агнозию, прозопагнозию (агнозия на знакомые лица), синдром отрицания слепоты (синдром Антона), дефицит зрительного внимания и оптико-моторную агнозию (синдром Балинта). Часто нарушения зрения сопровождаются афферентными нарушениями в виде парестезий, расстройств глубокой, болевой и температурной чувствительности. Последние указывают на вовлечение таламуса, теменной доли либо ствола мозга (вследствие окклюзии проксимальных отделов вертебробазилярного бассейна) [2, 8, 10, 20].
Нейропсихологические нарушения, ассоциированные с инфарктами в ЗМА, значительно варьируют и присутствуют более чем в 30% случаях. Инсульт в бассейне мозолистых ветвей левой ЗМА у правшей, затрагивающий затылочную долю и валик мозолистого тела, проявляется алексией без аграфии, иногда цветовой, предметной или фотографической аномией. Правополушарные инфаркты в бассейне ЗМА нередко вызывают контрлатеральный геминиглект. При обширных инфарктах с вовлечением медиальных отделов левой височной доли или двусторонних мезотемпоральных инфарктах развивается амнезия. Также при моно- или билатеральном мезотемпоральном инфаркте может развиться ажитированный делирий. Обширные инфаркты в бассейне левой задней височной артерии клинически могут проявляться аномией и/или сенсорной афазией. Таламические инфаркты в зонах кровоснабжения пенетрирующих ветвей ЗМА могут вызывать афазию (при заинтересованности левой подушки), акинетический мутизм, глобальную амнезию и синдром Дежерина – Русси (расстройства всех видов чувствительности, грубые дизестезии и/или таламическая боль и вазомоторные нарушения в контрлатеральной половине тела, сочетающиеся с обычно преходящим гемипарезом, хореоатетозом и/или баллизмом). Также инфаркты в бассейне ЗМА могут быть ассоциированы с дискалькулией, пространственной и временной дезориентацией. [6, 12, 21, 22].
Билатеральные таламические инфаркты нередко связаны с глубокой комой. Так, окклюзия артерии Першерона вызывает развитие двусторонних инфарктов в интраламинарных ядрах таламусов, что приводит к тяжелому нарушению сознания [2, 12].
Гемипарез при инфарктах в бассейне ЗМА встречается лишь у 1/5 больных, чаще является легким и преходящим и обычно ассоциирован с вовлечением в патологический процесс ножек мозга [23, 24]. Описаны случаи инфарктов в бассейне ЗМА, когда у больных выявлялся гемипарез без вовлечения ножек мозга. У этих пациентов имело место поражение дистальных отделов ЗМА, в первую очередь заинтересованность таламо-геникулятной, латеральной и медиальной задних хороидальных артерий [23, 25]. Предполагается, что гемипарез при инфарктах в бассейне задних хороидальных артерий может быть связан с поражением кортико-бульбарных и кортико-спинальных трактов, даже при отсутствии видимого поражения внутренней капсулы или среднего мозга по данным нейровизуализации [23]. Существуют мнения, что развитие гемипареза связано со сдавлением внутренней капсулы отечной тканью таламуса [12].
Инфаркты в бассейне ЗМА имитируют инфаркты в каротидном бассейне у 17,8% пациентов [24], особенно при сочетанном поражении поверхностных и глубоких ветвей ЗМА, которое наблюдается приблизительно в 38% случаев [7, 19, 26]. Дифференциальная диагностика бывает затруднена вследствие наличествующих афатических нарушений, ниглекта, сенсорного дефицита, а также обычно легкого и преходящего гемипареза, возникающего вследствие вовлечения пирамидных трактов. Кроме того, нарушения памяти и другие остро возникшие нейропсихологические нарушения могут существенно осложнять обследование таких пациентов [2, 18, 19].
Среди других состояний, нередко клинически имитирующих инфаркты в бассейне ЗМА, следует выделить некоторые инфекционные заболевания (в первую очередь токсоплазмоз), синдром задней обратимой лейкоэнцефалопатии, неопластические поражения, как первичные, так и метастатические, и таламические инфаркты, вызванные тромбозом глубоких мозговых вен [2, 27]. Зачастую при постановке диагноза определяющую роль играют методы нейровизуализации.
Основными требованиями к нейровизуализации в острейшем периоде ишемического инсульта являются быстрота проведения исследования и информативность полученных данных. Главными задачами, стоящими перед врачом при использовании этих методов, являются исключение неишемической причины симптомов у пациента, определение локализации и размеров ишемических очагов и наличия жизнеспособной мозговой ткани, определение состояния церебральных сосудов, выявление отека мозга и смещения срединных структур, а также наличия геморрагического пропитывания ишемических очагов. Эти данные должны помочь в скорейшем определении тактики лечения пациента — возможности проведения внутривенного или внутриартериального тромболизиса, механического удаления бляшки, операции по декомпрессии головного мозга [28, 29].
Компьютерная томография (КТ) обычно не выявляет ишемические изменения в паренхиме мозга в течение первых нескольких часов от начала инсульта, времени, наиболее важном для начала терапии, а иногда даже и в более поздние сроки заболевания. Особенно затруднительна визуализация задних отделов мозга вследствие артефактов, обусловленных костями черепа. Однако при инсультах в бассейне ЗМА, как и при инсультах в бассейне средней мозговой артерии, в ряде случаев КТ может показывать гиперинтенсивный сигнал от самой ЗМА, что является наиболее ранним признаком инсульта в ее бассейне и выявляется в 70% случаях в течение первых 90 минут от начала заболевания и в 15% случаях в сроки от 12 до 24 часов. Данный признак появляется за счет визуализации кальцифицированного эмбола или атеротромбоза in situ. На стандартной КТ плоскость срезов параллельна орбито-меатальной линии (линии, соединяющей наружный угол глаза с наружным слуховым проходом и далее идущей к первому шейному позвонку). Исходя из хода СМА ее просвет обычно визуализируется на одном срезе, что позволяет легко выявить гиперденсную СМА, особенно при наличии атрофических изменений мозга. Ход ЗМА более сложен. Обычно проксимальный ее сегмент восходит латерально вокруг ножек мозга и, достигая обводной цистерны, идет горизонтально внутрь к височной доле, в непосредственной близости от намета мозжечка. Циркулярная часть (Р1- и Р2-сегменты) заканчивается в квадригеминальной цистерне, где начинается кортикальная часть ЗМА. Только Р2-сегмент идет параллельно срезу внутри обводной цистерны и, соответственно, гиперденсность, при ее наличии, наиболее вероятно может быть обнаружена в этой области. Впоследствии КТ-признаки ишемических изменений проявляются в виде участков гипоинтенсивности в паренхиме головного мозга [2, 3, 30].
Магнитно-резонансная томография (МРТ) позволяет более точно определить наличие и характер ишемических изменений в головном мозге при инсульте. Получение диффузионно-взвешенных изображений (DWI) позволяет выявлять ранние ишемические изменения, часто в течение часа от начала симптомов, и определять локализацию и распространенность очагов более точно, чем КТ [2]. Совместное использование режимов DWI, ADC и FLAIR позволяет дифференцировать острые, подострые и хронические ишемические изменения в паренхиме мозга, а также отличать цитотоксический отек мозга, наблюдающийся при ишемическом инсульте, от вазогенного отека при синдроме задней обратимой лейкоэнцефалопатии и гипертонической энцефалопатии [2, 27, 31, 32].
В неинвазивной диагностике стено-окклюзивного поражения крупных экстра- и интракраниальных артерий немалую роль играет КТ ангиография (КТА). Эта методика позволяет выявить степень стеноза, морфологию бляшки, а также наличие артериальной диссекции как при поражениях сосудов вертебробазилярного, так и каротидного бассейнов. Кроме того, оцениваются анатомические особенности коллатералей и вариантов циркуляции ЗМА [2, 33, 34]. Дополнительную информацию о сосудистой анатомии можно получить с помощью МР ангиографии с контрастированием, которая в сочетании с КТА позволяет оперировать данными, которые раньше можно было получить только с помощью классической ангиографии. Кроме того, эти методы имеют значение в оценке эффективности тромболитической терапии в случае артериальной реканализации [2].
В настоящее время тромболитическая терапия ишемического инсульта может применяться при поражении артерий как каротидного, так и вертебробазилярного бассейнов. Тем не менее все существующие на сегодняшний день руководства по проведению тромболизиса ориентированы в первую очередь на сосудистую катастрофу в каротидном бассейне, в первую очередь средней мозговой артерии; это связано прежде всего с наличием у таких пациентов явного неврологического дефицита в виде грубых парезов и нарушений чувствительности. Типичный функциональный дефицит у больного с инфарктом в бассейне ЗМА в острейшем периоде не всегда расценивается врачом как инвалидизирующий. Оценка неврологического дефицита по шкале инсульта национального института здоровья (NIHSS), являющаяся одним из критериев отбора пациентов для тромболитической терапии, обычно не в состоянии в полной мере отразить тяжесть состояния больного с инфарктом в вертебробазилярном бассейне [7]. По отношению к изолированному дефекту зрительных полей при остром инфаркте в бассейне ЗМА вообще не существует каких-либо рекомендаций [2]. Поэтому тромболитическая терапия у больных с инфарктами в бассейне ЗМА используется недостаточно широко. Тем не менее, учитывая, что гемипарез в ряде случаев является значительной клинической составляющей инфарктов в бассейне ЗМА, таким пациентам при отсутствии противопоказаний обоснованно проводится системный и/или внутриартериальный тромболизис [35].
При сравнении профилей эффективности и безопасности внутривенного тромболизиса, проводимого в течение первых трех часов от появления симптомов, у пациентов с инфарктами в каротидном бассейне и инфарктами в бассейне ЗМА значимой разницы в безопасности и исходе лечения обнаружено не было [7]. При этом, по данным ряда авторов, при проведении внутривенной тромболитической терапии при ишемических поражениях в вертебробазилярном бассейне, и в частности ЗМА, возможно расширение терапевтического окна до 6,5-7 часов и даже больше по сравнению с 4,5 часами при инфарктах в каротидном бассейне [36, 37].
Проведение внутриартериального тромболизиса при окклюзии средней мозговой артерии рекомендуется в течение не позднее 6 часов от начала симптомов, при окклюзии основной артерии — не позднее 12 часов [28]. При этом на сегодняшний день не существует четких рекомендаций по временным пределам при проведении внутриартериального тромболизиса у пациентов с поражением ЗМА [15]. N. Meier и соавт. (2011) описали 9 случаев внутриартериального тромболизиса у пациентов с окклюзией ЗМА в течение первых 6 часов от начала заболевания. Через 3 месяца после лечения функциональная независимость (по модифицированной шкале Ренкина 0-2 балла) была выявлена у 67% пациентов, что соотносится с аналогичными данными по каротидному бассейну [15].
Установленный на ранних сроках диагноз ишемического инсульта в бассейне ЗМА позволяет врачу своевременно определить тактику лечения пациента и рассмотреть при отсутствии противопоказаний возможность проведения тромболитической терапии, что, несомненно, делает прогноз для больного более благоприятным.
ЛИТЕРАТУРА
1. Brandt T., Steinke W., Thie A., Pessin M.S., Caplan L.R. Posterior cerebral artery territory infarcts: clinical features, infarct topography, causes and outcome. Multicenter results and a review of the literature // Cerebrovasc. Dis. — 2000. — Vol. 10. — P. 170–182.
2. Finelli P. Neuroimaging in acute Posterior Cerebral Artery Infarction // The Neurologist. — 2008. — Vol. 14. — P. 170-180.
3. Krings T., Noelchen D., Mull M. et al. The hyperdense posterior cerebral artery sign // Stroke. — 2006. — Vol. 37. — P. 399-403.
4. Hill M.D. Posterior cerebral artery stroke // e-medicine, 2005.
5. Хасанов И.А. Особенности инфарктов в бассейне задних мозговых артерий // Неврологический вестник. — 2012. — Т. XLIV, вып. 3. — С. 69-74.
6. Caplan L. Posterior Circulation Ischemia: Then, Now, and Tomorrow: The Thomas Willis Lecture-2000 // Stroke. — 2000. — Vol. 31. — P. 2011-2023.
7. Breuer L., Huttner H.B., Jentsch K. et al. Intravenous Thrombolysis in Posterior Cerebral Artery Infarctions // Cerebrovasc Dis. — 2011. — Vol. 31. — P. 448-454.
8. Caplan L., Bogousslavsky J. Posterior cerebral artery syndromes // Cerebrovascular Disease: Pathology, Diagnosis and Management. — 1998. — P. 1028.
9. Caplan L., Estol C., Massaro A. Dissection of the posterior cerebral arteries // Arch Neurol. — 2005. — Vol. 62. — P. 1138-1143.
10. Бразис П. Топическая диагностика в клинической неврологии / П. Бразис, Д. Мэсдью, Х. Биллер — М.: МЕДпресс-информ, 2009. — 736 с.
11. Caplan L. Posterior Circulation disease: Clinical Findings, Diagnosis and Management / Boston, MA: Butterworth-Heinemann, 1996. — 533 p.
12. Бер М. Топический диагноз в неврологии по Петеру Дуусу / М. Бер, М. Фрот-шер. — М.: Практическая медицина, 2009. — 468 с.
13. Tatu L., Moulin T., Bogousslavsky J. et al. Arterial territories of the human brain // Neurology. — 1998. — Vol. 50 — P. 1699-1708.
14. de Monye C., Dippel D.W., Siepman T.A. et al. Is a fetal origin of the posterior cerebral artery a risk factor for TIA or ischemic stroke? A study with 16-multidetector-row CT angiography // J. Neurol. — 2008. — Vol. 255 — P. 239-245.
15. Meier N., Fischer U., Schroth G. Outcome after thrombolysis for acute isolated posterior cerebral artery occlusion // Cerebrovasc. Dis. — 2011. — Vol. 328. — P. 79-88.
16. Phan T., Fong A., Donnan G. et al. Digital map of posterior cerebral artery infarcts associated with posterior cerebral artery trunk and branch occlusion // Stroke. — 2007. — Vol. 38. — P.1805-1811.
17. Chaves C.J. Posterior cerebral artery. Stroke syndromes. 2nd edition / Chaves C.J., Caplan L.R. Cambridge, New York: Cambridge University Press. — 2001. — 747 p.
18. Cals N., Devuyst G., Afsar N. et al. Pure superficial posterior cerebral artery territory infarction in the Lausanne Stroke Registry // J. Neurol. — 2002. — Vol. 249. — P. 855-861.
19. Kumral E., Bayulkem G., Atac C., Alper Y. Spectrum of superficial posterior cerebral artery territory infarcts // Eur. J. Neurol. — 2004. — Vol. 11. — P. 237-246.
20. Ng Y.S., Stein J., Salles S.S. et al. Clinical characteristics and rehabilitation outcomes of patients with posterior cerebral artery stroke // Arch. Phys. Med. Rahabil. — 2005. — Vol. 86. — P. 2138-43.
21. Brandt T., Thie A., Caplan L. et al. Infarkte in Versorgungsgebiet der A. cerebri Posterior // Nervenarzt. — 1995. — Vol. 66. — P. 267-274.
22. Savitz S.I., Caplan L.R. Vertebrobasilar disease // N. Engl. J. Med. — 2005. — Vol. 352. — P. 2618-26.
23. Finelli P. Magnetic Resonance Correlate of Hemiparesis in Posterior Cerebral Artery Infarction // Journal of Stroke and Cerebrovascular Disease. — 2008. — Vol. 17. — P. 378-381.
24. Maulaz A.B., Bezerra D.C., Bogousslavsky J. Posterior cerebral artery infarction from middle cerebral artery infarction // Arch. Neurol. — 2005. — Vol. 62. — P. 938-941.
25. Neau J.-P., Bogousslavsky J. The syndrome of posterior choroidal artery territory infarction // Ann. Neurol. — 1996. — Vol. 39. — P. 779-788.
26. Lee E., Kang D.W., Kwon S.U., Kim J.S. Posterior cerebral artery infarction: diffusion-weighted MRI analysis of 205 patients // Cerebrovasc. Dis. — 2009. — Vol. 28. — P. 298-305.
27. Богданов Э.И., Хасанов И.А., Мамедов Х.И. и др. Cиндром задней обратимой лейкоэнцефалопатии у больных с преэклампсией и эклампсией // Неврологиче-ский журнал. — 2011. — № 5. — С. 35-40.
28. Adams H., Del Zoppo G., Alberts M. et al. Guidelines for the early management of adults with ischemic stroke // Stroke. — 2007. — Vol. 38. — P. 1655-1711.
29. Wahlgren N., Ahmed N., Davalos A. et al. Thrombolysis with alteplase for acute ischemic stroke & the Safe implementation of thrombolysis in stroke — monitoring study (SITS-MOST): an observational study // Lancet. — 2007. — Vol. 369. — P. 275-282.
30. Berge E., Nakstad P.H., Sandset P.M. Large middle cerebral artery infarctions and the hyperdense middle cerebral artery sign in patients with atrial fibrillation // Acta Radiol. — 2001. — Vol. 42. — P. 261-268.
31. Covarrubias D.J., Leutmer P.H., Caumpeau N.G. Posterior reversible leukoencephalopathy syndrome: prognostic utility of quantitative diffusion-weighted MR image // AJNR Am J. Neuroradiol. — 2002. — Vol. 23, N 6. — P. 1038-1048.
32. Garg R. Posterior leukoencephalopathy syndrome // Postgrad. Med. J. — 2001. — Vol. 77, N 903. — P. 24-28.
33. Choi C., Lee D., Lee J. et al. Detection of intracranial atherosclerotic steno-occlusive disease with 3D time-of-flight magnetic resonance angiography with sensitivity encoding at 3T // AJNR Am J. Neuroradiol. — 2007. — Vol. 28. — P. 439-446.
34. Lev M., Farkas J., Rodrigues V. et al. CT angiography in the rapid triage of patients with hyperacute stroke to intraarterial thrombolysis: accuracy in the detection of large vessel thrombus // J Comput Assist Tomogr. — 2001. — Vol. 25. — P. 520-528.
35. Ntaios G., Spengos K., Vemmou A. M. et al. Long-term outcome in posterior cerebral artery stroke // European Journal of Neurology. — 2011. — P. 156-162.
36. Forster A., Gass A., Kern R. et al. MR Imaging-Guided Intravenous Thrombolysis in Posterior Cerebral Artery Stroke // AJNR Am J. Neuroradiol. — 2011. — Vol. 32. — P. 419-421.
37. Montavont A., Nighoghossian N., Derex. L et al. Intravenous r-TPA in vertebrobasilar acute infarcts // Neurology. — 2004. — Vol. 62. — P. 1854-1856.
Причины и факторы инсульта мозжечка
Ишемическая разновидность мозжечкового инсульта, как правило, считается исходом атеросклеротической болезни. Тромб попадает по позвоночной или основной артерии с током крови. Также эмболия может произойти при свежем инфаркте миокарда или фибрилляции предсердий. Весьма опасны хирургические вмешательства на шее, так как во время их проведения возможна травматизация позвоночных артерий с дальнейшим нарушением кровотока.
Основные причины геморрагического инсульта мозжечка:
- повышенное артериальное давление или резкие его скачки;
- церебральная амилоидная ангиопатия — отложение амилоида в мелких кровеносных сосудах, по которым кровь попадает в центральную нервную систему;
- прием антитромботических препаратов («разжижающих кровь»);
- новообразования;
- воспалительные заболевания стенок сосудов.
Неправильный образ жизни
Кроме непосредственных причин, в развитии инсульта мозжечка весомую роль играют факторы риска. Один из ключевых — неправильный образ жизни. Он включает в себя:
- низкую подвижность в течение дня;
- питание на основе продуктов с высоким содержанием жиров, натрия;
- табакокурение, злоупотребление алкогольными напитками, прием наркотических препаратов;
- постоянное нервное напряжение, хронический стресс.
Эти факторы способствуют нарушению нормального кровообращения в органах, в том числе и в нервной системе.
Заболевания и лекарственные препараты
Спровоцировать инсульт мозжечка головного мозга способны заболевания внутренних органов. Доказана взаимосвязь нарушения церебрального кровообращения со следующими соматическими болезнями:
- артериальная гипертензия;
- метаболический синдром, сопровождающийся высоким уровнем холестерина и липопротеидов низкой плотности в крови;
- сахарный диабет и другая эндокринная патология;
- ишемическая болезнь сердца;
- заболевания, при которых повышается свертываемость крови.
Бесконтрольное употребление медикаментозных препаратов, влияющих на работу сердца, изменяющих гормональный фон, разжижающих кровь, также может вызвать острое нарушение церебрального кровообращения (в том числе и в мозжечке).
Другие причины
К другим причинам возникновения сосудистой катастрофы относятся генетическая предрасположенность и возрастной фактор. В настоящее время изучается ряд генов, которые потенциально ассоциируются с повышенным риском возникновения нарушений церебрального кровообращения.
Причины кровоизлияния
Спусковым механизмом, триггером кровоизлияния в мозжечок чаще всего является гипертония. В основном же причины такого типа кровоизлияния не отличаются от поводов для возникновения других типов инсультов, поражающих головной мозг. Чаще всего это следующие явления и состояния:
- Резкий подъем артериального давления;
- Сильное волнение, стресс;
- Физическое переутомление;
- Напряженная умственная деятельность;
- Прием неподходящих лекарственных препаратов;
- Употребление алкоголя;
- Чрезмерное перегревание (на солнце, в бане, очень горячая ванна и так далее);
- Курение может стать причиной поражения сосудов, что, в свою очередь, запустит целую цепочку заболеваний, в конце концов, приводящих больного к инсульту, параличу или летальному исходу.
Первая помощь при инсульте
Оказывая первую помощь, необходимо понимать, что такое инсульт мозжечка, иначе существует огромный риск навредить больному. Главная цель — предупредить дальнейшую гибель нейронов, а неумелые и неправильные действия могут привести к крайне негативным последствиям. Рекомендуют:
- Уложить больного на кровать, если нарушение кровообращения произошло дома, или на землю, слегка приподнять туловище.
- Повернуть голову набок, что позволит избежать попадания рвотных масс в дыхательные пути.
- Незамедлительно обратиться за медицинской помощью.
- Постараться успокоить пострадавшего, успокоиться самим.
- Обеспечить достаточный приток свежего воздуха, избавить от узкой одежды.
Лечение инсульта
Объем, тактика и срок лечения зависят от вида сосудистого нарушения. К общим мероприятиям можно отнести:
- Обеспечение поступления кислорода к тканям мозга.
- Коррекция показателей артериального давления.
- Профилактика судорожного синдрома.
- Поддержание водно-электролитного и энергетического баланса, нормальной температуры тела.
Медикаментозное лечение инсульта мозжечка
Использование лекарственных препаратов возможно только после установления причины сосудистой катастрофы. Для терапии ишемического инсульта мозжечка головного мозга применяют:
- Тромболитики. Такие препараты способны растворять тромбы в кровеносных сосудах, избавляя участки нервной ткани от ишемии.
- Нейропротекторы. Используются для уменьшения чувствительности нейронов к кислородному голоданию. Применение этих лекарственных препаратов позволяет избежать дальнейшей гибели нервных клеток и постепенно восстановить функции поврежденных участков.
- Диуретики — медикаменты, которые помогают бороться с отеком головного мозга.
В лечении острого нарушения кровообращения в мозжечке по геморрагическому типу также используют нейропротекторы и диуретики, однако ключевые препараты — кровоостанавливающие средства.
Объем медикаментозной терапии подбирается индивидуально для каждого пациента. Он расширяется при наличии параличей, сопутствующей соматической или эндокринной патологии.
Оперативное вмешательство
Параллельно с медикаментозным лечением решается вопрос хирургического вмешательства. Его функции:
- Удаление тромба или гематомы.
- Перераспределение кровотока для снабжения пострадавших участков нервной ткани.
- Остановка кровотечения при неэффективной медикаментозной помощи.
Традиционное оперативное вмешательство проводится открытым способом или с помощью эндоскопа.
Реабилитация
Во время восстановительного периода применяется комплекс мероприятий: физиотерапия, медикаментозное лечение, массаж, занятия с психологами и логопедами.
В зависимости от клинической картины и каждого отдельного случая, восстановительные курсы подбираются индивидуально.
Их основными целями являются:
- восстановление двигательных функций и моторики;
- возобновление бытовых навыков;
- восстановление речи;
- восстановление памяти.
Реабилитационный период зависит от степени тяжести заболевания. В среднем требуется от полугода и больше, чтобы пациент почувствовал значительные улучшения.
После инсульта, для минимизации возможности рецидива, необходимо придерживаться следующий рекомендаций:
- следить за уровнем холестерина в крови;
- периодически проходить МРТ;
- контролировать уровень артериального давления;
- избегать стрессовых ситуаций;
- не поддаваться вредным привычкам: курению, употреблению алкоголя;
- по-возможности заниматься спортом, вести здоровый образ жизни.
Восстановление и реабилитация после инсульта мозжечка
Раннее начало восстановительного лечения позволяет более эффективно активировать взаимосвязь между нейронами, возвращая нервным структурам утраченные функции. Реабилитационные мероприятия должны быть разноплановыми и включать в себя как медикаменты, так и физиопроцедуры, специальные физические упражнения, эрготерапию. Основные цели восстановительного лечения:
- возвращение контроля над двигательной активностью;
- нормализация речи;
- восстановление утраченных навыков самообслуживания;
- улучшение тонуса мышц после паралича;
- предотвращение осложнений (контрактур).
Мозжечок и его функции
Под затылочными полушариями в нижней части черепа, близко к позвоночному столбу находится мозжечок. Он состоит из двух полушарий и червячка. Вес у взрослого человека достигает 160 г. На момент рождения ребенка он очень мал, но отличается заметным развитием в течение первого года жизни. К 6 лет достигает минимального размера для взрослого человека.
Сверху мозжечок покрыт серым веществом, внутри состоит из белого – в нем расположены четыре ядра.
Питание осуществляется тремя мозжечковыми артериями, берущими начало от позвоночной и основной магистралей.
Мозжечок получает информацию о текущем положении тела или его отделов. Одновременно к нему приходит корректировка от коры полушарий в отношении того, какое следующее движение нужно совершить. Это позволяет ему корректировать произвольные и непроизвольные действия.
Основными функциями этого отдела мозга является координация движений, регуляция тонуса мышц, равновесия, мышечная память.
- Инсульт левой стороны: последствия и особенности восстановления. Сколько живут с таким диагнозом?
Инсульт в мозжечке: возможные последствия, прогноз
Несмотря на низкую распространенность, мозжечковый инсульт имеет неблагоприятный прогноз для пациента и сопровождается высокой летальностью, достигающей тридцати и более процентов. Частые последствия инсульта мозжечка:
- Инвалидизация. По статистике, только 20% пациентов, перенесших острое нарушение кровообращения в мозжечке, к полугоду от начала болезни способные обслуживать себя самостоятельно. Остальные же пострадавшие нуждаются в помощи окружающих.
- Парезы и параличи. Восстановление двигательной активности в поврежденных конечностях протекает медленно и не всегда в полном объеме.
- Нарушение речи. У части больных остается скандированная речь.
Часто такие тяжелые последствия инсульта мозжечка вызывают отчаяние у больного. Однако не стоит опускать руки: ежедневное проведение реабилитационных мероприятий способно частично или даже полностью восстановить утраченные навыки.
Прогноз
На данный момент острые проявления мозжечкового инсульта лечить практически не удается. К сожалению, практически все больные с яркими проявлениями кровоизлияния в мозжечок не выживают, даже если им будет своевременно оказана соответствующая медицинская помощь.
В основном, кровоизлияние в мозжечок, последствия которого могут быть весьма тяжелыми даже при выживании больного, характеризуется высокой летальностью и опасными осложнениями. Усугубляет ситуацию и возраст пациента — в основном старые люди имеют большой «набор» хронических заболеваний и сильно ослабленный организм, который с трудом сопротивляется такому серьезному поражению, как инсульт.
Для более быстрого и качественного выздоровления больному, пережившему кровоизлияние, важно создать спокойную, дружескую, эмоционально уравновешенную атмосферу. Его родным и близким придется проявить максимум такта, так как пациент может быть раздражительны, капризным и даже плаксивым. Только мягкое отношение и любовь в сочетании с грамотным профессиональным лечением смогут вернуть человека к нормальной, полноценной жизни.
Профилактика инсульта
Для предупреждения острых нарушений церебрального кровообращения специалистами ВОЗ разработаны простые рекомендации:
- Контроль и коррекция артериального давления.
- Профилактика нарушений сердечного ритма.
- Минимизация факторов риска.
- Ежегодное обследование состояния магистральных сосудов.
- Мониторинг показателей крови.
Инсульт мозжечка головного мозга — крайне тяжелое заболевание, но ряд современных методов диагностики и лечения повышают выживаемость пациентов и улучшают качество их жизни в дальнейшем.
Первая помощь
Если есть подозрение на развитие инсульта, то самое главное – сразу же вызывать скорую помощь. Затем нужно проверить, может ли человек дышать, помочь ему, освободив полость рта в положении лежа на боку. Если есть возможность, то зафиксировать показания артериального давления и пульса.
Если пациент находится на полу, то уложить его на спину, подложив под голову полотенце, сложенное в несколько слоев. Очень важно установить, когда случился приступ, это поможет правильному назначению терапии. Нельзя самостоятельно понижать давление крови, поить, а особенно кормить больного.
Первая помощь при инсульте