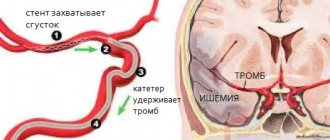
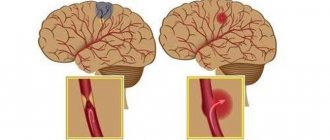
Геморрагический инсульт (ГИ) – клинический синдром, при котором происходит резкое развитие очаговой и/или общемозговой неврологической симптоматики по причине спонтанного кровоизлияния в вещество головного мозга или в подоболочечные участки. Патологический процесс запускают факторы нетравматического генеза. Этот вид кровоизлияния имеет самую высокую инвалидизирующую способность и сопряжен наивысшими рисками раннего смертельного исхода.
Факты статистики из достоверных источников
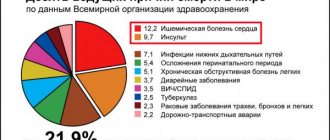
В общей структуре всех типов инсультов геморрагический занимает 10%-15%. Частота его распространения среди мирового населения составляет порядка 20 случаев на 100 тыс. человек. Специалисты, базируясь на ежегодную динамику, оповещают, что примерно через 50 лет все эти показатели увеличатся в два раза. Конкретно в Российской Федерации ежегодно диагностируют около 43000-44000 случаев ГИ. Что примечательно, приблизительно в 1,5 раза он чаще возникает у мужчин, однако летальность от его последствий преобладает у женщин.
Согласно клиническим наблюдениям, при данном диагнозе смерть наступает у 75% людей, которые находятся на ИВЛ, и у 25% людей, не нуждающихся в ней. Проведенные консолидированные исследования показали, что в среднем 30%-50% больных погибает в течение 1-го месяца с момента приступа геморрагии, причем 1/2 из них умирает уже в течение первых 2-х суток. Инвалидизация (из-за паралича лица и конечностей, афазии, слепоты, пр.) среди выживших пациентов достигает 75%, из них 10% остаются прикованными к постели. И лишь 25% больных спустя 6 месяцев независимы в повседневной жизни.
Патология представляет огромную социальную проблему, поскольку эпидемиологический пик приходится на трудоспособные годы – 40-60 лет. Геморрагические инсульты существенно «помолодели», сегодня они достаточно распространены даже среди молодежной группы людей (20-30 лет). Однозначно в категорию риска входят люди, страдающие артериальной гипертонией, так как в большинстве случаев подобного рода кровоизлияния случаются именно на почве хронически повышенного АД.
Первоочередной фактор, который влияет на прогноз исхода, – оперативность оказания адекватной медицинской помощи больному.
Инфаркт миокарда и геморрагический альвеолит при системной красной волчанке
есмотря на хорошо известные симптомы системной красной волчанки (СКВ), каждый случай этого заболевания уникален. Течение болезни характеризуется периодами обострений и ремиссий, возникающих на фоне приема лекарственных препаратов. Прекращение лечения, как правило, сопровождается обострением СКВ через разные промежутки времени. Заболевание может начинаться с поражения одного или нескольких органов или протекать молниеносно, заканчиваясь летально за короткий промежуток времени.
Главными причинами смерти в течение первого года после начала заболевания являются активность СКВ (поражение почек, центральной нервной системы – ЦНС) или присоединение инфекции. В дальнейшем смертельные исходы могут быть обусловлены кардиоваскулярными катастрофами, хронической почечной недостаточностью и злокачественными новообразованиями [1]. Применение глюкокортикостероидов позволяет снизить частоту смертельных исходов, развивающихся вследствие активности СКВ.
Мы приводим описание пациентки с СКВ, у которой активность заболевания явилась причиной развития синдрома диссеминированного внутрисосудистого свертывания (тромбогеморрагической стадии) и смертельного исхода в первый год после начала СКВ.
Больная К. 18 лет, поступила в стационар Института ревматологии РАМН в октябре 2003 г. с жалобами на геморрагические высыпания на коже, боли в правом локтевом, лучезапястном и пястно-фаланговых суставах правой кисти, припухлость этих суставов, выпадение волос, слабость, одышку при физической нагрузке.
Дебют заболевания в конце декабря 2002 г. характеризовался появлением на лице эритемы, развитием артрита мелких суставов кистей, субфебрильной температуры, резким снижением массы тела (за 2 мес. похудела на 6 кг). В январе 2003 г. была госпитализирована в ревматологическое отделение одной из больниц г. Москвы, где были выявлены изменения мочевого осадка (протеинурия, эритроцитурия и лейкоцитурия), анемия, повышение антител к ДНК и антинуклеарный фактор (АНФ, титры не известны), что позволило диагностировать СКВ. С момента установления диагноза постоянно получала преднизолон (ПЗ – 35 мг/сут.), а после консультации в Институте ревматологии (апрель 2003 г.) также плаквенил (400 мг/сут.). Несмотря на проводимую терапию, сохранялись изменения в анализах мочи (следовая протеинурия и микрогематурия) и иммунологические нарушения, в связи с чем был назначен циклофосфан – ЦФ (суммарно 1,2 г). Прекращение инъекций ЦФ и снижение дозы ПЗ до 20 мг/сут. спровоцировало обострение СКВ: в сентябре 2003 г. на коже голеней, а затем по всему телу появилась геморрагическая сыпь, во рту – болезненные афты, вновь рецидивировали артриты и артралгии, лихорадка, стала возрастать слабость. Эпизод резких болей в животе, тошнота, дегтеобразный стул возникли 30 сентября, отмечено снижение гемоглобина до 81 г/л. По месту жительства исключено развитие пищевой токсикоинфекции, проведена регидратационная терапия, после чего пациентка была направлена в Институт ревматологии. Краткая схема анамнеза представлена на рис. 1.
Провокаторы геморрагического инсульта
Пусковым механизмом появления ГИ могут послужить достаточно разнообразные факторы, оказывающие негативное воздействие на внутричерепную гемодинамику и состояние церебральных сосудов:
- стойкая артериальная гипертония (в 50% случаев);
- церебральная амилоидная ангиопатия (12%);
- оральный прием лекарств из спектра антикоагулянтов (10%);
- внутричерепные новообразования (8%);
- другие причины – артериовенозные и кавернозные мальформации, тромбозы синусов головного мозга, аневризмы, васкулиты интракраниальных сосудов и пр. (20%).
Многие из пациентов с геморрагическим ударом в анамнезе имеют сахарный диабет. Доказанный факт, что диабетики, как и гипертоники, входят в группу риска. При сахарном диабете с долгим сроком течения сосуды, включая церебральные, разрушаются из-за модификации химии крови с преобладанием глюкозы. Если на фоне повышенного сахара в крови есть склонность к постоянным повышениям АД, вероятность геморрагического инсульта возрастает в 2,5 раза.
Патогенетически геморрагический эффект может развиться вследствие разрыва сосуда (преобладающий механизм) или просачивания элементов крови в окружающие ткани мозга сквозь стенки капилляров из-за нарушенного их тонуса и проницаемости. Во втором варианте разрыва нет и как такового обильного кровоизлияния тоже. Просто мелкий сосуд пропускает кровь точечно. Но и мелкоточечные геморрагии, сливаясь, способны превратиться в весьма обширные очаги, с не меньшими роковыми последствиями, чем после разрыва артерии или вены.
Клинические проявления ГИ
Незадолго до приступа могут предшествовать предынсультные клинические симптомы-предвестники (не всегда), по которым можно заподозрить надвигающуюся опасность:
- покалывания, онемение одной лицевой половины;
- онемение пальцев рук или ног;
- внезапная слабость, головокружение, шум в голове;
- резкая болезненность в глазах, мушки, двоение, видение в красном цвете;
- внезапное пошатывание при ходьбе;
- беспричинная тахикардия;
- приступы гипергидроза;
- повышение артериального давления;
- необоснованное появление тошноты;
- заторможенность в общении и восприятии чужой речи;
- прилив крови к лицу, гипертермия.
Для мозгового удара с кровоизлиянием все же характерен мгновенный острый дебют без предвестников, который случается в процессе или почти сразу же после активной деятельности, стрессовой ситуации, волнения. О геморрагическом инсульте свидетельствуют классические симптомы, которые развиваются внезапно, они ярко выражены и бурно прогрессируют:
- резкая и сильная головная боль;
- неукротимая рвота;
- длительное угнетение сознания, кома;
- кровяное давление выше 220 мм.рт.ст.
Распространенными признаками состоявшегося шока также являются шумное дыхание, эпилептические припадки, отсутствие реакции зрачков на свет, спастический миоз. В зависимости от расположения очага может присутствовать поворот головы и обращение глазных яблок в направлении пораженного полушария или контрлатерально. Обнаружив признаки ГИ у пострадавшего, рядом находящийся человек обязан немедленно вызвать скорую помощь!
Остро развившаяся геморрагия приводит к тому, что кровь свободно поступает в определенные структуры мозга, пропитывая их и образуя полость с гематомой. Излитие крови длится несколько минут или часов, пока не образуется тромб. За небольшой отрезок времени гематома быстро увеличивается, оказывая на затронутые зоны механическое воздействие. Она растягивает, давит и смещает нервную ткань, вызывает ее отек и гибель, что ведет к интенсивному нарастанию неврологического дефицита (угнетению дыхания, выпадению чувствительности одной половины тела, речевым нарушениям, утрате зрения, парезу глотательных мышц и пр.).
По размерам кровяное скопление может быть небольшим (до 30 мл), средним (от 30 до 60 мл) и большим (более 60 мл). Объемы излившейся жидкости могут достигать и критических масштабов, вплоть до 100 мл. Клинические наблюдения показывают, что при внутричерепных кровоизлияниях, превышающих 60 мл, патология оканчивается смертью у 85% больных в течение 30 суток.
Типичная локализация кровоизлияний
Наиболее часто, а это порядка в 55% случаев, геморрагии происходят в путаментальной зоне. Путаментальное кровотечение образуется вследствие разрыва дегенерированных лентикулостриарных артерий, из-за чего кровь попадает в скорлупу мозга. Виновником патогенеза с такой локализацией обычно становится длительно существующая гипертония. В ряде случаев кровотечения путамента прорываются в желудочковую систему, что чревато тампонадой ЖС и острым окклюзионно-гидроцефальным кризом.
Следующей по распространенности локализацией является субкортикальная область (подкорковая). Субкортикальные ГИ наблюдаются в 17%-18% случаев. Как правило, ведущими источниками такого кровоизлияния являются разорвавшиеся АВМ и аневризмы на фоне повышенного давления. Подкорковые зоны, вовлеченные в геморрагический процесс, – лобная, теменная, затылочная или височная доля.
Третье по встречаемости место, где в 14%-15% случаев определяют геморрагию мозга, – это зрительный бугор, или таламус. Таламические геморрагии наступают по причине выхода крови из кровеносного сосуда вертебробазиллярного бассейна. Патогенез может быть связан с любым этиологическим фактором, однако, как всегда, достоверно чаще отмечена причастность гипертензивного синдрома.
На четвертом месте (7%) по частоте развития встречаются мостовые ГИ. Они концентрируются в задней части ствола мозга, то есть в варолиевом мосту. Через мост осуществляется связь коры с мозжечком, спинным мозгом и другими главнейшими элементами ЦНС. Этот отдел включает центры контроля над дыханием и сердцебиением. Поэтому мост – самая опасная локализация кровоизлияния, практически несопоставимая с жизнью.
Причины
Поскольку ишемический инсульт не рассматривается как отдельное заболевание, определение единого этиологического фактора для него невозможно. Однако существуют факторы риска, ассоциированные с повышенной частотой развития ишемического инсульта, которые можно разделить на две группы:
1. Модифицируемые.
- инфаркт миокарда
- артериальная гипертензия
- мерцательная аритмия
- сахарный диабет
- дислипопротеинемия
- бессимптомное поражение сонных артерий.
2. Немодифицируемые.
- наследственная предрасположенность
- возраст
Кроме этого, существуют и факторы риска, связанные с образом жизни: низкий уровень физической активности, острый стресс или длительное психоэмоциональное напряжение, избыточная масса тела, табакокурение.
Принципы диагностики заболевания
Золотым стандартом в установлении диагноза является метод компьютерной томографии (КТ). В раннем периоде после приступа (1-3 сутки) этот способ нейровизуализации наиболее информативен, чем МРТ. Свежий геморрагический материал, включающий 98% гемоглобина, на КТ отображается высокоплотным, хорошо очерченным, ярко-светлым включением на фоне более темной мозговой ткани. На основании компьютерной томограммы определяются зона эпицентра, объемы и форма образования, уровень поражения внутренней капсулы, степень дислокации мозговых структур, состояние ликворной системы.
С началом подострой фазы (через 3 суток) красные клетки гематомы по периферии разрушаются, в центре железосодержащий белок окисляется, очаг становится ниже по плотности. Поэтому наряду с КТ в сроки от 3 дней и позже обязательным является проведение МРТ. В подострой и хронической форме МР-сигнал, в отличие от КТ, лучше визуализирует гематому с производными окисления гемоглобина (метгемоглобином), переходящую в изоденсивную стадию. Ангиографические методы обследования применяются у пациентов с неопределенной причиной развития геморрагического инсульта. Ангиографию в первую очередь проводят лицам молодого возраста с нормальными показателями АД.
Для адекватного ведения пациентов после приступа внутримозгового кровоизлияния обязательно проводятся ЭКГ и рентген органов дыхания, берутся анализы на электролиты, ПТВ и АЧТВ.
Медицинская помощь в стационаре
Все больные на раннем этапе получают интенсивную терапевтическую помощь в нейрореанимационном стационаре. Первоначальные лечебные мероприятия направлены на:
- нормализацию микроциркуляции, гемореологических нарушений;
- купирование мозгового отека, лечение обструктивной гидроцефалии;
- коррекцию кровяного давления, температуры тела;
- функциональную регуляцию сердечно-сосудистой системы;
- поддержание водно-электролитного баланса;
- предупреждение возможных судорог;
- профилактику внечерепных последствий воспалительной и трофической природы (пневмонии, эмболии, отека легких, пиелонефрита, кахексии, ДВС-синдрома, эндокардита, пролежней, мышечной атрофии и др.);
- проведение респираторной поддержки (если больной в ней нуждается);
- устранение внутричерепной гипертензии при ГИ с дислокацией.
Профилактика
Зная ваши факторы риска инсульта, следуя рекомендациям высококвалифицированных специалистов, ежегодный комплексный чек-ап организма и здоровый образ жизни являются лучшими шагами, которые вы можете предпринять, чтобы предотвратить инсульт. Если у вас был инсульт или транзиторная ишемическая атака (ТИА), эти меры могут помочь предотвратить другой инсульт.
Помощь, которую вы получаете в клинике, играет значительную роль при купировании острого периода инфаркта мозга.
От того, насколько квалифицированную и скорую помощь окажет вам команда неврологов, кардиологов, нейрохирургов, реабилитологов и физиотерапевтов, будут завесить факторы риска возможных осложнений после приступа.
Многие протоколы профилактики инсульта совпадают с протоколами профилактики сердечно-сосудистых заболеваний. Основные рекомендации по здоровому образу жизни включают в себя:
- Постоянный контроль кровяного давления. Это одна из самых важных вещей, которые вы можете сделать, чтобы уменьшить риск инсульта. Если у пациента уже был инсульт, снижение артериального давления может помочь предотвратить последующую ТИА или инсульт.
- Физические упражнения, контроль над стрессом, поддержание здорового веса и ограничение количества натрия, алкоголя и табака. В дополнение к рекомендации изменения образа жизни, наш врач может назначить лекарства для лечения высокого кровяного давления, а также комплекс витамин и минералов, рыбий жир.
- Снижение количества холестерина и насыщенных жиров в вашем рационе. Употребление меньшего количества холестерина и жиров, особенно насыщенных жиров и транс-жиров, может уменьшить бляшки в артериях.
- Отказ от употребления табака. Курение повышает риск инсульта для курильщиков и некурящих, подверженных пассивному курению. Отказ от употребления табака снижает риск инсульта.
- Контроль диабета.
- Поддержание здорового веса. Избыточный вес способствует развитию других факторов риска инсульта, таких как высокое кровяное давление, сердечно-сосудистые заболевания и диабет.
- Диета, богатая фруктами и овощами. Диета, содержащая пять или более ежедневных порций фруктов или овощей, может снизить риск инсульта.
- Физические упражнения могут снизить кровяное давление. Это также поможет похудеть, контролировать диабет и уменьшить стресс.
Операция при гемморагическом инсульте
Вторым этапом лечебного процесса выступает нейрохирургическое вмешательство. Его целью является удаление жизнеугрожающей гематомы для повышения выживаемости и достижения максимально возможного удовлетворительного функционального исхода. Чем скорее проведут операцию, тем лучших прогнозов можно будет ожидать. Однако ранняя операция, как правило, предполагает выполнение хирургических манипуляций не раньше чем через 7-12 часов после инсульта. В ультра-раннем периоде она может привести к повторным кровотечениям.
В какой срок разумнее приступить к удалению сгустков крови, решается сугубо компетентными нейрохирургами. Отмечено, что к положительному эффекту могут приводить и операции, совершенные даже спустя 2-3 недели (включительно) после состоявшегося ГИ. Так что вопрос, когда прооперировать пациента, полностью берется под ответственность врача. Рассмотрим основополагающие методы операций, широко применяемые при геморрагических инсультах.
- Открытая декомпрессивная краниотомия показана при средних и крупных подкорковых, а также больших путаментальных и мозжечковых кровоизлияниях. К ней обращаются и при выраженном смещении и нарастающем отеке мозгового компонента, ухудшении неврологического статуса больного. Открытая операция выполняется под полной общей анестезией с применением микрохирургической оптики. Извлечение скопившегося сгустка реализуется через классический трепанационный доступ. Далее делается экономная энцефалотомия, затем патологический компонент отсасывается специальным прибором. Плотные скопления удаляются окончатым пинцетом. В конце операционное поле досконально промывается раствором хлорида натрия, выполняется тщательный гемостаз посредством коагуляции и антигеморрагических средств.
- Пункционно-аспирационная процедура рекомендуется при небольших геморрагиях таламического, путаментального, мозжечкового расположения. Способ заключается в создании маленького отверстия в черепной коробке, пункции гематомы с последующим освобождением мозга от ее жидкой массы посредством аспирации. Такая технология может быть реализована одним из двух миниинвазивных приемов: по принципу стереотаксической или нейроэндоскопической аспирации. Иногда их целесообразно сочетать с локальным фибринолизом. Фибринолиз подразумевает установку дренажа после пункции и аспирации в полость гематомы. Через дренаж в течение нескольких дней вводят фибринолитики для активации растворения (разжижжения) кровяного сгустка и выведения лизированных элементов крови.
Функции аппарата ЦНС, к сожалению, после геморрагических инсультов полностью восстановить невозможно. Но в любом случае, в интересах больного будет обращение в клинику, где работают врачи международного уровня по диагностике и хирургическому лечению внутримозговых поражений. Только так можно рассчитывать на организацию адекватного и безопасного хирургического обеспечения. Следовательно, минимизацию осложнений, более продуктивные результаты в восстановлении качества жизни.
Акцентируем, что идеальное исполнение операции в правильные сроки в 2-4 раза повышает процент выживаемости. Грамотный послеоперационный уход сокращает вероятность рецидива. Нельзя не предупредить, что повторный инсульт с кровоизлиянием у 99,99% пациентов приводит к летальному исходу.
В качестве рекомендации считаем важным сказать, что в уровне развития сферы нейрохирургии мозга на территории Европы Чехия показывает хорошие результаты. Чешские медцентры славятся безупречной репутацией и отличными показателями благополучного восстановления даже самых тяжелых пациентов. И это не все: в Чехии минимальные цены на нейрохирургическую помощь и одна из лучших послеоперационная реабилитация. Выбор медучреждения для прохождения оперативного вмешательства, безусловно, остается за пациентом и его родственниками.
МКБ-10
I63 Инфаркт мозга
- Причины
- Патогенез
- Классификация
- Симптомы ишемического инсульта Инфаркт мозга в бассейне СМА
- Инфаркт мозга в бассейне ПМА
- Инфаркт мозга в бассейне ЗМА
- Инфаркт мозга в вертебробазилярном бассейне
- Дифференциальный диагноз
- Терапия в острейшем периоде