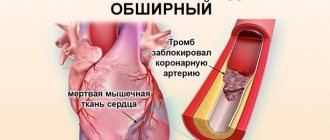
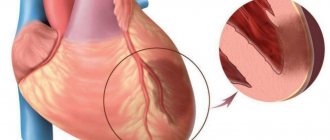
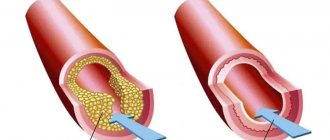
Миокард — это мышца, управляющая сокращениями сердца и регулирующая кровоснабжение всего организма. Для бесперебойной работы ей необходимо регулярное питание и кислород, снабжение которыми происходит по коронарным артериям.
Если по каким-то причинам дыхание и питание миокарда нарушаются, клетки мышцы начинают гибнуть. Некроз того или иного участка сердечной мышцы и называют инфарктом миокарда.
Инфаркт миокарда зачастую влечет за собой полную или частичную утрату трудоспособности, и это еще не самое худшее. В 10-12% случаев он угрожает самой жизни больного!
17,5 миллионов — по статистике, именно столько людей умирает ежегодно в мире от заболеваний сердца и сосудов. А к 2030 году, по прогнозам экспертов ВОЗ, этот показатель достигнет еще более страшных цифр — 23,6 млн смертей от ССЗ в год.
Причины инфаркта миокарда
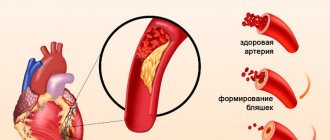
В большинстве случаев некроз тканей миокарда происходит из-за тромбоза венечной артерии, который провоцируется атеросклерозом — атеросклеротические бляшки закупоривают артерию, нарушая кровоснабжение.
Другие распространенные причины инфаркта — спазм коронарных сосудов и тромбоз коронарных сосудов.
1 УЗИ сердца при инфаркте
2 Диагностика инфаркта
3 Диагностика при угрозе инфаркта
Медикаментозная терапия
При медикаментозной терапии обширного инфаркта миокарда важно, соблюдение следующих условий:
- продолжительный постельный режим;
- полное психоэмоциональное спокойствие;
- специальное питание;
- постоянный мониторинг за функционированием абсолютно всех систем организма.
Вовремя выявленный инфаркт задней стенки сердца поддается излечению. Лечащий доктор устанавливает список необходимых препаратов, ориентированных на предотвращение симптомов разрыва миокарда и на нормализацию самочувствия больного и его кровеносных сосудов:
- антитромбоцитарная терапия – специальные вещества для разжижения сгустков крови и улучшения кровотока (Кислота ацетилсалициловая); анестезия (Нитроглицерин);
- освобождение от аритмии (Кордарон, Лидокаин);
- профилактика формирования тромбов (антикоагулянты – Полисахарид, Ловенокс, Гепарин, а также антиагреганты – Лиотон, Плавикс);
- средства рассасывающие имеющиеся в организме сгустки крови (тромболитические препараты – Фибринолизин, Алтеплаза).
Кому грозит инфаркт миокарда
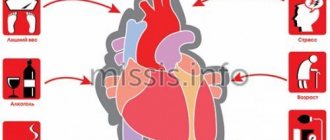
Факторами риска являются:
- гипертоническая болезнь;
- ранее перенесенный инфаркт;
- курение;
- малоподвижный образ жизни;
- наследственная предрасположенность;
- повышенный уровень «плохого» холестерина в крови;
- ожирение;
- сахарный диабет;
- пожилой возраст;
- состояние постменопаузы (у женщин);
- регулярные стрессы;
- чрезмерные нагрузки (физические и эмоциональные);
- нарушения свертываемости крови.
Хирургические методы лечения
Если обширный инфаркт миокарда не поддается медикаментозной терапии, врач принимает решение в пользу следующих операций:
- ангиопластика коронарных сосудов со стентированием, которая предполагает установку стента в артерию для поддержания естественного просвета в ней;
- коронарное шунтирование. Сложная оперативное вмешательство, при котором хирургом создается мост из неповрежденной вены, обеспечивающий естественный кровоток выше сужения.
Бывают случаи когда оперативное вмешательство, не дает положительной динамики и поражение продолжает увеличиваться в размерах. Данная ситуация предусматривает пересадку сердца.
Виды инфаркта миокарда
Поскольку некрозу могут подвергаться различные по размеру участки мышечной ткани, кардиологи различают мелкоочаговый и крупноочаговый инфаркт миокарда.
Также инфаркты делят, в зависимости от глубины поражения стенки сердца, на:
- трансмуральный — патологическими изменениями охвачена вся толщина мышечного слоя;
- интрамуральный — некроз кроется в глубине сердечной мышцы;
- субэпикардиальный — поражены участки миокарда, близкие к эпикарду;
- субэндокардиальный — некротический процесс сосредоточен в области соприкосновения миокарда с эндокардом.
В зависимости от локализации поражения выделяют 2 типа инфаркта миокарда:
- правожелудочковый;
- левожелудочковый.
По клиническим проявлениям кардиологи различают типичный и атипичный инфаркт миокарда.
1 ЭКГ при инфаркте
2 ЭКО-КГ при инфаркте
3 Исследование крови на маркеры инфаркта
Нозологические особенности повреждения миокарда: обзор симпозиума
Резюме. Главной темой симпозиума «Нозологические особенности повреждения миокарда: как распознать и что делать?» стала кардиопротективная терапия и применение безопасных и высокоэффективных метаболически активных препаратов для энергетической поддержки миокарда.
22-24 апреля 2021 г. при поддержке Европейс-кого общества кардиологов состоялся VIII Международный образовательный форум «Российские дни сердца». В рамках одного из наиболее значимых для кардиологического сообщества мероприятий ведущие специалисты России и Европы в офлайн- и онлайн-форматах обсудили наиболее актуальные проблемы кардиологии, включая трудности применения распространенных терапевтических и хирургических тактик лечения и особенности внедрения инновационных методов терапии сердечно-сосудистых заболеваний.
Симпозиум «Нозологические особенности повреждения миокарда: как распознать и что делать?», прошедший в первый день Форума при поддержке , был посвящен кардиометаболическим расстройствам и возможностям фармакологической поддержки сердечной мышцы в целях первичной и вторичной профилактики сердечно-сосудистых заболеваний (ССЗ) при различной коморбидной патологии.
| Сергей Анатольевич БОНДАРЕВ, д.м.н., профессор кафедры спортивной медицины и реабилитации ФГБОУ ВО Первый МГМУ им. И. М. Сеченова Минздрава России |
Первый спикер, Сергей Анатольевич Бондарев, д.м.н., профессор кафедры спортивной медицины и реабилитации ФГБОУ ВО Первый МГМУ им. И. М. Сеченова Минздрава России, посвятил свою лекцию теме «Излишество или необходимость? Коррекция метаболизма миокарда в кардиореабилитации после COVID-19».
Сергей Анатольевич обратил внимание коллег на то, что несмотря на то, что в последние недели количество заболевших новой коронавирусной инфекцией снижается, проблема сохраняет свою остроту. Сегодня уже известно, что крупные оболочечные несегментированные вирусы с положительной смысловой РНК, такие как SARS-CoV-2, могут привести не только к тяжелой пневмонии, но и к дистресс-синдрому и к сердечному поражению. SARS-CoV-2 проникает в клетки человека через рецептор ангиотензинпревращающего фермента (ACE2), обуславливая обилие и разнообразие проявлений со стороны сердечно-сосудистой системы.
Повреждение миокарда при COVID-19 обуславливается непосредственно блокадой и повреждением рецепторов ACE2 в эндотелии коронарных артерий, которые приводят к ускорению возникновения и развития ССЗ. Кроме того, патологический процесс усугубляется гипоксемией, вызванной вирусной инфекцией, гипоксией, провоцирующей воспалительные реакции, а также ацидозом и образованием свободных радикалов кислорода во время гипоксии и реперфузии.
На сегодняшний день более 2/3 пациентов с COVID-19 нуждаются в легочной, сердечно-сосудистой и психологической реабилитации. В связи с актуальностью задачи и особенностями патогенеза поражения миокарда при коронавирусной инфекции все большее внимание специалистов-кардиологов привлекает кардиопротективная терапия таких пациентов. В спектр возможностей кардиопротективной терапии входит восполнение энергетических затрат, стабилизация клеточных мембран, восстановление белковых структур клетки, оказание антиоксидантного эффекта.
Такими свойствами обладает целый ряд препаратов, включая мельдоний, триметазидин, витамины группы B и C. Тем не менее мельдоний и триметазидин, обладая эффектом стимуляции образования АТФ, требуют исходной затраты энергии на транспорт жирных кислот с целью блокады входа в клетку или накопления. В связи с этим особый интерес представляет применение в комплексной терапии миокардитов и/или повреждения миокарда, ассоциированного с вирусной инфекцией, натриевой соли фосфокреатинина (Неотон). Отечественные методические рекомендации 2021 г. по анестезиолого-реанимационному обеспечению пациентов с новой коронавирусной инфекцией COVID-19,а также зарубежные руководства предписывают назначение фосфокреатинина из расчета 1 г дважды в сутки в течение 7-10 дней. Фосфокреатинина натриевая соль улучшает микроциркуляцию в зоне ишемии, стабилизирует мембрану кардиомиоцитов, участвует в энергетической транспортной системе, поддерживая уровень АТФ в ишемизированном миокарде.
Метаанализ возможности применения фосфокреатинина, объединивший данные 41 исследования и почти 3,5 тыс. наблюдений, показал, что у пациентов с поражением миокарда применение препарата позволяет добиться снижения летальности более чем в 3 раза.
Профессор Бондарев поделился и собственными наблюдениями по данному вопросу. Было выполнено обследование 25 пациентов, перенесших вирусную пневмонию. Всей группе, согласно Временным рекомендациям, была назначена аэробная дыхательная гимнастика. Помимо этого, 15 пациентов получали медикаментозную поддержку в виде препарата Неотон в дозе 4 г на 100 мл физиологического раствора в течение 7 суток. Результаты терапии оценивались с помощью теста с 6-минутной ходьбой. Если до реабилитации пациенты проходили за 6 минут в среднем 200 м, то у пациентов после ЛФК этот показатель улучшился до 270 м, а в группе с дополнительным применением Неотона – до 300 м. Пациенты обеих групп отметили улучшение по показателям подвижности, уменьшение одышки, тревоги. Однако улучшение повседневной активности и уменьшение одышки в группе Неотона было выражено более значимо.
В заключение Сергей Анатольевич подчеркнул, что лечение коморбидных пациентов с SARS-CoV-2 требует максимального напряжения и усилий мультидисциплинарной бригады. Крайне важным представляется подбор безопасных и высокоэффективных препаратов для восстановления энергообмена в миокарде, а также мотивация пациента и комплаентность выполнения медикаментозных назначений.
| Юрий Александрович ВАСЮК, доктор медицинских наук, профессор, заведующий кафедрой клинической функциональной диагностики ФПДО, ученый секретарь ФГБОУ ВО МГМСУ им. А. И. Евдокимова Минздрава России |
Тему необходимости кардиометаболической поддержки продолжил Юрий Александрович Васюк, доктор медицинских наук, профессор, заведующий кафедрой клинической функциональной диагностики ФПДО, ученый секретарь ФГБОУ ВО МГМСУ им. А. И. Евдокимова Минздрава России, в своем выступлении «Прервать или продолжить? Кардиологические осложнения химиотерапии».
Юрий Александрович с сожалением констатировал, что количество онкологических пациентов неуклонно растет. Если в 2021 г. онкологическая заболеваемость во всем мире составила 17 млн человек и 10 млн нуждались в химиотерапии, то, по оценкам экспертов, к 2040 г. заболеваемость составит 26 млн человек и 15 млн будут нуждаться в химиотерапии. Так, относительное увеличение потребности в лечении рака составит 53%.
Химиотерапия, таргетная терапия и лучевая терапия обеспечили существенное улучшение выживаемости при сохраненной социальной адаптации на многие годы. Но, к сожалению, эти средства имеют ряд серьезных кардио- и вазотоксических побочных эффектов, развитие которых существенно повышает смертность больных. Даже если пациенты достигают выздоровления от основного заболевания, первой причиной смертности в отдаленном периоде становятся ССЗ: хроническая сердечная недостаточность (ХСН), ишемическая болезнь сердца (ИБС), артериальная гипертензия, миокардиты, перикардиты, клапанные поражения, тромбоэмболии, нарушения проводимости и т. д.
Исследование причин смертности онкологических больных, проводившееся по данным 7-летнего наблюдения за 1807 пациентами, показало, что причиной смерти в 51% является рак, а в 33% – ССЗ. В более отдаленном периоде доля летальности по сердечно-сосудистым причинам увеличивается до 50%. В большинстве случаев причиной смерти становится ХСН, развивающаяся на фоне кардиотоксичности, которой в той или иной степени обладают все 9 типов противоопухолевых агентов. На сегодняшний день в мире разрабатываются около 1500 новых препаратов для химиотерапии, но практически все из них также обладают кардиотоксичностью.
Риск кардиотоксичности зависит от противоопухолевого лечения (типа, дозы, режима и способа введения) и от пациента (возраст старше 65 или моложе 15, наличие факторов сердечно-сосудистого риска или сопутствующей сердечно-сосудистой или другой патологии, особенностей самой опухоли). Профессор Васюк подчеркнул, что этот риск необходимо внимательно оценивать и контролировать, регулярно мониторировать больных. Достаточно эффективными инструментами мониторинга являются ЭхоКГ, двух- и особенно трехмерная новая методика оценки деформации миокарда (в частности, глобальной продольной), а также МРТ и оценка целого ряда лабораторных показателей, включая натрийуретические пептиды и высокочувствительный тропонин.
Сегодня существует много алгоритмов ведения больных с выявленной кардиотоксичностью и даже ведения больных на фоне химиотерапии с целью первичной профилактики кардиотоксичности. Они предусматривают ограничение дозы или длительности инфузии антрациклинов, использование дексразоксана, кардиопротекторов, бета-блокаторов, ингибиторов РААС, статинов. В последние годы широко назначаются миокардиальные цитопротекторы, поскольку механизм их действия позволяет скорректировать неблагоприятное влияние антрациклинов: если противоопухолевые препараты нарушают синтез АТФ, то миокардиальные цитопротекторы нормализуют синтез и транспорт энергии.
Так, один из наиболее перспективных кардиопротекторных препаратов – фосфокреатинин поддерживает структурную целостность мембраны кардиомиоцитов, обеспечивает ресинтез АТФ в митохондриях, транспорт энергии к местам потребления и поддерживает работу ионных каналов и сократительную функцию сердца в условиях ишемии, токсического и инфекционного повреждения миокарда. Использование фосфокреатинина при токсическом воздействии на миокард за счет мембранопротекции в 2 раза уменьшает число погибших кардиомиоцитов.
Исследования показывают, что фосфокреатинин улучшает сократимость миокарда у пациентов с его повреждением на фоне лечения эпирубицином и доцетакселом, на 5% повышая фракцию выброса. Другая работа продемонстрировала, что использование фосфокреатинина на протяжении всех 6 циклов полихимиотерапии больных раком молочной железы уменьшает повреждение миокарда, что проявляется более низким уровнем сердечного тропонина Т и С-реактивного белка. Как следствие, фосфокреатинин улучшает качество жизни и переносимость терапии антрациклинами за счет уменьшения их кардиотоксического эффекта. Профессор Васюк подчеркнул, что раннее начало кардиопротекторной терапии у пациентов на фоне лечения химиопрепаратами повышает ее эффективность и уменьшает риск осложнений.
| Игорь Александрович КОЗЛОВ, д.м.н, профессор кафедры анестезиологии и реаниматологии ГБУЗ МО МОНИКИ им. М. Ф. Владимирского |
В следующем выступлении «Оперировать или отложить? Выявляем и снижаем периоперационные кардиологические риски» Игорь Александрович Козлов, д.м.н, профессор кафедры анестезиологии и реаниматологии ГБУЗ МО МОНИКИ им. М. Ф. Владимирского, привлек внимание коллег к одной из наиболее актуальных проблем – высоким сердечно-сосудистым рискам некардиальных операций. По словам спикера, вопрос, оперировать или нет, все острее встает в последние годы в связи с увеличением количества пациентов пожилого и старческого возраста, среди которых много больных с высоким кардиальным риском.
Среди 100 млн пациентов старше 45 лет, которым во всем мире ежегодно выполняют обширные некардиальные операции, 3 млн переносят периоперационный инфаркт миокарда. Целенаправленное исследование по выявлению и прогнозированию рисков кардиальных осложнений у больных пожилого и старческого возраста, проведенное в российском Институте общей реаниматологии, показало, что общая частота кардиологических осложнений составляет примерно 9%. Эта цифра сама по себе велика, но гораздо драматичнее оказался показатель летальности при развитии кардиологических осложнений у таких пациентов – 45,5%.
Совсем недавнее исследование, выполненное совместно со специалистами из Ярославля, было также посвящено оценке частоты кардиальных осложнений после некардиохирургических операций в течение 12 месяцев после выписки из стационара. Результаты показали, что кардиальная летальность среди пациентов 45-83 лет достигает почти 3%, а частота комбинированной конечной точки, в которую входит кардиальная летальность, инфаркт, инсульт, госпитализация в связи с обострением ССЗ, составила почти 28%.
Таким образом, актуальность проблемы крайне высока, и соответственно высока и необходимость реализации риск-снижающей стратегии, которая должна складываться из прогнозирования риска осложнений, оптимизации периоперационного мониторинга и свое-временной диагностики осложнений, а также фармакологической кардиопротекции в периоперационный период.
Тем не менее реализация такой стратегии в России встречается с серьезными трудностями. Профессор Козлов отметил, что уверенно прогнозировать осложнения мы сегодня, к сожалению, не можем, так как современные индексы, рекомендованные зарубежными и отечественными специалистами, не обеспечивают достаточную прогностическую мощность моделей. Однако сам факт наличия у пациента ИБС или ХСН уже должны насторожить врача.
Ситуация с диагностикой в нашей стране тоже, к сожалению, далека от идеальной. Анкетирование 125 стационаров в 59 городах показало, что использование широко рекомендуемого V грудного отведения реализуется только в 37% стационаров, плановая ЭКГ после некардиальных операций – в 26% стационаров и ни в одном стационаре не применяется плановый контроль кардиоспецифических тропонинов. Поэтому особый интерес вызывает третий компонент риск-снижающей стратегии – фармакологическая кардиопротекция.
Идея кардиопротекции привлекает пристальное внимание международного медицинского сообщества – постоянно проводятся исследования, публикуются работы и обновляются рекомендации. Однако пока большинство обновлений сводятся к отказу от тех или иных мер по фармакологической кардиопротекции. Так, апробированы и не рекомендованы для профилактического применения накануне и/или во время операции агонисты альфа2-адренорецепторов, блокаторы кальциевых каналов, нитраты, использование бета-блокаторов также подвергается сомнению. В связи с этим закономерным представляется интерес к кардиопротекции путем метаболической модуляции миокарда. Вполне достойное место в когорте метаболически активных препаратов занимает экзогенный фосфокреатинин.
При рассмотрении состояния биоэнергетики миокарда на фоне заболеваний сердца и сердечной недостаточности оказывается, что именно фосфокреатинин и компоненты фосфокреатининкиназной системы подвергаются наибольшему угнетению. Это создает несомненные предпосылки к применению экзогенного фосфокреатинина, биологически активного вещества, способного регулировать сарколеммальные и внутриклеточные ферментные системы, способного к цвиттер-ионным взаимодействиям, а также опосредованно влияющего на транспорт кислорода за счет улучшения реологии крови.
В результате целого ряда исследований было доказано, что добавление фосфокреатинина к стандартной терапии уменьшает степень повреждения миокарда, предупреждает развитие аритмий, уменьшает ремоделирование сердца, улучшает ЭхоКГ-показатели систолической и диастолической функции левого желудочка, уменьшает уровень BNP крови, выраженность симптомов ХСН, повышает толерантность к физической нагрузке.
Фосфокреатинин исследован и для применения во внекардиальной хирургии. Одной из первых работ было изучение его назначения при сосудистых операциях высокого риска. Оказалось, что периоперационное односуточное применение препарата позволяет обеспечить достоверно больший уровень фракции изгнания левого желудочка и многократное снижение частоты серьезных желудочковых нарушений ритма сердца в периоперационном периоде по данным холтеровского мониторирования.
Данные исследования применения фосфокреатинина при ортопедических операциях у пожилых больных в условиях эпидуральной анестезии продемонстрировали, что введение 2 г фосфокреатинина в интраоперационном периоде позволяет добиться многократного снижения риска угрожающих нарушений сердечного ритма и возникновения дискомфорта в области сердца.
Совсем недавно в Обнинске было проведено рандомизированное исследование кардиопротекторных эффектов фосфокреатинина при онкологических операциях у пожилых больных. Оказалось, что назначение фосфокреатинина в течение 5 суток до операции и 3 после не только практически полностью ликвидировало вероятность развития острого коронарного синдрома, но и существенно снизило общую частоту осложнений и сократило длительность пребывания больного в стационаре.
Совсем недавно группой клиницистов во главе с профессором Яворовским в результате многоцентрового проспективного рандомизированного исследования оценки эффективности и безопасности экзогенного фосфокреатинина у пациентов, которым проводится общехирургическое вмешательство, были получены новые интересные данные. Предварительные итоги показывают, что фосфокреатинин позволяет существенно снизить частоту интраоперационной и послеоперационной ишемии, а также уровень кардиоспецифических тропонинов Т в послеоперационном периоде.
Таким образом, отвечая на вопрос, оперировать ли пациентов пожилого и старческого возраста с высоким кардиальным риском или нет, можно уверенно сказать, что да, но в условиях грамотной кардиопротекции.
| Юрий Михайлович ЛОПАТИН, д.м.н., профессор, заведующий кафедрой кардиологии, сердечно-сосудистой и торакальной хирургии Института непрерывного медицинского и фармацевтического образования ФГБОУ ВО ВолгГМУ Минздрава России |
Юрий Михайлович Лопатин, д.м.н., профессор, заведующий кафедрой кардиологии, сердечно-сосудистой и торакальной хирургии Института непрерывного медицинского и фармацевтического образования ФГБОУ ВО ВолгГМУ Минздрава России, посвятил свой доклад теме «Возможности метаболической терапии ХСН у больных ИБС».
Юрий Михайлович также отметил, что в последнее время вопрос энергетической поддержки при ССЗ стал очень актуальным. По его мнению, это представляется весьма логичным, так как механизмы развития сердечной недостаточности и ишемии обязательно включают нарушение энергетических функций сердечной мышцы.
Профессор Лопатин акцентировал внимание на том, что изучение кардиометаболических эффектов различных препаратов или продуктов питания проводится давно, но препаратов с доказанной эффективностью пока очень немного. Дело в том, что в данном вопросе мало понимания патофизиологии энергетического дефицита и теоретического знания, как то или иное средство может на нее повлиять. Крайне важным представляется возможность клинически доказать их эффективность, и именно эту стадию, несмотря на обилие долгосрочных работ, многие из перспективных препаратов не прошли.
Одним из наиболее интересных средств, показывающих хорошие результаты в различных испытаниях, является Неотон. Сегодня имеются публикации об эффективности применения фосфокреатинина при самом широком спектре состояний. Он доказал свои возможности в предупреждении разрыва миокарда, снижении частоты аритмий, влиянии на ремоделирование сердца и не только. Метаанализ использования фосфокреатинина показывает убедительное снижение летальности (3,5% против 10,6%) и аритмии (12% против 22%), повышение фракции выброса левого желудочка (50% против 46%) и уменьшение необходимости использования инотропных препаратов (17% против 35%) по сравнению с контролем.
Исследования применения фосфокреатинина для интраоперационной защиты миокарда представляются очень оптимистичными, потому что пациенты кардиохирургического профиля, безусловно, нуждаются в фармакологической поддержке, достоверно приводящей к уменьшению повреждения миокарда. В период обострения ХСН фосфокреатинин является хорошим потенциальным помощником тем препаратам, которые есть в распоряжении врачей. Введение препарата в лечебных дозах и последующая терапия поддерживающими дозами позволяют не только выиграть время, но и создать условия для благоприятного действия других препаратов.
КОНФЛИКТ ИНТЕРЕСОВ. Автор статьи подтвердил отсутствие конфликта интересов, о котором необходимо сообщить.
CONFLICT OF INTERESTS. Not declared.
Е. О. Гируцкая
Журнал «Лечащий Врач», Москва, Россия
Нозологические особенности повреждения миокарда: обзор симпозиума/ Е. О. Гируцкая Для цитирования: Гируцкая Е. О. Нозологические особенности повреждения миокарда: обзор симпозиума // Лечащий Врач. 2021; 6 (24): 56-59. DOI: 10.51793/OS.2021.24.6.012 Теги: сердце, миокард, энергетическая поддержка, коронавирусная инфекция
Симптомы инфаркта миокарда
Выраженность признаков инфаркта зависит от стадии заболевания.
Предынфарктный период наблюдается не у всех пациентов, протекает в виде обострения и учащения приступов стенокардии и может продолжаться как часы и дни, так и несколько недель.
Острейший период сопровождается развитием ишемии миокарда и образованием участка некроза, продолжается от 20 минут до 3 часов. Основной признак — жгучая или давящая боль, которая часто появляется на фоне физической нагрузки или серьезного стресса. Боль может отдавать в левую руку, плечо, шею, лопатку или нижнюю челюсть.
Болевые ощущения отличаются продолжительностью (более 30 минут) и не снимаются даже повторным приемом нитроглицерина.
Другие симптомы инфаркта миокарда:
- холодный пот;
- страх смерти, резкая слабость;
- одышка, удушье;
- иногда рвота.
Первая помощь при инфаркте миокарда: при обнаружении хотя бы нескольких перечисленных симптомов необходимо немедленно вызвать скорую помощь! Больного нужно положить, обеспечить доступ свежего воздуха. До прибытия врачебной бригады возможны прием нитроглицерина 1 таблетки (или изокета 1 дозы) под язык.
Острый период инфаркта миокарда начинается с момента образования очага некроза на миокарде и длится от 2 до 14 суток.
В этом периоде человек может не испытывать боли. Из-за образования участка некроза и воспаления тканей сердца повышается температура тела. У больного сохраняются и нарастают признаки сердечно-сосудистой недостаточности. Артериальное давление понижено или нормальное.
Первая помощь та же: незамедлительное обращение в скорую.
Подострый период сопровождается формированием рубцовой ткани, продолжается 4-8 недель. Для этого периода инфаркта миокарда не характерны боли в сердце и лихорадка.
Состояние больного нормализуется, АД и частота пульса постепенно приближаются к норме, ослабевают проявления сердечно-сосудистой недостаточности.
Постинфарктный период — все симптомы проходят, лабораторные показатели постепенно возвращаются к норме. Организм приспосабливается к последствиям изменений структуры сердечной мышцы.
Симптомы инфаркта миокарда при атипичных формах болезни:
Абдоминальная — симптомы маскируются под признаки заболеваний брюшной полости: боли и вздутие в животе, тошнота. Астматическая — у больного наблюдаются одышка, приступы удушья. Церебральная — проявления мозговых нарушений: головная боль, головокружение, спутанность сознания. Аритмическая — человек жалуется на учащенное сердцебиение или сбои в сердцебиении. Отечная форма — имеются выраженные периферические отеки мягких тканей.
1 Диагностика инфаркта в «МедикСити»
2 Диагностика инфаркта в «МедикСити»
3 Диагностика инфаркта в «МедикСити»
Признаки обширного инфаркта
Причины и последствия обширного инфаркта страшны своей внезапностью, поскольку в большинстве случаев он настигает человека врасплох. Зная, что это такое и имея представление о возможных результатах, вам удастся распознать патологию и вовремя обратиться за медицинской помощью. Инфаркт характеризуется:
- сильными давящими болями за грудиной, которые могут отдавать в левую верхнюю часть туловища;
- повышенным потоотделением;
- онемением левой руки;
- изменением цвета кожи (бледностью);
- увеличением частоты сердечных сокращений;
- наступлением чувства страха;
- снижением давления;
- нарушением сердечного ритма;
- слабостью;
- болевыми ощущениями в животе, рвотой, не приносящей облегчения (при повреждении задней стенки миокарда).
Развитие острого инфаркта в некоторых случаях не сопровождается болевыми ощущениями, но, несмотря на это, данное состояние также требует принятия экстренных мер, поскольку повторный инфаркт может случиться спустя несколько часов (или даже минут) после первого.
Чтобы избежать необратимых последствий, пострадавшему необходимо оказать помощь до приезда врача. Во-первых, нужно дать человеку нитроглицерин. После этого больного следует разместить на ровной поверхности и запрокинуть его голову вверх (при рвоте человека нужно перевернуть набок). В случаях, когда нитроглицерин не оказывает должного действия, пациенту вводят инъекцию анальгина или промедола.
Обязательно помогите больному избавиться от съемных протезов (если таковые имеются), поскольку препятствий к максимальному поступлению кислорода в легкие должно быть как можно меньше. А если человек находится без сознания и не может дышать самостоятельно, ему потребуется искусственная вентиляция легких.
Осложнения инфаркта миокарда
Подавляющая часть смертей от инфаркта случается в первые часы и сутки и связана с осложнениями инфаркта миокарда:
- Жизнеугрожающие аритмии — желудочковая тахикардия, фибрилляция желудочков, остановка сердца;
- Кардиогенный шок — состояние, развивающееся при обширном поражении миокарда левого желудочка и характеризующееся прогрессирующим снижением АД и нарушением кровоснабжения жизненно-важных органов;
- Аневризма сердца и ее разрыв — истончение сердечной стенки и выпячивание ее под давлением крови в желудочках. В случае разрыва аневризмы — возникает тампонада и остановка сердца;
- Тампонада сердца — смертельно опасное осложнение сердечной аневризмы, при котором после разрыва аневризмы кровь вытекает в полость перикарда. В результате быстрого наполнения перикарда кровью сердце уже не может осуществлять насосную функцию и останавливается;
- Разрыв межжелудочковой перегородки;
- Острая сердечная недостаточность (отек легких);
- Возникновение полной атриовентрикулярной блокады и урежение частоты сердечных сокращений до 20-30 в мин.
Инфаркт миокарда задней стенки левого желудочка
Инфаркт миокарда задней стенки электрокардиографически диагностируется труднее, чем инфаркт передней стенки. По данным сопоставления ЭКГ и вскрытия почти половина таких инфарктов не видны на ЭКГ.
Задняя стенка левого желудочка условно подразделяется на 2 части:
— диафрагмальный отдел задней стенки, — базальный отдел задней стенки.
Заднедиафрагмальный (задний) инфаркт миокарда.
Характерные для такого инфаркта признаки определяются в III стандартном, aVF и обычно поддерживаются II стандартным отведением.
Зубец Q в отведения III и aVF считается патологическим если он превышает 1/2 зубца R и шире 0.03 с. При трансмуральном инфаркте обычно в отведениях III и aVF регистрируется QS. Патологический зубец Q III, aVF обычно сочетается с уменьшенным R в этих отведениях и с характерными изменениям ST и Т. Так как зубец Q в III стандартном отведении может быть даже у здоровых людей, то патологический Q III при инфаркте обязательно сочетается с патологическими Q в aVF и зубцом Q во II стандартном отведении, который в нем должен превышать 10% зубца R. Для инфаркта миокарда такой локализации характерно также Q(II)>Q(I) (в норме QI>QII). Для рубцового инфаркта характерно также, что R(aVF)
В острую стадию заднедиафрагмального инфаркта наблюдаются реципрокные изменения в V1 — V3: снижается ST и появляется высокий положительный «коронарный» зубец Т, причем динамика ST и Т в грудных отведениях наступает быстрее, чем в III и aVF.(См. ЭКГ
)
Заднебазальный (базальный) инфаркт миокарда.
Этот инфаркт миокарда высоких отделов левого желудочка особенно труден для диагностики и часто не диагностируется. Это связано с тем, что прямые признаки в 12 обязательных отведениях отсутствуют.Большей частью диагноз заднебазального инфаркта миокарда ставится по реципрокным изменениям электрокардиограммы. Иногда прямые признаки инфаркта базальных отделов задней стенки могут определяться в дополнительных грудных отведениях V7 — V9, в дорзальном отведении по Небу. В этих отведениях может регистрироваться патологический зубец Q с типичной динамикой ST и Т.
Реципрокные изменения регистрируются в отведениях V1 — V3.
Наиболее специфичны следующие изменения:
— увеличение амплитуды V1 и V2, причем R(V1) > S(V1), — уменьшение глубины зубцов S(V1) и S(V2), — отношение R/S в V1, V2 >= 1.0? — уширение начального R(V1), когда R(V1)>= 0.04 c., — зазубривание R (V1-2), напоминающее неполную блокаду правой ножки пучка Гиса, — снижение ST (V1-2) в острую фазу инфаркта с постепенной обратной динамикой, — появление в острую фазу высоких положительных «коронарных» зубцов Т в V1 — V3-4, причем высота их постепенно увеличивается. (
См. ЭКГ
).
Несмотря на многочисленные косвенные признаки, все они могут отсутствовать при заведомом базальном инфаркте миокарда.
Часто изменения при заднебазальном инфаркте приходится дифференцировать с электрокардиографическими признаками гипертрофии правого желудочка. В отличие от инфаркта, при гипертрофии правого желудочка имеются характерные изменения в левых грудных отведениях.
Диагностика инфаркта миокарда
Сначала врач осматривает пациента и собирает сведения от пациента или его близких о характере и продолжительности болей, силе и повторяемости приступов, принятых медикаментах, их влиянии на самочувствие.
Далее проводится лабораторная и инструментальная диагностика инфаркта миокарда:
- общий и биохимический анализы крови( чаще в условиях стационара);
- исследование кардиоспецифических ферментов и маркеров повреждения сердечной мышцы (чаще в условиях стационара);
- электрокардиография;
- эхокардиография (УЗИ сердца);
- коронарография (в условиях стационара).
Диагностика обширного инфаркта
Помимо анализа клинических проявлений, обширный инфаркт миокарда можно диагностировать при помощи электрокардиографии и ряда лабораторных исследований. Данные методы особенно актуальны для обнаружения нетипичных и неоднозначных форм патологий сердца и сосудов.
Последствиями обширного инфаркта являются изменения показателей анализа крови, а именно:
- лейкоцитоз;
- увеличение скорости оседания эритроцитов;
- появление С-реактивного белка;
- повышение уровня фибриногена, сиаловых кислот.
При диагностике заболевания очень важно исключить возможность наступления других отклонений, схожих с инфарктом по своим клиническим признакам. К примеру, загрудинные боли могут беспокоить пациента при наличии у него острого перикардита, стенокардии, межреберной невралгии и т. д.
Лечение инфаркта миокарда
В мероприятия по интенсивной терапии при остром инфаркте миокарда могут входить:
- введение тромболитических средств для растворения тромба и восстановления кровотока в миокарде;
- обезболивание (чаще применяются наркотические анальгетики);
- стабилизация АД;
- применение антиангинальных, антиаритмических препаратов, антикоагулянтов, антиагрегантов, бета-блокаторов, ингибиторов АПФ и др.
Зачастую в лечении инфаркта миокарда применяются хирургические методики:
- ангиопластика (расширение суженного сосуда с помощью баллонного катетера);
- коронарное стентирование (установка стента в место сужения коронарной артерии, после его расширения баллоном);
- шунтирование (пришивание шунта, которые обходит суженное место).
Постстационарное лечение инфаркта миокарда (амбулаторное ведение после выписки из стационара) также включает в себя целый ряд мероприятий:
- наблюдение кардиолога;
- фармакотерапия;
- контроль АД и ЧСС;
- соблюдение диеты;
- избегание стресса, переутомления и нагрузок;
- рекомендованная двигательная активность;
- отказ от вредных привычек.
Диагностика инфаркта миокарда и лечение пациентов, перенесших инфаркт миокарда, в «МедикСити»
В клинике «МедикСити» диагностика инфаркта миокарда и лечение пациентов, перенесших инфаркт миокарда, а также страдающих другими кардиологическими заболеваниями, осуществляются на высочайшем профессиональном уровне.
На вооружении наших врачей-кардиологов — лучшая аппаратура экспертного уровня, обширные научные знания и новейшие разработки!
У нас адекватные цены и индивидуальный подход. Узнать расписание специалистов и стоимость услуг можно по телефону: +7 (495) 604-12-12.
«МедикСити» — это правильный выбор!
Тактика лечения обширного инфаркта
Для того чтобы последствия после обширного инфаркта оказали минимальное влияние на дальнейшее функционирование всех систем организма, необходимо следовать поэтапному лечению данной патологии.
- Догоспитальный этап – оказание помощи до приезда медицинской бригады и доставка больного в лечебное учреждение.
- Госпитальный – применение медикаментозных средств в условиях стационара с целью стабилизации сердечного ритма, ликвидации и предупреждения образования новых тромбов и т. д.
- Реабилитационные процедуры.
- Наблюдение и амбулаторное лечение.
Острый приступ должен сопровождаться обязательным помещением пострадавшего в стационар. Для того чтобы устранить препятствия на пути кровяного потока к пораженному участку, назначается тромболитическая терапия.
Данные препараты позволяют ликвидировать бляшки в сосудах и восстановить кровоток. Оптимальным временем для принятия тромболитиков считаются первые шесть часов после обширного инфаркта. Это позволяет избежать наступления наиболее опасных последствий.
Вышеописанным действием обладают следующие лекарственные препараты:
- Гепарин.
- Аспирин.
- Плавикс.
- Прасугрел.
- Фраксипарин.
- Алтеплаза.
- Стрептокиназа.
Помимо этого, в целях устранения болевого синдрома назначают:
- Промедол.
- Морфин.
- Фентанил с дроперидолом.
Читайте материал по теме: Обслуживание пожилых людей: от сиделки до роботов
Стабилизировать сердечный ритм после обширного инфаркта можно при помощи капельниц с раствором магнезии. Помимо этого, для активизации кровоснабжения назначают антагонисты кальция, нитраты и β-адреноблокаторы. Ярко выраженное чувство страха у больного подавляют транквилизаторами.
Когда прием лекарственных препаратов противопоказан либо не оказывает должного эффекта, на помощь приходит экстренное аортокоронарное шунтирование. Иногда это единственный возможный вариант улучшения состояния пациента.
Перенесенный обширный инфаркт требует обязательной реабилитации. Частью лечения и ликвидации последствий случившейся патологии является соблюдение постельного режима на протяжении 14 дней после приступа. При этом стоит минимизировать все физические нагрузки на организм: даже ходить нужно с большой осторожностью. Стандартное время пребывания в медицинском учреждении составляет примерно 21 день. Нахождение под наблюдением врачей обязательно и для тех больных, которые перенесли инфаркт на ногах.
Причины заболевания
- Инфаркт миокарда почти всегда развивается на фоне атеросклероза сосудов сердца, т.н. коронарных артерий. При нарушении целостности атеросклеротической бляшки в просвете сосуда образуется тромб, что ведет к внезапному прекращению кровотока в артерии сердца и инфаркту сердечной мышцы.
- Очень редко острое нарушение кровоснабжения сердечной мышцы может произойти во время длительного спазма венечных артерий, например, во время физической или психо-эмоциональной перегрузки.
В ЦЭЛТ вы можете получить консультацию специалиста-кардиолога.
- Первичная консультация — 3 500
- Повторная консультация — 2 300
Записаться на прием
Профилактика патологии
Жизнь после обширного инфаркта не заканчивается, однако таким пациентам следует полностью поменять свои привычки. Чтобы снизить вероятность рецидива, следует строго соблюдать следующие рекомендации специалистов:
- Регулярно посещать врача в целях профилактики осложнений, проходить полное медицинское обследование и неукоснительно исполнять предписания специалиста.
- Прием ацетилсалициловой кислоты.
- Полный отказ от вредных привычек.
- Продолжительные прогулки на свежем воздухе.
- Ежедневные занятия лечебной гимнастикой.
- Сбалансированной питание, с низким содержанием жиров и поваренной соли.