Применение при беременности и кормлении грудью:
Безопасность применения Милдроната при беременности не доказана. Во избежание возможного неблагоприятного влияния на плод Милдронат не следует назначать при беременности. В настоящее время имеются данные клинических исследований по применению Милдроната в составе комбинированной терапии регуляции дискоординированной родовой деятельности, а также в составе комплексного лечения плацентарной недостаточности с целью профилактики и лечения функциональных нарушений развития ЦНС у плода.
Неизвестно, выделяется ли Милдронат с грудным молоком. При необходимости применения Милдроната в период лактации грудное вскармливание следует прекратить.
Побочные действия:
Со стороны сердечно-сосудистой системы: тахикардия, гипотензия.
Со стороны ЦНС: психомоторное возбуждение.
Со стороны пищеварительной системы: диспептические явления.
Аллергические реакции: покраснение, высыпания, зуд, отек.
Особые указания и меры предосторожности:
Пациентам с хроническими заболеваниями печени и почек при длительном применении Милдроната следует соблюдать осторожность.
Применение Милдроната в составе комбинированной терапии пациентов с хронической сердечной недостаточностью повышает толерантность к физической нагрузке.
При инфаркте миокарда Милдронат не является препаратом первого ряда.
В клинических исследованиях выявлено благоприятное воздействие Милдроната на состояние липидного обмена (уменьшение содержания атерогенных липидов в крови).
Следует иметь в виду, что 1 мерная ложка (5 мл) сиропа Милдроната содержит 2,75 г сорбита и 0,25 г глицерина.
Данных о безопасности и эффективности применения Милдроната у детей младше 12 лет недостаточно.
Нет данных о неблагоприятном воздействии Милдроната на скорость реакции.
Лекарственное взаимодействие:
Милдронат можно сочетать с антиангинальными средствами, антикоагулянтами, антиагрегантами, антиаритмическими средствами, сердечными гликозидами, диуретиками, бронхолитиками.
Поскольку Милдронат может вызвать умеренную тахикардию и снижение артериального давления, следует соблюдать осторожность при комбинации Милдроната с гипотензивными средствами и периферическими вазодилататорами.
Условия хранения:
Хранить в сухом, недоступном для детей месте, при температуре не выше 25°C.
Уважаемые друзья, коллеги!
Добро пожаловать на сайт Национального общества по атеротромбозу (НОАТ). Национальное общество по атеротромбозу было организовано в 2004 году по инициативе Всероссийского научного общества кардиологов (ВНОК), Российского общества ангиологов и сосудистых хирургов и Национальной ассоциации по борьбе с инсультом (НАБИ). В состав НОАТ вошли известные кардиологи и неврологи, сосудистые хирурги, липидологи и специалисты в области коагулологии, клинические фармакологи и патофизиологи. НОАТ является ассоциированным членом Российского кардиологического общества
Основная задача Общества — содействие развитию научных исследований и объединение усилий врачей по профилактике и лечению сердечно-сосудистых заболеваний, в основе которых лежит атеротромбоз. Для этого силами специалистов НОАТ ежегодно проводится более 20 школ и семинаров в различных регионах страны. На них повышают свою квалификацию тысячи кардиологов, терапевтов, неврологов и врачей общей практики. Специалисты НОАТ принимают участие в работе крупнейших российских и международных медицинских конгрессов.
С 2008 г в России выпускается журнал «Атеротромбоз», который входит в перечень. изданий, рекомендованных ВАК. Экспертами НОАТ и ВНОК (теперь РКО) созданы рекомендации для практических врачей по диагностике и лечению стабильных проявлений атеротромбоза, утвержденные съездом кардиологов РФ. Эксперты НОАТ принимали активное участие в создании национальных рекомендаций, посвящённых проблеме фибрилляции предсердий, острых коронарных синдромов, венозных тромбоэмболических осложнений.
С созданием сайта НОАТ появился новый источник информации о проблеме тромбообразоваеия, болезнях системы кровообращения, осложнениях, антитромботической терапии. Мы надеемся, что представленная на сайте информация поможет не только практикующим специалистам, но и пациентам, которые смогут ознакомиться с новыми терапевтическими (лекарственными и нелекарственными) возможностями снижения риска атеротромбоза, в том числе инфарктов миокарда и инсультов.
С помощью сайта появилась возможность получать наиболее полную информацию о работе Атерошкол и о других научных событиях, организуемых под эгидой НОАТ. На сайте опубликованы основные материалы, представляемые в школах для практических врачей, представлены все выпуски журнала «Атеротромбоз». Научное направление НОАТ и основные результаты исследований одобрены бюро клинической медицины РАН.
Мы надеемся, что сайт Национального общества по атеротромбозу, являясь сочетанием науки и практики, поможет нам активно и продуктивно бороться с этим опасным недугом.
Председатель наблюдательного совета НОАТ д.м.н., профессор Е.П.Панченко
Несмотря на успехи, достигнутые в лечении больных с сердечно-сосудистыми заболеваниями (ССЗ), до настоящего времени они остаются основной причиной смертности и инвалидности населения. По эпидемиологическим данным, в России 74,9% мужчин и 72,2% женщин в возрасте 25-64 лет умирают от ишемической болезни сердца (ИБС) и цереброваскулярных заболеваний [1].
Средствами базисной терапии ИБС являются препараты антиагрегантного, гиполипидемического, а также гемодинамического и нейрогормонального действия, обеспечивающие оптимизацию соотношения между потребностями миокарда в кислороде и его доставкой. Однако возможности терапии в этом направлении ограничены условиями функционирования миокарда при ишемии, наличием других адаптационно-дезадаптационных процессов, оказывающих существенное влияние на кардиомиоциты (КМЦ) и миокард в целом. Кроме того, в раннем постинфарктном периоде (РПИП) развивается ишемическое ремоделирование миокарда, что служит мощным предиктором сердечно-сосудистой смерти [2]. Пусковым механизмом постинфарктного ремоделирования является потеря КМЦ, которая приводит к возникновению условий, способствующих развитию поражения миокарда в пограничных и удаленных от очага поражения зонах [3]. Ремоделирование сердца в раннем периоде после перенесенного инфаркта миокарда (ИМ) может носить различный характер, но важную роль в этом процессе играет повышение активности симпатико-адреналовой (САС) и ренин-ангиотензиновой систем, активация локального и системного воспалительного ответа [4]. Ишемическое ремоделирование в этот период — это динамический обратимый процесс. Безусловно, основным методом его профилактики заключается в своевременной реперфузии миокарда. В то же время понимание сущности нарушений, происходящих в метаболизме КМЦ при ИМ, описание новых адаптационных ишемических синдромов (оглушенность, гибернация миокарда) [5] открывают возможность для нового направления медикаментозного воздействия на ишемизированный миокард в этот период — цитопротекцию миокарда.
Высокая антиишемическая эффективность одного из цитопротекторов миокарда — мельдония продемонстрирована в целом ряде последних исследований при стенокардии (исследования MILSS, MILSS I, MILSS II), отмечены его положительное действие на толерантность к физической нагрузке, уменьшение клинических проявлений стенокардии, снижение потребности в нитратах, в том числе у пожилых пациентов. Однако комплексное изучение влияния мельдония при кратковременном парентеральном введении на показатели структурно-функционального состояния сердца и вариабельность ритма сердца (ВРС) в РПИП до настоящего времени не проводилось.
Целью исследования стала оценка влияния мельдония при его кратковременном парентеральном использовании в составе комбинированной терапии в РПИП у больных с хронической сердечной недостаточностью (ХСН) на клиническое течение восстановительного периода, антиишемическую и антиангинальную эффективность, структурно-функциональные показатели и ВРС.
Материалы и методы
Проведено открытое рандомизированное исследование по изучению влияния мельдония (идринол, ЗАО Фарм, Россия) в составе комбинированной терапии на течение восстановительного периода у больных в РПИП. В исследование включили 60 пациентов, мужчин и женщин, в возрасте от 45 до 75 лет на 3-4-й неделе после перенесенного ИМ с наличием симптомов сердечной недостаточности II-III функционального класса — ФК (ОССН, 2002). После разделения методом простой рандомизации на 2 группы пациентам 1-й (основной) группы (n
=30) в дополнение к базисной терапии ИБС (эналаприл, бисопролол, ацетилсалициловая кислота, клопидогрел, спиронолактон, торасемид, симвастатин, при необходимости антагонисты кальция, нитраты) назначали мельдоний в дозе 1000 мг/сут внутривенно. Пациенты 2-й (контрольной) группы (
n
=30) получали только базисную терапию. Продолжительность исследования составляла от 10 до 14 дней (в среднем 12,4±0,8 дня). Больные основной и контрольной групп были сопоставимы по возрасту, полу, тяжести заболевания, характеру проводимой базисной терапии. Средние дозировки препаратов базисной терапии в 1-й и 2-й группах достоверно не различались. Исходная характеристика групп больных представлена в
табл. 1
.
Для верификации ФК ХСН были использованы критерии ОССН (2002) и тест с 6-минутной ходьбой (ТШХ). Для диагностики и оценки эффективности терапии ХСН всем пациентам определяли уровень N-концевого предшественника мозгового натрийуретического пептида (NT-proBNP) в плазме с помощью иммуноферментного анализа (набор для определения NT-proBNP, «Biomedica», Словакия) на анализаторе Liasis (Италия).
Для установления эпизодов нарушения ритма сердца и частоты эпизодов ишемии на протяжении 24 ч проводилось суточное мониторирование (СМ) электрокардиограммы (ЭКГ) на аппаратно-программном комплексе с цифровой записью ЭКГ Кардиотехника-04 ЗАО («ИНКАРТ», Россия).
У всех пациентов изучали структурно-функциональных параметры сердца с помощью эхокардиографии на аппарате Sonoline G50 (Германия) в М-модальном и двухмерном режимах в стандартных эхокардиографических позициях в соответствии с рекомендациями по количественной оценке структуры и функций камер сердца [6]. Для характеристики систолической функции сердца оценивали фракцию выброса (ФВ) левого желудочка (ЛЖ) по Симпсону (норма >45%). Диастолическую функцию ЛЖ исследовали путем оценки трансмитрального кровотока при проведении пробы Вальсальвы и потока в легочных венах. Гипертрофию миокарда ЛЖ диагностировали при индексе массы миокарда (ИММ) ЛЖ более или равных 125 г/м2 для мужчин и 110 г/м2 для женщин. Определяли типы ремоделирования ЛЖ с учетом относительной толщины стенок (ОТС) ЛЖ и ИММЛЖ: а) концентрическое ремоделирование (КР): нормальный ИММ ЛЖ и ОТС >0,42; б) концентрическая гипертрофия (КГ): увеличение ИММ ЛЖ и ОТС >0,42; в) эксцентрическая гипертрофия (ЭГ): увеличение ИММ ЛЖ при нормальной ОТС (<0,42).
Для оценки функционального состояния вегетативной нервной системы (ВНС) применялось исследование ВРС. Запись ЭКГ выполняли на приборе ВАРИКАРД-1.41 (Россия) в течение 5 мин утром в состоянии покоя (через 15 мин после адаптации больного к обстановке) в одном из стандартных отведений в положении лежа и во время проведения 10-минутной активной ортостатической пробы [7]. Учитывали следующие показатели ВРС: SDNN (в мс) — стандартное отклонение величин интервалов RR за весь рассматриваемый период; ИН — индекс напряжения (в усл. ед.), TP (в мс2) — суммарная мощность спектра ВРС; HF, LF, VLF (в %) — соответственно мощность спектра высокочастотного, низкочастотного и очень низкочастотного компонента вариабельности в % от суммарной мощности колебаний; ИЦ (в усл. ед.) — индекс централизации, отражающий степень централизации управления ритмом сердца.
Исходный вегетативный тонус (ВТ) оценивали по фоновой пробе (лежа, в состоянии покоя) путем расчета ИН регуляторных систем. ИН — важнейший показатель, характеризующий состояние центрального контура регуляции, отличается очень высокой чувствительностью к усилению тонуса симпатической части ВНС (С-ВНС) и при стрессе увеличивается в несколько раз [8]. Направленность исходного ВТ и характер симпатико-парасимпатических отношений оценивали следующим образом: нормотония — при ИН от 30 до 90 усл. ед., ваготония — ИН менее 30 усл. ед., симпатикотония с умеренным преобладанием тонуса С-ВНС — ИН от 90 до 160 усл. ед., гиперсимпатикотония — ИН более 160 усл. ед.
Вегетативные реакции, возникающие в ответ на внешние и внутренние раздражители, характеризуют собой вегетативную реактивность (ВР). Функциональные резервы вегетативной регуляции деятельности сердца позволяет оценить ортостатическая проба. Поэтому для оценки ВР обоих отделов ВНС проводили пробу, предложенную Р.М. Баевским [7], и оценивали ВР с помощью отношения показателя ИН во время ортопробы к фоновому ИН с учетом его значения. При этом выделяли нормальную, гипер- и асимпатикотоническую ВР [7].
В целом исходный ВТ и ВР дают представление о гомеостатических возможностях организма, а вегетативное обеспечение деятельности — о его адаптационных возможностях [8].
Статистическую обработку данных проводили с помощью программы Statistica 7. Для оценки достоверности различий между группами вычисляли критерий t
Стьюдента, критерий знаков, метод углового преобразования (?). Вычисление значимости качественных различий оценивали с помощью точного метода Фишера. Статистически значимыми считали различия при
р
<0,05. Протокол исследования одобрен Региональным этическим комитетом.
Результаты
В обеих группах у перенесших ИМ больных через 10-14 дней от начала терапии выявлены улучшение клинического состояния и положительная динамика ФК ХСН. Отмечено уменьшение уровня симптомов ХСН, более выраженное в группе больных, принимающих мельдония.
В обеих группах существенно улучшились показатели переносимости нагрузки, оцененной при ТШХ. Толерантность к физической нагрузке по данным ТШХ в группе пациентов, получающих мельдоний, выросла на 22,4% против 17,9% в контрольной группе (р
>0,05). Отмечено уменьшение ФК ХСН, более выраженное в 1-й группе больных, принимающих мельдоний (на 9,3% по сравнению со 2-й группой, где аналогичный показатель составил 7,8%;
р
>0,05). Положительное влияние применения мельдония в течение 10-14 дней дополнительно к базисной терапии на течение ХСН в РПИП подтверждено уменьшением уровня NT-proBNP у пациентов основной, 1-й группы на 18,7% (с 494,9±209,5 до 402,4±124,5 пг/мл;
р
>0,05), тогда как в контрольной (2-й) группе уровень NT-proBNP уменьшился на 4,8% (с 486,3±238,8 до 462,6±206,3 пг/мл;
р
>0,05). Различие между конечными результатами в 1-й и 2-й группах были на уровне тенденции (
р
<0,1).
Назначение мельдония в РПИП в составе комбинированной терапии у больных с ХСН в конце 10-14-дневного парентерального использования сопровождалось значимым антиангинальным эффектом в виде достоверного урежения приступов стенокардии на 78,7% в основной против 20,3% в контрольной группе и уменьшением потребности в дополнительном использовании нитратов до 1,2±0,12 применения нитроспрея в неделю в основной группе против 1,83±0,19 в группе контроля (р
<0,05).
Кроме того, нами констатировано антиаритмическое и антиишемическое действие мельдония по данным СМ ЭКГ [9]. Так, по результатам СМ ЭКГ, применение мельдония в составе комбинированного лечения в 1-й группе сопровождалось достоверным уменьшением числа пациентов с эпизодами нарушения ритма сердца (желудочковой, предсердной экстрасистолии, а также кратковременных эпизодов фибрилляции предсердий) по сравнению со 2-й (контрольной) группой: –84 и –17,6% соответственно Различия между группами по конечному результату были статистически значимыми. Число пациентов с эпизодами бессимптомной ишемии по данным СМ ЭКГ достоверно уменьшились в 1-й группе на фоне добавления к базисной терапии мельдония на –87,5% против –42,9% во 2-й (контрольной) группе. Пациентам как основной, так и контрольной группы в связи с наличием эпизодов аритмии и ишемии по данным СМ ЭКГ проводилась коррекция базисной терапии (увеличение дозы β-адреноблокаторов).
Следует отметить, что антиангинальный и антиишемический эффекты не были опосредованы влиянием мельдония на гемодинамические показатели: уровни САД и ДАД, а также ЧСС в ходе терапии статистически значимых изменений не претерпели.
Отмечено позитивное влияние мельдония в составе комбинированной терапии на структурно-функциональные параметры сердца в РПИП (табл. 2)
.
У пациентов 1-й группы, получавших в течение 10-14 дней мельдоний, к концу исследования ФВ увеличилась на 5,2% (р
>0,05), тогда как в контрольной группе — на 1,1%.
Исходно в 1-й группе ДД диагностирована у 93% пациентов (см. табл. 2)
. В ходе 10-14-дневного применения мельдония частота выявления ДД снизилась до 83%. Во 2-й (контрольной) группе исходно ДД определялась также у 93% больных, а к концу исследования число больных уменьшилось до 87% (различия между группами по конечному результату статистически незначимы).
Благоприятные изменения на фоне лечения мельдонием выявлены и в геометрии сердца. Обнаружено уменьшение КДР ЛЖ в обеих группах, более значимое при дополнительном парентеральном введении мельдония (&Dgr; –3,6 и –1,6%; р
>0,05 в основной и контрольной группах соответственно). Размеры ЛП у пациентов 1-й группы статистически незначимо уменьшились на 3,8%, во 2-й группе — на 3,1%.
Исходно у всех пациентов, включенных в исследование, выявлены все типы ремоделирования ЛЖ: КР, ЭГ и КГ. К концу исследования в 1-й группе, получавшей мельдоний, отмечены уменьшение числа больных с наиболее неблагоприятными типами — ЭГ и КГ ЛЖ — с 90 до 83% и увеличение числа пациентов с КР ЛЖ с 10 до 17% (р
>0,05). Во 2-й (контрольной) группе наблюдалось уменьшение числа пациентов с ЭГ и КГ ЛЖ с 87 до 83% и увеличение числа лиц с КР ЛЖ — с 13 до 17% (
р
>0,05).
Несомненный интерес представляла оценка влияния мельдония в составе комбинированной терапии ХСН в РПИП при его кратковременном парентеральном введении на показатели ВРС, отражающие состояние ВНС, так как активация САС играет немаловажную роль в формировании ремоделирования ЛЖ в РПИП [3]. При изучении показателей ВРС исходно у пациентов обеих групп выявлено снижение среднего квадратического отклонения (SDNN) <50 мс: 37,9±2,4 мс в 1-й группе и 38,3±2,27 мс во 2-й. Это указывает на повышение активности С-ВНС и является прогностически неблагоприятным признаком (свидетельствует о высоком риске возникновения опасных аритмий и внезапной коронарной смерти) [7, 10]. Установлено, что у больных с ХСН в РПИП отмечалась выраженная централизация управлением ритма сердца. Это нашло отражение в увеличении средних значений ИН (292,5±29,1 и 287,25±24,7 усл. ед.) и ИЦ (6,93±0,8 и 6,61±0,73 ед.) в основной и контрольной группах соответственно. В ходе 10-14-дневного применения мельдония у пациентов в РПИП в составе комбинированной терапии отмечено вегетонормализующее действие препарата. Оно проявилось в виде достоверного увеличения SDNN на 56,9% против 20,6% в контрольной группе, статистически значимого уменьшения стресс ИН на 48,8% против 11,3% в группе контроля, а также достоверного снижения ИЦ на 32,9% в основной группе, тогда как в контрольной группе пациентов этот показатель увеличился на 12,7% [9].
При оценке исходного ВТ сердечно-сосудистой системы в ходе анализа фонового ИН по данным ВРС у пациентов обеих групп в начале исследования выявлено состояние симпатико- и гиперсимпатикотонии (рис. 1)
.
Рисунок 1. Динамика исходного ВТ у больных с ХСН в РПИП. Здесь и на рис. 2: * — достоверность различий между исходными и конечными результатами; **- достоверность различий между процентными долями 1-й и 2-й групп (p
<0,05). Однако на фоне дополнительного назначения к базисной терапии мельдония в 1-й группе больных отмечены благоприятные изменения исходного ВТ в виде уменьшения числа случаев гиперсимпатикотонией и появления больных с нормотонией. Во 2-й (контрольной) группе к концу исследования гиперсимпатикотонический тип исходного ВТ остался преобладающим. Различия между группами по конечному результату статистически значимы.
При анализе результатов пробы на ВР исходно в обеих группах преобладали пациенты с а- и гиперсимпатикотонической ВР (рис. 2)
.
Рисунок 2. Динамика ВР у больных с ХСН в РПИП. После 10-14-дневного применения мельдония в РПИП в составе комбинированной терапии в 1-й группе у пациентов достоверно стал преобладать нормальный тип ВР: доля пациентов с гипер- и асимпатикотонией уменьшилась. Во 2-й (контрольной) группе к концу исследования гиперсимпатикотонический тип ВР стал наиболее часто встречающимся.
Обсуждение
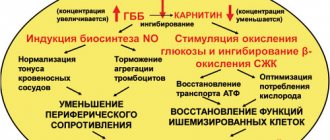
Мельдоний — препарат их группы парциальных ингибиторов свободных жирных кислот (СЖК); известен прежде всего как лекарственное средство, оказывающее негемодинамическое антиишемическое действие. Наиболее доказана и востребована в клинической практике его антиангинальная эффективность [11, 12], которая отмечена и в настоящем исследовании. Особенности фармакологического антиишемического действия мельдония опосредуются снижением зависимого от карнитина транспорта жирных кислот в митохондрии мышечной ткани [13, 14], усилением синтеза γ-бутиробетаина и, как следствие, индукцией образования оксида азота (NO) — одного из наиболее эффективных природных агентов, связывающих свободные радикалы в организме. NO обусловливает такие эффекты мельдония, как снижение периферического сопротивления сосудов, уменьшение вызванного норадреналином или ангиотензином II спазма кровеносных сосудов, торможение агрегации тромбоцитов и повышение эластичности мембран эритроцитов. Мельдоний оказывает селективное действие именно на ишемизированную зону различных тканей, в том числе миокарда, практически не влияя на незатронутые ишемией участки (противодействие эффекту обкрадывания) [15]. Кроме того, антиишемический эффект мельдония может опосредоваться вегетонормализующим влиянием препарата, которое отмечено и описано нами ранее [9]. Полученные в ходе настоящего исследования данные СМ ЭКГ продемонстрировали значимое уменьшение числа пациентов с эпизодами ишемии в основной группе, принимающих мельдоний, тогда как в контрольной группе, несмотря на проведение базисной терапии, продолжали фиксироваться кратковременные эпизоды ишемии.
Выявленные нами антиаритмические эффекты терапии с назначением в течение 10-14 дней мельдония у пациентов в РПИП могут объясняться снижением внутриклеточной концентрации СЖК, которые обладают проаритмогенным свойством [16], а также уменьшением проницаемости мембран для ионов кальция и угнетением ассоциированного с ним ?-адренергического ответа миокарда [17, 18]. Кроме того, антиаритмогенный эффект мельдония может опосредоваться благоприятным влиянием препарата на показатели исходного ВТ и ВР, что в исследовании подтверждено статистически значимым уменьшением числа больных с гиперсимпатикотонией и увеличением числа пациентов с нормальным типом ВР. По мнению В.М. Михайлова [10], благоприятные изменения показателей ВРС сопровождаются не только снижением риска развития желудочковой тахикардии, фибрилляции желудочков, но и риска внезапной смерти у больных с ИМ.
Мельдоний при кратковременном парентеральном введении в РПИП у больных с ХСН оказывает благоприятное влияние на структурно-функциональные параметры сердца и показатели вегетативной регуляции, что может иметь большое клиническое значение. Положительное влияние мельдония на показатели вегетативного гомеостаза сердца по результатам исследования ВРС также может быть опосредовано возможностью индуцировать образование NO, так как известно, что реализация вегетативного влияния на ритм сердца существенно зависит от адекватной продукции NO нейронального происхождения [19]. По данным экспериментальной работы Е.В. Артюшковой и соавт. [20], на модели L-NAME-индуцированного дефицита NO показана способность мельдония в дозе 80 мг/кг не только увеличивать концентрацию стабильных метаболитов NO, но и снижать коэффициент дисфункции эндотелия до уровня у интактных животных.
Заключение
Внутривенное применение в течение 10-14 дней мельдония в дозе 1000 мг/сут в составе комбинированной терапии в РПИП у больных с сердечной недостаточностью оказывает позитивное влияние на течение восстановительного периода: уменьшает проявления ХСН, что сопровождается увеличением результатов ТШХ, снижением тяжести ФК ХСН и уменьшением содержания в крови больных уровня NT-proBNP; дает антиишемический и антиаритмический эффекты, что улучшает клиническое состояние пациентов в РПИП благодаря достоверному снижению частоты приступов стенокардии и потребности в дополнительном приеме нитратов, уменьшает количество эпизодов аритмии и ишемии; благоприятно влияет на структурно-функциональные параметры сердца (уменьшается число пациентов с неблагоприятными типами ремоделирования ЛЖ и улучшается диастолическая функция сердца); оказывает нормализующее влияние на основные показатели ВРС, увеличивает число больных с нормотонией и достоверно уменьшает число больных с гиперсимпатикотоническим ВТ, что сопровождается увеличением числа больных с нормальной ВР и значимым уменьшением числа пациентов с гиперсимпатикотоническим типом ВР.
Милдронат
Действующее вещество
Мельдоний (в виде фосфата)
Механизм действия
Фармакологическое действие — кардиопротективное, антигипоксическое, ангиопротективное, антиангинальное.
Препарат хорошо всасывается ЖКТ. Биодоступность – 78% в первые два часа после приема. Способствует улучшению метаболизма.
При повышенных нагрузках препарат Милдронат, обеспечивает потребности клеток в кислороде, оказывает на них тонизирующее влияние, защищает от повреждений и устраняет накопление токсинов.
В ходе применения препарата организм быстро восстанавливается энергетически, приобретает способность выдерживать высокую нагрузку.
Милдронат используют для лечения нарушений кровоснабжения мозга, сердечно-сосудистой системы и в целях повышения физической и умственной работоспособности.
Милдронат применяют в целях замедления образований некротических зон, для сокращения реабилитационного периода при остром ишемическом повреждении миокарда.
В лечении сердечной недостаточности для уменьшения частоты приступов стенокардии, повышения сократимости миокарда, увеличения толерантности к физическим нагрузкам.
Используют при патологиях глазного дна (сосудистой и дистрофической)
При абстинентном синдроме в лечении хронического алкоголизма в целях устранения функциональных нарушений нервной системы.
Показания к применению
Препарат применяется как один из компонентов при комплексной терапии ишемической болезни сердца (хроническая недостаточность сердца, инфаркт миокарда, стенокардия, дисгормональная кардиопатия и), нарушения кровоснабжения мозга (хроническая недостаточность кровообращения мозга, мозговые инсульты). Также препарат Милдронат показан при тромбозе центральной вены сетчатки и ее ветвей, при гемофтальме и кровоизлиянии в сетчатку различной этиологии, ретинопатии различной этиологии (гипертоническая, диабетическая), физическое нагрузок (в том числе у спортсменов), снижение работоспособности, абстинентном синдроме при хроническом алкоголизме (как часть комплексной терапии).
Противопоказания
Гиперчувствительность к компонентам препарата Милдронат.Препарат противопоказано лицам, с повышенным внутричерепным давлением (при внутри черепных опухолях, при нарушении венозного оттока). Препарат Милдронат не принимать детям до 12 лет.Более подробно читайте в официальной инструкции препарата.
Побочные действия
В редких случаях: зуд, снижение АД (гипотония), тахикардия, диспептические расстройства.