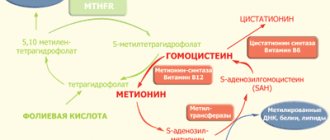
Бета-2-адреностимуляторы, также бета-2-агонисты, Β-2-агонисты, Стимуляторы β-2-адренорецепторов, Β-2-адреномиметики — группа лекарственных препаратов, механизм действия которых заключается в стимуляции бета-2-адренорецепторов, и которые применяются преимущественно для лечения хронических заболеваний дыхательной системы, сопровождающихся бронхоспазмом, а также в акушерстве для снижения тонуса и расслабление гладких мышц матки при угрозе преждевременных родов.
История создания
Начало применения препаратов, стимулирующих адренорецепторы, для лечения бронхиальной астмы и других обструктивных заболеваний легких приходится на 1900 год, когда для лечения бронхиальной астмы впервые применен адреналин — неселективный α- и β-адреностимулятор. Но при применении адреналина часто наблюдались побочные эффекты (тахикардия, аритмогенное действие, головная боль), при ингаляциях этого препарата часто наблюдались повреждения слизистой оболочки верх дыхательных путей, недостатком применения адреналина также кратковременность действия (1-1,5 часов). Эти факторы стали стимулом для дальнейшей разработки более эффективных и безопасных препаратов для лечения бронхоспазма.
В 1940 году впервые синтезирован изопреналин — синтетический катехоламин, производное адреналина, является неселективным β 2 -адренорецепторов, и обладает свойствами также β 1 -адреномиметиков. При его применении наблюдалось меньше побочных эффектов. Но этот препарат также имел короткий период действия (1-1,5 ч), что связано с разрушением препарата ферментом легочной катехол-О-метилтрансферазой, и кроме этого, биотрансформация изопреналина приводила к образованию метаболитов, обладающих свойствами β-блокаторов. В 1963 году в лаборатории синтезированный орципреналин — неселективный β 2 -адренорецепторов, что хотя и имеет более низкую активность по сравнению с изопреналином, но имеет более длительный период действия и сродство к адренорецепторов бронхов и меньшую — до адренорецепторов миокарда и кровеносных сосудов.
Но неконтролируемое применение неселективных бета-агонистов привело к повышению смертности среди больных бронхиальной астмой, повьязають с накоплением в результате передозировки этих препаратов их метаболитов, обладающих свойствами бета-блокаторов и способствуют бронхоспазма, а также увеличению частоты осложнений со стороны сердечно-сосудистой системы и смертности больных. Дальнейшие научные исследования в области фармакологии привели к синтезу в 1967 году в Великобритании первого селективного β 2 -адренорецепторов короткого действия — сальбутамола, который был разработан в лаборатории структурного подразделения . В начале 80-х годов ХХ века также в лаборатории синтезирован первый β 2 -адренорецепторов с длительным периодом действия — сальметерол, а в 1986 году в Японии разработан другой адреностимулятор длительного действия — формотерол. Параллельно с разработкой β 2 -адренорецепторов длительного действия продолжаются работы по синтезу β 2 агонистов ультратривалои действия (более 24 часов), которые привели к созданию первого ультратривало действующего β 2 -адренорецепторов в 2009 году в лаборатории — индакатеролу.
Особенности лечения препаратами β-адреномиметиков
Сальбутамол и фенотерол обладают быстрым (эффект развивается в течение 1-3 минут), но непродолжительным (3-6 часов) действием, поэтому их используют для купирования (устранения) приступов бронхиальной астмы.
Салметерол и формотерол оказывают продолжительное действие – более 12 часов, кроме того, эффект этих препаратов развивается не сразу, а лишь через 30 минут после применения. Именно поэтому салметерол и формотерол применяют для профилактики развития бронхоспазмов.
В длительном лечении бронхиальной астмы и хронической обструктивной болезни легких используют комбинированные препараты, в состав которых входят как β2-адреномиметики, так и М-холиноблокаторы (ипратропия бромид, тиотропия бромид, умеклидиния бромид, аклидиния бромид, гликопиррония бромид), а также гормональные средства класса глюкокортикостероидов (флутиказон, будесонид).
Классификация
Все препараты группы бета-2-адренорецепторов можно поделить по селективности их действия на β 2 -адренорецепторы. К препаратам неселективной действия, что, кроме β 2 -адренорецепторов, действуют также и на β 1 -адренорецепторы (в том числе адренорецепторы, расположенные в миокарде, кровеносных сосудах и других органах), и имеют короткий период действия, относятся изопреналин, орципреналин и гексопреналин. Селективные β 2 -адреностимуляторы делятся по длительности действия на препараты короткого действия, к которым относятся сальбутамол (а также левовращающий изомер сальбутамола — левосальбутамол), фенотерол и тербуталин. К β 2 -адренорецепторов длительного действия относятся сальметерол, формотерол, кленбутерол и бамбутерол. Выделяют также β 2 -адреностимуляторы ультратривалои действия, первым представителем которых является индакатерол.
Механизм действия
Механизм действия всех бета-2-адренорецепторов заключается в стимуляции β 2 -адренорецепторов, которые в основном находятся в гладкой мускулатуре бронхов, а также миометрия и кровеносных сосудов, путем активации внутриклеточной аденилатциклазы, которая образует комплекс с G-протеином, под влиянием которого повышается образование циклического АМФ и стимуляция протеинкиназы типа А, что приводит к расслаблению гладкой мускулатуры внутренних органов. Селективные β 2 агонисты не разрушаются ферментом легочной катехол-О-метилтрансферазой, поэтому имеют более длительный период действия, и могут применяться как ингаляционно, так и перорально и парентерально. Фенотерол и формотерол является являются конкурентными антагонистами β 2 -адренорецепторов, что обеспечивает быстрый начало действия препаратов, но и большую вероятность возникновения побочных эффектов (в том числе «синдрома рикошета» — усиление бронхоспазма при превышении рекомендуемых доз препарата, и повышение толерантности к этим лекарственным препаратам ). Сальбутамол и сальметерол является неконкурентным антагонистами β 2 -адренорецепторов, поэтому при их применении наблюдается медленный начало действия по сравнению с конкурентными антагонистами бета-адренорецепторов, но и меньшее количество побочных эффектов даже при длительном применении. Длительный период действия сальметерол и формотерола обусловлен высокой липофильностью этих препаратов. Формотерол, в отличие от сальметерола, имеет незначительную липофильностью, поэтому после проникновения в клетки дыхательных путей препарат быстро диффундирует в плазматическую мембрану, в которой создается своеобразное депо формотерола, из которого препарат проходит в межклеточное пространство и одновременно связывается с адренорецепторами гладких мышц и липидами, обеспечивает как быстрое начало действия (1-3 минуты после ингаляции), так и продолжительность (до 12:00) эффекта применения формотерола. Внутриклеточный механизм действия сальметерол несколько отличается от механизма действия других β 2 агонистов. Сальметерол в связи с наличием длинного липофильного салигининового цепочки («хвоста» молекулы) имеет очень высокой липофильностью (в 10000 раз выше липофильностью сальбутамола). Во время прохождения в клетки дыхательных путей сальметерол быстро проникает в мембраны клеток и закрепляется у структур смежных с β 2 -адренорецепторов, а длинная липофильное часть молекулы препарата связывается с неактивной частью рецептора, обеспечивает длительный эффект сальметерола. Мембраны клеток дыхательной системы становятся своеобразным «депо» для препарата, из которых сальметерол медленно диффундирует в клетки гладких мышц дыхательных путей. Под влиянием β 2 -адренорецепторов уменьшается выделение медиаторов воспаления с тучных клеток (в том числе выделение гистамина и лейкотриенов), уменьшается проницаемость капилляров (что способствует предупреждению развития отека слизистой оболочки бронхов) и модуляция выработку слизи бронхиальных желез, что приводит к оптимизации мукоцилиарного клиренса. Но снижение выделения медиаторов воспаления и снижения проницаемости капилляров при применении β 2 -адренорецепторов не сопровождаются уменьшением количества клеток воспаления в слизистой оболочке бронхов (в том числе активированных — макрофагов, эозинофилов и лимфоцитов), что теоретически может привести к усилению воспалительного процесса в дыхательных путях ( например, при появлении после применения адреностимуляторов возможности сделать свободных дыхание, и при этом вдохнуть большое количество экзогенных аллергенов). При ингаляционном применении препараты группы действуют практически только на β 2 -адренорецепторы бронхов и лишь незначительно влияют на адренорепторы в других органах. Повышение эффективности бета-2-адренорецепторов при ингаляционном применении наблюдается при совместном применении с ингаляционными кортикостероидами и м холинолитиками. Часть препаратов группы (неселективные адреностимуляторы, а также сальбутамол и фенотерол) имеют токолитическое действие, что приводит к снижению тонуса и расслабление гладких мышц матки, и применяются при угрозе преждевременных родов и истмико-цервикальной недостаточности. Кленбутерол кроме свойств Бронхолитики имеет анаболические свойства, и используется для быстрого наращивания мышечной массы культуристами или для поддержания формы тела совместно с посещением тренажерных залов.
Бета-адреноблокаторы III поколения в лечении сердечно-сосудистых заболеваний
Современную кардиологию невозможно представить без препаратов группы бета-адреноблокаторов, которых в настоящее время известно более 30 наименований. Необходимость включения бета-адреноблокаторов в программу лечения сердечно-сосудистых заболеваний (ССЗ) очевидна: за последние 50 лет кардиологической клинической практики бета-адреноблокаторы заняли прочные позиции в профилактике осложнений и в фармакотерапии артериальной гипертонии (АГ), ишемической болезни сердца (ИБС), хронической сердечной недостаточности (ХСН), метаболическом синдроме (МС), а также при некоторых формах тахиаритмий. Традиционно в неосложненных случаях медикаментозное лечение АГ начинают с бета-адреноблокаторов и диуретиков, снижающих риск развития инфаркта миокарда (ИМ), нарушения мозгового кровообращения и внезапной кардиогенной смерти.
Концепция опосредованного действия лекарственных средств через рецепторы тканей различных органов была предложена N.?Langly в 1905 г., а в 1906 г. H.?Dale подтвердил ее в практике.
В 90-е годы было установлено, что бета-адренорецепторы подразделяются на три подтипа:
- бета1-адренорецепторы, которые расположены в сердце и через которые опосредуются стимулирующие влияния катехоламинов на деятельность сердца — насоса: учащение синусового ритма, улучшение внутрисердечной проводимости, повышение возбудимости миокарда, усиление сократимости миокарда (положительные хроно-, дромо-, батмо-, инотропный эффекты);
- бета2-адренорецепторы, которые расположены преимущественно в бронхах, гладкомышечных клетках сосудистой стенки, скелетных мышцах, в поджелудочной железе; при их стимуляции реализуются бронхо- и вазодилятационные эффекты, релаксация гладких мышц и секреция инсулина;
- бета3-адренорецепторы, локализованные преимущественно на мембранах адипоцитов, принимают участие в термогенезе и липолизе. Идея использования бета-адреноблокаторов в качестве кардиопротекторов принадлежит англичанину J.?W.?Black, которому в 1988 году вместе с сотрудниками, cоздателями бета-адреноблокаторов, была присуждена Нобелевская премия. Нобелевский комитет счел клиническую значимость этих препаратов «величайшим прорывом в борьбе с болезнями сердца после открытия дигиталиса 200 лет назад».
Способность блокировать влияние медиаторов на бета1-адренорецепторы миокарда и ослабление влияния катехоламинов на мембранную аденилатциклазу кардиомиоцитов с уменьшением образования циклического аденозинмонофосфата (цАМФ) определяют основные кардиотерапевтические эффекты бета-адреноблокаторов.
Антиишемический эффект бета-адреноблокаторов объясняется снижением потребности миокарда в кислороде, вследствие уменьшения частоты сердечных сокращений (ЧСС) и силы сердечных сокращений, возникающих при блокировании бета-адренорецепторов миокарда.
Бета-блокаторы одновременно обеспечивают улучшение перфузии миокарда за счет уменьшения конечного диастолического давления в левом желудочке (ЛЖ) и увеличения градиента давления, определяющего коронарную перфузию во время диастолы, длительность которой увеличивается в результате урежения ритма сердечной деятельности.
Антиаритмическое действие бета-адреноблокаторов, основанное на их способности уменьшать адренергическое влияние на сердце, приводит к:
- уменьшению ЧСС (отрицательный хронотропный эффект);
- снижению автоматизма синусового узла, АВ-соединения и системы Гиса–Пуркинье (отрицательный батмотропный эффект);
- сокращению длительности потенциала действия и рефрактерного периода в системе Гиса–Пуркинье (укорачивается интервал QT);
- замедлению проводимости в АВ-соединении и увеличению продолжительности эффективного рефрактерного периода АВ-соединения, удлинению интервала РQ (отрицательный дромотропный эффект).
Бета-адреноблокаторы повышают порог возникновения фибрилляции желудочков у больных острым ИМ и могут рассматриваться как средства профилактики фатальных аритмий в остром периоде ИМ.
Гипотензивное действие бета-адреноблокаторов обусловлено:
- уменьшением частоты и силы сердечных сокращений (отрицательное хроно- и инотропное действие), что суммарно приводит к снижению минутного сердечного выброса (МОС);
- снижением секреции и уменьшением концентрации ренина в плазме;
- перестройкой барорецепторных механизмов дуги аорты и синокаротидного синуса;
- центральным угнетением симпатического тонуса;
- блокадой постсинаптических периферических бета-адренорецепторов в венозном сосудистом русле, с уменьшением притока крови к правым отделам сердца и снижением МОС;
- конкурентным антагонизмом с катехоламинами за рецепторное связывание;
- повышением уровня простагландинов в крови.
Препараты из группы бета-адреноблокаторов отличаются по наличию или отсутствию кардиоселективности, внутренней симпатической активности, мембраностабилизирующим, вазодилятирующим свойствам, растворимости в липидах и воде, влиянию на агрегацию тромбоцитов, а также по продолжительности действия.
Влияние на бета2-адренорецепторы определяет значительную часть побочных эффектов и противопоказаний к их применению (бронхоспазм, сужение периферических сосудов). Особенностью кардиоселективных бета-адреноблокаторов по сравнению с неселективными является большое сродство к бета1-рецепторам сердца, чем к бета2-адренорецепторам. Поэтому при использовании в небольших и средних дозах эти препараты оказывают менее выраженное влияние на гладкую мускулатуру бронхов и периферических артерий. Следует учитывать, что степень кардиоселективности неодинакова у различных препаратов. Индекс ci/бета1 к ci/бета2, характеризующий степень кардиоселективности, составляет 1,8:1 для неселективного пропранолола, 1:35 — для атенолола и бетаксолола, 1:20 — для метопролола, 1:75 — для бисопролола (Бисогамма). Однако следует помнить, что селективность дозозависима, она снижается с повышением дозы препарата (рис. 1).
В настоящее время клиницисты выделяют три поколения препаратов с бета-блокирующим эффектом.
I поколение — неселективные бета1- и бета2-адреноблокаторы (пропранолол, надолол), которые наряду с отрицательными ино-, хроно- и дромотропными эффектами обладают способностью повышать тонус гладкой мускулатуры бронхов, сосудистой стенки, миометрия, что существенно ограничивает их использование в клинической практике.
II поколение — кардиоселективные бета1-адреноблокаторы (метопролол, бисопролол), благодаря высокой селективности в отношении бета1-адренорецепторов миокарда обладают более благоприятной переносимостью при длительном применении и убедительной доказательной базой долгосрочного прогноза жизни при лечении АГ, ИБС и ХСН.
В середине 1980-х годов на мировом фармацевтическом рынке появились бета-адреноблокаторы III поколения с низкой селективностью к бета1, 2-адренорецепторам, но с сочетанной блокадой альфа-адренорецепторов.
Препараты III поколения — целипролол, буциндолол, карведилол (его дженерический аналог с брендовым названием Карведигамма®) обладают дополнительными вазодилятирующими свойствами за счет блокады альфа-адренорецепторов, без внутренней симпатомиметической активности.
В 1982–1983 годах в научной медицинской литературе появились первые сообщения о клиническом опыте применения карведилола при лечении ССЗ.
Ряд авторов выявили протективное действие бета-адреноблокаторов III поколения на клеточные мембраны. Это объясняется, во-первых, ингибированием процессов перекисного окисления липидов (ПОЛ) мембран и антиоксидантным действием бета-блокаторов и, во-вторых, снижением влияния катехоламинов на бета-рецепторы. Некоторые авторы связывают мембранстабилизирующее действие бета-блокаторов с изменением проводимости натрия через них и ингибированием ПОЛ.
Указанные дополнительные свойства расширяют перспективы применения данных лекарственных средств, поскольку нивелируют характерное для первых двух поколений отрицательное влияние на сократительную функцию миокарда, углеводный и липидный обмен и в то же время обеспечивают улучшение перфузии тканей, позитивное влияние на показатели гемостаза и уровень оксидативных процессов в организме.
Карведилол метаболизируется в печени (глюкуронирование и сульфатация) с помощью ферментной системы цитохрома Р450, с использованием семейства ферментов — CYP2D6 и CYP2C9. Антиоксидантное действие карведилола и его метаболитов обусловлено наличием в молекулах карбазольной группы (рис. 2).
Метаболиты карведилола — SB 211475, SB 209995 угнетают ПОЛ в 40–100 раз активнее, чем сам препарат, а витамин Е — примерно в 1000 раз.
Применение карведилола (Карведигаммы®) при лечении ИБС
Согласно результатам целого ряда завершенных многоцентровых исследований, бета-адреноблокаторы оказывают выраженный антиишемический эффект. Необходимо отметить, что антиишемическая активность бета-адреноблокаторов соизмерима с активностью антагонистов кальция и нитратов, но, в отличие от этих групп, бета-адреноблокаторы не только улучшают качество, но и увеличивают продолжительность жизни пациентов с ИБС. Согласно результатам метаанализа 27 многоцентровых исследований, в которых приняло участие более 27 тыс. человек, селективные бета-адреноблокаторы без внутренней симпатомиметической активности у больных с острым коронарным синдромом в анамнезе снижают риск развития повторного ИМ и смертность от инфаркта на 20% [1].
Однако не только селективные бета-адреноблокаторы положительно влияют на характер течения и прогноз у пациентов с ИБС. Неселективный бета-адреноблокатор карведилол также продемонстрировал очень хорошую эффективность у больных со стабильной стенокардией. Высокая антиишемическая эффективность данного препарата объясняется наличием дополнительной альфа1-блокирующей активности, способствующей дилятации коронарных сосудов и коллатералей постстенотической области, а значит — улучшению перфузии миокарда. Кроме того, карведилол обладает доказанным антиоксидантным эффектом, связанным с захватом свободных радикалов, высвобождающихся в период ишемии, что обусловливает его дополнительное кардиопротекторное действие. Одновременно карведилол блокирует апоптоз (программируемая смерть) кардиомиоцитов в зоне ишемии, сохраняя объем функционирующего миокарда. Как было показано, метаболит карведилола (ВМ 910228) обладает меньшим бета-блокирующим эффектом, но является активным антиоксидантом, блокируя перекисное окисление липидов, «отлавливая» активные свободные радикалы OH–. Этот дериват сохраняет инотропный ответ кардиомиоцитов на Ca++, внутриклеточная концентрация которого в кардиомиоците регулируется Ca++-насосом саркоплазматического ретикулума. Поэтому карведилол оказывается более эффективным в лечении ишемии миокарда через ингибирование повреждающего действия свободных радикалов на липиды мембран субклеточных структур кардиомиоцитов [2].
Благодаря этим уникальным фармакологическим свойствам, карведилол может превосходить традиционные бета1-селективные адреноблокаторы в плане улучшения перфузии миокарда и способствовать сохранению систолической функции у больных ИБС. Как показано Das Gupta et al., у больных с дисфункцией ЛЖ и сердечной недостаточностью, развившейся вследствие ИБС, монотерапия карведилолом снижала давление наполнения, а также увеличивала фракцию выброса (ФВ) ЛЖ и улучшала показатели гемодинамики, при этом не сопровождаясь развитием брадикардии [3].
Согласно результатам клинических исследований у больных хронической стабильной стенокардией, карведилол снижает ЧСС в покое и при физической нагрузке, а также увеличивает ФВ в покое. Сравнительное исследование карведилола и верапамила, в котором принимало участие 313 пациентов, показало, что, по сравнению с верапамилом, карведилол в большей степени уменьшает ЧСС, систолическое АД и произведение ЧСС ´ АД при максимально переносимой физической нагрузке. Более того, карведилол обладает более благоприятным профилем переносимости [4]. Важно, что карведилол, по-видимому, более эффективен при лечении стенокардии, чем обычные бета1-адреноблокаторы. Так, в ходе 3-месячного рандомизированного многоцентрового двойного слепого исследования карведилол напрямую сравнивали с метопрололом у 364 пациентов со стабильной хронической стенокардией. Они принимали карведилол по 25–50 мг два раза в сутки или метопролол по 50–100 мг два раза в сутки [5]. В то время как оба препарата продемонстрировали хорошее антиангинальное и противоишемическое действие, карведилол более значительно увеличивал время до депрессии сегмента ST на 1 мм при физической нагрузке, чем метопролол. Переносимость карведилола была очень хорошей, и, что важно, при увеличении дозы карведилола не произошло заметных изменений типов нежелательных явлений.
Примечательно, что карведилол, не обладающий, в отличие от других бета-адреноблокаторов, кардиодепрессивным действием, улучшает качество и продолжительность жизни пациентов с острым ИМ (CHAPS) [6] и постинфарктной ишемической дисфункцией ЛЖ (CAPRICORN) [7]. Многообещающие данные были получены в ходе исследования Carvedilol Heart Attack Pilot Study (CHAPS) — пилотного исследования влияния карведилола на развитие ИМ. Это было первое рандомизированное исследование, в котором сравнивали карведилол с плацебо у 151 больного после острого ИМ. Лечение начинали в течение 24 часов с момента появления болей в грудной клетке, а дозу препарата увеличивали до 25 мг два раза в сутки. Главными конечными точками исследования были функция ЛЖ и безопасность препарата. Больных наблюдали в течение 6 месяцев с момента начала заболевания. Согласно полученным данным, частота развития серьезных кардиальных событий уменьшилась на 49%.
Полученные в ходе исследования CHAPS эхографические данные 49 пациентов со сниженной ФВ ЛЖ (< 45%) показали, что карведилол значительно улучшает восстановление функции ЛЖ после острого ИМ, как через 7 дней, так и через 3 месяца. При лечении карведилолом масса ЛЖ достоверно уменьшалась, в то время как у пациентов, принимавших плацебо, она увеличивалась (р = 0,02). Толщина стенки ЛЖ также значительно уменьшилась (р = 0,01). Карведилол способствовал сохранению геометрии ЛЖ, предупреждая изменение индекса сферичности, эхографического индекса глобального ремоделирования и размера ЛЖ. Следует подчеркнуть, что эти результаты были получены при монотерапии карведилолом. Кроме того, исследования с таллием-201 в этой же группе пациентов показали, что только карведилол значимо снижает частоту событий при наличии признаков обратимой ишемии. Собранные в ходе вышеописанных исследований данные убедительно доказывают наличие явных преимуществ карведилола перед традиционными бета-адреноблокаторами, что обусловлено его фармакологическими свойствами.
Хорошая переносимость и антиремоделирующий эффект карведилола указывают на то, что данный препарат способен снизить риск смерти у пациентов, перенесших ИМ. Крупномасштабное исследование CAPRICORN (CArvedilol Post InfaRct Survival COntRol in Left Ventricular DysfunctioN) было посвящено изучению влияния карведилола на выживаемость при дисфункции ЛЖ после ИМ. Исследование CAPRICORN впервые продемонстрировало, что карведилол в комбинации с ингибиторами АПФ способен снизить общую и сердечно-сосудистую смертность, а также частоту повторных не смертельных инфарктов в этой группе пациентов. Новые доказательства того, что карведилол является, по меньшей мере, столь же, если не более эффективным в отношении обратного развития ремоделирования у пациентов с ХСН и ИБС, подтверждают необходимость более раннего назначения карведилола при ишемии миокарда. Кроме того, особого внимания заслуживает действие препарата на «спящий» (гибернирующий) миокард [8].
Таким образом, все эти данные позволяют рекомендовать применение карведилола для лечения больных с ИБС.
Карведилол в лечении АГ
Ведущая роль нарушения нейрогуморальной регуляции в патогенезе АГ сегодня не вызывает сомнений. Оба основных патогенетических механизма гипертонии — увеличение сердечного выброса и повышение периферического сосудистого сопротивления — контролируются симпатической нервной системой. Поэтому бета-адреноблокаторы и диуретики долгие годы были стандартом гипотензивной терапии.
В рекомендациях JNC-VI бета-адреноблокаторы рассматривались в качестве препаратов первого ряда при неосложненных формах гипертонической болезни, так как в контролируемых клинических исследованиях была доказана только способность бета-адреноблокаторов и диуретиков снижать сердечно-сосудистую заболеваемость и смертность [9, 10]. Согласно результатам метаанализа проведенных ранее многоцентровых исследований бета-адреноблокаторы не оправдали ожиданий в отношении эффективности снижения риска развития инсультов. Отрицательные метаболические эффекты и особенности влияния на гемодинамику не позволили им также занять ведущее место в процессе уменьшения ремоделирования миокарда и сосудов [11]. Однако следует отметить, что включенные в метаанализ исследования касались только представителей второго поколения бета-адреноблокаторов — атенолола, метопролола и не включали данных о новых препаратах класса. С появлением новых представителей этой группы была в значительной степени нивелирована опасность их применения у больных с нарушением сердечной проводимости, сахарным диабетом, нарушениями липидного обмена, почечной патологией. Применение именно этих препаратов позволяет расширить область применения бета-адреноблокаторов при АГ.
Наиболее перспективными при лечении пациентов с АГ из всех представителей класса бета-адреноблокаторов являются препараты с вазодилятирующими свойствами, одним из которых является карведилол.
Карведилол обладает длительным гипотензивным действием. Согласно результатам метаанализа гипотензивного действия карведилола более чем у 2,5 тыс. больных АГ, АД снижается уже после однократного приема препарата, однако максимальный гипотензивный эффект развивается через 1–2 недели [12]. В этом же исследовании приводятся данные об эффективности препарата в разных возрастных группах: достоверных различий в уровне АД на фоне 4-недельного приема карведилола в дозе 25 или 50 мг у лиц в возрасте моложе или старше 60 лет не установлено.
Важным является тот факт, что в отличие от неселективных и некоторых бета1-селективных адреноблокаторов, бета-блокаторы с вазодилятирующей активностью не только не снижают чувствительность тканей к инсулину, но даже немного усиливают ее [13]. Возможность карведилола уменьшать инсулинорезистентность — эффект, который в большой степени обусловлен бета1-адреноблокирующей активностью, которая повышает активность липопротеинлипазы в мышцах, что в свою очередь усиливает клиренс липидов и улучшает периферическую перфузию, которая способствует более активному поглощению глюкозы тканями. Сравнение эффектов различных бета-блокаторов подтверждает эту концепцию. Так, в рандомизированном исследовании назначали карведилол и атенолол больным сахарным диабетом 2-го типа и АГ [14]. Было показано, что после 24-недельной терапии уровни гликемии натощак и инсулина при лечении карведилолом снизились, а при лечении атенололом повысились. Кроме того, карведилол оказывал более выраженное положительное влияние на чувствительность к инсулину (р = 0,02), уровни липопротеидов высокой плотности (ЛПВП) (р = 0,04), триглицеридов (р = 0,01) и перекисное окисление липидов (р = 0,04).
Как известно, дислипидемия является одним из четырех основных факторов риска развития ССЗ. Особенно неблагоприятно сочетание ее с АГ. Однако прием некоторых бета-адреноблокаторов также может приводить к нежелательным изменениям уровня липидов крови [15]. Как уже упоминалось, карведилол не оказывает негативного влияния на сывороточный уровень липидов [14]. В многоцентровом слепом рандомизированном исследовании изучено влияние карведилола на профиль липидов у больных мягкой и умеренной АГ и дислипопротеинемией [16]. В исследование были включены 250 пациентов, которые методом рандомизации были распределены в группы лечения карведилолом в дозе 25–50 мг/сут или ингибитором АПФ каптоприлом в дозе 25–50 мг/сут. Выбор каптоприла для сравнения определялся тем, что он либо не оказывает эффекта, либо положительно влияет на обмен липидов. Длительность лечения составила 6 месяцев. В обеих сравниваемых группах отмечена положительная динамика: оба препарата сопоставимо улучшали липидный профиль. Благоприятный эффект карведилола на обмен липидов, скорее всего, связан с его альфа-адреноблокирующей активностью, поскольку было показано, что блокада бета1-адренорецепторов вызывает вазодилятацию, вследствие чего улучшается гемодинамика, а также уменьшается выраженность дислипидемии [17].
Помимо блокады бета1-, бета2- и альфа1-рецепторов, карведилол обладает также дополнительными антиоксидантными и антипролиферативными свойствами [18, 19], что важно учитывать в плане воздействия на факторы риска ССЗ и обеспечения защиты органов-мишеней у больных АГ.
Таким образом, метаболическая нейтральность препарата допускает его широкое применение у пациентов с АГ и сахарным диабетом, а также у пациентов с МС, что особенно важно при лечении лиц пожилого возраста [20].
Альфа-блокирующее и антиоксидантное действия карведилола, обеспечивающие периферическую и коронарную вазодилятацию, способствуют влиянию препарата на параметры центральной и периферической гемодинамики, доказано положительное влияние препарата на фракцию выброса и ударный объем ЛЖ, что особенно важно при лечении больных АГ с ишемической и неишемической сердечной недостаточностью [21].
Как известно, АГ часто сочетается с поражением почек и при выборе гипотензивной терапии необходимо учитывать возможные неблагоприятные воздействия медикаментозного препарата на функциональное состояние почек. Применение бета-адреноблокаторов в большинстве случаев может быть сопряжено с уменьшением почечного кровотока и скорости клубочковой фильтрации. Наличие у карведилола бета-адреноблокирующего эффекта и обеспечение вазодилятации, как было показано, положительно влияет на функцию почек [22, 23].
Таким образом, карведилол сочетает в себе бета-блокирующие и сосудорасширяющие свойства, что обеспечивает его эффективность в лечении АГ.
Бета-адреноблокаторы в лечении ХСН
ХСН — одно из наиболее неблагоприятных патологических состояний, существенно ухудшающих качество и продолжительность жизни больных. Распространенность сердечной недостаточности очень велика, это самый частый диагноз у пациентов старше 65 лет. В настоящее время сохраняется устойчивая тенденция роста количества больных с ХСН, что связывают с повышением выживаемости при других ССЗ, в первую очередь, при острых формах ИБС. По данным ВОЗ, 5-летняя выживаемость больных с ХСН не превышает 30–50%. В группе пациентов, перенесших ИМ, до 50% умирает в течение первого года после развития недостаточности кровообращения, связанной с коронарным событием. Поэтому наиболее важной задачей оптимизации терапии по поводу ХСН является поиск препаратов, увеличивающих продолжительность жизни больных с ХСН.
Одним из наиболее перспективных классов препаратов, эффективных как для профилактики развития, так и для лечения ХСН, признаны бета-адреноблокаторы [6, 24], поскольку активация симпатоадреналовой системы является одним из ведущих патогенетических механизмов развития ХСН. Компенсаторная, на начальных этапах заболевания, гиперсимпатикотония в последующем становится основной причиной ремоделирования миокарда, возрастания триггерной активности кардиомиоцитов, повышения периферического сосудистого сопротивления и нарушения перфузии органов-мишеней.
История применения бета-адреноблокаторов при терапии больных с ХСН насчитывает 25 лет [25]. Крупномасштабные международные исследования CIBIS-II, MERIT-HF, US Carvedilol Heart Failure Trials Program, COPERNICUS утвердили в качестве препаратов первого ряда бета-адреноблокаторы для лечения пациентов с ХСН [26, 27, 28], подтвердив их безопасность и эффективность при лечении таких больных (.). Метаанализ результатов основных исследований по изучению эффективности бета-адреноблокаторов у больных с ХСН показал, что дополнительное назначение к ингибиторам АПФ бета-адреноблокаторов, наряду с улучшением гемодинамических показателей и самочувствия пациентов, способствует улучшению течения ХСН, показателей качества жизни, снижает частоту госпитализации — на 41% и риск смерти больных ХСН на 37% [29].
Согласно Европейским рекомендациям 2005 года применение бета-адреноблокаторов рекомендовано у всех пациентов с ХСН в дополнение к терапии ингибиторами АПФ и симптоматическому лечению [30]. Причем согласно результатам мультицентрового исследования COMET, которое явилось первым прямым сравнительным испытанием влияния карведилола и селективного бета-адреноблокатора II поколения метопролола в дозах, обеспечивающих эквивалентный антиадренергический эффект, на выживаемость при среднем сроке наблюдения 58 месяцев, карведилол на 17% эффективнее метопролола снижал риск смерти [20].
Это обеспечило средний «выигрыш» в расчетной продолжительности жизни на 1,4 года в группе карведилола при максимальной продолжительности наблюдения пациентов до 7 лет. Указанное преимущество карведилола обусловлено отсутствием кардиоселективности и наличием альфа-блокирующего эффекта, что способствует уменьшению гипертрофического ответа миокарда на норадреналин, снижению периферического сосудистого сопротивления, подавлению выработки ренина почками. Кроме того, в клинических испытаниях у больных с ХСН доказано антиоксидантное, противовоспалительное (снижение уровней ФНО-альфа (фактора некроза опухоли), интерлейкинов 6–8, С-пептида), антипролиферативное и антиапоптотическое действие препарата, что также обусловливает его значительные преимущества при лечении данного контингента больных не только среди препаратов своей, но и других групп [27].
На рис. 3 представлена схема титрования доз карведилола при различных патологиях сердечно-сосудистой системы.
Таким образом, карведилол, обладая бета- и альфа-адреноблокирующим эффектом с антиоксидантной, противовоспалительной, антапоптической активностью, стоит в ряду самых эффективных препаратов из класса бета-адреноблокаторов, применяемых в настоящее время при лечении ССЗ и МС.
Литература
- Devereaux P.?J., Scott Beattie W., Choi P.?T. L., Badner N.?H., Guyatt G.?H., Villar J.?C. et al. How strong is the evidence for the use of perioperative b-blockers in non-cardiac surgery? Systematic review and meta-analysis of randomised controlled trials // BMJ. 2005; 331: 313–321.
- Feuerstein R., Yue T.?L. A potent antioxidant, SB209995, inhibits oxy gen-radical-mediated lipid peroxidation and cytotoxicity // Pharmacology. 1994; 48: 385–91.
- Das Gupta P., Broadhurst P., Raftery E.?B. et al. Value of carvedilol in congestive heart failure secondary to coronary artery disease // Am J Cardiol. 1990; 66: 1118–1123.
- Hauf-Zachariou U., Blackwood R.?A., Gunawardena K.?A. et al. Carvedilol versus verapamil in chronic stable angina: a multicentre trial // Eur J Clin Pharmacol. 1997; 52: 95–100.
- Van der Does R., Hauf-Zachariou U., Pfarr E. et al. Comparison of safety and efficacy of carvedilol and metoprolol in stable angina pec toris // Am J Cardiol 1999; 83: 643–649.
- Maggioni A. Review of the new ESC quidelines for the pharmacological management of chronic heart failure // Eur. Heart J. 2005; 7: J15–J21.
- Dargie H.?J. Effect of carvedilol on outcome after myocardial infarc tion in patients with left-ventricular dysfunction: the CAPRICORN randomised trial // Lancet. 2001; 357: 1385–1390.
- Khattar R.?S., Senior R., Soman P. et al. Regression of left ventricular remodeling in chronic heart failure: Comparative and combined effects of captopril and carvedilol // Am Heart J. 2001; 142: 704–713.
- Dahlof B., Lindholm L., Hansson L. et al. Morbility and mortality in the Swedish Trial in Old Patients with Hypertension (STOP-hypertension) // The Lancet, 1991; 338: 1281–1285.
- Rangno R.?E., Langlois S., Lutterodt A. Metoprolol withdrawal phenomena: mechanism and prevention // Clin. Pharmacol. Ther. 1982; 31: 8–15.
- Lindholm L., Carlsberg B., Samuelsson O. Shoued b-blockers remain first choice in the treatment of primary hypertension? A meta-analysis // Lancet. 2005; 366: 1545–1553.
- Steinen U. The once-daily dose regimen of carvedilol: a meta-analysis approach //J Cardiovasc Pharmacol. 1992; 19 (Suppl. 1): S128–S133.
- Jacob S. et al. Antihypertensive therapy and insulin sensitivity: do we have to redefine the role of beta-blocking agents? // Am J Hypertens. 1998.
- Giugliano D. et al. Metabolic and cardiovascular effects of carvedilol and atenolol in non-insulin-dependent diabetes mellitus and hypertention. A randomized, controlled trial // Ann Intern Med. 1997; 126: 955–959.
- Kannel W.?B. et al. Initial drug therapy for hypertensive patients with dyslipidaemia // Am Heart J. 188: 1012–1021.
- Hauf-Zahariou U. et al. A double-blind comparison of the effects of carvedilol and captopril on serum lipid concentration in patients with mild to moderate essential hypertention and dislipidaemia // Eur J Clin Pharmacol. 1993; 45: 95–100.
- Fajaro N. et al. Long-term alfa 1-adrenergic blockade attenuates diet-indused dyslipidaemia and hyperinsulinemia in the rat // J Cardiovasc Pharmacol. 1998; 32: 913–919.
- Yue T.?L. et al. SB 211475, a metabolite of carvedilol, a novel antihypertensive agent, is a potent antioxidant // Eur J Pharmacol. 1994; 251: 237–243.
- Ohlsten E.?H. et al. Carvedilol, a cardiovascular drug, prevents vascular smooth muscule cell proliferation, migration and neointimal formation following vascular injury // Proc Natl Acad Sci USA. 1993; 90: 6189–6193.
- Poole-Wilson P.?A. et al. Comparison of carvedilol and metoprolol on clinical outcomes in patients with chronic heart failure in the carvedilol or metoprolol European trial (COMET): randomized controlled trial // Lancet. 2003; 362 (9377): 7–13.
- ner G. Vasodilatory action of carvedilol //J Cardiovasc Pharmacol. 1992; 19 (Suppl. 1): S5–S11.
- Agrawal B. et al. Effect of antihypertensive treatment on qualitative estimates of microalbuminuria // J Hum Hypertens. 1996; 10: 551–555.
- Marchi F. et al. Efficacy of carvedilol in mild to moderate essential hypertention and effects on microalbuminuria: multicenter, randomized.
- Tendera M. Epidemiology, treatment and quidelines for the treatment of heart failure in Europe // Eur. Heart J., 2005; 7: J5–J10.
- Waagstein F., Caidahl K., Wallentin I. et al. Long-term beta-blockade in dilated cardiomyopathy: effects of short-term and long-term metoprolol followed by withdrawal and readministration of metoprolol // Circulation 1989; 80: 551–563.
- The International Steering Commitee on behalf of the MERIT-HF Studi Group // Am. J.?Cardiol., 1997; 80 (suppl. 9 B): 54J–548J.
- Packer M., Bristow M.?R., Cohn J.?N. et al. The effect of carvedilol on morbidity and mortality in patients with chronic heart failure. US Carvedilol Heart Failure Study Group // N Engl J Med. 1996; 334: 1349.
- COPERNICUS investigators resource. F.?Hoffman-La Roche Ltd, Basel, Switzerland, 2000.
- Does R., Hauf-Zachariou U., Praff E. et al. Comparison of safety and efficacy of carvedilol and metoprolol in stable angina pectoris // Am. J.?Cardiol. 1999; 83: 643–649.
- Randomized, pacebo-controlled trial of carvedilol in patients with congestive heart failure due to ischemic heart disease. Australia/New Zealand Heart Failure Research CollaborativeGroup // Lancet, 1997; 349: 375–380.
А. М. Шилов*, доктор медицинских наук, профессор М. В. Мельник*, доктор медицинских наук, профессор А. Ш. Авшалумов**
*ММА им. И. М. Сеченова, Москва **Клиника Московского института кибернетической медицины, Москва
Контактная информация об авторах для переписки
Фармакокинетика
Большинство препаратов группы β 2 -адренорецепторов хорошо всасываются при пероральном применении, но биодоступность при пероральном применении адреностимуляторов низкая в связи с наличием в метаболизме этих препаратов эффекта первого прохождения через печень. Основным путем применения препаратов группы является ингаляционный, при котором при различных фомах применения (через небулайзер, вдыхание сухого порошка или аэрозоля) биодоступность препаратов составляет от 5 до 38%. Исключение составляет препарат с ультратривалою действием индакатерол, биодоступность которого при ингаляционном применении составляет 43%. Часть препаратов группы применяется также парентерально, преимущественно внутривенно, при этом биодоступность препаратов составляет 100%. Препараты группы плохо связываются с белками плазмы крови (в среднем 14-25%). Большинство препаратов из группы β 2 -адренорецепторов создают высокие концентрации в большинстве тканей организма, проникают через плацентарный барьер и выделяются в грудное молоко. Метаболизируются препараты группы преимущественно в печени, а также в других тканях организма под действием ферментов МАО и катехол-О-метилтрансферазы. Период полувыведения препаратов группы варьирует от 2 минут в изопреналина до 24 часов в индакатеролу. Выводятся β 2 -адреностимуляторы из организма как с мочой, так и с калом, частично в виде неактивных метаболитов, частично в неизмененном виде.
Показания к применению
Основными показаниями к применению β 2 -адренорецепторов является бронхообструктивные заболевания дыхательной системы (бронхиальная астма, хронические обструктивные заболевания легких, эмфизема легких), при которых агонисты β 2 -адренорецепторов применяются преимущественно ингаляционно, часто в сочетании с ингаляционными ГКС или м холинолитиками. В случае бронхообструктивных заболеваний адреностимуляторы могут применяться в небулайзер, дозированных аэрозолях и в виде дозированных сухих порошков. Сальбутамол, фенотерол, орципреналин, гексопреналин и изопреналин применяются также в акушерской практике преимущественно внутривенно при истмико-цервикальной недостаточности, при угрозе преждевременных родов. Кленбутерол применяется также для быстрого наращивания мышечной массы культуристами или для поддержания формы тела и похудения совместно с посещением тренажерных залов.
Основы лечения препаратами β-адреномиметиков
β-Адреностимуляторы относят к категории средств рецептурного отпуска – препараты отпускаются из аптек только по рецепту врача.
β1-Адреномиметик добутамин вводят внутривенно капельно в условиях стационара под постоянным контролем врача. Эффект препарата развивается через 1-2 минуты, максимальное действие отмечается через 10 минут.
Для лечения бронхиальной астмы и хронической обструктивной болезни легких препараты β2-адреномиметиков используют ингаляционно.
Для профилактики преждевременных родов β2-адреностимуляторы применяют в виде внутривенных инъекций, инфузий или используют в виде таблеток перорально (внутрь).
Мирабегрон используют в виде таблеток перорально 1 раз в сутки.
Побочное действие
При применении селективных бета-2-адренорецепторов чаще всего наблюдаются тремор рук и тахикардия (чаще при применении сальбутамола). При применении неселективных β 2 -адренорецепторов чаще наблюдаются побочные эффекты со стороны сердечно-сосудистой системы, вызванные стимуляцией адренорецепторов миокарда и кровеносных сосудов — аритмии (в том числе фибрилляция предсердий, суправентрикулярная тахикардия и экстрасистолия), артериальная гипертензия или гипотензия, явления ишемии миокарда. При длительном неконтролируемом применении β 2 -адренорецепторов может наблюдаться «синдром рикошета» — парадоксальный бронхоспазм при повышении дозы препарата, а также повышение толерантности к препаратам группы. Среди других побочных эффектов чаще наблюдаются аллергические реакции в виде крапивницы или высыпаний на коже, тошнота, рвота, стоматит и фарингит (вследствие раздражения слизистых оболочек при ингаляционном применении), возбуждение, судороги, метаболические нарушения (гипергликемия, гипокалиемия, гиперлипидемия , лактататацидоз).
Противопоказания
Бета-2-адреностимуляторы противопоказаны при повышенной чувствительности к препаратам группы, тахиаритмиях, ишемической болезни сердца,, декомпенсированном тиреотоксикозе и сахарном диабете, выраженной сердечной недостаточности, некорригированной артериальной гипертензии. С осторожностью применяются препараты группы при печеночной и почечной недостаточности, эпилепсии. Β 2 -адреностимуляторы не применяется одновременно с бета-блокаторами в связи с антагонизмом их действия, а также с другими адреностимуляторами в связи с увеличением риска побочных эффектов. Препараты группы не применяется с сердечными гликозидами в связи с увеличением риска интоксикации гликозидами, трициклическими антидепрессантами и ингибиторами МАО в связи с риском развития гипотонии.
Запрет использования у спортсменов
Некоторые препараты из группы бета-2-адренорецепторов, а именно сальбутамол, сальметерол и формотерол, запрещен для использования спортсменами во время соревнований по решению Всемирного антидопингового агентства как стимуляторы дыхательной системы, а кленбутерол также и как препарат с анаболическим действием., И выявление этих препаратов в организме спортсменов во время соревнований может служить причиной их дисквалификации. Но часть спортсменов, страдающих бронхиальной астмой, имеют разрешение на использование сальбутамола, формотерола и сальметерола (но не кленбутерола) от Всемирного антидопингового агентства.
Центр экспертизы безопасности лекарственных средств обращает внимание специалистов на появление новой информации, касающейся безопасности бета – адреномиметиков длительного действия.
Бета–адреномиметики длительного действия (БАМДД) – группа лекарственных препаратов, предназначенных для лечения бронхиальной астмы и хронической обструктивной болезни легких (ХОБЛ).
В ходе пострегистрационных клинических исследований, проведенных с целью определения эффективности и безопасности бета-адреномиметиков длительного действия в терапии заболеваний легких, появилась информация об ухудшении течения бронхиальной астмы у детей и взрослых, вплоть до развития летального исхода от осложнений бронхиальной астмы.
В связи с этим Агентство по контролю лекарственных препаратов и пищевых продуктов США (US FDA) приняло решение о необходимости внесения соответствующих предостережений в инструкцию по медицинскому применению всех представителей фармакотерапевтической группы бета-адреномиметиков длительного действия (МНН Салметерол, Формотерол, Арформотерол). Предостережения и дополнения, коснувшиеся разделов «Показания к применению» и «Противопоказания», включали следующую информацию:
- Монотерапия БАМДД с целью длительного лечения бронхиальной астмы противопоказана;
- Бета-адреномиметики длительного действия не рекомендуется назначать пациентам, у которых бронхиальная астма контролируется низкими или средними дозами кортикостероидов;
- Бета-адреномиметики длительного действия разрешены в качестве дополнительной терапии тогда, когда не удается достигнуть необходимого результата при проведении базисной терапии (например, кортикостероидами). При достижении необходимого контроля при совместной терапии БАМДД и ингаляционными кортикостероидами, необходимо постепенно снижать дозу адреномиметиков вплоть до их полной отмены.
- Детям и подросткам для более удобного контролируемого введения препаратов рекомендуется назначать комбинированные ингаляционные препараты, имеющие в своем составе БАМДД и кортикостероиды.
Кроме того, врачам не рекомендуется назначать препараты длительного действия пациентам с бронхиальной астмой, выявленной впервые.
С целью профилактики развития астматических приступов у таких больных целесообразно применять адреномиметики короткого действия (например, Сальбутамол). При соблюдении рекомендаций, предложенных выше, польза от терапии бронхиальной астмы бета-адреномиметиками длительного действия оценивается выше, чем возможный риск развития серьезных осложнений данного заболевания.
В таблице №1 дается перечень зарегистрированных в РФ бета-адреномиметиков длительного действия (БАМДД) и их комбинаций с глюкокортикостероидами (ГКС).
Табл. № 1
| Торговое наименование | БАМДД | ГКС |
| Серобид-Ципла | Салметерол | |
| Бекситрол | Салметерол | |
| Сальметер | Салметерол | |
| Серевент | Салметерол | |
| Серетид Мультидиск | Салметерол | Флутиказон |
| Серетид | Салметерол | Флутиказон |
| Тевакомб | Салметерол | Флутиказон |
| Тевакомб Мультихалер | Салметерол | Флутиказон |
| Серофло | Салметерол | Флутиказон |
| Фортулин Новолайзер | Формотерол | |
| Теватераль | Формотерол | |
| Форадил | Формотерол | |
| Формоспир | Формотерол | |
| Форлонг Легкое Дыхание | Формотерол | |
| Форадил Cертихалер | Формотерол | |
| Атимос | Формотерол | |
| Форадил | Формотерол | |
| Оксис Турбухалер | Формотерол | |
| Симбикорт | Формотерол | Будесонид |
| Симбикорт Турбухалер | Формотерол | Будесонид |
| Форакорт | Формотерол | Будесонид |
| Комбитеваль | Формотерол | Будесонид |
| Комбитеваль Мультихалер | Формотерол | Будесонид |
| Форацип | Формотерол | Будесонид |