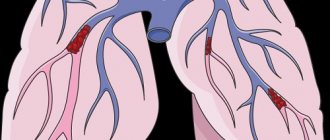
Тромбоэмболия лёгочной артерии (ТЭЛА) — это серьезное, потенциально опасное для жизни состояние. Тромбоэмболия лёгочной артерии происходит из-за закупорки кровеносных сосудов тромботическими массами в лёгких. Тромбоэмболия легочной артерии (ТЭЛА) может вызывать такие симптомы, как боль в груди и (или) одышка. Также в отдельных случаях у ТЭЛА может не быть симптомов вовсе, и её трудно обнаружить без специализированного обследования. Массивная тромбоэмболия лёгочной артерии может вызвать коллапс и смерть. ТЭЛА обычно возникает из-за формирования тромбоза в нижней конечности — тромбоза глубоких вен (ТГВ).
Тромбоэмболия лёгочной артерии (ТЭЛА)
Своевременное лечение важно и может спасти жизнь. Беременность, различные заболевания и лекарства, неподвижность и серьезное хирургическое вмешательство — все это увеличивает риск ТЭЛА. Антикоагулянтная терапия, включающая препараты гепарина, прямые оральные антикоагулянты или варфарин, является обычным лечением ТЭЛА.
Общие сведения
Тромбоз — это образование сгустка крови в кровеносном сосуде, который нарушает кровоток. Опасность его состоит в том, что имеется опасность перемещения тромба или его фрагмента по кровотоку — возникает эмболия и закупорка другого сосуда. Например, снабжающего головной мозг или сердце. Часто встречается эмболия легочной артерии, что приводит к тяжелым нарушениям работы органа или r смертельному исходу.
Что такое ТЭЛА в медицине? Тромбоэмболия легочной артерии — это острая окклюзия (закупорка) ствола легочной артерии или ее ветвей (главных, долевых или сегментарных). Окклюзия возникает чаще из-за эмболизации тромба из правой половины сердца или вен нижних конечностей. Встречаемость данного заболевания увеличивается с возрастом и возраст таких больных составляет 62 года.
Тромбоз легочной артерии является неотложным состояниям в кардиореаниматологии и часто является причиной смерти больного. Тяжелыми больными с высоким риском ТЭЛА и смерти являются больные с нарушениями сердечного ритма, онкопатологией и тромбозом вен нижних конечностей. Диагностика часто вызывает затруднения, поэтому заболевание часто не распознается. Ранняя диагностика и начало интенсивного лечения имеют важное значение в прогнозе данного заболевания. Код ТЭЛА по МКБ-10 — I 26.
Прогноз и профилактика
Источник: Mark Stebnicki: Pexels При своевременном выявлении патологии и назначении комплексной терапии прогноз благоприятный. Однако существует сразу несколько факторов риска:
- преклонный возраст;
- постельный режим;
- наличие опухолевых новообразований;
- случаи тромбоза в анамнезе.
Все эти факторы ухудшают прогноз выживаемости. При заболеваниях сердечно-сосудистой и дыхательной системы примерно треть всех случаев ТЭЛА заканчиваются летально.
Профилактические мероприятия:
- регулярное ультразвуковое исследование вен нижних конечностей;
- отказ от вредных привычек (особенно важно отказаться от курения);
- максимальное сокращение вынужденного постельного режима при различных заболеваниях и послеоперационном периоде;
- ношение компрессионного белья.
Отдельно следует коснуться вопросов питания. Важно свести к минимуму употребление продуктов, богатых витамином К, поскольку он увеличивает свертываемость крови. Сюда относятся молоко и творог, брокколи, цветная и белокачанная капуста, отруби, оливковое масло. Также необходимо уменьшить количество жирной и острой пищи в своем рационе. Рекомендуется отказаться и от продуктов с высоким гликемическим индексом – проще говоря, сладости тоже стоит значительно ограничить.
Следует избегать малоподвижного образа жизни. Подойдет любой вид физической активности: ходьба (не менее получаса в день), бег, плавание, умеренные силовые нагрузки (гантели, тренажеры). При длительных перелетах или переездах важно употреблять не менее 1,5 литров жидкости в день и обеспечить минимальный уровень физической активности: достаточно будет примерно раз в полтора часа просто встать и пройтись в течение хотя бы нескольких минут.
Патогенез
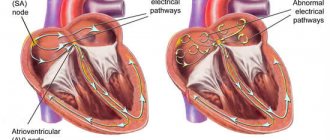
Основное в патогенезе ТЭЛА — окклюзия эмболом легочной артерии и ее ветвей, что приводит к нарушению гемодинамики и газообмена. При окклюзии давление в легочной артерии увеличивается почти на 50% за счет сужения сосудов, связанных с выделением серотонина и тромбоксана А2. Резкое увеличение легочного сопротивления вызывает расширение правого желудочка, растяжение миоцитов и напряжение стенок желудочка. Удлинение времени его сокращения к диастоле вызывает выпячивание перегородки в левый желудочек. Поэтому наполнение левого желудочка затрудняется, снижается сердечный выброс и развивается системная гипотензия.
В миокарде желудочка обнаруживаются массивные инфильтраты, что еще более дестабилизирует гемодинамику. Недостаточность правого желудочка из-за перегрузки давлением является основной причиной смерти. Дыхательная недостаточность также связана с гемодинамическими нарушениями. Снижение сердечного выброса вызывает десатурацию венозной крови. Появление зон пониженного кровотока вызывает несоответствие перфузии и вентиляции. Небольшие эмболы на периферии не влияют на гемодинамику, однако вызывают легочное кровотечение с кровохарканьем, плевритом и плевральным выпотом («инфарктом легкого»).
Классификация ТЭЛА
Классификация Европейского общества кардиологов 2008г выделяет:
- ТЭЛА с низким риском.
- Промежуточным.
- Высоким.
Клиническая классификация учитывает калибр легочных артерий и процент вовлечения легочного русла:
- Массивная (прекращение кровотока менее, чем в 50% легочного русла). Имеет большое клиническое значение, поскольку сопровождается шоком или снижением давления, легочной гипертензией. При окклюзии ствола развиваются резко выраженные кардиореспираторные расстройства. В таких условиях правый желудочек не может выполнять функцию насоса и быстро расширяются его полости, развивается недостаточность трехстворчатого клапана. Перегородка между желудочками смещается влево (в сторону левого желудочка), что сопровождается плохим его наполнением в диастолу. Легочная паренхима в связи с прекращением кровотока не кровоснабжается, но вентилируется. В зоне поражения возникает обструкция бронхов, спадаются альвеолы и в них не образуется сурфактант, сто способствует развитию ателектаза (спадания) легких на 1-2 сутки эмболии. Такие гемодинамические нарушения и нарушение функции легких часто влекут смерть больного.
- ТЭЛА мелких ветвей легочной артерии (отмечается прекращение кровотока менее, чем в 30% легочного русла). В данном случае имеет место окклюзия долевых и сегментарных мелких ветвей. Заболевание протекает нетяжело без нарушений гемодинамики и и больным достаточно проведения только антикоагулянтной терапии. Малый круг кровообращения имеет компенсаторные возможности и есть вероятность самостоятельного растворения тромбов при активизации в организме фибринолиза.
- Субмассивная— тромбоэмболия ветвей легочной артерии (прекращение кровотока менее в 30-50% русла). Проявляется правожелудочковой недостаточностью, а в легких образуются геморрагические инфаркты.
Лечение ТЭЛА
Как правило, лечение осуществляется в отделении интенсивной терапии. Причем направляют туда не только пациентов с острой формой ТЭЛА, но и тех, чей диагноз еще окончательно не подтвержден: это делается с учетом высокого риска внезапного начала болезни и стремительного развития жизнеугрожающих осложнений.
Лечение пациентов высокого риска
Чтобы не допустить продолжения образования тромба (у разных пациентов этот процесс занимает от нескольких часов до нескольких дней), необходимо как можно быстрее начать использование быстродействующих прямых антикоагулянтов (гепарин натрия, надропарин кальция).
Поскольку системная гипотензия усугубляет правожелудочковую недостаточность, необходимо применение кардиотонических средств с вазопрессорным действием (допамин, добутамин) — чтобы повысить давление, за счет сосудосуживающего эффекта.
Также проводится тромболитическая терапия (стрептокиназа, урокиназа, альтеплаза). При наличии противопоказаний к тромболизису (ишемический и геморрагический инсульт, кровотечения, опухоль мозга) рекомендуется проведение чрескожной катетерной эмболэктомии. Это малоинвазивная хирургическая манипуляция, в ходе которой тромб вырезается из сосудов при помощи катетера.
Лечение пациентов невысокого риска
Для этой группы пациентов тромболизис не рекомендован – предпочтительным вариантом считается антикоагулянтная терапия (фондапаринукс натрия или гепарин натрия).
Средняя продолжительность курса антикоагулянтной терапии составляет 2-3 месяца. Точные сроки определяет лечащий врач, исходя из общего состояния пациента и гемодинамических показателей.
Пациентам также рекомендуется ношение компрессионного ортопедического белья и пероральный прием антагонистов витамина К (варфарин, аценокумарол).
При беременности применяется низкомолекулярный гепарин, который не проходит через плацентарный барьер, не причиняет вреда плоду и практически не выделяется с грудным молоком. Что касается варфарина, то специалисты сходятся во мнении, что этот препарат для беременных женщин противопоказан, поскольку оказывает негативное влияние на развитие центральной нервной системы будущего ребенка.
Причины ТЭЛА
Рассматривая причины тромбоэмболии легочной артерии, нужно выделить ряд заболеваний и состояний, которые сопровождаются образованием тромбов, являющихся основой эмболии:
- Варикозное расширение вен и флеботромбоз глубоких вен нижних конечностей. Данная патология в 90% вызывает тромбоэмболию. Угрозу представляют флотирующие тромбы, которые свободно располагаются в просвете сосуда и соединены со стенкой вены только одной частью.
- Застойная сердечная недостаточность, перерастяжение правого желудочка, что создает условия для образования в полости правого желудочка тромбов.
- Применение оральных контрацептивов и беременность, которые сопряжены с повышенным риском тромбообразования.
- Антифосфолипидный синдром (аутоиммунная тромботическая васкулопатия), проявляющийся венозными и артериальными тромбозами. Могут поражаться сосуды разного калибра — капилляры и крупные артериальные стволы. Тромбоз глубоких вен нижних конечностей — типичное проявление антифосфолипидного синдрома. Характерными являются повторные эмболии легочных артерий.
- Катетеризация центральных вен.
- Наличие злокачественных заболеваний.
- Проведение химиотерапии.
- Повреждение спинного мозга.
- Вынужденная иммобилизация после операций, во время инсульта, переломов костей таза и конечностей.
- Протезирование тазобедренного сустава.
- Мерцательная аритмия.
- Политравма и обширное хирургическое вмешательство.
- Наследственная предрасположенность к тромбозу (тромбофилии), которая обусловлена мутациями определенных генов, дефицитом антитромбина III, дефицитом протеина С и S.
Рассматривая тромбоз легких, нужно отметить факторы риска этого состояния:
- Повреждение венозного эндотелия.
- Ожирение.
- Возраст.
- Гиперкоагуляция.
- Замедление венозного кровотока.
- Инфекция.
- Гемотрансфузии.
- Мигрень.
- Сочетание нескольких факторов сопровождается высоким риском эмболии тромба.
Венозные тромбоэмболические осложнения
Тромбоэмболия лёгочной артерии (ТЭЛА) является частью группы клинических проблем, вместе известных как венозные тромбоэмболические осложнения (ВТЭ).
Тромбозом является закупорка кровеносного сосуда сгустком крови (тромбом). Эмболии возникают, когда часть или весь тромб смещается от того места, где он формируется. Далее тромботические массы двигаются с током крови, пока не застревают в более узких кровеносных сосудах, в других частях тела. В этом случае тромб называется эмболом. Тромбоз глубоких вен (ТГВ) является причиной венозной тромбоэмболии, в том числе тромбоэмболии лёгочной артерии (ТЭЛА). Тромбоз наиболее часто возникает в венах нижних конечностей.
Симптомы тромбоэмболии легочной артерии (ТЭЛА)
Постановка диагноза на ранних стадиях затруднена, только при остром течении симптомы тромбоза легочной артерии появляются манифестно и внезапно: одышка, боль за грудиной, тахикардия, снижение АД. При этом у больного имеются факторы риска тромбоэмболии — варикозное расширение вен и флеботромбоз.
Артериальная гипотензия и шок указывают на центральную тромбоэмболию. Выраженная острая одышка также развивается при центральной ТЭЛА. При этой же локализации боль в грудной клетке имеет стенокардический характер. Массивная тромбоэмболия сопровождается признаками перегрузки правого желудочка — это выбухание яремных вен на шее и правожелудочковый ритм галопа.
Признаки ТЭЛА при подостром течении мало специфичны. Прогрессирует дыхательная и правожелудочковая недостаточность, развивается инфарктная пневмония и появляется кровохарканье. При рецидивирующем течении возникают повторные приступы одышки, есть признаки пневмонии и периодически возникают обмороки. Если тромбом перекрываются мелкие артерии на периферии, одышка незначительная и преходящая. Только в случае хронической патологии легких или сердечной недостаточности одышка усугубляется. Иногда ТЭЛА протекает бессимптомно.
Клиника зависит от калибра закупоренного сосуда и, соответственно, степени вовлечения сосудистого русла легких. Массивная ТЭЛА (чаще всего тромбоз главной ветви) протекает с явлениями шока или снижения давления на 40 мм рт. ст. в течение короткого времени, которое не связано с аритмией, сепсисом или уменьшением объема крови. Характерны одышка, цианоз, иногда возникают обмороки.
Субмассивная легочная эмболия (обструкция долевых или сегментарных ветвей) проявляется правожелудочковой недостаточностью (набухание вен шеи, бледность, цианоз), но без артериальной гипотензии. У больного развивается одышка, тахикардия, инфаркт легкого (температура, кашель, легочно-плевральная боль, мокрота с прожилками крови). При немассивной признаки правожелудочковой недостаточности отсутствуют, а давление в норме.
Анализы и диагностика ТЭЛА
Инструментальная диагностика данного состояния включает:
- Рентгенография грудной клетки. В легких выявляют дисковидные ателектазы, приподнятый купол диафрагмы или плевральный выпот. Все эти признаки неспецифичны, но исключают различные причины боли и одышки.
- ЭКГ.
- Эхокардиография. Имеет ключевое значение в диагностике, прежде всего у больных с нестабильной гемодинамикой. Это исследование непосредственно выявляет тромбы в правых отделах сердца, и тромбы в крупных артериях легких (ствол и главные ветви). Косвенным признаком ТЭЛА, выявляемым при эхокардиографии, является перегрузка правых камер. Выявляют косвенный признак тромбоза легочной артерии — перегрузку правого желудочка: расширение полости желудочка, необычное движение перегородки между желудочками и D-образную форму левого желудочка.
- УЗИ глубоких вен конечностей.
- Специальный метод исследования — вентиляционно-перфузионная сцинтиграфия. Это безопасное исследование, которое заключается в введении альбуминовых микросфер внутривенно, которые мечены технецием. Альбуминовые микросферы блокируют легочные капилляры и по этому признаку оценивают перфузию легких. Данное исследование дополняют исследованием вентиляции, что повышает специфичность обследования (при тромбозе вентиляция в сегментах легких, в которых плохое кровоснабжение, остается нормальной). То есть, выявляется несоответствие вентиляции и перфузии. Радиоактивное излучение при сцинтиграфии ниже, чем при выполнении КТ-ангиографии. Выполнение только перфузионной сцинтиграфии можно проводить больным с нормальной рентгенограммой.
- КТ-ангиография. Это исследование стало методом выбора диагностики патологии сосудов легких. Можно просматривать легочные артерии до сегментарных ветвей. Специфичность метода составляет 96%. Методика является оптимальной для диагностики у больного, состояние которого стабильно. В другом случае больной не может быть транспортирован из реанимации.
- Легочная ангиография считается золотым стандартом диагностики ТЭЛА. Однако выполняется редко, поскольку появилась менее инвазивное исследование КТ-ангиография. Диагностика основана на выявлении тромба, который дает дефект наполнения ветви легочной артерии или оно полностью отсутствует. Метод позволяет получить снимки периферических легочных артерий и выявить тромбы 1-2 мм в самых мелких артериях. Для исследования вводится контрастное вещество.
ЭКГ признаки ТЭЛА и рентгенографические признаки
Исследования крови:
- D-димер — продукт деградации фибрина. Повышение его в плазме отмечается при остром тромбозе — это объясняется активацией фибринолиза и коагуляции. Нормальный уровень D-димера говорит о том, что диагноз ТЭЛА маловероятен. Также этот показатель неспецифичен, поскольку гиперпродукция фибрина отмечается при воспалении, кровотечении, инфаркте миокарда, аневризме аорты, онкологических процессах, травме, хирургических операциях. Специфичность D-димера при тромбозе уменьшается с возрастом. На этот показатель обращают внимание во время лечения, поскольку повышение его уровня после окончания лечения антикоагулянтами свидетельствует о риске рецидива.
- При тромбоэмболии повышается уровень мозгового натрийуретического пептида, что связано с растяжением правого желудочка. Степень повышения пропорциональна тяжести больного. Однако, повышение данного маркера неспецифично, поскольку может наблюдаться при ишемии миокарда, гипертрофии левого желудочка, сепсисе и тахикардии. Тем не менее, отсутствие значительного повышения свидетельствует о благоприятном прогнозе ТЭЛА.
Диагностика тромбоэмболии
Зачастую диагностировать ТЭЛА бывает очень трудно из-за того, что ее симптоматика сходна со многими другими ССЗ. Поэтому для правильного дифференцирования недуга очень важен опыт врача и достойная техническая оснащенность клиники.
Поговорив с пациентом и проанализировав его жалобы, доктор проводит физический осмотр, измеряет давление и пульс, прослушивает стетоскопом сердце и легкие. Далее назначается лабораторная и инструментальная диагностика:
- клинический анализ крови, биохимический анализ крови, анализ крови на Д-димер;
- электрокардиография (ЭКГ);
- эхокардиография (УЗИ сердца);
- рентгенография грудной клетки;
- дуплексное/триплексное сканирование вен нижних конечностей;
- МСКТ органов грудной клетки;
- вентиляционно-перфузионная сцинтиграфия легких.
1 ЭКГ при тромбоэмболии
2 Диагностика ТЭЛА в «МедикСити»
3 ЭХО-КГ при тромбоэмболии
У детей
Тромбозы у детей возникают значительно реже. Для возникновения их необходимо сочетание приобретенных и врожденных и факторов. Из наследственных стоит отметить наследственное снижение активности антитромбина III и протеинов С, S, которые являются естественными антикоагулянтами. Приобретенные факторы:
- тяжелые соматические заболевания
- инфекционные заболевания;
- системные заболевания соединительной ткани;
- злокачественные опухоли;
- соединительнотканные дисплазии;
- гемолитические анемии;
- антифосфолипидный синдром.
Важнейший фактор тромбоза — применение внутрисосудистого катетера. До 80% тромбозов связывают с катетеризацией. У детей ТЭЛА часто связана с тромбозом глубоких вен. Венозным тромбозам у детей предшествует инфекция, тромбоцитопеническая пурпура, антифосфолипидный синдром, а у некоторых — избыточная инсоляция. Также встречается рецидивирующая ТЭЛА, но очаг тромбоза установить не удается. ТЭЛА у детей часто ошибочно расценивают как пневмонию.
Профилактика ТЭЛА
- Первичная профилактика эмболий после операций на органах малого таза и в ортопедии.
- При низком уровне риска тромбоэмболий профилактика заключается в применении компрессионного трикотажа или эластической компрессии эластичным бинтом нижних конечностей.
- При умеренном риске тромбоэмболий помимо применения компрессионного трикотажа больным до момента выписки назначают эноксапарин или фондапаринукс или дабигатран.
- При высоком риске эти рекомендации должны выполняться в течение месяца.
- Новые пероральные антикоагулянты зарегистрированы для первичной профилактики после ортопедических операций.
Также есть больные нехирургического профиля (хроническая сердечная недостаточность III-IV класса), которые также находятся в группе риска по ТЭЛА. Выбор антикоагулянта у них такой же. Эталоном лечения является эноксапарин.
Вторичная профилактика — профилактика рецидивов тромбоэмболий. Без проведения профилактики рецидив ТЭЛА в течение первых трех месяцев отмечается у 20-45% больных. При профилактике количество рецидивов снижается до 1%. Обычно для профилактики применяется Варфарин, а онкологическим больным первые полгода назначаются низкомолекулярные гепарины (Фраксипарин, Фраксипарин Форте, Клексан, Эниксум, Фрагмин, Дальтеп, затем их переводят на оральные препараты (антагонисты витамина K — Варфарин, Варфарекс).
Как долго их принимать? Для этого оценивают риск кровотечения по факторам риска (возраст 65 лет и старше, наличие инсульта в прошлом, злокачественная опухоль, почечная и печеночная недостаточность, сахарный диабет, сниженный уровень тромбоцитов, анемия и другие). Риск кровотечения высокий, если в сумме более двух факторов риска.
Также возможно применение для вторичной профилактики «новых» антикоагулянтов, которые внесены в американские Рекомендации по профилактике ТЭЛА. Ривароксабан (Ксарелто) при продленном лечении имеет превосходство, поэтому может назначаться на 6-12 месяцев при низком риске кровотечений, обеспечивая защиту от рецидива.
Профилактика венозных тромбозов и ТЭЛА
Профилактика венозных тромбозов и тромбоэмболии легочной артерии (ТЭЛА) основана на определении степени риска их возникновения для каждого конкретного больного и отнесение его к одной из трёх категорий риска: низкой, умеренной или высокой.
Категория риска возникновения венозных тромбозов определяется в зависимости от наличия у каждого больного факторов риска развития венозных тромбозов, к которым относят: злокачественные новообразования, сердечная недостаточность, инфаркт миокарда, сепсис, ДКМП, мерцательная аритмия, инсульт, бронхообструктивные болезни, эритремия, воспалительные заболевания кишечника, ожирение, нефротический синдром, операции, травмы, возраст старше 40 лет, прием эстрогенов, длительная неподвижность, беременность, варикозное расширение вен нижних конечностей, венозные тромбозы в анамнезе, постельный режим более 4 суток, тромбофилии.
При хирургических вмешательствах степень риска возникновения венозной тромбоэмболии определяется оценкой тяжести хирургической операции и состоянием больного. Основой профилактики венозных тромбозов у этой категории больных является их ранняя активизация, эластическая компрессия нижних конечностей и гепаринотерапия.
Эластическая компрессия нижних конечностей, влияет на стаз крови и гемодинамический фактор тромбоза являясь методом неспецифической профилактики и включает в себя следующие методы.
Эластичные компрессионные гольфы и чулки
в отличие от бинтов создают компрессию, необходимую для нормализации венозного оттока и обеспечивают физиологически распределенное давление по всей длине конечности.
Для профилактики тромбоза глубоких вен и тромбоэмболических осложнений применяют специальный вид медицинского компрессионного трикотажа, получивший название «противоэмболический» или «госпитальный» трикотаж. В своей практике мы используем госпитальный трикотаж компании Tyco Healthcare/Kendall. При этом максимальное давление создается на уровне лодыжек и измеряется в мм рт ст, соответствующее для каждого класса компрессии, с последующим его постепенным снижением в проксимальном направлении, что исключает угрозу (как в случае с эластическими бинтами) ятрогенного венозного застоя.
Эти изделия длительно сохраняют компрессионные свойства, подвергаются обработке, легко надеваются и снимаются, что позволяет экономить время медицинского персонала. Применение противоэмболического трикотажа в 3 — 4 раза повышает эффективность специфической антикоагулянтной профилактики ТЭЛА. У компрессионного белья «Ластошир» («Lastosheer») есть 3 класса компрессии и широкий спектр современных расцветок (телесный, бронзовый, синий, серый, черный, коричневый).
К противопоказаниям для использования компрессионного трикотажа относят следующие случаи:
- Прогрессирующий атеросклероз сосудов нижних конечностей (степень ишемии выше IIА ст.);
- Окружность щиколотки более 35 см;
- После операции по аутодермопластике, пластике ротационным лоскутом или на свободной питающей ножке с целью закрытия варикозных язв;
- Сильная деформация ног.
Размер компрессионного трикотажа подбирается строго индивидуально, с учетом морфометрических данных пациента. При использовании компрессионных гольфов проводится измерение четырех параметров — длина стопы, окружность щиколотки, максимальная окружность голени, длина голени (рис. 1).
При выборе размера чулок следует проводить шесть измерений: длина стопы, окружность щиколотки, максимальная окружность голени, максимальная окружность бедра, длина бедра.
Следует отметить, что данный вид медицинских изделий практически не вызывает контактной реакции кожных покровов, что очень важно для большинства пациентов, поскольку не содержит латекс.
Новая генерация госпитального трикотажа — антиэмболические чулки Т.Е.D. — обладают более надежной фиксацией на ноге благодаря наличию гибкого силиконового эластомера по краю изделия. Силиконовое покрытие комфортно для кожи и прекрасно удерживает чулки. Длительное время антиэмболические изделия поддерживают постоянную градуированную компрессию на ноге.
Рис. 1. Дифференцированное распределение давления в компрессионном белье TED (Tyco Healthcare / Kendall)
Это позволяет увеличить ток крови на 138%. Мозаичная круговая вязка, направленная в одну сторону, правильно распределяет давление по ноге, а отсутствие давления в области подколенной вены обеспечивает свободный ток крови через этот критический участок. Эргономичность создает также прерывающий бандаж и двухслойная V-образная вставка в фиксирующей резинке чулка, предотвращающая эффект жгута на бедренной вене. Выпускаются 3 вида компрессионного трикотажа Т.Е.D.: гольфы, чулки, чулки с поясом, а 27 возможных размеров позволяют подобрать трикотаж большинству пациентов. Высокоточные производственные технологии и строгий контроль качества гарантируют правильное распределение давления и отсутствие дефекта.
Преимущества госпитального трикотажа, перед «классическим бинтованием ног» очевидно. Практически все клиники осознают, что дозированную вертикальную (стопа-голень-бедро) и горизонтальную (передняя поверхность голени – задняя поверхность голени, подколенная ямка) создать с помощью эластичных бинтов невозможно. Однако, знания не повсеместно переросли в убеждения, и тем более в клиническую практику, что послужило причиной достаточно подробного написания данного раздела.
Прерывистая пневматическая компрессия
проводится с помощью специального компрессора и манжет, разделенных на несколько камер. Последовательное раздувание камер создает эффект «бегущей волны», что особенно полезно при отсутствии собственных активных мышечных сокращений. В результате даже у обездвиженных пациентов существенно увеличивается скорость венозного кровотока, т.е. устраняется один из ключевых факторов тромбогенеза. Прерывистая пневмокомпрессия наиболее эффективна при использовании устройств с микропроцессорным управлением и электронным хронометражем (например, пневмокомпрессионное устройство пятого поколения SCD, рис. 2), позволяющих индивидуально устанавливать время заполнения манжет и поддерживать разный уровень давления на отдельные венозные сегменты.
Рис. 2. Прибор регулируемой пневмокомпрессии SCD Response (Tyco Healthcare / Kendall)
При наличии цифрового дисплея и специальных приспособлений для фиксации прибора к кровати, проведение прерывистой пневмокомпрессии становится относительно простым, безопасным и высокоэффективным способом профилактики венозного тромбоза, который можно использовать во время оперативного вмешательства, в послеоперационном периоде, а также в отделении реанимации у больных, находящихся в критическом состоянии. В тех случаях, когда из-за высокого риска кровотечений или по другим причинам использование прямых антикоагулянтов (операции на головном и спинном мозге, органах зрения и слуха, острый геморрагический инсульт и пр.) противопоказано, прерывистая пневматическая компрессия в современном варианте ее проведения является методом выбора.
Специфическая профилактика включает в себя периоперационное применение фармакологических препаратов различных групп.
Для тромбопрофилактики у хирургических больных все чаще используются низкомолекулярные гепарины (НМГ) (ардепарин, дальтепарин, надропарин, парнапарин, ревипарин, сандопарин, тинзапарин, цертопарин, эноксапарин и др.), из которых наибольшее распространение в настоящее время получили надропарин кальциевая соль (фраксиларин), эноксапарин натриевая соль (клексан, ловенокс) и дальтепарин натриевая соль (фрагмин). В сравнении с НФГ, эти препараты имеют высокую биодоступность (более 90%), более длительный период полувыведения (40 — 90 мин. у НФГ и 1 90 — 270 мин. — у НМГ) и антитромботическое действие (8 — 12 ч и 17 — 24 ч), в меньшей степени связываются с белками острой фазы, т.е. сохраняют свой эффект на фоне эндогенной интоксикации, обладают более предсказуемым дозозависимым антикоагулянтным эффектом, не стимулируют, а ослабляют агрегацию тромбоцитов, реже (менее 0,5%) вызывают тромбоцитопению и не требуют лабораторного мониторинга.
Эти свойства НМГ обусловлены химическим составом препаратов. Молекулы гепарина, состоящие на 25 — 50% из менее, чем 18 сахаридов (с молекулярной массой менее 5400 Да), не способны связывать одновременно ATIII и тромбин, поэтому не могут ускорять инактивацию последнего, но сохраняют способность катализировать процесс ингибирования фактора Ха. В результате соотношение анти-Ха и анти-IIa активности у коммерческих НМГ составляет не 1:1-2, как у НФГ,аЗ-4:1, они обладают меньшей, чем НФГ антикоагулянтной активностью, но имеют более выраженные антитромботические свойства. Поскольку состав каждого из коммерческих НМГ различен, они отличаются, как ранее отмечалось нами, друг от друга по физико-химическим, биологическим и фармакокинетическим свойствам, не являются взаимозаменяемыми и имеют разную клиническую эффективность и безопасность.
Надропарин кальций (Фраксипарин) — представляет собой официнальный раствор в предварительно наполненных шприцах, объемом — 0,3 — 0,6 -0,8 — 1,0 мл с содержанием 2850 — 5700 — 7600 — 9500 МЕанти-Ха активности соответственно. После однократного подкожного введения анти-Ха факторная активность достигает максимума примерно через 4 — б ч. Активность в отношении Па меняется незначительно и максимальна через 3 ч после введения препарата.
Основными показаниями к применению являются: профилактика тромбоэм-болических осложнений в общей хирургии, ортопедии, гинекологии, а также у других хирургических и нехирургических больных, имеющих высокой риск венозных тромбозов на фоне острой дыхательной или сердечной недостаточности; пациентов, находящихся на лечении в отделении интенсивной терапии; больных с хирургической инфекцией. Препарат также применяется при лечении больных с острым коронарным синдромом, лечении тромбоэмболических осложнений и для профилактики свертывания крови при гемодиализе.
Профилактическое использование надропарина предусматривает ежедневное введение препарата в дозе 0,3 мл 1 раз/сут. до и после оперативного вмешательства в виде курса продолжительностью не менее 7 дней или до полного восстановления двигательной активности пациента. При плановых операциях первую дозу вводят за 2 — 4 ч до операции, в неотложной хирургии введение начинают через 1 2 ч после окончания оперативного вмешательства.
Эноксапарин натрий (Клексан)
— низкомолекулярный гепарин, состоящий из коротких мукополисахаридных цепей со средней молекулярной массой 4500 дальтон, выпускаемый в виде водного раствора для инъекций, содержащего 1 00 мг/мл в готовых шприцах по 0,2-0,4-0,6-0,8-1,0 мл. 1 мг эноксапарина соответствует 1 00 МГ анти-Ха активности. Пик анти-Ха факторной активности достигает максимума примерно через 3 — 5 ч после подкожного введения и сохраняется в течение 24 ч.
Для профилактики венозных тромбозов и тромбоэмболии больным хирургического профиля эноксапарич начинают вводить до операции: при умеренном риске 20 мг (0,2 мл) за 2 ч до операции, при высоком 40 мг (0,4 мл) за 1 2 ч до оперативного вмешательства и продолжают в послеоперационном периоде в течение 7-10 дней по одной инъекции в сутки в тех же дозах. Использование более высоких доз эноксапарина для профилактики тромбозов у хирургических больных нецелесообразно, так как увеличение дозы сопровождается статистически значимым повышением и анти-Ха активности, и анти-lla, что достоверно увеличивает частоту геморрагии. Поэтому бо¬лее высокие дозы эноксапарина применяют только при лечении тромбозов глубоких вен, а также для профилактики тромбозов во время проведения операций экс-тракорпоральной гемокоррекции и гемодиализа. При лечении тромбоэмболических осложнений лучшее соотношение безопасности/активности эноксапарина достигается при дозе 1 мг/кг, которую вводят подкожно два раза в сутки через 1 2 ча¬сов. При гемодиализе эноксапарин вводят первоначально в дозе 1 мг/кг для 4- часовой процедуры. Для больных с высоким риском кровотечения дозу уменьшают до 0,5 — 0,75 мг/кг. При признаках отложения фибрина и угрозе тромбоза системы, при более длительной процедуре можно вводить дополнительно 0,5 — 1 мг/кг.
В дозах, используемых для профилактики венозных тромбозов, эноксапарин практически не влияет на время кровотечения, время свертывания крови, АПТВ, не оказывает влияние на агрегацию тромбоцитов. В первые дни лечения эноксапарином может появиться умеренная транзиторная асимптоматическая тромбоцитопения. Возможно асимптоматическое и обратимое увеличение числа тромбоцитов, повышение уровня печеночных трансаминаз. При снижении количества тромбоцитов на 30 — 50% от исходной величины лечение эноксапарином следует прекратить.
Эноксапарин должен назначаться с осторожностью больным с потенциальным риском развития кровотечений, гипокоагуляции, больным с тяжелыми заболеваниями печени.
Последствия и осложнения
- Нарушения гемодинамики (увеличение сосудистого сопротивления в системе легочной артерии и увеличение постнагрузки на правый желудочек).
- Дыхательная недостаточность.
- Гипоксия.
- Легочно-плевральные осложнения (ателектазы, плеврит, абсцесс легкого, инфаркт легкого, пневмония, пиопневмоторакс, эмпиема плевры).
- Постэмболическая легочная гипертензия.
Список источников
- Ватутин Н.Т., Склянная Е.В., Ещенко Е.В. /Тромбоэмболия легочной артерии. Обзор рекомендаций Европейского общества кардиологов по диагностике и лечению (2014 // Практическая ангиология. — 2015.— № 1 (68). — С 5-18.
- Российские клинические рекомендации по диагностике, лечению и профилактике венозных тромболэмболических осложнений // Флебология. — 2015.— №4, выпуск 2. 46 с.
- Ватутин Н.Т. Неотложная кардиология. — Донецк, 2011. – 236 с.
- Ватутин Н.Т., Калинкина Н.В., Перуева И.А. /Тромбоэмболия легочной артерии // Практическая ангиология. – 2011. – № 2. – С. 32-40.
- Ватутин Н.Т., Калинкина Н.В., Ещенко Е.В. и др. Тромбоэмболия легочной артерии (основные сведения и собственное наблюдение) // Сердце и сосуды. – 2013. – № 1. – С. 120-123.