Медицинский редактор: Строкина О.А. — терапевт, врач функциональной диагностики. Сентябрь, 2021.
Код МКБ-10: I35.0 , I06.8 , I35.8.
Аортальная недостаточность — нарушение работы аортального клапана с формированием обратного тока крови из аорты в полость левого желудочка. Симптоматика напрямую зависит от количества крови, попадающей обратно в желудочек. Диагностика патологии возможна только с помощью эхокардиографического исследования (УЗИ сердца). Лечение также зависит от степени недостаточности и может подразумевать как консервативное, так и хирургические методики.
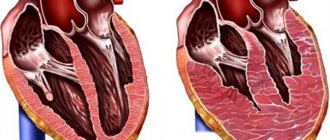
Аортальная недостаточность — порок сердца, который характеризуется развитием регургитации (обратного тока крови) на аортальном клапане в фазу расслабления сердечной мышцы. В результате кровь из аорты попадает снова в желудочек. Возникает переполнение его объемом, что в будущем может грозить расширением полости левых камер сердца с развитием сердечной недостаточности.
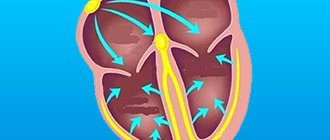
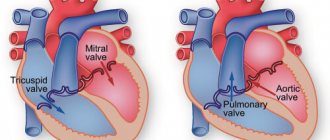
В фазу сокращения левый желудочек выбрасывает кровь в аорту, после чего наступает фаза расслабления желудочков. В этот момент кровь стремится вернуться назад. Путь ей преграждают 3 створки аортального клапана, которые представляют собой “мешочки”. По ходу наполнения их кровью, створки расправляются, смыкаются друг с другом и полностью закрывают аортальное отверстие.
На митральном и трикуспидальном клапанах в норме допустим небольшой сброс крови в обратном направлении,при этом термин “недостаточность” здесь не применяется. В случае аортального клапана даже минимальная регургитация является патологией, за которой необходимо наблюдать.
Причины и факторы риска
Недостаточность аортального клапана развивается из-за неплотного смыкания створок в фазу расслабления желудочков, что может развиться по целому ряду причин:
- идиопатические (неизвестной причины) расширения аорты;
- врожденные пороки аортального клапана (чаще двустворчатый аортальный клапан);
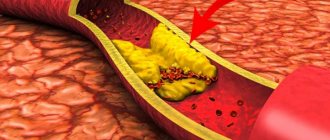
- склероз створок (вследствие атеросклероза);
- ревматизм;
- инфекционный эндокардит;
- артериальная гипертензия;
- миксоматозная дегенерация (нарушение развития соединительной ткани);
- расслоение восходящего отдела аорты;
- синдром Марфана;
- травмы аортального клапана;
- анкилозирующий спондилит;
- сифилитический аортит;
- ревматоидный артрит.
Большая часть из перечисленных причин приводят к хронической аортальной недостаточности, которая может длительное время протекать бессимптомно. Другие же, в частности инфекционный эндокардит, расслоение аорты, травма часто сопровождаются резким развитием аортальной недостаточности тяжелой степени. Это приводит к серьезным нарушениям гемодинамики. В результате кровь в гораздо меньшем количестве достигается до жизненно важных органов: мозг, почки, печень, сердце.
Причины
Патология развивается в период внутриутробного развития, потому это врождённый порок сердца. Происходит это на 6 – 8 неделе. В этот промежуток времени начинается активный процесс формирования внутренних органов у детей. Две створки срастаются между собой, образуя всего две подвижные части. Они берут на себя функции недостающего компонента сердечной мышцы. У ребёнка такая патология развивается под действием ряда провоцирующих факторов. К основным причинам, из-за которых формируется двустворчатый аортальный клапан, относят:
- перенесённые мамой в период вынашивания плода разных заболеваний инфекционного характера;
- влияние радиационных излучений, облучений, вызванных проводимым рентгенологическим исследованием;
- пагубное воздействие окружающей среды при плохой экологии;
- сильные стрессы, переживания, психоэмоциональные расстройства и потрясения;
- злоупотребление алкогольной и табачной продукцией при вынашивании малыша;
- предрасположенность, передающаяся по наследству при наличии у родителей малыша пороков сердечно-сосудистой системы;
- генетическая предрасположенность к патологиям, связанным с соединительными тканями.
Если у родителей присутствует двустворчатый аортальный клапан как врождённая патология, при планировании зачатия и во время вынашивания плода нужно тщательно контролировать все процессы, проводить комплексную диагностику и вовремя принимать меры для обеспечения нормальной работы сердечно-сосудистой системы малыша.
Симптоматика
У ребёнка врождённая патология может никак не проявляться в течение длительного времени. Симптомы способны активизироваться при взрослении и постепенно увеличении нагрузок на его организм, который находится в стадии активного развития и формирования. Есть случаи, когда врождённый порок клапанного отдела обнаруживался при достижении ребёнком юношеского и взрослого возраста. При таком ВПС как двухстворчатый аортальный клапан симптоматика проявляется в виде следующих характерных признаков:
- Сильная пульсация, которая ощущается в районе шеи, головы или проекции сердечной мышцы. Пульсация усиливается, когда больной принимает лежачее положение. Такая симптоматика проявляется по причине высоких миокардных выбросов и завышенных показателей пульса.
- Тахикардия синусового типа. Её проявления характеризуются учащённым биением сердца. Может возникать без видимых на то причин, то есть в состоянии покоя.
- Обморок, головокружение. Наблюдаются у больных довольно часто. Могут развиваться при умеренных физических нагрузках, или когда человек резко меняет положение своего тела. Это происходит, если больной резко встаёт. Вызывает такие симптомы дефицит кровообращения в головном мозге. Такие признаки актуальны тогда, когда происходят серьёзные изменения в строении клапанов.
- Одышка. Сначала появляется, если больной перенёс существенные физические нагрузки. Но со временем симптомы наблюдаются и при состоянии полного покоя. Если падает систолическая функция, возложенная на левый желудочек, у человека отмечают признаки ортопноэ. Когда болезнь прогрессирует, постепенно развивается миокардиальная астма и отёк лёгких. Из-за них пациент сталкивается с опасными приступами удушья.
- Повышенная и чрезмерная утомляемость при минимальной активности, ощущение общей слабости во всём организме.
- У человека заметно падает зрение, даже если изначально оно было 100%.
- В районе миокарда чувствуется боль за грудной клеткой, у которой нет эмоциональных или физических провоцирующих факторов. Может наблюдаться в состоянии покоя. Если аортальный клапан сильно повреждён, боль становится давящей и сжимающей, продолжается долгое время и не проходит после приёма сильнодействующих препаратов. Тяжелее всего больному даются приступы боли, которые происходят ночью. При этом активно выделяется пот. Такое состояние обусловлено гипертрофией поражённых желудочков.
Только аппаратная диагностика может выявить у человека двухстворчатый аортальный клапан как врождённую патологию сердечно-сосудистой системы. Потому при первых же признаках обращайтесь за консультацией к кардиологу. Если вовремя обнаружить симптомы, подтвердить диагноз и начать лечение, функционально сердечно-сосудистая система пострадает минимально. Часто удаётся вернуть пациентов к нормальной жизни и восстановить кровоток. Прогнозирование делают исходя из результатов обследования и назначенных для лечения терапевтических методов.
Виды и стадии
Для аортальной недостаточности врачи используют классификацию по степени тяжести регургитации (обратного тока крови). степень определяет лишь врач функциональной диагностики по результатам эхокардиографии:
- Мягкая (легкая);
- Умеренная;
- Выраженная.
Есть масса способов ее определения. Но все они возможны благодаря доплеровскому исследованию. Этой функцией обладают все аппараты для эхокардиографии. Она позволяет обнаружить патологические потоки внутри сердца с помощью ультразвукового датчика. Так или иначе это наиболее объективная оценка тяжести аортальной недостаточности.
Также выделяют острую и хроническую недостаточность. Это по большей части клиническая классификация, основанная на симптомах и скорости их развития.
Методы диагностики
Исследовать двустворчатый клапан аорты можно только с помощью инструментальных методов диагностики. Но сначала врач-кардиолог проводит визуальный осмотр при подозрениях на такую патологию. При ДАК у пациентов наблюдается побледнение кожных покровов или некоторых участков с наличием синеватых оттенков. Также к числу внешних признаков относят усиленную пульсацию. Есть несколько основных методов инструментальной диагностики, которые могут подтвердить факт врождённого порока и оценить текущее состояние пациента.
- С помощью ультразвукового исследования или эхокардиографии удаётся определить степени повреждения поражённых клапанов, а также подтвердить или опровергнуть факт развития аневризмы аорты.
- Метод допплерографии сосудов или УЗДГ используется для определения текущего состояния структуры клапанов, скорости течения крови по ним и полостям.
- Чтобы выявить симптомы застоя крови, факт расширенного желудочка и аорты, используют метод рентгенограммы. Рентген сканирует грудную клетку и выдаёт врачу соответствующую информацию.
- Если требуется проверить сердечную мышцу на предмет патологических шумов, прибегают к помощи фонокардиографии.
Самым эффективным и полезным методом обследования для такой патологии считается УЗДГ. Опираясь на полученные результаты инструментального исследования, врач формирует индивидуальную тактику по лечению нарушения.
Симптомы аортальной недостаточности
Скорость развития симптомов зависит от причины формирования аортальной недостаточности.
Острая форма
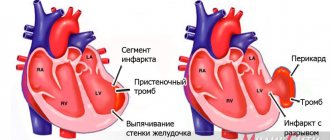
Острая аортальная недостаточность развивается резко, буквально за несколько минут-часов, реже — в течение дня. Причиной часто является какая-то остро возникшая патология, например травма клапана или расслоение аорты. В результате развивается тяжелая аортальная недостаточность с большим обратным сбросом крови в левый желудочек. Он переполняется объемом. Быстро развивается недостаточность митрального клапана и возникает застой крови в малом круге кровообращения, что может привести к отеку легких. В случае принятия экстренных мер сердце может восстановиться практически полностью.
При острой форме развивается острая сердечная недостаточность с отеком легких и кардиогенный шок:
- резко выраженная одышка,
- затруднение дыхания,
- кашель,
- вынужденное положение больного сидя,
- хрипы в легких,
- появление пенистой розовой мокроты,
- снижение артериального давления вплоть до потери сознания.
Даже при интенсивной медикаментозной терапии нередко наступает смерть от желудочковых аритмий, кардиогенного шока, отека легких.
Хроническая форма
Хроническая развивается медленно. Клиника не развивается годами. Человек может не знать о патологии и недостаточность часто становится случайной находкой. Либо пациент обращается уже с какими-либо симптомами, когда сердце сильно изменено. Лечение при этом носит в основном симптоматический характер.Хотя в некоторых случаях возможна хирургическая коррекция.
Хроническая аортальная недостаточность годами может протекать бессимптомно. Первыми симптомами могут быть вялость, снижение работоспособности, обмороки и предобморочные состояния. Постепенно развивается клиника сердечной недостаточности, обусловленная перегрузкой левого желудочка объемом:
- одышка при физической нагрузке, затем со временем — в покое;
- приступы удушья;
- боль в области сердца давящего, сжимающего характера, проходящая после приема нитроглицерина;
- отеки нижних конечностей, а в дальнейшем при отсутствии адекватного лечения появляется жидкость в брюшной, плевральных и даже перикардиальной полостях;
- нарушения ритма сердца — от мерцательной аритмии до желудочковых тахикардий. опасных для жизни.
Двустворчатый аортальный клапан
Двустворчатый аортальный клапан (ДАК)-наиболее частый врожденный порок сердца (ВПС), встречающийся у 1−2% людей.
Анатомия
В здоровом сердце человека в аортальном клапане в норме-три створки. Они обеспечивают нормальный приток крови в сердце.
Когда происходит развитие сердца у плода, примерно на восьмом месяце беременности, две створки могут соединиться в одну, и вместо трех створок будет две. Поэтому женщинам во время первого триместра рекомендовано меньше себя перегружать и подвергать стрессам.
Патогенез и генетика.
ДАК -результат нарушения формирования створок аорты в течение вальвулогенеза. Смежные створки сращиваются и формируют одну большую створку, она больше противоположной, но меньше 2-х нормальных. ДАК является следствием комплексного дефекта процесса развития. Более обоснована генетическая теория возникновения ДАК, поэтому этот порок часто связан с врожденными патологиями аорты-открытым артериальным протоком и коарктацией аорты. А в последующем заболевание нередко связано с дилатацией, аневризмой или расслоением аорты. Также недостаток белка фибриллина в стадию вальвулогенеза ведет к формированию двустворчатого аортального клапана.
Клиника
Одним из характерных симптомов ДАК является нарушение тока крови. Соответственно к основным проявлениям болезни можно отнести:
- ощущение пульсации в голове;
- синусовая тахикардия;
- головокружение, вплоть до обмороков;
- одышка;
- проблемы со зрением;
- кратковременные боли в области сердца, которые появляются из-за гипертрофии желудочков.
Прогноз и осложнения
При слиянии правой коронарной и некоронарной створок может сформироваться стеноз, если нет избыточной ткани створки, и недостаточность АК, если есть пролапс или избыточная ткань створки. Аортальный стеноз развивается у 15−71%, аортальная регургитация-у 1,5−3%, инфекционный эндокардит-у 9,5−40%, дилатация и расслаивающая аневризма-у 5%. Аортальный стеноз чаще встречается в среднем возрасте, инфекционный эндокардит-в молодом.
Аортальный стеноз
Во многих случаях развившийся аортальный стеноз требует имплантации протеза. У пациентов с ДАК -склонность к преждевременному фиброзу, увеличению жесткости створок и депонированию кальция. Эхо — исследования показали, что склероз ДАК начинается во 2-й декаде жизни, а кальциноз-в 4-й декаде, при этом клапанный градиент увеличивается примерно на 18 мм рт ст каждые 10 лет. Также на развитие стеноза может влиять гиперхолестеринемия и курение, которые способствуют более быстрому изнашиванию створок.
Аортальная регургитация
Этиология аортальной регургитации у пациентов с ДАК более комплексная, чем при аортальном стенозе. Аортальная регургитация может быть изолированной и возникает при пролапсе большей, эксцентрично расположенной створки или при расширении корня аорты из-за того, что утрачиваются эластические свойства кольца клапана. Из-за связи с сопутствующими поражениями пациенты с ДАК и аортальной регургитацией имеют более худший прогноз, чем пациенты с аортальным стенозом.
Инфекционный эндокардит (ИЭ)
ИЭ может развиться у 10−30% пациентов с ДАК. Чаще в молодом возрасте, так что тетрада Фалло, дефект межжелудочковой перегородки, ДАК и пролапс митрального клапана являются субстратом для 80−90% случаев заболевания у молодых.
Выводы:
Пациенту с ДАК и дилатацией аорты необходимо объяснить:
- ДАК-наиболее частый врожденный порок сердца;
- Необходимо ЭхоКГ-исследование у родственников, так как ДАК-это генетически обусловленное заболевание;
- ДАК часто сопровождается патологией корня аорты и имеет склонность к клапанным и аортальным осложнениям, которые требуют хирургического вмешательства
- Инфекционный эндокардит-частое осложнение заболевания, поэтому требуется прфилактика антибиотиками;
- Раннее направление к кардиохирургу может облегчить наблюдение и предотвратить жизнеугрожаемые осложнения;
- Пациент должен ежегодно проходить осмотр кардиолога с выполнением ЭхоКГ для выявления прогрессии дилатации аорты и профилактики расслоения. Гиперхолестеринемия и артериальная гипертензия должны тщательно контролироваться. Курение должно быть исключено.
Будьте здоровы!
Записаться на функциональную диагностику
Врач функциональной диагностики — Андриенко Ольга Леонидовна
Записаться можно по телефону (391) 205−00−48 или через личный кабинет
Обследования
Обследование пациента всегда начинается с его осмотра и выслушивания сердца. Уже на этом этапе врач способен заподозрить порок клапана по наличию шумов в сердце. Также возможно снижение диастолического (нижней границы) артериального давления и в следствие — увеличение пульсового давления (разница между верхней и нижней границами артериального давления). Однако такие признаки аортальной недостаточности выявляются лишь при хронической патологии, когда уже четко проявляется клиника сердечной недостаточности, описанная выше.
Инструментальные методы — единственный способ обнаружить регургитацию на аортальном клапане.
Эхокардиография (УЗИ сердца)
Метод диагностики первой линии. Он позволяет обнаружить обратный ток крови через аортальный клапан. Врач определяет степень его тяжести и возможную причину — например, травма, вегетации на клапане (скопления бактерий на створках — признак инфекционного эндокардита), объемы левых камер сердца, фракцию выброса левого желудочка и множество других морфо-функциональных показателей..
Магнитно-резонансная томография (МРТ)
Используется только при условии, если эхокардиография недоступна или визуализация сердца и его структур крайне затруднительна.
Мультиспиральная компьютерная томография-ангиография и магнитно-резонансная томография-ангиография (обе процедуры с контрастированием) используются у пациентов с двустворчатым аортальным клапаном, чтобы оценить начальный отдел аорты до ее дуги, но только если результаты эхокардиографии неудовлетворительные.
Рентгенография органов грудной клетки
Используется для оценки размеров сердца и восходящего отдела аорты.
Электрокардиограмма (ЭКГ)
Позволяет выявить нарушения ритма, проводимости в сердце и признаки гипертрофии миокарда.
Перечисленных методов более чем достаточно чтобы поставить точный диагноз аортальной недостаточности и вовремя начать лечение.
Синдром соединительнотканной дисплазии сердца у детей
В последние годы отмечается увеличение числа врожденных пороков развития и наследственных заболеваний, а также нарастание распространенности различных вариантов соединительнотканной дисплазии из-за ухудшения экологической обстановки. По современным представлениям синдром соединительнотканной дисплазии определяют как самостоятельный синдром полигенно-мультифакториальной природы, проявляющийся внешними фенотипическими признаками в сочетании с диспластическими изменениями соединительной ткани и клинически значимой дисфункцией одного или нескольких внутренних органов (В. А. Гаврилова, 2002).
Под термином «дисплазия соединительной ткани сердца» (ДСТС) подразумевается аномалия тканевой структуры, в основе которой лежит генетически детерминированный дефект синтеза коллагена. Синдром ДСТС был выделен в самостоятельную нозологическую форму на симпозиуме в г. Омске (1990), посвященном проблеме врожденной дисплазии соединительной ткани. Проблема синдрома ДСТС привлекает к себе внимание в связи с большим риском развития таких осложнений, как нарушения ритма и проводимости сердца, инфекционный эндокардит, тромбоэмболия различных сосудов и внезапная сердечная смерть.
Высокая частота синдрома ДСТС при различных заболеваниях свидетельствует о системности поражения, что связано с «вездесущностью» соединительной ткани, составляющей строму всех органов и тканей.
Диспластическое сердце — сочетание конституциональных, топографических, анатомических и функциональных особенностей сердца у человека с дисплазией соединительной ткани (ДСТ). В западной литературе используется термин «миксоидная болезнь сердца» (Morales A. B., Romanelli B. E. A., 1992), однако эта формулировка используется преимущественно зарубежными авторами.
Частота диспластического сердца составляет 86% среди лиц с первичной недифференцированной ДСТ (Г. Н. Верещагина, 2008).
По современным представлениям к синдрому ДСТС относят пролапсы клапанов сердца, аневризмы межпредсердной перегородки и синусов Вальсальвы, эктопически крепящиеся хорды митрального клапана и многие другие.
В основе патологии лежит неполноценность внеклеточного матрикса, его коллагеновых структур.
Диспластическое сердце формируют:
I. Конституциональные особенности — «капельное», «висячее» сердце, поворот его вокруг сагиттальной и продольной оси.
II. Костно-вертебральные дисплазии и деформации со сдавлением, ротацией, смещением сердца и перекрутом крупных сосудов: по данным Урмонаса В. К. и др. (1983). Деформации грудной клетки и позвоночника приводят к развитию торако-диафрагмального синдрома, ограничивающего работу всех органов грудной клетки.
III. Особенности строения сердца и сосудов:
- избыточность ткани створок митрального, трикуспидального и аортального клапанов;
- пролабирование створок митрального клапана (ПМК) с регургитацией;
- миксоматозная дегенерация створок, хорд, клапанного кольца;
- вальвулярно-вентрикулярная диссоциация;
- двустворчатый аортальный клапан;
- удлинение, избыточная подвижность хорд;
- эктопически крепящиеся хорды;
- повышенная трабекулярность левого желудочка (ЛЖ);
- открытое овальное окно;
- аневризма межпредсердной перегородки (небольшая);
- дилятация синусов Вальсальвы;
- вентрикуло-септальные особенности ЛЖ: транзиторный систолический валик верхней трети межжелудочковой перегородки (МЖП), S-образный изгиб МЖП;
- извитость, гипоплазия, аплазия, фибромускулярная дисплазия коронарных артерий;
- аневризмы коронарных артерий;
- миокардиальные мостики;
- аномалии проводящей системы;
- расширение проксимальной части аорты, легочного ствола;
- гипоплазия аорты, погранично узкий корень аорты, гипоплазия легочного ствола;
- системная несостоятельность венозной стенки — варикозное расширение вен верхних и нижних конечностей, малого таза, вульвы, варикоцеле.
IV. Патология органов дыхания со снижением жизненной емкости легких:
- диффузная и буллезная эмфизема;
- множественные свищи;
- повторные спонтанные пневмотораксы;
- бронхоэктазы;
- кистозная гипоплазия легких.
Миксоматозная дегенерация створок, хорд, подклапанных структур — генетически детерминированный процесс разрушения и утраты архитектоники коллагеновых и эластических структур соединительной ткани с накоплением в рыхлом фиброзном слое кислых мукополисахаридов. При этом признаки воспаления отсутствуют. В основе — дефект синтеза коллагена III типа, что приводит к истончению фиброзного слоя, створки увеличены, рыхлые, избыточные, края закручены, иногда определяется бахрома. Первичный локус аутосомно-доминантного миксоматоза при ПМК локализован в хромосоме 16. Morales A. B. (1992) выделяет миксоидную болезнь сердца.
В популяционных исследованиях феномен ПМК выявлен у 22,5% детей в возрасте до 12 лет. У детей с ДСТ ПМК обнаруживается значительно чаще — у 45–68%.
Клинические проявления ПМК у детей варьируют от минимальных до значительных и определяются степенью соединительнотканной дисплазии сердца, вегетативными и психоневрологическими отклонениями.
Большинство детей старшего возраста жалуются на кратковременные боли в грудной клетке, сердцебиение, одышку, ощущение перебоев в сердце, головокружение, слабость, головные боли. Боли в сердце дети характеризуют как колющие, давящие, ноющие и ощущают в левой половине грудной клетки без какой-либо иррадиации. Они возникают в связи с эмоциональным напряжением и сопровождаются, как правило, вегетативными нарушениями: неустойчивым настроением, похолоданием конечностей, сердцебиением, потливостью, проходят самопроизвольно или после приема седативных средств. Отсутствие в большинстве случаев ишемических изменений в миокарде по данным комплексного обследования позволяет расценить кардиалгии как проявление симпаталгии, связанной с психоэмоциональными особенностями детей с ПМК. Кардиалгии при ПМК могут быть связаны с региональной ишемией папиллярных мышц при их чрезмерном натяжении. С нейровегетативными нарушениями также связаны сердцебиение, ощущение «перебоев» в работе сердца, «покалывание», «замирание» сердца. Головные боли чаще возникают при переутомлении, переживаниях, в утренние часы перед началом занятий в школе и сочетаются с раздражительностью, нарушением сна, тревогой, головокружением.
При аускультации характерными признаками пролапса митрального клапана являются изолированные щелчки (клики), сочетание щелчков с позднесистолическим шумом, изолированный позднесистолический шум, голосистолический шум.
Происхождение шума связано с турбулентным током крови, связанным с выбуханием створок и вибрацией натянутых хорд. Позднесистолический шум выслушивается лучше в положении лежа на левом боку, усиливается при проведении пробы Вальсальвы. Характер шума может меняться при глубоком дыхании. На выдохе шум усиливается и иногда приобретает музыкальный оттенок. Нередко сочетание систолических щелчков и позднего шума наиболее отчетливо выявляется в вертикальном положении после физической нагрузки. Иногда при сочетании систолических щелчков с поздним шумом в вертикальном положении может регистрироваться голосистолический шум.
Голосистолический шум при первичном пролапсе митрального клапана наблюдается редко и свидетельствует о наличии митральной регургитации. Этот шум занимает всю систолу и практически не меняется по интенсивности при перемене положения тела, проводится в подмышечную область, усиливается при проведении пробы Вальсальвы.
Основными методами диагностики ПМК являются двухмерная Эхо-КГ и допплерография. ПМК диагностируют при максимальном систолическом смещении створок митрального клапана за линию кольца митрального клапана в парастернальной продольной позиции на 3 мм и более. Наличия изолированного смещения передней створки за линию кольца митрального клапана в четырехкамерной верхушечной позиции недостаточно для диагностики ПМК, это служит основной причиной его гипердиагностики.
Эхо-КГ-классификация миксоматозной дегенерации (МД) (Г. И. Сторожаков, 2004):
- МД 0 — признаков нет.
- МД I — минимально выраженная: утолщение створок 3–5 мм, аркообразная деформация митрального отверстия в пределах 1–2 сегментов. Смыкание створок сохранено.
- МД II — умеренно выраженная: утолщение створок 5–8 мм, удлинение створок, деформация контура митрального отверстия, его растяжение, нарушение смыкания створок. Митральная регургитация.
- МД III — резко выраженная: утолщение створок больше 8 мм, створки удлинены, множественные разрывы хорд, значительное расширение митрального кольца, смыкание створок отсутствует. Многоклапанное поражение. Дилятация корня аорты. Митральная регургитация.
Степень регургитации при ПМК зависит от наличия и выраженности миксоматозной дегенерации, количества пролабирующих створок и глубины пролабирования.
Степени регургитации:
- 0 — регургитация не регистрируется.
- I — минимальная — струя регургитации проникает в полость левого предсердия не более чем на одну треть предсердия.
- II — средняя — струя регургитации достигает середины предсердия.
- III — тяжелая — регургитация по всему левому предсердию.
В состоянии покоя митральная регургитация (МР) первой степени диагностируется у 16–20%, вторая степень — у 7–10% и третья степень — у 3–5% детей с ПМК.
Прогноз больного с ПМК определяет степень митральной регургитации. При этом любая степень пролабирования приводит к изменениям перфузии миокарда, изменениям чаще в области передней стенки ЛЖ и межжелудочковой перегородки (Нечаева Г. И., Викторова И. А., 2007)).
Тяжелые осложнения при ПМК у детей встречаются нечасто. Ими являются: жизнеугрожаемые аритмии, инфекционный эндокардит, тромбоэмболия, острая либо хроническая митральная недостаточность и даже внезапная смерть.
Острая митральная недостаточность возникает из-за отрыва сухожильных нитей от створок митрального клапана (синдром «болтающегося» клапана — loppy mitral valve), в детском возрасте наблюдается казуистически редко и в основном связана с травмой грудной клетки у больных на фоне миксоматозной дегенерации хорд. Основным патогенетическим механизмом острой митральной недостаточности является легочная венозная гипертензия, возникающая из-за большого объема регургитации в недостаточно растяжимое левое предсердие. Клиническая симптоматика проявляется внезапным развитием отека легких.
У детей митральная недостаточность при ПМК протекает чаще всего бессимптомно и диагностируется при допплерэхокардиографическом исследовании. В последующем при прогрессировании регургитации появляются жалобы на одышку при физической нагрузке, снижение физической работоспособности, слабость, отставание в физическом развитии.
Факторами риска развития «чистой» (не воспалительной) митральной недостаточности при синдроме пролабирования по данным двухмерной эхокардиографии являются:
- Дилятация левого атриовентрикулярного отверстия.
- Пролапс преимущественно задней митральной створки.
- Утолщенность задней митральной створки.
ПМК является высоким фактором риска возникновения инфекционного эндокардита. Абсолютный риск возникновения заболевания выше, чем в популяции, в 4,4 раза.
Диагностика инфекционного эндокардита при ПМК представляет определенные трудности. Поскольку створки при пролапсе избыточно фестончатые, это не позволяет выявить начало формирования бактериальных вегетаций по данным эхокардиографии. Поэтому основное значение в диагностике эндокардита играют: 1) клиническая симптоматика инфекционного процесса (лихорадка, ознобы, сыпь, и другие симптомы), 2) появление шума митральной регургитации и факт обнаружения возбудителя при повторных высевах крови.
Частота внезапной смерти при синдроме ПМК зависит от многих факторов, основными из которых являются электрическая нестабильность миокарда при наличии синдрома удлиненного интервала QT, желудочковых аритмий, сопутствующая митральная недостаточность, нейрогуморальный дисбаланс.
Риск внезапной смерти при отсутствии митральной регургитации низкий и не превышает 2:10 000 в год, в то время как при сопутствующей митральной регургитации увеличивается в 50–100 раз.
В большинстве случаев внезапная смерть у больных с ПМК носит аритмогенный генез и обусловлена внезапным возникновением идиопатической желудочковой тахикардии (фибрилляции) или на фоне синдрома удлиненного интервала QT.
В редких случаях в основе внезапной сердечной смерти у больных с ПМК может лежать врожденная аномалия коронарных артерий (аномальное отхождение правой или левой коронарной артерии), приводящая к острой ишемии миокарда и его некрозу.
Таким образом, основными факторами риска внезапной смерти у детей с синдромом ПМК являются: желудочковые аритмии III–V градации по Lown; удлинение корригированного интервала QT более 440 мс; появление ишемических изменений на ЭКГ во время физической нагрузки; кардиогенные обморочные состояния в анамнезе.
ДСТС являются одними из неблагоприятных факторов, предрасполагающих к развитию аритмических осложнений в детском и подростковом возрасте, в том числе гемодинамически значимых. В структуре нарушений ритма у детей с ДСТС чаще выявляются наджелудочковая экстрасистолия в патологическом количестве и желудочковая экстрасистолия, взаимосвязанные со степенью кардиальной дисплазии (Гнусаев С. Ф., соавт., 2006).
Морфологическими проявлениями синдрома ДСТС у детей с сопутствующей патологией почек, по данным Домницкой Т. М., Гавриловой В. А. (2000), являются: шаровидная или треугольная форма сердца, закругление верхушки сердца, увеличение массы сердца в 1,4–2,5 раза, утолщение и укорочение хорд митрального клапана, отхождение хорд в виде веера, гипертрофия сосочковых мышц, воронкообразная форма митрального клапана, открытое овальное окно. Миксоматозная дегенерация створок атриовентрикулярных клапанов наблюдалась у большинства больных с синдромом ДСТС и заболеваниями органов мочевой системы (частота ее колебалась от 66,7% до 77%). Фиброэластоз эндокарда был выявлен у 10 детей анализируемой группы.
В популяции детей наиболее часто выявлялись смещение септальной створки трехстворчатого клапана в полость желудочка в пределах 10 мм, нарушенное распределение хорд передней створки митрального клапана, дилятация синусов Вальсальвы, увеличенная евстахиева заслонка более 1 см, дилятация ствола легочной артерии, ПМК, диагонально расположенные трабекулы в полости левого желудочка.
Тактика ведения детей с первичным ПМК различается в зависимости от степени выраженности пролабирования створок, характера вегетативных и сердечно-сосудистых изменений. Основными принципами лечения являются: 1) комплексность; 2) длительность; 3) учет направленности функционирования вегетативной нервной системы.
Обязательным является нормализация труда, отдыха, распорядка дня, соблюдение правильного режима с достаточным по продолжительности сном.
Вопрос о занятиях физкультурой и спортом решается индивидуально после оценки врачом показателей физической работоспособности и адаптивности к физической нагрузке. Большинство детей при отсутствии митральной регургитации, выраженных нарушений процесса реполяризации и желудочковых аритмий удовлетворительно переносят физическую нагрузку. При наличии врачебного контроля им можно вести активный образ жизни без каких-либо ограничений физической активности. Детям можно рекомендовать плавание, лыжи, коньки, катание на велосипеде. Не рекомендуются спортивные занятия, связанные с толчкообразным характером движений (прыжки, борьба каратэ и др.). Обнаружение у ребенка митральной регургитации, желудочковых аритмий, изменений обменных процессов в миокарде, удлинения интервала QT диктует необходимость ограничения физической активности и занятий спортом. Этим детям разрешается занятие лечебной физкультурой под контролем врача.
Лечение строится по принципу общеукрепляющей и вегетотропной терапии. Весь комплекс терапевтических мероприятий должен строиться с учетом индивидуальных особенностей личности больного и функционального состояния вегетативной нервной системы.
Важной частью комплексного лечения детей с ДСТС является немедикаментозная терапия: психотерапия, аутотренинг, физиотерапия (электрофорез с магнием, бромом в области верхнешейного отдела позвоночника), водные процедуры, иглорефлексотерапия, массаж позвоночника. Внимание врача должно быть направлено на санацию хронических очагов инфекции, по показаниям проводится тонзиллэктомия.
Медикаментозная терапия должна быть направлена на: 1) лечение вегетативно-сосудистой дистонии; 2) предупреждение возникновения нейродистрофии миокарда; 3) психотерапию; 4) антибактериальную профилактику инфекционного эндокардита.
При умеренных проявлениях симпатикотонии назначается фитотерапия седативными травами, настойка валерианы, пустырника, сбор трав (шалфей, багульник, зверобой, пустырник, валериана, боярышник), обладающий одновременно легким дегидратационным эффектом. При наличии изменений процесса реполяризации на ЭКГ, нарушениях ритма проводятся курсы лечения препаратами, улучшающими обменные процессы в миокарде (панангин, карнитин, Кудесан, витамины). Карнитин назначают в дозе 50 мг/кг в сутки на 2–3 мес. Карнитин выполняет центральную роль в липидном и энергетическом обмене.
Являясь кофактором бета-окисления жирных кислот, он переносит ацильные соединения (жирные кислоты) через митохондриальные мембраны, предупреждает развитие нейродистрофии миокарда, улучшает его энергетический обмен. В наших исследованиях 35 детям с экстрасистолией (более 15 в одну минуту) в состав комплексной терапии был включен карнитин. По окончании лечения у 25 детей экстрасистолия значительно уменьшилась, у 10 детей — не определялась.
Отмечен благоприятный эффект от применения препарата Коэнзим Q10®, который значительно улучшает биоэнергетические процессы в миокарде и особенно эффективен при вторичной митохондриальной недостаточности.
Ранняя диагностика ДСТ у детей позволяет осуществлять соответствующую реабилитационную терапию и предотвращать прогрессирование заболевания. Одним из наиболее ярких терапевтических результатов является эффективное лечение детей с ДСТ (главным образом с ПМК) при помощи магнийсодержащего препарата магния оротата — Магнерот®. Выбор препарата был обусловлен известными свойствами иона магния, отмечающимися у антиаритмических препаратов I и IV класса (мембраностабилизирующие и антагонисты кальция), а также отсутствием побочных эффектов, которые могут появляться при применении традиционной антиаритмической терапии. Учитывалось также и то, что действующим веществом препарата является магния оротат, который, индуцируя синтез протеинов, участвуя в обмене фосфолипидов, являющихся составной частью клеточных мембран, необходим для фиксации внутриклеточного магния (Громова О. А., 2007).
Препарат Магнерот® применялся в виде монотерапии в дозе 40 мг/кг в сутки в течение первых 7 дней приема, затем по 20 мг/кг в сутки в течение 6 месяцев. Результатом лечения явилось уменьшение на 20–25% глубины пролабирования створок митрального клапана и уменьшение степени регургитации на 15–17%. Терапия препаратом Магнерот® не влияла на размеры левых отделов сердца и сократимость миокарда, показатели которых до лечения находились в пределах нормы.
В исследованиях, проведенных Е. Н. Басаргиной (2008), выявлен антиаритмический эффект препарата Магнерот®. При проведении суточного мониторирования ЭКГ у детей 2-й и 3-й групп было отмечено уменьшение количества желудочковых комплексов на 50% и более у 18 (27,7%) больных. Причем у 6 детей отмечено исчезновение желудочковой аритмии или уменьшение количества желудочковых комплексов до 30–312 за сутки. У 14 (21,5%) детей количество желудочковых комплексов уменьшилось не менее чем на 30%. У двух больных отмечено увеличение количества желудочковых экстрасистол до 30% от исходного уровня. Таким образом, антиаритмическая эффективность препарата Магнерот® составила 27,7%. Подобные результаты ранее получены и в других исследованиях (Домницкая Т. М. и соавт., 2005).
В то же время редкие суправентрикулярные и желудочковые экстрасистолы, если не сочетаются с синдромом удлиненного интервала QT, как правило, не требуют назначения каких-либо антиаритмических препаратов.
Таким образом, дети с синдромом ДСТС нуждаются в своевременной диагностике с использованием допплерэхокардиографии, электрокардиографии, в ряде случаев суточного мониторирования ЭКГ, назначении индивидуальной терапии и наблюдении детским кардиологом.
Терапия препаратом Магнерот® у детей с синдромом ДСТС приводит к уменьшению признаков пролапса клапанов, частоты выявления митральной регургитации, уменьшению выраженности клинических проявлений вегетативной дисфунуции, частоты желудочковых аритмий, сопровождается повышением уровня внутриэритроцитарного магния.
Литература
- Земцовский Э. В. Диспластические синдромы и фенотипы. Диспластическое сердце. Спб: «Ольга». 2007. 80 с.
- Гаврилова В. А. Синдром дисплазии соединительной ткани сердца у детей с заболеваниями органов мочевой системы. Автореф. дисс. д.м.н. М., 2002.
- Morales A. B., Romanelli B., Boucek R. J. et al. Myxoid heart disease: an assessment of extravalvular cardiac pathology in severe mitrae valve prolapse // Hum.Pathol. 1992, v. 23, № 2, p. 129–137.
- Верещагина Г. Н. Системная дисплазия соединительной ткани. Клинические синдромы, диагностика, подходы к лечению. Методическое пособие для врачей. Новосибирск, 2008, 37 с.
- Урмонас В. К., Кондрашин Н. И. Воронкообразная грудная клетка. Вильнюс: Мокслас, 1983, 115 с.
- Гнусаев С. Ф. Значение малых аномалий сердца у здоровых детей и при сердечно-сосудистой патологии. Автореф. дисс. д.м.н., М., 1996.
- Белозеров Ю. М., Гнусаев С. Ф. Пролапс митрального клапана у детей. М.: Мартис, 1995. 120 с.
- Сторожаков Г. И., Верещагина Г. С., Малышева Н. В. Оценка индивидуального прогноза при пролапсе митрального клапана // Кардиология, 2004, 4, с. 14–18.
- Нечаева Г. И., Викторова И. А. Дисплазия соединительной ткани: терминология, диагностика, тактика ведения пациентов. Омск: Изд-во «Типография Бланком», 2007. 188 с.
- Гнусаев С. Ф., Белозеров Ю. М., Виноградов А. Ф. Клиническое значение малых аномалий сердца у детей // Российский вестник перинатологии и педиатрии. 2006, № 4. С. 20–24.
- Домницкая Т. М., Гаврилова В. А. Синдром дисплазии соединительной ткани сердца у детей с заболеваниями мочевой системы / Материалы Второго Съезда педиатров-нефрологов России. М., 2000. С. 159.
- Громова О. А, Гоголева И. В. Применение магния в зеркале доказательной медицины и фундаментальных исследований в терапии // Фарматека. 2007, т. 146, № 12, с. 3–6.
- Басаргина Е. Н. Синдром дисплазии соединительной ткани сердца у детей // Вопросы современной педиатрии. 2008, т. 7, № 1, 129–133.
- Домницкая Т. М., Дьяченко А. В., Куприянова О. О., Домницкий М. В. Клиническая оценка использования оротата магния улиц молодого возраста с синдромом дисплазии соединительной ткани сердца // Кардиология. 2005; 45 (3): 76–81.
С. Ф. Гнусаев, доктор медицинских наук, профессор
ГОУ ВПО Тверская ГМА Росздрава, Тверь
Контактная информация об авторе для переписки
Лечение
Лечением аортальной недостаточности занимается врач-кардиолог и сердечно-сосудистый хирург.
Медикаментозное лечение
Медикаментозное лечение назначается в зависимости от причины появления аортальной недостаточности. Оно рассматривается как вариант подготовки к хирургической операции или для уменьшения симптомов сердечной недостаточности и облегчения состояния больных, которые имеют противопоказания к оперативному лечению.
При ревматизме и инфекционном эндокардите назначают курс антибактериальной терапии. В первом случае как профилактика обострения заболевания используются антибиотики пенициллинового ряда (бензатин бензилпенициллин). При инфекционном эндокардите назначают обычно длительным курсом от 2 недель амоксициллин, цефтриаксон, гентамицин, реже ванкомицин. Препараты назначаются исходя из клиники и устойчивости бактерий к ним. Могут использоваться как один препарат, так и комплексно.
Лечение артериальной гипертензии заключается в назначении ингибиторов АПФ (периндоприл, эналаприл, лизиноприл) или сартанов (валсартан, лозартан) и антагонистов кальция дигидропиридинового ряда (нифедипин, амлодипин).
Бета-блокаторы (бисопролол, метопролол, небиволол) добавляют к лечению в случае сниженной фракции выброса сердца по результатам эхокардиографии.
Хирургическое лечение
Протезирование аортального клапана — единственный возможный метод коррекции клапана.
Он рекомендован пациентам с:
- тяжелой аортальной регургитацией и наличием симптомов вне зависимости от фракции выброса;
- бессимптомной хронической тяжелой аортальной регургитацией и фракцией выброса менее 50%;
- хронической аортальной регургитацией параллельно с операцией аорто-коронарного шунтирования или операции на аорте и других сердечных клапанах;
- бессимптомной тяжелой аортальной регургитацией с нормальной фракцией выброса. на значительным расширением левого желудочка (КДР — более 75 мм).
Сроки лечения пациентов с аортальной недостаточностью сильно варьируют в зависимости от тяжести состояния и причины, вызвавшей патологию. После операции рекомендуется проведение курса реабилитации в санатории кардиологического профиля или реабилитационном центре. Срок восстановления — минимум 3 месяца, после чего пациент может возобновить трудовую деятельность по разрешению врача.
Публикации в СМИ
Недостаточность клапана аорты — патологическое состояние, характеризующееся ретроградным током крови из аорты в полость левого желудочка через дефектный аортальный клапан.
Частота. Среди умерших от различной патологии сердца недостаточность аортального клапана выявлена в 14% случаев, из них в 3,7% — в изолированном виде, а в 10,3% — в сочетании с другими пороками. Начиная с 1999 г. более 80% операций на клапанах сердца приходится на долю протезирования клапана аорты.
Этиология • Ревматизм, включая случаи вторичного инфекционного эндокардита (46,5%) • Медионекроз (18%) • Первичный инфекционный эндокардит (12,8%) • Врождённые аномалии (синдром «хлопающей створки», изолированная недостаточность клапана аорты, аннуло-аортальная эктазия, аномалии количества створок аортального клапана), включая случаи вторичного инфекционного эндокардита — 13,5% • Сифилис (2,1%) • Аортит при болезни Райтера, анкилозирующем спондилите, ревматоидном артрите (2,1%) • Болезни соединительной ткани, например синдром Марфана и др. (1,9%) • Травматический и спонтанный разрывы клапанов аорты (1,3%) • Атеросклероз (0,9%) • Артериальная гипертензия (0,9%).
Патофизиология • Нарушения гемодинамики обусловлены регургитацией крови из аорты в левый желудочек во время диастолы. Объём регургитации зависит от площади дефекта, величины диастолического градиента давления между аортой и левым желудочком, длительности диастолы • Увеличение диастолического объёма левого желудочка приводит к его тоногенной дилатации • Согласно закону Франка–Старлинга, левый желудочек выбрасывает в аорту увеличенный объём крови, что, вместе с регургитацией, приводит к уменьшению диастолического АД, увеличению систолического и пульсового АД • По мере развития миогенной дилатации нарастают конечный диастолический объём и конечное диастолическое давление левого желудочка, что приводит к застою крови в малом круге кровообращения • Застой в малом круге кровообращения усиливается при развитии относительной недостаточности митрального клапана вследствие дилатации левого желудочка • Механизмы компенсации: снижение ОПСС, тахикардия, гипертрофия левого желудочка.
Клиническая картина и диагностика • Жалобы •• Отсутствие жалоб — 4,5% •• Эпизоды стенокардии — 20,1% •• Синкопальные эпизоды — 1,0% •• Одышка при нагрузке — 31,4% •• Ортопноэ — 2,8% •• Симптомы системной венозной гипертензии — 25,6% •• Пароксизмальные ночные диспноэ (сердечная астма) или отёк лёгких — 32,4% •• Сочетание диспноэ с синкопальными эпизодами и эпизодами стенокардии — 0,8% •• Другие симптомы — 1,3%.
• Периферические симптомы обусловлены низким диастолическим и высоким пульсовым АД. Следует учитывать, что все периферические симптомы неспецифичны и возможны при неврозах, анемиях, тиреотоксикозе, артериовенозных мальформациях и т.д. •• Симптом Корригена (пляска каротид) — выраженная пульсация сонных артерий •• Высокий и быстрый пульс •• Симптом Мюссе — покачивание головы при каждой пульсовой волне •• Симптом Мюллера — пульсирующий язычок •• Пульсация артериол сетчатки •• Симптом Квинке — пульсирующее изменение цвета губ или ногтевого ложа, синхронное с пульсом; определяют при надавливании на них предметным стеклом •• Симптом Хилла — разница между АД на руках и ногах более 20 мм рт.ст •• Двойной тон Траубе — выслушивание громких (похожих на выстрел из пистолета) тонов на бедренных артериях •• Симптом Дюрозье — систолический шум на бедренной артерии при пережатии её проксимальнее места аускультации и диастолический шум при пережатии бедренной артерии дистальнее места аускультации •• Выслушивание тонов сердца на ладонной поверхности кисти •• Выслушивание сердечных тонов на ладонной поверхности кисти при подъёме руки вверх •• Выслушивание пульса над поверхностной ладонной дугой.
• Клапанные симптомы •• Мягкий (льющийся) диастолический убывающий шум, следующий сразу за аортальным компонентом II тона (лучше всего выслушивается во втором межреберье справа от грудины на выдохе при наклоне туловища больного вперёд), проводящийся в точку Боткина •• Грубый музыкальный шум (шум «воркующего голубя») возникает при хлопающей створке или перфорации створки •• При декомпенсации и выраженном повышении конечного диастолического давления левого желудочка интенсивность шумов аортальной регургитации ослабевает •• Шум Остина Флинта — мезодиастолический низкочастотный шум относительного митрального стеноза, возникающий в связи с прикрытием переднебоковой створки митрального клапана струёй регургитации при тяжёлой аортальной недостаточности. Степень ослабления I тона отражает выраженность декомпенсации порока по той же причине •• Систолический шум над аортой, обусловленный увеличением объёма выброса из левого желудочка, может выслушиваться и при отсутствии аортального стеноза.
• Левожелудочковые симптомы обусловлены гипертрофией, дилатацией и недостаточностью насосной и сократительной функций левого желудочка •• Разлитой, продолжительный верхушечный толчок, смещённый влево и вниз •• Пальпаторно определяемый III тон •• Увеличение площади относительной тупости сердца влево •• Аускультативные признаки застоя в лёгких — диффузные влажные разнокалиберные хрипы, лучше выслушиваемые в базальных отделах.
• Симптомы основного заболевания, например синдрома Марфана, аневризмы аорты, сифилиса, инфекционного эндокардита.
Специальные исследования • ЭКГ: признаки гипертрофии и перегрузки левых отделов сердца, в первую очередь левого желудочка. • Рентгенологическое исследование органов грудной клетки: выбухание дуги левого желудочка и аорты, обогащение лёгочного рисунка при лёгочной гипертензии.
• ЭхоКГ •• Расширение полости и гипертрофия миокарда левого желудочка •• Нарушение локальной и глобальной систолической, а также диастолической функций левого желудочка •• Расширение восходящей части аорты •• Поражение створок клапана аорты (дефекты, вегетации, аномалии количества створок, расширение фиброзного кольца, пролапс створок) •• В допплеровском режиме — патологический поток из аорты в левый желудочек во время диастолы, объём которого (регистрируют в режиме цветового картирования) соответствует степени тяжести порока •• Повышение систолического давления правого желудочка при застое крови в малом круге кровообращения •• Признаки поражения других клапанов сердца при комбинированных пороках •• С целью определения размера протеза обязательно измеряют диаметр аорты на уровне фиброзного кольца, синусов и восходящего отдела ••
Чреспищеводную ЭхоКГ проводят с целью детальной диагностики состояния грудного отдела аорты, более точного выявления вегетаций на клапанах, тромбоза левого предсердия при наличии фибрилляции предсердий, а также пациентам, у которых трансторакальная визуализация оказалась затруднённой (вследствие ожирения, эмфиземы лёгких и т.д.).
• Катетеризация левого и правого желудочков и аорты •• При недостаточности левого желудочка — повышение конечного диастолического давления левого желудочка •• При застое в малом круге — повышение давления в правом желудочке, давления заклинивания лёгочной артерии •• Для определения прогноза в отношении лёгочной гипертензии проводят пробы с аминофиллином и ингаляцией кислорода •• В зависимости от объёма регургитации в процентах по отношению к ударному объёму крови выделяют четыре степени недостаточности аортального клапана ••• I степень — 15% ••• II степень — 15–30% ••• III степень — 30–50%, ••• IV степень — более 50%.
• Левая вентрикулография, восходящая аортография •• Наличие и степень регургитации определяют по количеству сокращений, необходимых для полного изгнания контрастного вещества из полости левого желудочка •• Наличие зон гипо- и акинезии левого желудочка свидетельствует об ишемии миокарда •• Также диагностируют комбинированные клапанные поражения.
• Коронарная ангиография •• Выполняют при наличии эпизодов стенокардии и положительных результатов нагрузочного тестирования, а также всем женщинам старше 45 лет, мужчинам старше 40 лет и всем кандидатам на протезирование аортального клапана для исключения сопутствующей ИБС.
ЛЕЧЕНИЕ • Лекарственная терапия •• При бессимптомной аортальной недостаточности лёгкой степени показаны лишь ежегодное динамическое наблюдение (осмотр, ЭхоКГ, ЭКГ) и ограничение изометрических физических нагрузок (возможны увеличение аортальной регургитации и повреждение корня аорты) •• При умеренной бессимптомной аортальной недостаточности применяют ингибиторы АПФ и проводят клиническое обследование каждые 6 мес •• При тяжёлоё бессимптомной аортальной недостаточности необходимы постоянный приём периферических вазодилататоров и клиническое обследование каждые 6 мес (или немедленно при декомпенсации) •• Лечение декомпенсированной аортальной недостаточности проводят по общим принципам лечения недостаточности кровообращения (вазодилататоры, сердечные гликозиды, диуретики).
• Хирургическое лечение •• Показания: аортальная регургитация III–IV степени или II степени при наличии хотя бы одного из следующих состояний: сердечная недостаточность III–IV функционального класса (по классификации Нью-Йоркской ассоциации кардиологов), стенокардия, синкопальные состояния, острая левожелудочковая недостаточность (сердечная астма или отёк лёгких), конечное диастолическое давление в левом желудочке выше 15 мм рт.ст •• Противопоказания: тяжёлая сопутствующая патология, угрожающая жизни больного; терминальная стадия недостаточности кровообращения •• Методы хирургического лечения ••• Протезирование аортального клапана механическим искусственным клапаном сердца в условиях искусственного кровообращения ••• У детей используют биологические протезы ••• При наличии аневризмы восходящей аорты — одномоментное протезирование аортального клапана и восходящей аорты клапансодержащим кондуитом по методу Бенталла или Каброля.
Специфические послеоперационные осложнения • Тромбоэмболии • Вторичный инфекционный эндокардит протезов • Дегенеративные изменения биологических клапанов и необходимость репротезирования • Аневризмы восходящей части аорты при использовании дисковых протезов с небольшим углом открытия.
Прогноз • При естественном течении 5-летняя выживаемость не превышает 45%, а 10-летняя — 38% • После выявления симптомов заболевания средняя продолжительность жизни — 2–5 лет • После выявления дилатации левого желудочка 10-летняя выживаемость не превышает 56% • При остром развитии порока (обычно при инфекционном эндокардите) средняя продолжительность жизни составляет 7 мес •• При хирургическом лечении госпитальная летальность — 1–3%, 12-летняя выживаемость превышает 70% (при исходной сердечной недостаточности III функционального класса по классификации Нью-Йоркской ассоциации кардиологов). Синоним. Недостаточность аортального клапана
МКБ-10 • I06.1 Ревматическая недостаточность аортального клапана • I06.2 Ревматический аортальный стеноз с недостаточностью • I35.1 Аортальная (клапанная) недостаточность • I35.2 Аортальный (клапанный) стеноз с недостаточностью • Q23.1 Врождённая недостаточность аортального клапана
Осложнения
Осложнения аортальной недостаточности развиваются по мере увеличения ее степени тяжести. В начале могут появляться обычные синкопальные состояния (обмороки) из-за недостаточного кровоснабжения мозга. Нарушения проводимости в виде блокад левой ножки пучка Гиса и атриовентрикулярного проведения импульса также нередко могут встречаться у пациентов с аортальной недостаточностью.
Коронарная недостаточность может сопутствовать аортальной, но чаще в совокупности со стенозом аортального клапана. У пациента развиваются приступы стенокардии (боли в сердце давящего, сжимающего характера) и даже инфаркта миокарда.
Сердечная недостаточность — самое частое осложнение уже тяжелой аортальной недостаточности. Больной жалуется на одышку при физической нагрузке, приступы удушья, отеки нижних конечностей.
Внезапная смерть часто развивается в результате жизнеугрожающих аритмий — пароксизмальные желудочковые тахикардии, фибрилляция желудочков. В таком случае человек даже не успевает вызвать скорую медицинскую помощь — настолько быстро развивается аритмия.
В чем заключается лечение пациентов с двустворчатым аортальным клапаном?
Если пациента ничего не беспокоит, он способен выполнять необходимые ему физические нагрузки и по данным УЗИ нет признаков нарушения функции клапана и перегрузки сердца, то в лечении нет необходимости. Пациент должен регулярно наблюдаться у кардиолога.
Если у пациента появились характерные жалобы и по данным УЗИ сердца выявлено выраженное нарушение функции клапана (например, недостаточность высокой степени или критический стеноз) и признаки перегрузки сердца, то врач может принять решение о протезировании аортального клапана.
Запишитесь на прием через заявку или по телефону +7 +7 Мы работаем каждый день:
- Понедельник—пятница: 8.00—20.00
- Суббота: 8.00—18.00
- Воскресенье: выходной
Ближайшие к клинике станции метро и МЦК:
- Шоссе энтузиастов или Перово
- Партизанская
- Шоссе энтузиастов
Схема проезда
Прогноз
Прогноз аортальной недостаточности тем лучше, чем меньше степень регургитации и чем раньше начато лечение. Профилактический осмотр у терапевта, кардиолога, полноценная антибиотикотерапия в случае инфекционного эндокардита и ревматической лихорадки — все это способствует улучшению прогноза. Очень важно прислушиваться к себе, своему организму, чтобы не пропустить первые симптомы (вялость, снижение работоспособности, обморочные состояния, одышка при физической нагрузке).
Обычно при выраженной клинике сердечной недостаточности прогноз ухудшается, поскольку происходят необратимые изменения в структуре сердца.